Fsica de 3 de ESO Leyes de los

























- Slides: 29

Física de 3º de ESO Leyes de los gases Ley De Avogadro Ley De Boyle Y Mariotte Ley De Charles* Ley De Gay-Lussac* Ley De Los Gases Ideales Ley Generalizada Animaciones: Enlaces a Educaplus Jesús Peñas Cano http: //www. educaplus. org/ Cruz Martínez

Repaso Cruz Martínez

Recuerda Los gases: • Son fluidos • Se expanden hasta ocupar todo el volumen del recipiente • No tienen forma fija • Son fácilmente compresibles • Son homogéneos • Se difunden y tienden a mezclarse con otros gases Cruz Martínez

Recuerda Modelo cinético: Robert Boyle (propone la idea) Bernouille (50 años más tarde completa la teoría) “Un gas está formado por numerosas partículas que se mueven rápidamente en todas direcciones” De aquí surgió la teoría cinético-molecular Cruz Martínez

Recuerda Teoría cinético-molecular: • Un gas es un conjunto de partículas individuales en movimiento rectilíneo al azar (movimiento en zigzag), que chocan contra las paredes del recipiente o entre ellas sin pérdida de energía. • El modelo representa las partículas de gas como si tuviesen masa pero no volumen. (El volumen de cada partícula es tan pequeño comparado con el del recipiente que lo desprecian) • El movimiento y disposición de las partículas queda determinado por dos tipos de fuerzas: –Atractivas o de cohesión, que las mantienen unidas –Repulsivas o de dispersión, que tienden a separarlas Cruz Martínez

Recuerda Temperatura y Presión en la T. cinética : • La temperatura de un sistema material (en nuestro caso un gas) es proporcional a la energía cinética (Ec = ½ mv 2) media de sus partículas. Al aumentar la temperatura aumenta la energía cinética y con ella las fuerzas de repulsión. La medimos en grados Kelvin (K) (Tª en K = Tª en ºC + 273, 15) • La presión que ejerce un gas es consecuencia de los choques de sus partículas contra las paredes del recipiente. La medimos en atmósferas (atm) (1 atm = 1013 mb = 760 mm. Hg) Cruz Martínez

Leyes de los gases Cruz Martínez

Ley de Avogadro • Volúmenes iguales de gases diferentes, sometidos a las mismas condiciones de presión y temperatura, contienen un número idéntico de partículas. Animación: Avogadro Cruz Martínez

Ley de Avogadro (Otra forma de decirlo) • “En estado gaseoso y en las mismas condiciones de presión y temperatura, volúmenes iguales de distintas sustancias, contienen igual número de moléculas” Animación: Avogadro Cruz Martínez

Ley de Avogadro (Otra forma de decirlo) • A temperatura y presión constantes, el volumen que ocupa un gas es directamente proporcional a la cantidad (nº de moles) de dicho gas. Animación: Avogadro Cruz Martínez

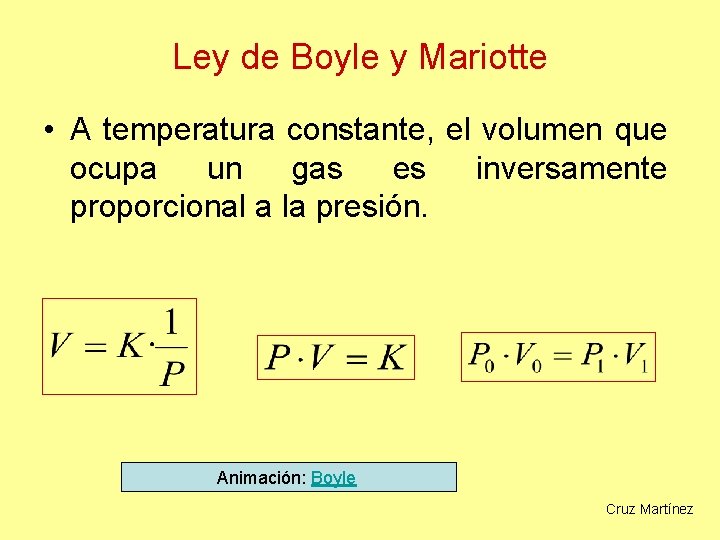
Ley de Boyle y Mariotte • A temperatura constante, el volumen que ocupa un gas es inversamente proporcional a la presión. Animación: Boyle Cruz Martínez

Ley de Charles (* 1ª Ley de Charles y Gay-Lussac) • A presión constante el volumen que ocupa un gas es directamente proporcional a la temperatura. Animación: Charles Cruz Martínez

Ley de Gay-Lussac (* 2ª Ley de Charles y Gay-Lussac) • A volumen constante la presión de un gas es directamente proporcional a su temperatura. Animación: Gay-Lussac Cruz Martínez

Ley de los gases ideales (Ecuación de los gases perfectos) • En condiciones “normales” se cumple que: (P=1 atm; T=273’ 15 K; n=1 mol; V=22’ 4 l) ¿De dónde sale esta fórmula? Cruz Martínez

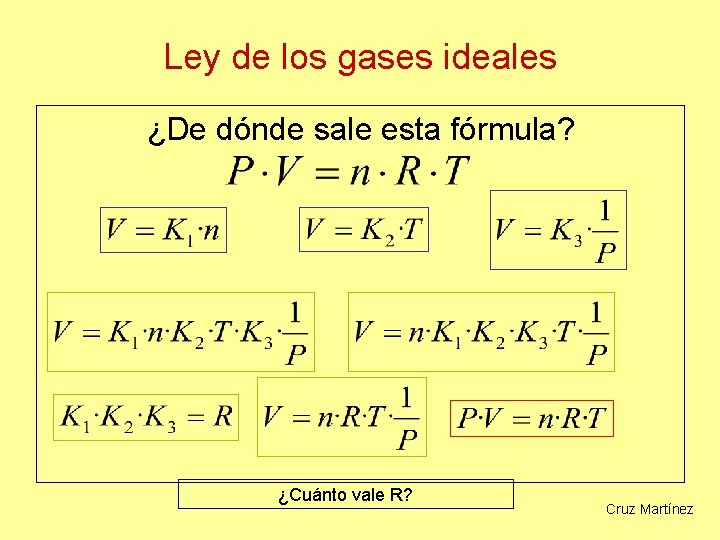
Ley de los gases ideales ¿De dónde sale esta fórmula? ¿Cuánto vale R? Cruz Martínez

Ley de los gases ideales ¿Cuánto vale R? Partiendo de las “condiciones normales” (P=1 atm; T=273’ 15 K; n=1 mol; V=22’ 4 l) Sustituimos en la fórmula: Despejando y resolviendo: Animación: Gases Ideales Cruz Martínez

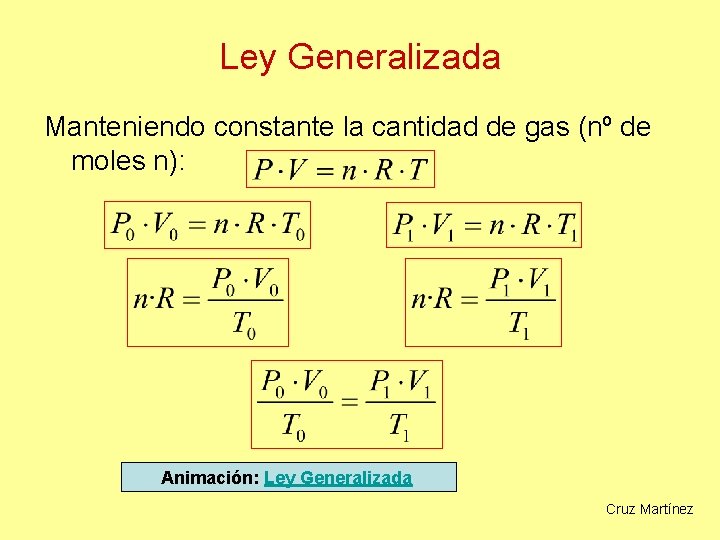
Ley Generalizada Manteniendo constante la cantidad de gas (nº de moles n): Animación: Ley Generalizada Cruz Martínez

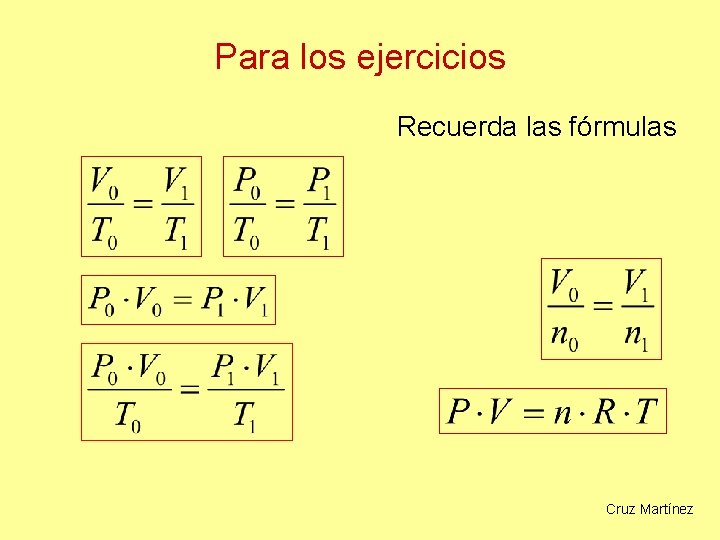
Para los ejercicios Recuerda las fórmulas Cruz Martínez

Ejercicios Cruz Martínez

LEY DE BOYLE Y MARIOTTE • Ejemplo: Si un gas ocupa un volumen de 6 litros a la presión de 1 atm ¿Cuál será el volumen si aumentamos la presión a 1140 mm. Hg? • En primer lugar expresaremos 1140 mm. Hg en atm: recuerda 760 mm. Hg 1 atm Cruz Martínez

LEY DE BOYLE Y MARIOTTE • Ejemplo: Si un gas ocupa un volumen de 6 litros a la presión de 1 atm ¿Cuál será el volumen si aumentamos la presión a 1140 mm. Hg? • Ahora podemos aplicar la ley de Boyle y Mariotte, tomando los valores del ejemplo: V 0 = 6 l P 0 = 1 atm P 1 = 1140 mm. Hg = 1. 5 atm Cruz Martínez

LEY DE BOYLE Y MARIOTTE • Ejemplo: Si un gas ocupa un volumen de 6 litros a la presión de 1 atm ¿Cuál será el volumen si aumentamos la presión a 1140 mm. Hg? • Ahora podemos aplicar la ley de Boyle y Mariotte, tomando los valores del ejemplo: Como la presión ha aumentado, el volumen tiene que disminuir. Si la presión disminuyera, el volumen aumentaría, ya que se comportan de forma opuesta. Cruz Martínez

LEY DE BOYLE Y MARIOTTE • Ejemplo: ¿Qué presión tendrán unas ruedas cuya presión sea de 1’ 9 atm a 20 ºC, tras circular el coche y calentarse hasta los 50 ºC? • En primer lugar debemos expresar las temperaturas en la escala absoluta, para lo que sumaremos 273: • T 0 = 20ºC + 273 = 293 K • T 1 = 50ºC + 273 = 323 K Cruz Martínez

LEY DE CHARLES Y GAY-LUSSAC. • Ejemplo: ¿Qué presión tendran unas ruedas cuya presión sea de 1. 9 atm a 20 ºC, tras circular el coche y calentarse hasta los 50 ºC? • P 0 = 1. 9 atm • Podemos aplicar la ley de Charles y Guy. Lussac: Cruz Martínez

LEY DE CHARLES Y GAY-LUSSAC. • Ejemplo: Si introducimos un globo en el congelador y la temperatura baja de 30ºC a -20ºC, ¿Cómo verá reducido su volumen un globo de 2 l ? • En primer lugar debemos expresar las temperaturas en la escala absoluta, para lo que sumaremos 273: • T 0 = 30ºC + 273 = 303 K • T 1 = -20ºC + 273 = 253 K Si, por el contrario, se expone al sol, al aumentar su temperatura, aumentará su volumen. Cruz Martínez

LEY DE CHARLES Y GAY-LUSSAC. • Ejemplo: Si introducimos un globo en el congelador y la temperatura baja de 30ºC a -20ºC, ¿Cómo verá reducido su volumen un globo de 2 l ? • Y como: V 0 = 2 l • Podemos aplicar la ley de Charles y Guy. Lussac: Cruz Martínez

LEY DE LOS GASES PERFECTOS • Ejemplo: un globo de feria se ha inflado hasta alcanzar 3 litros, a la presión de 1 atmósfera y a la temperatura de 27 ºC ¿Cuántos moles de gas contiene? • En primer lugar debemos expresar las temperaturas en la escala absoluta, para lo que sumaremos 273: • T = 20ºC + 273 = 293 K Cruz Martínez

LEY DE LOS GASES PERFECTOS • Ejemplo: un globo de feria se ha inflado hasta alcanzar 3 litros, a la presión de 1 atmósfera y a la temperatura de 27 ºC ¿Cuántos moles de gas contiene? • Y como: P = 1 atm y V = 3 l • Podemos aplicar la ley de los gases: Cruz Martínez

Enlaces gases educaplus Conceptos – – Temperatura Presión Volumen Cantidad de gas Leyes – – – Avogadro Boyle Charles Gay-Lussac Gases Ideales Ley Generalizada Ejercicios – Avogadro – Boyle – Charles – Gay-Lussac – Gases Ideales Cruz Martínez