FRM 204106 Anvendt farmakokinetikk bruk av farmakokinetikk i

FRM 2041/06 Anvendt farmakokinetikk - bruk av farmakokinetikk i farmakoterapeutiske problemstillinger [krever forståelse for farmakokinetiske prosesser/parametere og modeller] Espen Molden (cand pharm, dr scient) Farmasøytisk inst, Ui. O (rom 484 B, emolden@farmasi. uio. no) Psykofarmakologisk avd, Diakonhjemmet sykehus Aktuell litteratur: Herfindal kap 1 og 3, Walker kap 1 og 2, Rang & Dale kap 7 og 8

: paradoks – legemiddelpåført skade/sykdom • ca. 5 -20% av alle sykehusinnleggelser er relatert til legemiddelbruk (ca. 25% av disse tilfellene er knyttet til interaksjonsproblematikk) - Tall basert på amerikansk materiale JAMA 1998; 279: 1200 Ann Pharmacother 2002; 36: 1331. ● Legemidler trukket fra markedet – ferske eksempler terbinafin/Teldanex® cisaprid/Prepulsid® Farmakokinetisk/ mibefradil/Posicor® farmakodynamisk cerivastatin/Lipobay® problem rofecoksib/Vioxx® tioridazin/Melleril® valdecoksib/Bextra®

Kontraindiserte CYP-interaksjoner – mer og mer vanlig Seroquel® (quetiapin) – utdrag fra SPC 4. 3 Kontraindikasjoner: . . . Samtidig administrering av cytokrom P 450 3 A 4 inhibitorer, slik som HIV-protease hemmere, azol-antifugale stoffer, erytromycin, klaritromycin, og nefazodon er kontraindisert… 4. 5 Interaksjoner: . . . Enzymet CYP 3 A 4 er hovedansvarlig for cytokrom P 450 mediert metabolisme av quetiapin. I en interaksjonsstudie på friske frivillige førte samtidig administrering av quetiapin 25 mg og ketokonazol, en CYP 3 A 4 hemmer, til en 5 -8 dobling av AUC for quetiapin. . Bør ikke tas med grapefrukt juice… Inspra® (eplerenon) – utdrag fra SPC 4. 3 Kontraindikasjoner: . . . Pasienter som får kaliumsparende diuretika, kaliumtilskudd eller sterke hemmere av CYP 3 A 4 (f. eks itrakonazol, ketokonazol, ritonavir, nelfinavir, klaritromycin, telitromycin og nefazodon) 4. 5 Interaksjoner: . . . En sterk hemmer av CYP 3 A 4 (ketokonazol 200 mg to ganger daglig) førte til en 441% økning i AUC for eplerenon (5, 4 -dobling; egen anm). . .
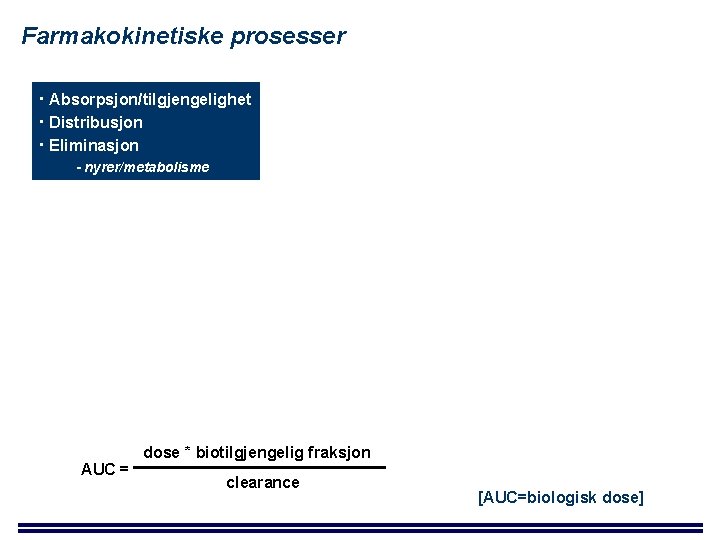
Farmakokinetiske prosesser Absorpsjon/tilgjengelighet Distribusjon Eliminasjon - nyrer/metabolisme AUC = dose * biotilgjengelig fraksjon clearance [AUC=biologisk dose]
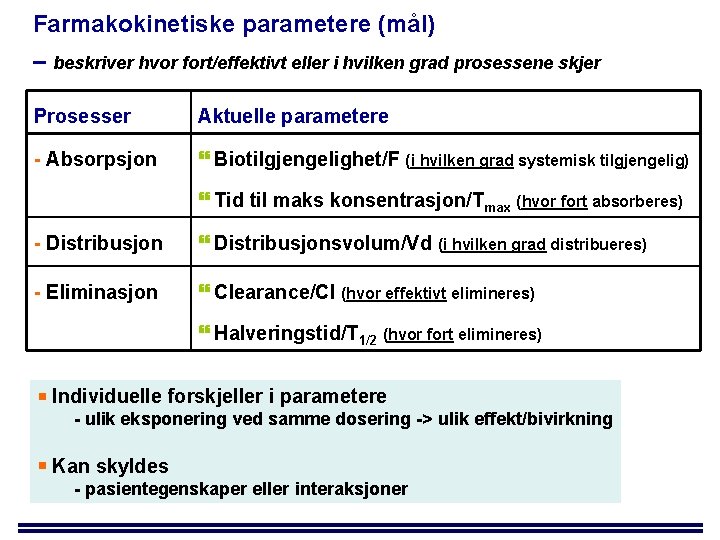
Farmakokinetiske parametere (mål) – beskriver hvor fort/effektivt eller i hvilken grad prosessene skjer Prosesser Aktuelle parametere - Absorpsjon Biotilgjengelighet/F (i hvilken grad systemisk tilgjengelig) Tid til maks konsentrasjon/Tmax (hvor fort absorberes) - Distribusjonsvolum/Vd (i hvilken grad distribueres) - Eliminasjon Clearance/Cl (hvor effektivt elimineres) Halveringstid/T 1/2 (hvor fort elimineres) Individuelle forskjeller i parametere - ulik eksponering ved samme dosering -> ulik effekt/bivirkning Kan skyldes - pasientegenskaper eller interaksjoner
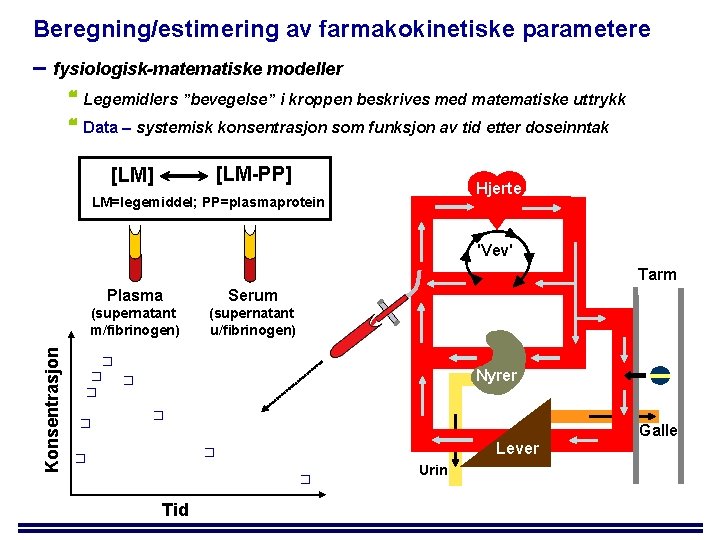
Beregning/estimering av farmakokinetiske parametere – fysiologisk-matematiske modeller Legemidlers ”bevegelse” i kroppen beskrives med matematiske uttrykk Data – systemisk konsentrasjon som funksjon av tid etter doseinntak [LM-PP] [LM] Hjerte LM=legemiddel; PP=plasmaprotein 'Vev' Konsentrasjon Tarm Plasma Serum (supernatant m/fibrinogen) (supernatant u/fibrinogen) � � � Nyrer � Galle Lever � � � Tid Urin
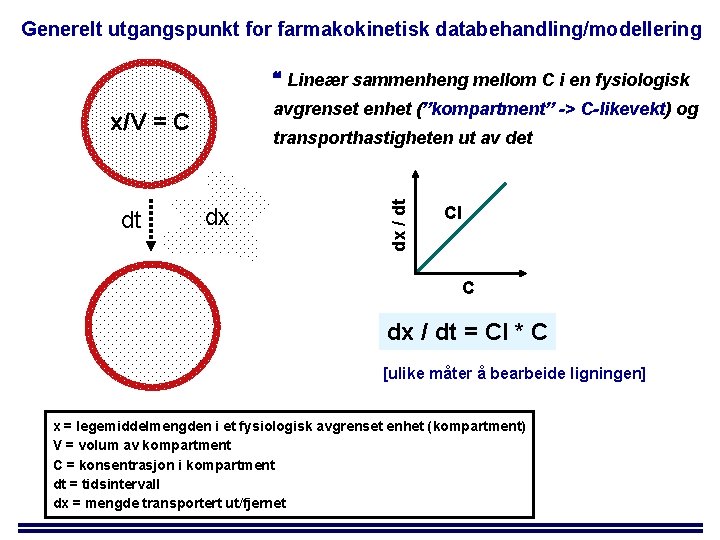
Generelt utgangspunkt for farmakokinetisk databehandling/modellering Lineær sammenheng mellom C i en fysiologisk avgrenset enhet (”kompartment” -> C-likevekt) og x/V = C dx dx / dt dt transporthastigheten ut av det Cl C dx / dt = Cl * C [ulike måter å bearbeide ligningen] x = legemiddelmengden i et fysiologisk avgrenset enhet (kompartment) V = volum av kompartment C = konsentrasjon i kompartment dt = tidsintervall dx = mengde transportert ut/fjernet

Ulike typer modellering/databehandling ● Non-kompartment-modellering 1970 -tallet rigid, fast oppskrift totaleksponering i hele tidsforløpet; integral/areal-under-kurve estimere F, ofte også Cl ● Kompartment-modellering 1920 -tallet fritt, selvdefinerbart modellerer C(t); som regel eksponentialfunksjon(er) estimere Vd/T 1/2, eventuelt også Cl
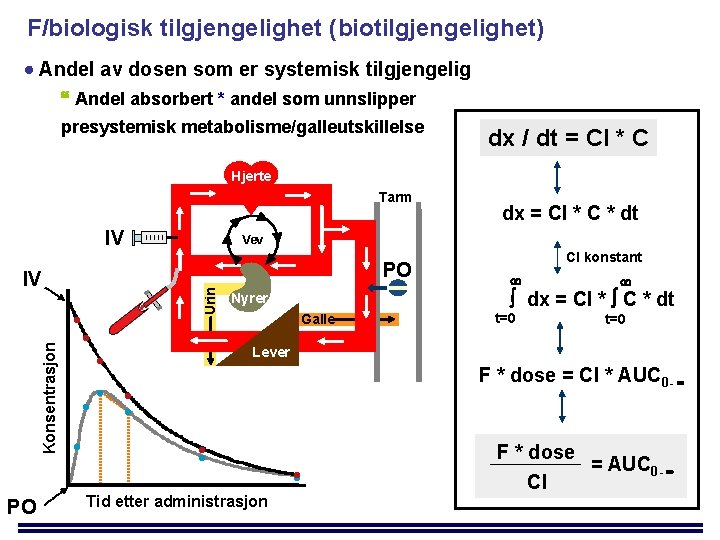
F/biologisk tilgjengelighet (biotilgjengelighet) Andel av dosen som er systemisk tilgjengelig Andel absorbert * andel som unnslipper presystemisk metabolisme/galleutskillelse dx / dt = Cl * C Hjerte Tarm IV Konsentrasjon Urin • PO Vev PO IV • Cl konstant dx = Cl * C * dt Nyrer Galle t=0 Lever • • dx = Cl * C * dt F * dose = Cl * AUC 0 - • • Tid etter administrasjon • F * dose = AUC 0 - Cl

Cl/clearance – eliminasjonseffektivitet fra systemisk kretsløp Kan beregnes slik: Cl = Dose. IV/AUC (F=1 ved IV-dosering) Clearancemekanismer – varierer fra legemiddel til legemiddel Metabolisme i lever (primært) Eks. cytokrom P 450 + UDP-glukuronosyl-transferaser Direkte utskillelse/ekskresjon via pumpeproteiner i urin eller galle Eks. ATP-binding-cassette (ABC)-transportører; P-glykoprotein Nyrefiltrasjon Har benevnelsen volum/tid (eks. L/time, eller m. L/min) Kan ikke overstige blodforsyning til eliminerende organer (blodforsyning nyrer ca. 1, 1 L/min; lever ca. 1, 4 L/min) Ingen nedre grense T 1/2/kel beskriver hvor fort legemidlet elimineres fra kroppen Bestemt av både Cl og Vd

Vd/distribusjonsvolum – grad av fordeling til vev Vd = legemiddelmengden i kroppen total plasmakonsentrasjon Plasma Hvorfor er Vd ofte annerledes enn kroppsvolumet (ca. 40 L)? Vev LM LM LM-PP LM-VM Ulik bindingsgrad/totalkonsentrasjon i vev og plasma (unbundet konsentrasjon lik/”ganske lik”) LM=legemiddel PP=plasmaprotein VM=vevsmolekyl Vd < 40 L totalkonsentrasjon større i plasma enn i vev Vd = 40 L totalkonsentrasjon lik i plasma og i vev Vd > 40 L totalkonsentrasjon større i vev enn plasma [nedre grense for Vd er 3 L, men ingen øvre grense]
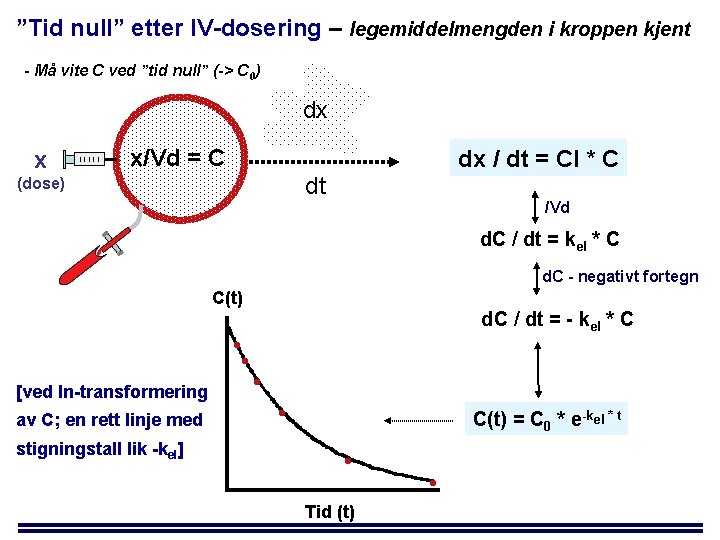
”Tid null” etter IV-dosering – legemiddelmengden i kroppen kjent - Må vite C ved ”tid null” (-> C 0) dx x x/Vd = C dx / dt = Cl * C dt (dose) /Vd d. C / dt = kel * C d. C - negativt fortegn C(t) • • [ved ln-transformering av C; en rett linje med stigningstall lik -kel] d. C / dt = - kel * C • • C(t) = C 0 * e-kel * t • Tid (t) •
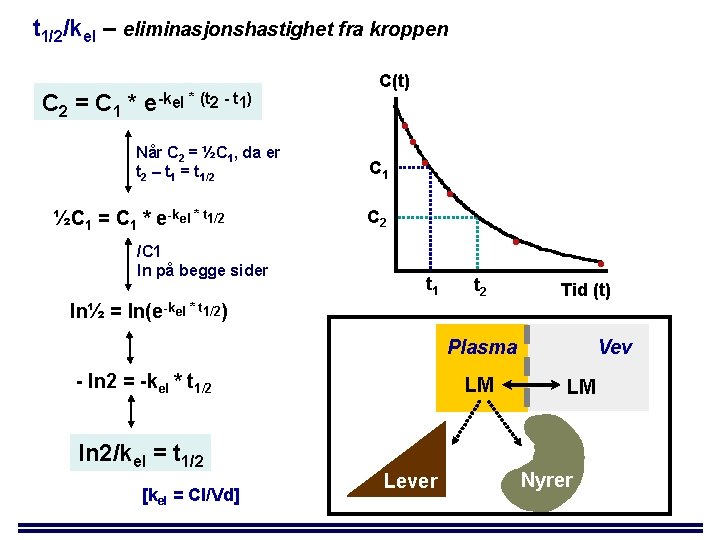
t 1/2/kel – eliminasjonshastighet fra kroppen C 2 = C 1 * e-kel * (t 2 - t 1) Når C 2 = ½C 1, da er t 2 – t 1 = t 1/2 ½C 1 = C 1 * e-kel * t 1/2 /C 1 ln på begge sider C(t) • • C 1 • • C 2 • t 1 t 2 • Tid (t) ln½ = ln(e-kel * t 1/2) Vev Plasma - ln 2 = -kel * t 1/2 ln 2/kel = t 1/2 [kel = Cl/Vd] LM Lever LM Nyrer
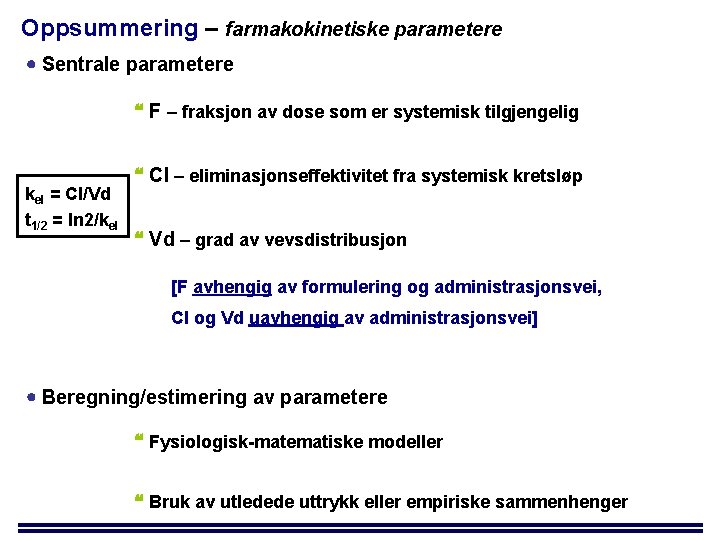
Oppsummering – farmakokinetiske parametere Sentrale parametere F – fraksjon av dose som er systemisk tilgjengelig kel = Cl/Vd t 1/2 = ln 2/kel Cl – eliminasjonseffektivitet fra systemisk kretsløp Vd – grad av vevsdistribusjon [F avhengig av formulering og administrasjonsvei, Cl og Vd uavhengig av administrasjonsvei] Beregning/estimering av parametere Fysiologisk-matematiske modeller Bruk av utledede uttrykk eller empiriske sammenhenger

Farmakokinetisk info om legemidler ”Summary of product characteristics” (SPC): SPC: 1. Produktnavn 2. Sammensetning 3. Legemiddelform 4. Kliniske opplysninger 4. 1 Indikasjoner, 4. 2 Dosering, 4. 3 Kontraindikasjoner, 4. 4. Advarsler/forsiktighetsregler, 4. 5. Interaksjoner o. s. v. 5. Farmakologiske opplysninger 5. 1 Farmakodynamiske, 5. 2 Farmakokinetiske, 5. 3 Prekliniske sikkerhetsdata 6. Farmasøytiske opplysninger 6. 1 Hjelpestoffer, 6. 2 Uforlikeligheter SPC`er finnes via www. legemiddelverket. no

Farmakokinetikk i farmakoterapeutiske problemstillinger Individuelle forskjeller i parametere: Ulik eksponering ved samme dosering -> ulik effekt/bivirkning Årsaker Interaksjoner - påvirkning av andre legemidler, rusmidler, næringsmidler eller naturmidler Pasientegenskaper - genetikk, alder, organfunksjon, sykdom, graviditet m. m. Doseringstilpasning og oppfølging (på forelesning 30/5) Design av doseregime Oppfølgning basert på konsentrasjonsmåling - ”therapeutic drug monitoring”

Interaksjoner Farmakodynamiske Forsterkende eller svekkende mekanismer på selve effekt/bivirkningssted I en del tilfeller terapeutisk tilsiktet Farmakokinetiske Endring i eksponering overfor effekt/bivirkningsstedet Mange ulike mekanismer, men endret cytokrom P 450 (CYP)-metabolisme er vanligst/best beskrevet Sjelden terapeutisk tilsiktet
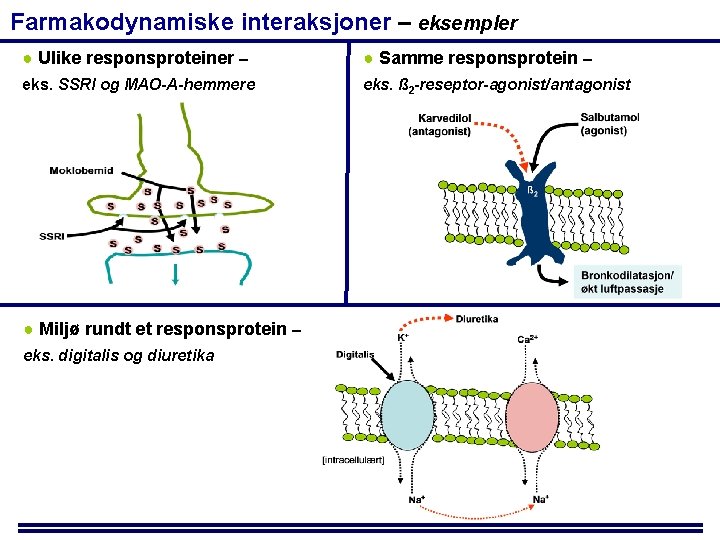
Farmakodynamiske interaksjoner – eksempler ● Ulike responsproteiner – ● Samme responsprotein – eks. SSRI og MAO-A-hemmere eks. ß 2 -reseptor-agonist/antagonist ● Miljø rundt et responsprotein – eks. digitalis og diuretika
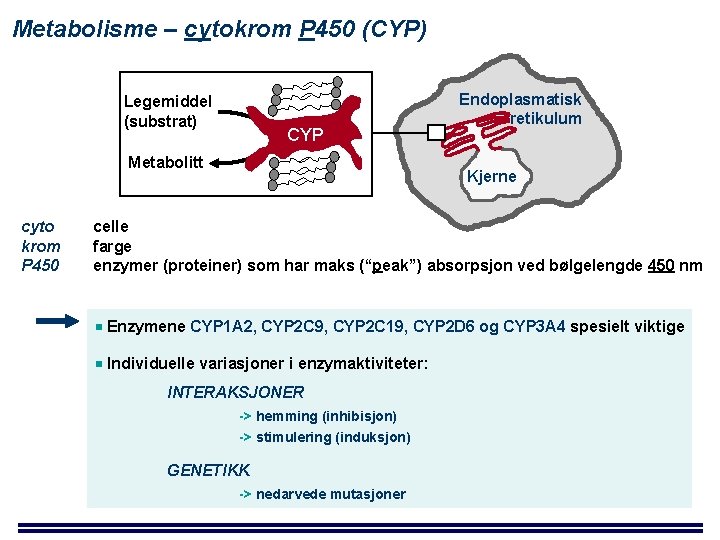
Metabolisme – cytokrom P 450 (CYP) Legemiddel (substrat) CYP Metabolitt cyto krom P 450 Endoplasmatisk retikulum Kjerne celle farge enzymer (proteiner) som har maks (“peak”) absorpsjon ved bølgelengde 450 nm Enzymene CYP 1 A 2, CYP 2 C 9, CYP 2 C 19, CYP 2 D 6 og CYP 3 A 4 spesielt viktige Individuelle variasjoner i enzymaktiviteter: INTERAKSJONER -> hemming (inhibisjon) -> stimulering (induksjon) GENETIKK -> nedarvede mutasjoner
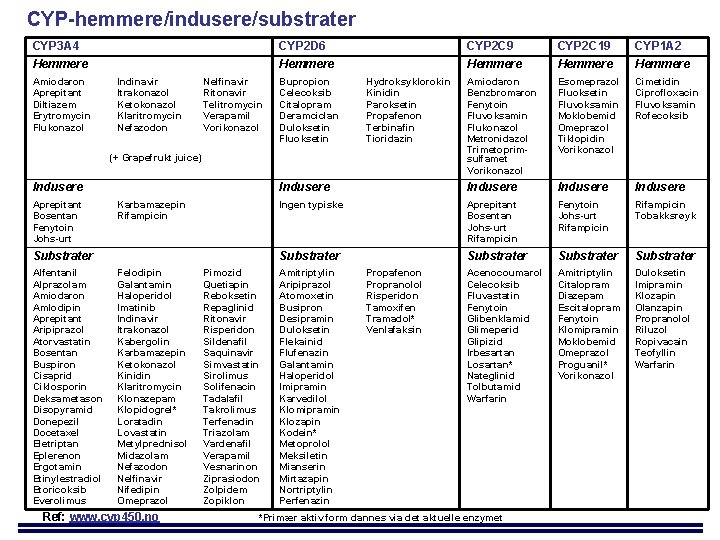
CYP-hemmere/indusere/substrater CYP 3 A 4 CYP 2 D 6 CYP 2 C 9 CYP 2 C 19 CYP 1 A 2 Hemmere Hemmere Amiodaron Benzbromaron Fenytoin Fluvoksamin Flukonazol Metronidazol Trimetoprimsulfamet Vorikonazol Esomeprazol Fluoksetin Fluvoksamin Moklobemid Omeprazol Tiklopidin Vorikonazol Cimetidin Ciprofloxacin Fluvoksamin Rofecoksib Indusere Ingen typiske Aprepitant Bosentan Johs-urt Rifampicin Fenytoin Johs-urt Rifampicin Tobakksrøyk Substrater Acenocoumarol Celecoksib Fluvastatin Fenytoin Glibenklamid Glimeperid Glipizid Irbesartan Losartan* Nateglinid Tolbutamid Warfarin Amitriptylin Citalopram Diazepam Escitalopram Fenytoin Klomipramin Moklobemid Omeprazol Proguanil* Vorikonazol Duloksetin Imipramin Klozapin Olanzapin Propranolol Riluzol Ropivacain Teofyllin Warfarin Amiodaron Aprepitant Diltiazem Erytromycin Flukonazol Indinavir Itrakonazol Ketokonazol Klaritromycin Nefazodon Nelfinavir Ritonavir Telitromycin Verapamil Vorikonazol Bupropion Celecoksib Citalopram Deramciclan Duloksetin Fluoksetin Hydroksyklorokin Kinidin Paroksetin Propafenon Terbinafin Tioridazin (+ Grapefrukt juice) Indusere Aprepitant Bosentan Fenytoin Johs-urt Karbamazepin Rifampicin Substrater Alfentanil Alprazolam Amiodaron Amlodipin Aprepitant Aripiprazol Atorvastatin Bosentan Buspiron Cisaprid Ciklosporin Deksametason Disopyramid Donepezil Docetaxel Eletriptan Eplerenon Ergotamin Etinylestradiol Etoricoksib Everolimus Felodipin Galantamin Haloperidol Imatinib Indinavir Itrakonazol Kabergolin Karbamazepin Ketokonazol Kinidin Klaritromycin Klonazepam Klopidogrel* Loratadin Lovastatin Metylprednisol Midazolam Nefazodon Nelfinavir Nifedipin Omeprazol Ref: www. cyp 450. no Pimozid Quetiapin Reboksetin Repaglinid Ritonavir Risperidon Sildenafil Saquinavir Simvastatin Sirolimus Solifenacin Tadalafil Takrolimus Terfenadin Triazolam Vardenafil Verapamil Vesnarinon Ziprasiodon Zolpidem Zopiklon Amitriptylin Aripiprazol Atomoxetin Busipron Desipramin Duloksetin Flekainid Flufenazin Galantamin Haloperidol Imipramin Karvedilol Klomipramin Klozapin Kodein* Metoprolol Meksiletin Mianserin Mirtazapin Nortriptylin Perfenazin Propafenon Propranolol Risperidon Tamoxifen Tramadol* Venlafaksin *Primær aktiv form dannes via det aktuelle enzymet
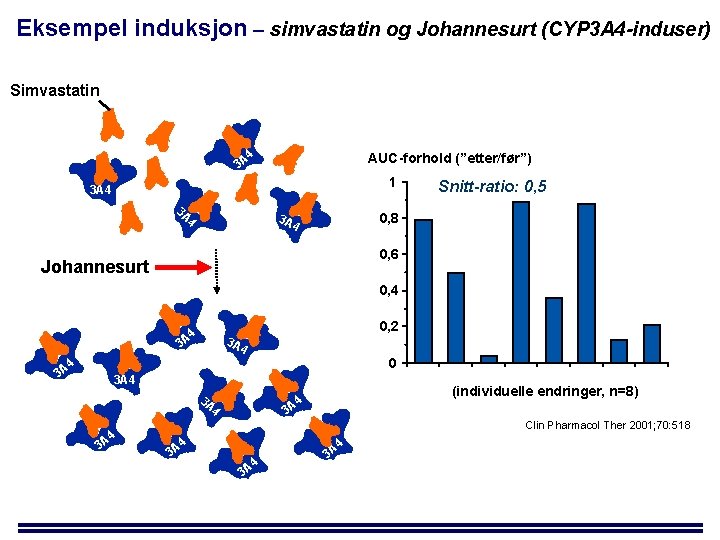
Eksempel induksjon – simvastatin og Johannesurt (CYP 3 A 4 -induser) Simvastatin 4 AUC-forhold (”etter/før”) 3 A 1 3 A 4 3 A 0, 8 3 A 4 Snitt-ratio: 0, 5 4 0, 6 Johannesurt 0, 4 A 4 0, 2 3 A 4 3 0 4 3 A 3 A 4 4 3 A (individuelle endringer, n=8) 4 3 A Clin Pharmacol Ther 2001; 70: 518 4 4 3 A 3 A

Eksempel hemming – simvastatin og CYP 3 A 4 -hemmere Hemmer Relativ simvastatin-AUC Erytromycin x 4 Diltiazem x 5 Grapefrukt juice x 7 Itrakonazol x 19 Ritonavir x 32 Clin Pharmacol Ther 1998; 64: 177 Clin Pharmacol Ther 2000; 67: 267 Clin Pharmacol Ther 1998; 63: 332 Clin Pharmacol Ther 1998; 64: 477 Aids 2002; 16: 569 Metabolisme av andre aktuelle statiner: Atorvastatin (Lipitor®) CYP 3 A 4 Fluvastatin (Lescol®) CYP 2 C 9 Pravastatin (Pravachol®) Fase II/non-metabolisme/(CYP 3 A 4)
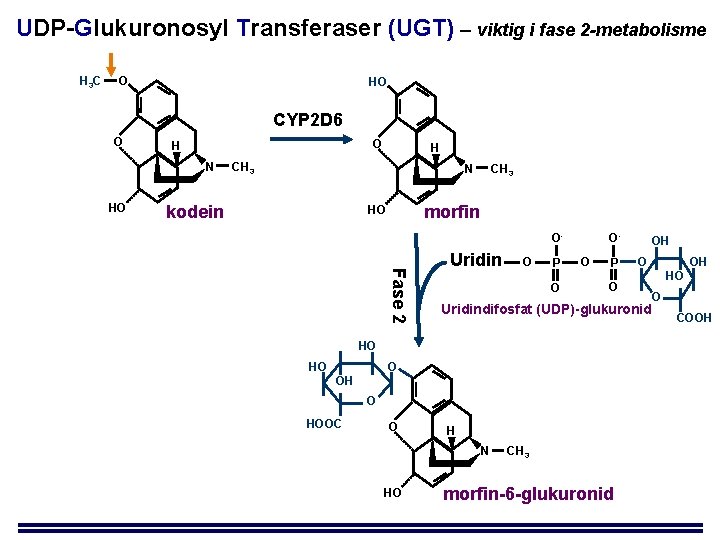
UDP-Glukuronosyl Transferaser (UGT) – viktig i fase 2 -metabolisme H 3 C O HO CYP 2 D 6 O O H N HO H CH 3 N kodein CH 3 morfin HO O- Fase 2 Uridin O P O OO P Uridindifosfat (UDP)-glukuronid O OH O HOOC O H N HO O O HO HO OH CH 3 morfin-6 -glukuronid OH HO O COOH
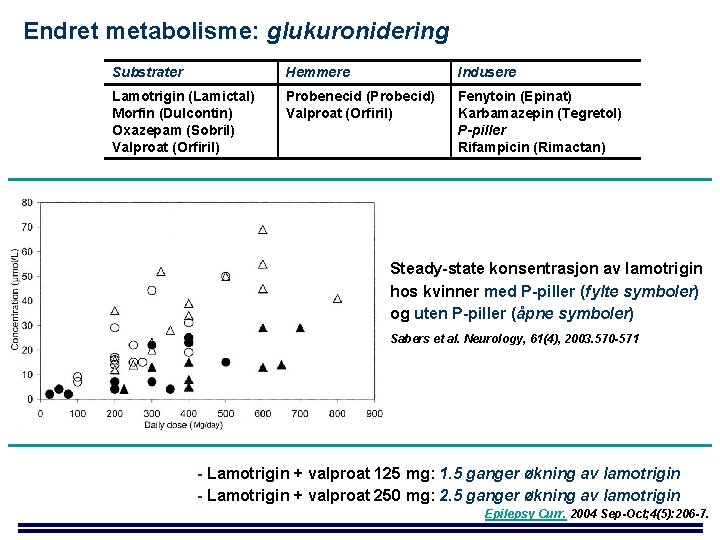
Endret metabolisme: glukuronidering Substrater Hemmere Indusere Lamotrigin (Lamictal) Morfin (Dulcontin) Oxazepam (Sobril) Valproat (Orfiril) Probenecid (Probecid) Valproat (Orfiril) Fenytoin (Epinat) Karbamazepin (Tegretol) P-piller Rifampicin (Rimactan) Steady-state konsentrasjon av lamotrigin hos kvinner med P-piller (fylte symboler) og uten P-piller (åpne symboler) Sabers et al. Neurology, 61(4), 2003. 570 -571 - Lamotrigin + valproat 125 mg: 1. 5 ganger økning av lamotrigin - Lamotrigin + valproat 250 mg: 2. 5 ganger økning av lamotrigin Epilepsy Curr. 2004 Sep-Oct; 4(5): 206 -7.
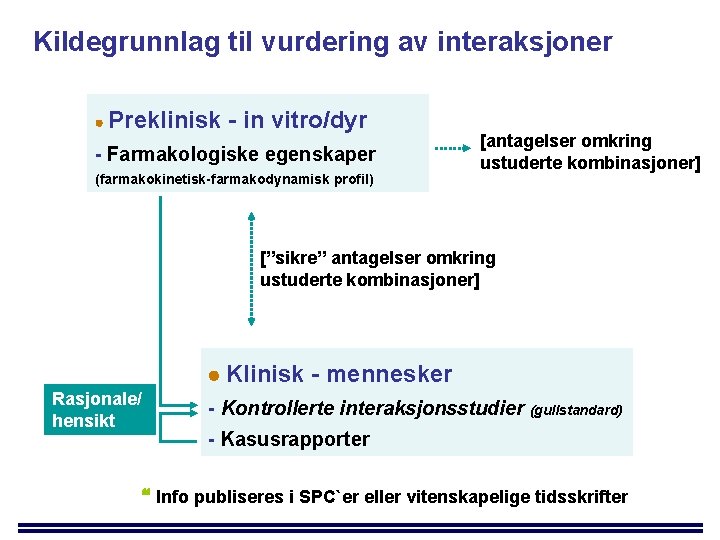
Kildegrunnlag til vurdering av interaksjoner Preklinisk - in vitro/dyr - Farmakologiske egenskaper (farmakokinetisk-farmakodynamisk profil) [antagelser omkring ustuderte kombinasjoner] [”sikre” antagelser omkring ustuderte kombinasjoner] Klinisk - mennesker Rasjonale/ hensikt - Kontrollerte interaksjonsstudier (gullstandard) - Kasusrapporter Info publiseres i SPC`er eller vitenskapelige tidsskrifter
Raffinert informasjon – interaksjonsdatabaser Publisert informasjon omkring interaksjonsproblematikk Legemiddelkombinasjoner med interaksjonsrisiko Evt. klassifisering av risiko/ ”klinisk relevans”

Aktuelle interaksjonsdatabaser DRUID: www. interaksjoner. no Akademisk interesse Ta forhåndsregler Bør unngås FASS: www. janusinfo. se Drug Interaction Checker: www. drugs. com/drug_interactions cyp 450. no: www. cyp 450. no CYP 3 A 4 Substrater Hemmere Karbamazepin (Tegretol) 1. 2 -1. 3/K Erytromycin Itrakonazol Ketokonazol Klaritromycin 1. 3 1. 4 -1. 6/K Quetiapin (Seroquel) ≥ 5. 0 Tadalafil (Cialis) 2. 1 Vardenafil (Levitra) 4. 0 K 10. 0

Likhet mellom DRUID og FASS – 85% når det gjelder interaksjon/ikke-interaksjon 55% når det gjelder gradering av risiko Årsak til manglende faglig konsensus begrenset klinisk informasjonsgrunnlag studier i friske frivillige og/eller spontanrapporter hos enkeltpasienter [også mye indirekte data] ulike fagfolk – ulike mening/fortolkning, ulik oversikt

Løsninger på interaksjoner ● Dosejustering - Tradisjonell løsning, men ofte vanskelig å ”treffe” p. g. a. svært variabel interaksjonsgrad ● Terapeutiske alternativer uten interaksjonsrisiko - Eliminerer problemstillingen - Alternativer finnes ofte, men terapeutisk likhet et diskusjonstema Forskrivingsansvar er legens – ”bestemmer” vedr. terapeutisk likhet ● Pasientinformasjon/oppfølging - Be pasient om å kontakte lege/farmasøyt ved evt. symptomer - Be lege om å følge opp problemstillingen
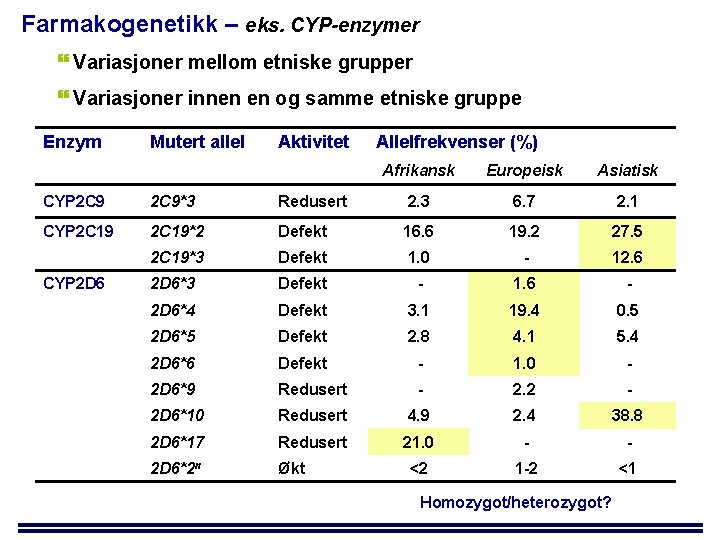
Farmakogenetikk – eks. CYP-enzymer Variasjoner mellom etniske grupper Variasjoner innen en og samme etniske gruppe Enzym Mutert allel Aktivitet CYP 2 C 9*3 CYP 2 C 19 Allelfrekvenser (%) Afrikansk Europeisk Asiatisk Redusert 2. 3 6. 7 2. 1 2 C 19*2 Defekt 16. 6 19. 2 27. 5 2 C 19*3 Defekt 1. 0 - 12. 6 CYP 2 D 6*3 Defekt - 1. 6 - 2 D 6*4 Defekt 3. 1 19. 4 0. 5 2 D 6*5 Defekt 2. 8 4. 1 5. 4 2 D 6*6 Defekt - 1. 0 - 2 D 6*9 Redusert - 2. 2 - 2 D 6*10 Redusert 4. 9 2. 4 38. 8 2 D 6*17 Redusert 21. 0 - - 2 D 6*2 n Økt <2 1 -2 <1 Homozygot/heterozygot?
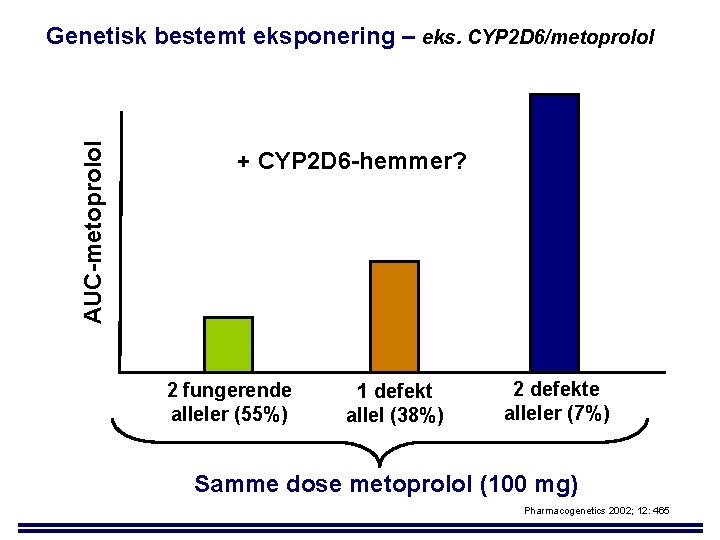
AUC-metoprolol Genetisk bestemt eksponering – eks. CYP 2 D 6/metoprolol + CYP 2 D 6 -hemmer? 2 fungerende alleler (55%) 1 defekt allel (38%) 2 defekte alleler (7%) Samme dose metoprolol (100 mg) Pharmacogenetics 2002; 12: 465
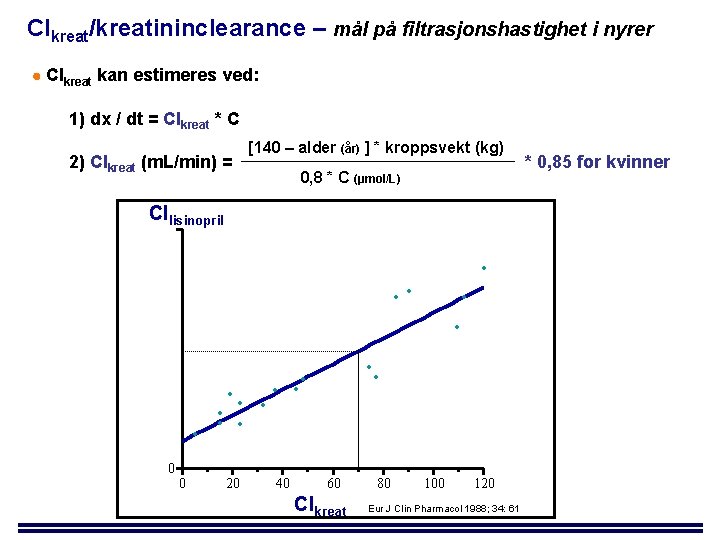
Clkreat/kreatininclearance – mål på filtrasjonshastighet i nyrer Clkreat kan estimeres ved: 1) dx / dt = Clkreat * C [140 – alder (år) ] * kroppsvekt (kg) 2) Clkreat (m. L/min) = * 0, 85 for kvinner 0, 8 * C (µmol/L) Cllisinopril 0 0 20 40 60 Clkreat 80 100 120 Eur J Clin Pharmacol 1988; 34: 61

Forelesninger 3/5: kl 0915 -1100 Biotilgjengelighet Mer inngående om begrensende mekanismer Variasjon i biotilgjengelighet Absorpsjonsinteraksjoner Betydning av matinntak Bioekvivalens - likhetstesting av preparater med samme virkestoff Doseringstilpasning og oppfølging Design av doseregime Oppfølging basert på konsentrasjonsmåling - ”therapeutic drug monitoring” (TDM) [Espen Molden: emolden@farmasi. uio. no]
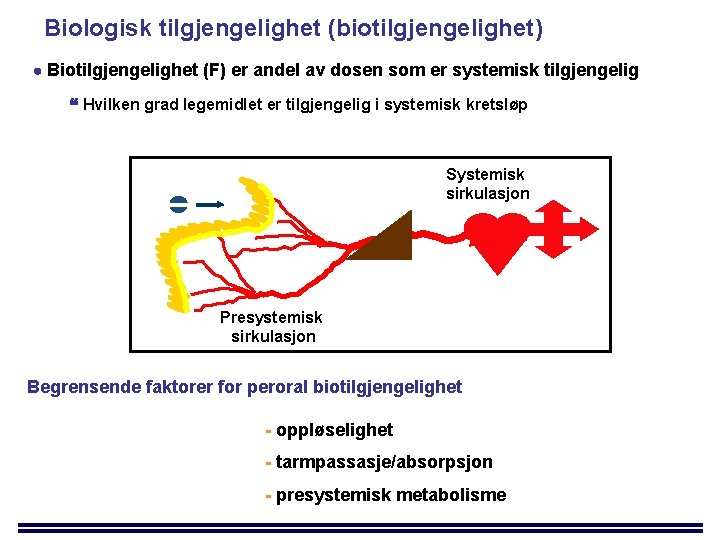
Biologisk tilgjengelighet (biotilgjengelighet) Biotilgjengelighet (F) er andel av dosen som er systemisk tilgjengelig Hvilken grad legemidlet er tilgjengelig i systemisk kretsløp Systemisk sirkulasjon Presystemisk sirkulasjon Begrensende faktorer for peroral biotilgjengelighet - oppløselighet - tarmpassasje/absorpsjon - presystemisk metabolisme
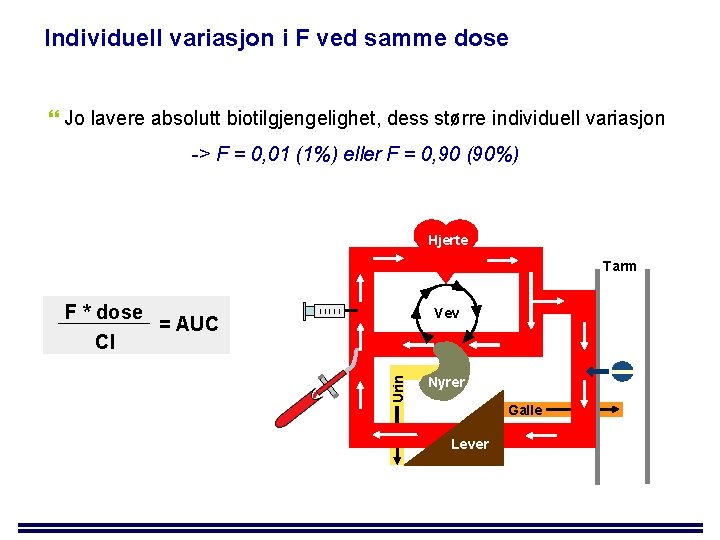
Individuell variasjon i F ved samme dose Jo lavere absolutt biotilgjengelighet, dess større individuell variasjon -> F = 0, 01 (1%) eller F = 0, 90 (90%) Hjerte Tarm F * dose = AUC Cl Urin Vev Nyrer Galle Lever
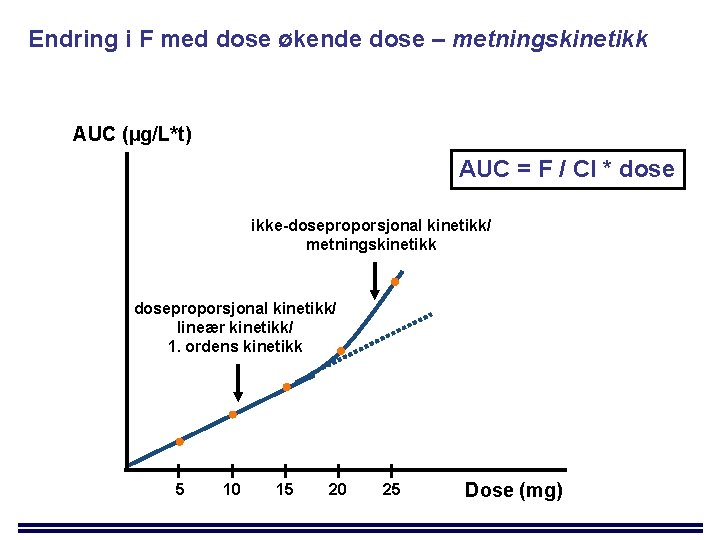
Endring i F med dose økende dose – metningskinetikk AUC (µg/L*t) AUC = F / Cl * dose ikke-doseproporsjonal kinetikk/ metningskinetikk doseproporsjonal kinetikk/ lineær kinetikk/ 1. ordens kinetikk 5 10 15 20 25 Dose (mg)

Metningskinetikk: eks. atorvastatin (Lipitor®) AUC Dose (mg) T 1/2 ≈ lik i hele doseområdet Clin Pharmacol Ther 1996; 60: 687 -95

Absorpsjonsinteraksjoner Kompleksbinding Endret p. H Hemming/induksjon av transportproteiner (eks. P-glykoprotein)
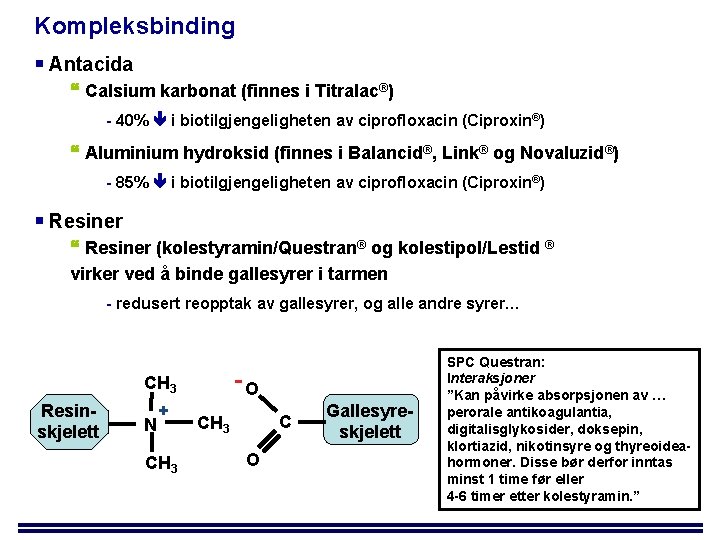
Kompleksbinding Antacida Calsium karbonat (finnes i Titralac®) - 40% i biotilgjengeligheten av ciprofloxacin (Ciproxin®) Aluminium hydroksid (finnes i Balancid®, Link® og Novaluzid®) - 85% i biotilgjengeligheten av ciprofloxacin (Ciproxin®) Resiner (kolestyramin/Questran® og kolestipol/Lestid ® virker ved å binde gallesyrer i tarmen - redusert reopptak av gallesyrer, og alle andre syrer… -O CH 3 Resinskjelett N + CH 3 C CH 3 O Gallesyreskjelett SPC Questran: Interaksjoner ”Kan påvirke absorpsjonen av … perorale antikoagulantia, digitalisglykosider, doksepin, klortiazid, nikotinsyre og thyreoideahormoner. Disse bør derfor inntas minst 1 time før eller 4 -6 timer etter kolestyramin. ”

Endret p. H H 2 -antagonister og syrepumpehemmere Redusert absorpsjon av legemidler gitt som uladet base BH+ H+ + B Ketokonazol AUC Cmax Monoterapi 37, 1 8, 2 Kombinert med ranitidin (ad p. H 6) 1, 6 0, 6 J Pharm Sci 1997; 86: 269 -282
Hemming/induksjon av P-glykoprotein Svært mange legemidler er P-glykoprotein-substrater - kombinasjon med stoffer som hemmer/induserer kan i betydelig grad endre absorpsjonen “P-glykoprotein - en pumpe av betydning for legemiddelrespons”: Tidsskr Nor Lægeforen 2004; 124: 2921 -3

Matinntak påvirker p. H ( ) magetømningshastigheten ( ) blodforsyning til tarmen ( ) galleutskillelsen ( ) Mulig endring av - absorpsjonshastighet (Cmax/Tmax) - absorpsjonsgrad (F/AUC) [type mat og timing]

Mat og fenoksymetylpenicillin (FP) Espen Molden 1 tablett morgen 1 tablett middag 2 tabletter kveld TAS 1 TIME FØR ELLER 2 TIMER ETTER MÅLTID Dr. O. Hansen V. nr. 159822 1 2 Acta Pharmacol Toxicol 1981: 49; 301 -4: Best absorpsjon med minst 2 timers faste før inntak av FP når mat heller ikke ble gitt innen 1 time etter inntak av FP ”Når inntak av FP ble gjort sammen med mat ble plasma- konsentrasjonen redusert til en viss grad”
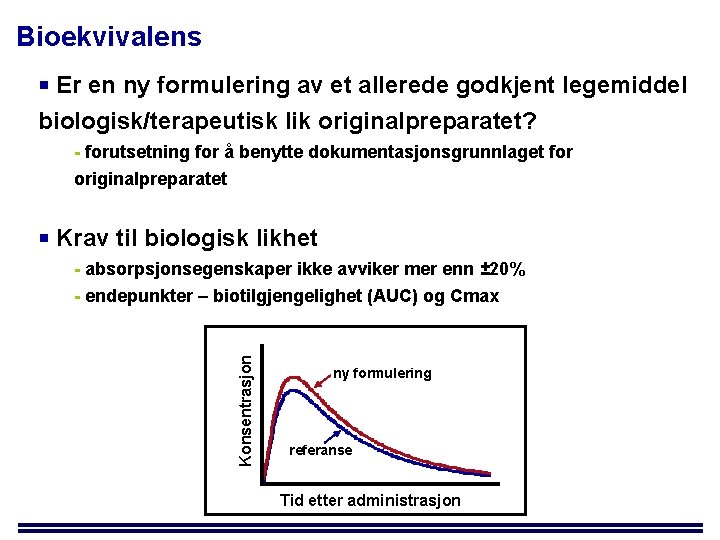
Bioekvivalens Er en ny formulering av et allerede godkjent legemiddel biologisk/terapeutisk lik originalpreparatet? - forutsetning for å benytte dokumentasjonsgrunnlaget for originalpreparatet Krav til biologisk likhet Konsentrasjon - absorpsjonsegenskaper ikke avviker mer enn ± 20% - endepunkter – biotilgjengelighet (AUC) og Cmax ny formulering referanse Tid etter administrasjon
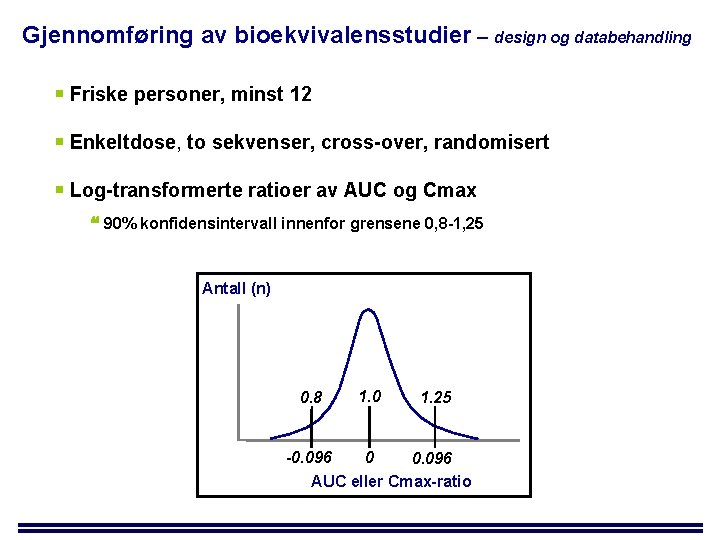
Gjennomføring av bioekvivalensstudier – design og databehandling Friske personer, minst 12 Enkeltdose, to sekvenser, cross-over, randomisert Log-transformerte ratioer av AUC og Cmax 90% konfidensintervall innenfor grensene 0, 8 -1, 25 Antall (n) 0. 8 1. 0 1. 25 -0. 096 0 0. 096 AUC eller Cmax-ratio

Bioekvivalens i en populasjon betyr nødvendigvis ikke individuell bioekvivalens
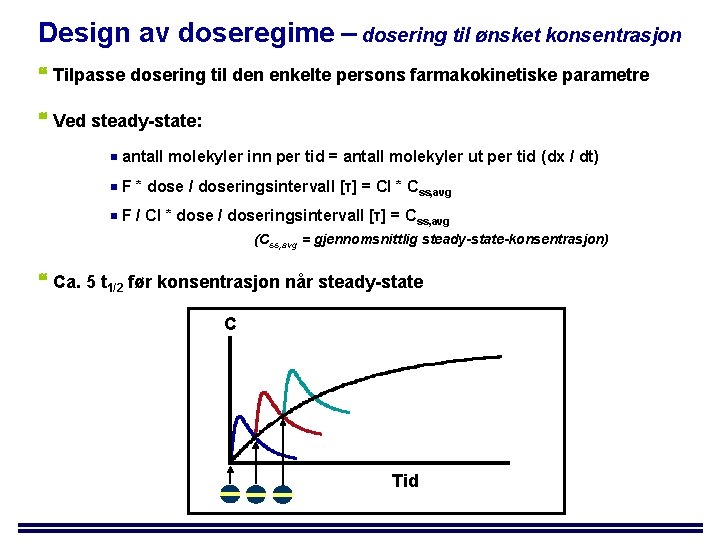
Design av doseregime – dosering til ønsket konsentrasjon Tilpasse dosering til den enkelte persons farmakokinetiske parametre Ved steady-state: antall molekyler inn per tid = antall molekyler ut per tid (dx / dt) F * dose / doseringsintervall [τ] = Cl * Css, avg F / Cl * dose / doseringsintervall [τ] = Css, avg (Css, avg = gjennomsnittlig steady-state-konsentrasjon) Ca. 5 t 1/2 før konsentrasjon når steady-state C Tid
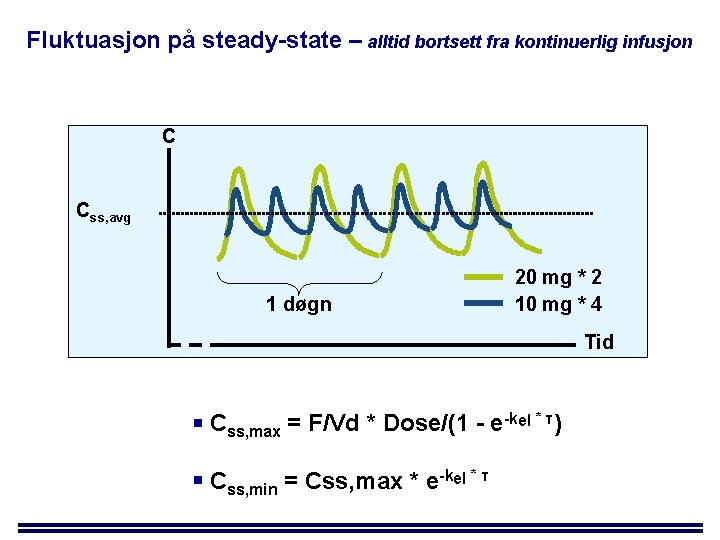
Fluktuasjon på steady-state – alltid bortsett fra kontinuerlig infusjon C Css, avg 1 døgn 20 mg * 2 10 mg * 4 Tid Css, max = F/Vd * Dose/(1 - e-kel * τ) Css, min = Css, max * e-kel * τ

Utledning av max/min-uttrykk ved steady-state Ved steady-state, så er per definisjon den mengden som forsvinner ut i løpet av et doseringsintervall den samme som den tilførte/systemisk tilgjengelige dosen ved hvert doseringstidspunkt: [1]. F * Dose = Ass, max - Ass, min (A = mengde = C * Vd) Høyre siden er altså et uttrykk for den mengden som forsvinner ut i løpet av doseringsintervallet. Dette blir riktignok bare helt korrekt ved intravenøs administrasjon, der vi får Ass, max umiddelbart etter administrasjon. Ved peroral administrasjon kommer Ass, max en stund etter administrasjon, hvilket innebærer at vi allerede har hatt eliminasjon for vi "når toppen på kurven" (feilen blir større jo lengre Tmax legemidlet har). Vi omskriver det som står på høyre siden litt; Ass, min kan nemlig uttrykkes som: [2]. Ass, max * e-kel * tau (tau/τ=doseringsintervallet) Da får vi nytt uttrykk (F * Dose = Ass, max - Ass, max *e-kel * tau) som vi går videre med: [3]. F * Dose = Ass, max * (1 - e-kel * tau) Vi lar så Ass, max stå alene på høyre side og får: F * Dose/(1 - e-kel * tau) = Ass, max. Til slutt deler vi på Vd på begge sider, hvilket betyr at vi får Css, max på høyre side: [4]. F/Vd * Dose/(1 - e-kel * tau) = Css, max …vi har fått et uttrykk for Css, max ; -) Uttrykket for Css, min har vi egentlig allerede etablert i [2]: [5]. Css, min = Css, max * e-kel * tau
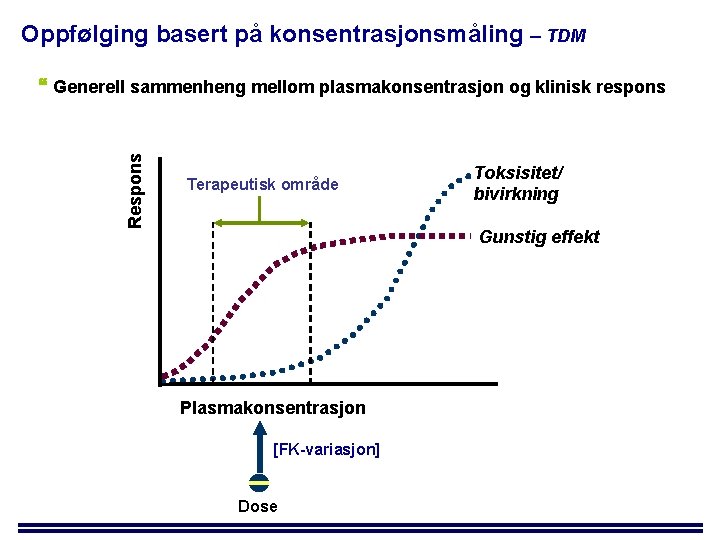
Oppfølging basert på konsentrasjonsmåling – TDM Respons Generell sammenheng mellom plasmakonsentrasjon og klinisk respons Terapeutisk område Toksisitet/ bivirkning Gunstig effekt Plasmakonsentrasjon [FK-variasjon] Dose

TDM Gir mulighet for å tilpasse dose ut i fra konsentrasjonsmåling + avdekke non-compliance Sammenligner måling med et terapeutisk område/referanseområde områder basert på konsentrasjoner rett før neste dose (”trough”/bunn) ved steady-state Legemidler med smalt-terapeutisk vindu eks. teofyllin, digitalisglykosider Begrense bivirkninger/terapisvikt ved lengre tids behandling eks. psykiatri, epilepsi
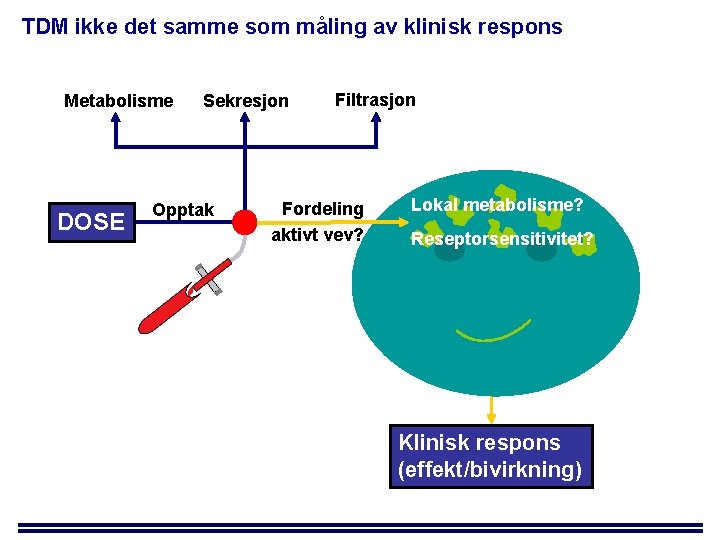
TDM ikke det samme som måling av klinisk respons Metabolisme DOSE Sekresjon Opptak Filtrasjon Fordeling aktivt vev? Lokal metabolisme? Reseptorsensitivitet? Klinisk respons (effekt/bivirkning)
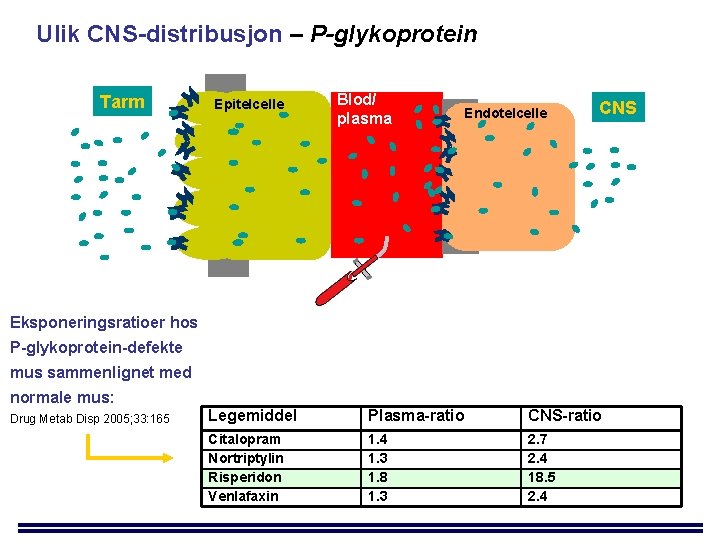
Ulik CNS-distribusjon – P-glykoprotein Tarm Epitelcelle Blod/ plasma Endotelcelle CNS Eksponeringsratioer hos P-glykoprotein-defekte mus sammenlignet med normale mus: Drug Metab Disp 2005; 33: 165 Legemiddel Plasma-ratio CNS-ratio Citalopram Nortriptylin Risperidon Venlafaxin 1. 4 1. 3 1. 8 1. 3 2. 7 2. 4 18. 5 2. 4

Oppsummering Farmakokinetikk – essensielt i optimalisering av farmakoterapi Forebygge/håndtere ugunstige interaksjoner Tilpasse dose til den enkelte pasient
- Slides: 55