FRA DE FRSTE ELEKTROKJEMISKE CELLENE TIL DAGENS BATTERIER

FRA DE FØRSTE ELEKTROKJEMISKE CELLENE TIL DAGENS BATTERIER

• Det første batteriet som er kjent er fra ca. 250 f. Kr. Batteriet besto av en jerntråd inne i en sylinder av kobber. Denne ble fylt med eddik, og man tror strømmen fra det ble brukt til forsølving.

Fra ”vår” tid: • 1791: Galvani oppdaget ”animalsk” strøm. • 1800: Volta demonstrerte sitt batteri for Napoleon i Paris. • 1836: Daniell oppfant Cu-Zn-elementet. • 1839: Grove lagde den første brenselcella. • 1859: Planté fant opp blybatteriet. • 1868: Leclanché fant opp sitt element (tørrelementet).

• 1899: Svensken Jungner oppdaget Ni-Cdelemnet. • 1965: Det første alkaliske batteriet. • 1972: de første Li-batteriene ble laget. • 1990: Ni-MH-batteriene ble kommersielle. • 1991: Li-ionbatteriene ble kommersielle.

HVA SKAL TIL FOR Å LAGE ET BATTERI? • Vi trenger to forkjellige elektroder og et medium som leder elektrisk strøm. • Elektrodene var i starten to ulike metaller, men kan i dag være ”mye rart”.
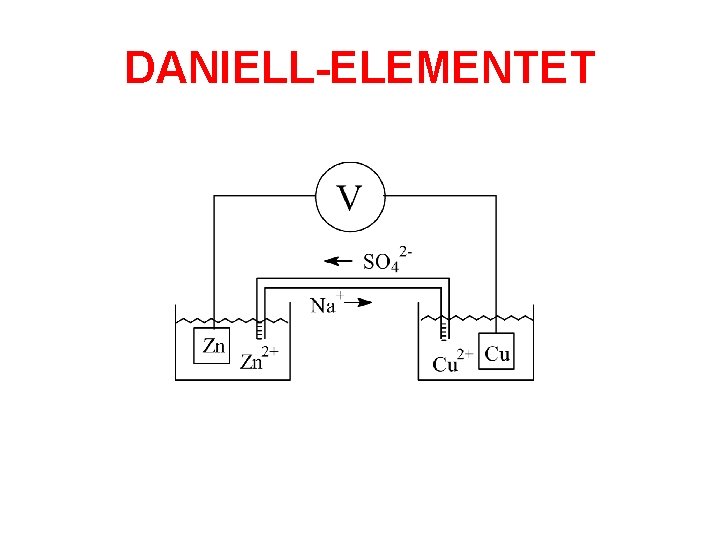
DANIELL-ELEMENTET

NOEN VIKTIGE BEGREPER: • ANODE: Den polen der det skjer • en OKSIDASJON. • KATODE: Den polen der det skjer • en REDUKSJON. • I et batteri er KATODEN POSITIV POL og ANODEN NEGATIV POL.

HVA SKJER KJEMISK I CELLA? • • Zn → Zn 2+ + 2 e- (oks) Cu 2+ + 2 e- → Cu (red) Totalreaksjon: Zn + Cu 2+ → Zn 2+ + Cu • SALTBRUA skal sørge for at elektrolyttene holder nøytral ladning

SPENNINGSREKKA • Spenningsrekka er plassert etter rekkefølgen av reduksjonspotensialene i forhold til en standard hydrogenelektrode med spenningnen 0. 00 V per def.
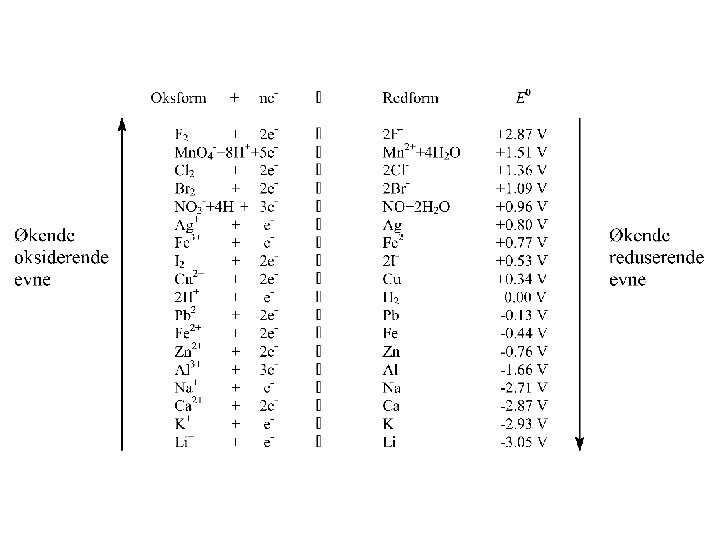

BETINGELSER FOR Å FÅ REAKSJON I MELLOM TO STOFF I SPENNINGSREKKA • 1) Det ene stoffet står på oksform og det andre står på redform • 2) Oksformen står over redformen i spenningsrekka

• I Daniellelementet er halvreaksjonene • Cu 2+ + 2 e- → Cu, E 0 red = +0. 34 V Zn 2+ + 2 e- → Zn, E 0 red = 0. 76 V • Den siste reaksjonen snus: • Cu 2+ + 2 e- → Cu, E 0 red = +0. 34 V • Zn → Zn 2+ + 2 e- , E 0 oks = +0. 76 V • Totalreaksjon: Zn + Cu 2+ → Cu + Zn 2+

• I en elektrokjemisk celle er standard cellepotensial E 0 gitt ved E 0 = E 0 red + E 0 oks • Her: E 0 = (0. 34 + 0. 76) V = 1. 10 V

NERNSTS LIKNING • Standardtilstanden er definert ved 1 atm trykk, 25 o. C og 1 M konsentrasjon på elektrolyttene. • Cellepotensialet E må korrigeres ved Nernsts likning Dersom vi ikke har standardtilstanden i cella.

• E er cellepotensialet • E 0 standard cellepotensial • n er antall elektroner som overføres i totalreaksjonen • Q er reaksjonskvotienten for totalreaksjonen
![• Hva blir spenningen i et Daniellelement dersom [Cu 2+] = 0. 050 • Hva blir spenningen i et Daniellelement dersom [Cu 2+] = 0. 050](http://slidetodoc.com/presentation_image_h2/a936deb480fe8e0b5e9b4a6b417039af/image-16.jpg)
• Hva blir spenningen i et Daniellelement dersom [Cu 2+] = 0. 050 M og [Zn 2+] = 2. 5 M?

BATTERIER – NOEN BEGREPER • Kapasitet: Et mål for energimengden som er lagret i batteriet. Måles i Ah eller m. Ah. • Ladning: Produktet av strømstyrke og tid. Kapasiteten er derfor et mål for hvor stor ladningen i batteriet er. • 1 Coulomb (C) = 1 As • Faradays konstant F: 96500 C/mol, som betyr at 1 mol e- gir en ladning på 96500 C.

• Energitettheten til et batteri er energien batteriet kan levere per masseenhet av batteriet. Den måles gjerne i k. Wh/kg. • Et lett batteri som gir fra seg samme energimengde som et tungt batteri har derfor mye større energitetthet.

ALKALISKE BATTERIER • Anode: Zn Katode: Mn. O 2 (brunstein) Elektrolytt: KOH • Kapasiteten er avhengig av hvor mye strøm batteriet skal levere. Mye energi går tapt som varme dersom strømmen skal være høy. • Batteriet er ikke oppladbart!
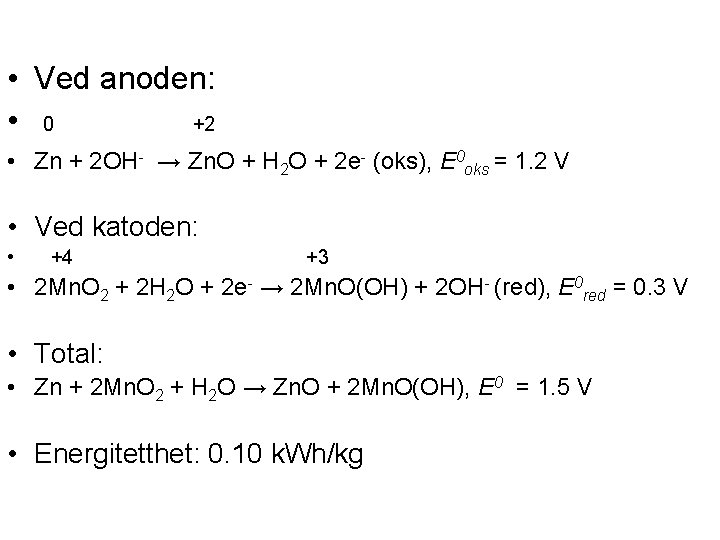
• Ved anoden: • 0 +2 • Zn + 2 OH- → Zn. O + H 2 O + 2 e- (oks), E 0 oks = 1. 2 V • Ved katoden: • +4 +3 • 2 Mn. O 2 + 2 H 2 O + 2 e- → 2 Mn. O(OH) + 2 OH- (red), E 0 red = 0. 3 V • Total: • Zn + 2 Mn. O 2 + H 2 O → Zn. O + 2 Mn. O(OH), E 0 = 1. 5 V • Energitetthet: 0. 10 k. Wh/kg

BLYBATTERIET • Anode: Pb Katode: Pb. O 2 Elektrolytt: Ca 5 M H 2 SO 4 Energitetthet: 0. 03 k. Wh/kg

• Ved katoden: • +4 +2 • Pb. O 2(s) + SO 42 -(aq) + 4 H+(aq) + 2 e- → Pb. SO 4(s) + 2 H 2 O(l) (red) , • E 0 red = 0. 36 V • Ved anoden: • 0 +2 • Pb(s) + SO 42 -(aq) → Pb. SO 4(s) + 2 e- (oks), E 0 oks = 1. 69 V • Total: Pb. O 2(s) + Pb(s) + 2 SO 42 -(aq) → 2 Pb. SO 4(s) + 2 H 2 O(l), • E 0 = 2. 05 V

• Ved overlading vil det bli vannspalting til hydrogen og oksygen i batteriet! • Derfor må batteriet etterfylles med vann. • Ved ladingen vil noe blysulfat løsne fra elektrodene og falle ned som bunnfall. Dette fører til at [H 2 SO 4] minker, og massetettheten minker. Vi kan derfor måle batteriets tilstand ved å måle tettheten av svovelsyra.

Ni. Cd-BATTERIET • Anode: Ni. O(OH) Katode: Cd Elektrolytt: KOH(aq) Energitetthet: 0. 04 k. Wh/kg

• Ved katoden: • +3 +2 • Ni. O(OH)(s) + H 2 O(l) + e-→ Ni(OH)2(s) + OH- (red), E 0 red = 0. 49 V • • Ved anoden: • 0 +2 • Cd(s) + 2 OH- → Cd(OH)2(s) + 2 e- (oks), E 0 oks = 0. 71 V • Totalreaksjon: • 2 Ni. O(OH)(s) + 2 H 2 O(l) + Cd(s) → 2 Ni(OH)2(s) + Cd(OH)2(s), • E 0 = 1. 2 V

• • • Fordeler: Rask lading Lang levetid – tåler mer enn 1000 oppladinger Kan lagres i 5 år uten å ødelegges Fungerer bra i lave temperaturer Billig • Ulemper: • Relativ lav energitetthet • Har memoryeffekt – må derfor utlades / opplades fullstendig en gang imellom • Miljømessig meget giftig • Har relativt høy egenutlading – må lades opp dersom det ikke er brukt på en tid

Ni. MH-BATTERIET • Anode: Ni. O(OH) Katode: H absorbert i en metallegering Elektrolytt: KOH(aq) Energitetthet: 0. 08 k. Wh/kg

• Ved katoden: • +3 +2 • Ni. O(OH)(s) + H 2 O(l) + e-→ Ni(OH)2(s) + OH- (red), E 0 red = 0. 49 V • • Ved anoden: • 0 +1 • MH + OH- → M + H 2 O(l) + e- (oks), E 0 oks = 0. 83 V • Totalreaksjon: • 2 Ni. O(OH)(s) + MH → 2 Ni(OH)2(s) + M • E 0 = 1. 32 V

• • Fordeler: 30 -40% høyere kapasitet enn Ni. Cd-batteriet Mindre ”memoryeffekt” enn Ni. Cd-batteriet Lite giftig miljømessig • Ulemper: • Ikke så lang levetid som Ni. Cd-batteriet – starter å degradere allerede etter 3 -400 oppladinger • Vanskeligere å lade opp – lengre ladetid enn Ni. Cd og må ikke overlades. • 50 % høyere egenutlading enn Ni. Cd • Krever full utlading for å hindre krystalldannelse i batteriet

LITIUM-ION-BATTERIET • Anode: Li. Co. O 2 Katode: C Elektrolytt: Et litiumsalt, f. eks. Li. BH 4 eller Li. PF 6. Energitetthet: 0. 16 k. Wh/kg
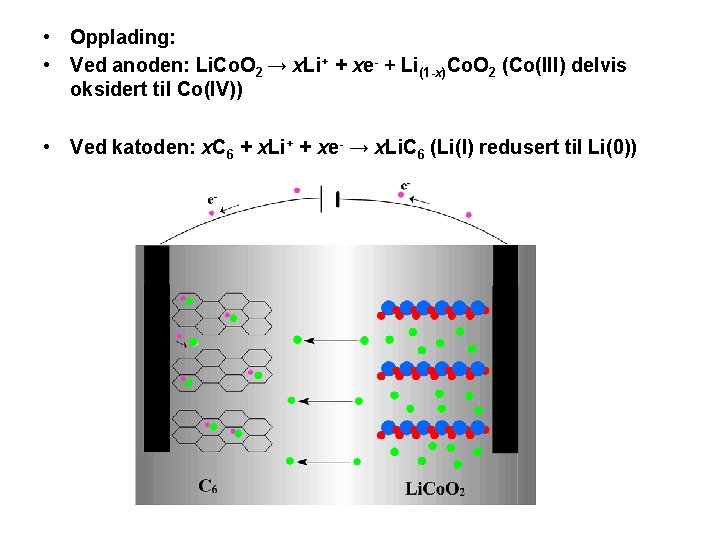
• Opplading: • Ved anoden: Li. Co. O 2 → x. Li+ + xe- + Li(1 -x)Co. O 2 (Co(III) delvis oksidert til Co(IV)) • Ved katoden: x. C 6 + x. Li+ + xe- → x. Li. C 6 (Li(I) redusert til Li(0))

• Fordeler: • Høy energitetthet pga høy spenning (> 3. 0 V) og lav vekt på batteriet • Ganske lav selvutlading – under halvparten av nikkelbatteriene • Ingen memoryeffekt – lite vedlikehold – trenger ikke å lades ut en gang imellom • Kan gi svært høy strømstyrke til spesielle instrumenter • • • Ulemper: Må ikke utlades fullstendig! Mange batterier er ødelagte etter 2 -3 år Bør lagres kjølig med ca. 40 % effekt på batteriet Kostbart, ca. 40 % dyrere enn Ni. Cd

LITIUM-POLYMER-BATTERIET • Anode: Li. Co. O 2 Katode: C Elektrolytt: Fast polymer tilsatt litt gelelektrolytt Energitetthet: 0, 13 – 0, 20 k. Wh/kg Brukes særlig som små batterier – kredittkort og liknende

BRENSELCELLA • En brenselcelle har svært høy virkningsgrad • Lite energi går tapt som varme • Andre brennstoffer enn hydrogen kan brukes
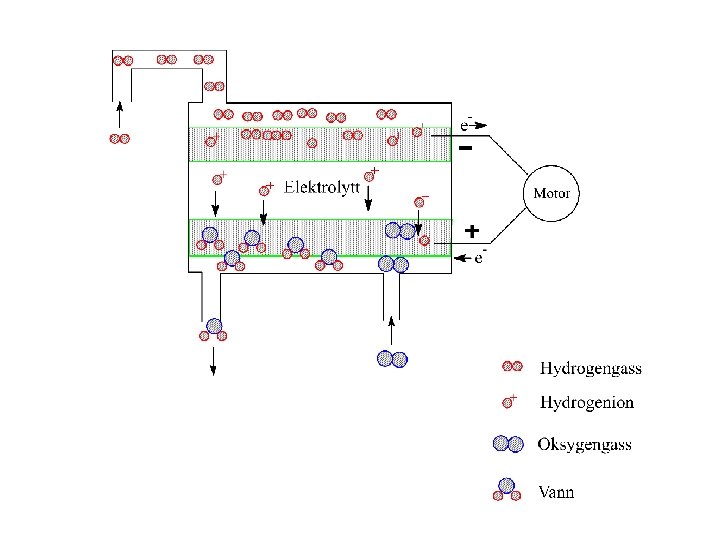

• Ved anoden: 2 H 2(g) → 4 H+(aq) + 4 e- (oks), E 0 oks = 0. 00 V • Ved katoden: O 2(g) + 4 H+(aq) + 4 e- → 2 H 2 O(l) (red), E 0 red = 1. 23 V • Totalreaksjon: 2 H 2(g) + O 2(g) → 2 H 2 O(l), E 0 = 1. 23 V

ELEKTROLYSE • I en elektrolyse tvinger vi strømmen til å gå i motsatt retning i hva den naturlig ville ha gjort. • Men dette koster mye energi! • Vi må minst ha en spenning som er større enn det naturlige cellepotensialet for cella. • Opplading av batterier er egentlig en form for elektrolyse.

• Spenningsrekka forteller oss også hvilke produkter som lages i en elektrolyse. • Jo lengre opp et stoff står på redform i spenningsrekka, desto vanskeligere er det å oksidere det. • Jo lengre ned et stoff står på oksform i spenningsrekka, desto vanskeligere er det å redusere det. • Dette er spesielt viktig når det er vann til stede i elektrolysen.
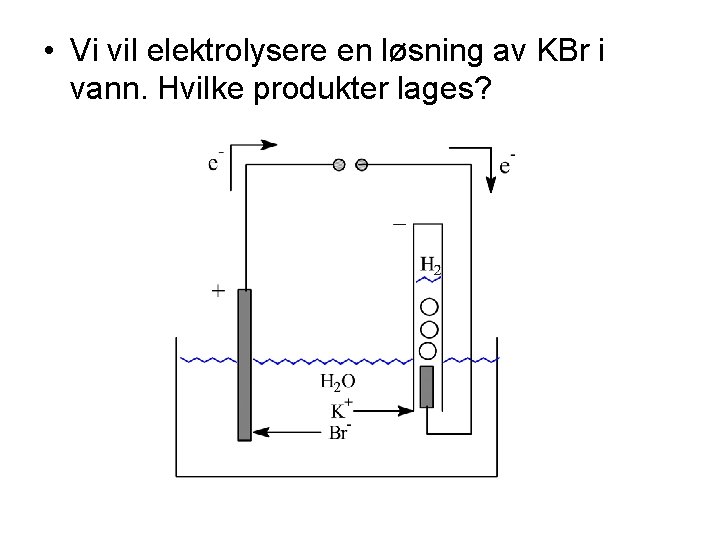
• Vi vil elektrolysere en løsning av KBr i vann. Hvilke produkter lages?

• Oksform Redform • 4 H+(aq) + 4 e- + O 2(g) 2 H 2 O(l) • Br 2(aq) + 2 e- 2 Br-(aq) • 2 H 2 O(l)+ 2 e- H 2(g) + 2 OH-(aq) • K+(aq) + e- K(s)

• Vi får altså Br 2 ved anoden og H 2 ved katoden. • Dersom vi elektrolyserer en K 2 SO 4 løsning, har vi følgende muligheter i spenningsrekka:

• Oksform • 2 S 2 O 82 - + 2 e- Redform 2 SO 42 - • 4 H+(aq) + 4 e- + O 2(g) 2 H 2 O(l) • 2 H 2 O(l)+ 2 e- H 2(g) + 2 OH-(aq) • K+(aq) + e- K(s)

• Produktene blir nå H 2 og O 2, altså en vannspalting. • 2 H 2 O(l) → 2 H 2(g) + O 2(g)

OVERPOTENSIAL • Hvor høy spenning må vi minst ha for å elektrolysere en Zn. SO 4 -løsning? • Vi tenker oss en elektrokjemisk celle som består av to elektroder av Zn og Pt dyppet ned i en 1 M Zn. SO 4 -løsning, og beregner et standardpotensial på + 1. 99 V.

• • • 2 Zn → 2 Zn 2+ + 4 e- (oks), E 0 oks = +0, 76 V O 2 + 4 H+ + 4 e- → 2 H 2 O (red), E 0 red = +1. 23 V Totalreaksjonen er 2 Zn + O 2 + 4 H+ → 2 Zn 2+ + 2 H 2 O , E 0 = (0. 76 + 1. 23) V = 1. 99 V • Skal vi få reaksjonen til å gå i motsatt retning ved en elektrolyse, trenger vi altså minst en spenning på 1. 99 V som skal overvinne det naturlige cellepotensialet.

• Men det viser seg at dette ikke er nok. Bl. a. det at oksygengass adsorberes på Ptelektroden, gjør at det lages en ekstra motspenning til elektrolysen på ca. 0. 5 V. • Denne motspenningen kalles overpotensialet, og gjør at halvreaksjonen • O 2 + 4 H+ + 4 e- → 2 H 2 O (red), E 0 red = +1. 23 V • får spenningen +1. 73 V istedet.

• Den vil da komme over halvreaksjonen • Cl 2(aq) + 2 e- 2 Cl-(aq), E 0 red = +1. 36 V • Dersom vi nå elektrolyserer en løsning av Zn. Cl 2 i vann, får vi laget klorgass og ikke oksygen ved anoden.
- Slides: 47