Foszfor phosphorum fnyhordoz Az elemet elszr Henning Brandt

Foszfor phosphorum = “fényhordozó”

Az elemet először Henning Brandt alkimista állította elő 1669 -ben, úgy hogy először napokig vizeletet desztillált, és a lombikban maradt anyagot vörösizzásig hevítette. A lombik és a belőle távozó gáz sötétben is világított, láng nélkül. A világító anyagot „hideg tűz”-nek nevezte el. A foszfor szó a görög phosphoros, fényt hordozó szóból származik. A foszfor egyedülálló az elemek között azzal, hogy először fedezték fel állati/emberi testnedvben, majd utána a növény- és az ásványvilágban, valamint az első elem, melynek ismerjük felfedezőjét.

• Allotróp módosulatai: • fehérfoszfor: • viasz keménységű, késsel vágható, erősen mérgező anyag, • szobahőmérsékleten is hevesen oxidálódik, öngyúlékony. • Víz alatt kell tartani, oxigéntől elzárva. • Zsírokban, olajokban jól oldódik, ezért nem tanácsos szabad kézzel hozzányúlni, mivel a bőrőn zsír található. • Lenyelve már 0, 05 g is halálos belőle. Át tud alakulni vörösfoszforrá.

• vörösfoszfor: sötétvörös színű por, nem oldódik semmiben, így nem is mérgező, levegőn tartható • Gyulladási hőmérsékletek • fehérfoszfor 60 °C • vörösfoszfor 400 °C • Kémiai tulajdonságai • A két foszfor kémiailag azonos módon viselkedik. A foszfor égésekor foszforpentaoxid keletkezik.

Miért különbözik a két allotróp módosulat? Fehérfoszfor 4 atomos molekulákból áll, kristályszerkezete molekularács (kicsi a molekulák közötti összetartó erő). Képlete P 4
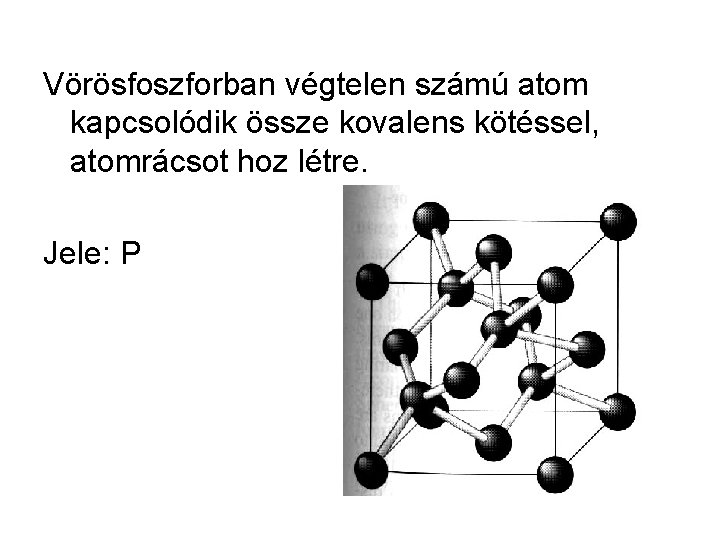
Vörösfoszforban végtelen számú atom kapcsolódik össze kovalens kötéssel, atomrácsot hoz létre. Jele: P

• Előfordulása csak vegyületekben (pl. guanoban) • Az emberi szervezetben nagy mennyiségben található (700 -800 g/felnőtt). Szükséges a csontok, fogak felépüléséhez, az idegrendszer működéséhez, a fehérje-, szénhidrát-, zsíranyagcseréhez, a fehérjeszintézishez és az enzimek működéséhez. • Felhasználása Irinyi János a vörösfoszfort a mai biztonsági gyufa elődjéhez használta.

Irinyi János, a gyufa feltalálója: Ki volt ő? Nézz utána!
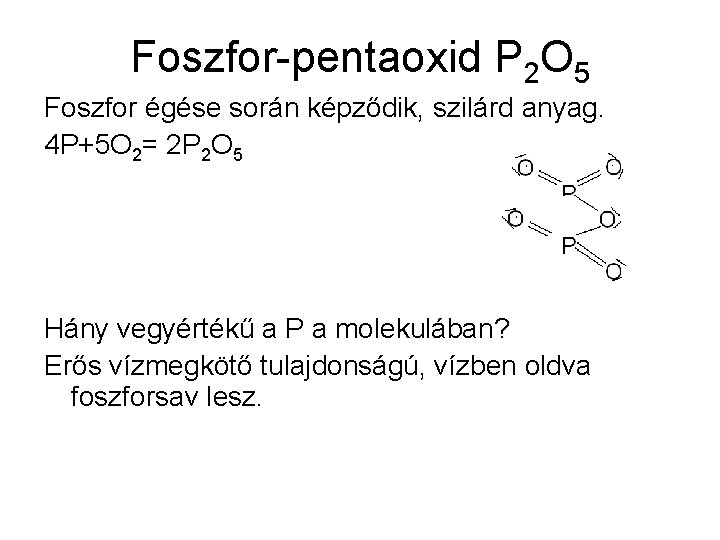
Foszfor-pentaoxid P 2 O 5 Foszfor égése során képződik, szilárd anyag. 4 P+5 O 2= 2 P 2 O 5 Hány vegyértékű a P a molekulában? Erős vízmegkötő tulajdonságú, vízben oldva foszforsav lesz.
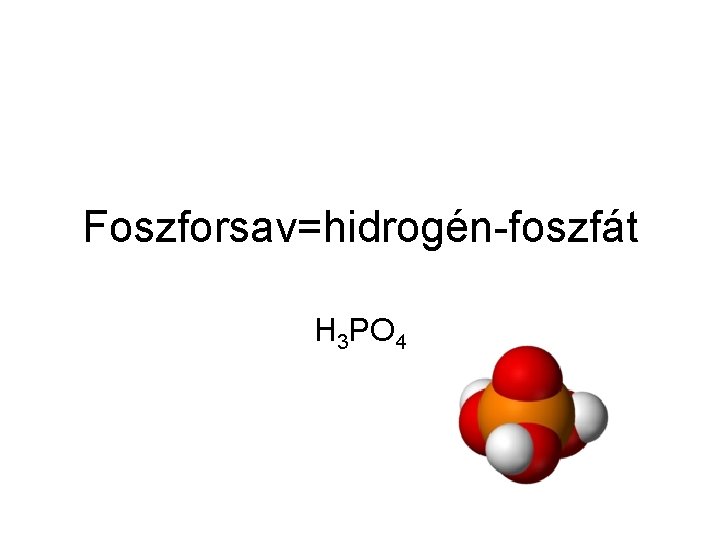
Foszforsav=hidrogén-foszfát H 3 PO 4

Előállítása: 1. Foszfor oxidációja 4 P + 5 O 2 = 2 P 2 O 5 foszfor-pentaoxid 2. Az oxidot vízben oldják P 2 O 5 +3 H 2 O = 2 H 3 PO 4 Savmaradék ion: foszfát ion PO 4 3 -

Felhasználása: Híg vizes oldata fogyasztásra alkalmas: pl. Cola, üdítő italok. Hatásuk: a fogakat, csontokat roncsolja, „kalciumrabló”. Vízkőoldószerként háztartásban. Műtrágya gyártás - szuperfoszfát Mosószerek gyártása-vízlágyító, de az élővizek elalgásodnak.

Sói a foszfátok • Ca 3 (PO 4)2 kalcium-foszfát, szuperfoszfát műtrágya • Na 3 PO 4 nátrium-foszfát, trisó Zsíróldó, fémtisztító, vízlágyító
- Slides: 13