Fosfor Poloha v periodick tabulce V A skupina

Fosfor
Poloha v periodické tabulce V. A skupina (skupina dusíku)
![Elektronová konfigurace a možná oxidační čísla n [Ne] 3 s 2 3 p 3 Elektronová konfigurace a možná oxidační čísla n [Ne] 3 s 2 3 p 3](http://slidetodoc.com/presentation_image_h/74e6847dac2495019fa4b554235c69fd/image-3.jpg)
Elektronová konfigurace a možná oxidační čísla n [Ne] 3 s 2 3 p 3 n Oxidační čísla: -III, I, III, IV, V

Výskyt n n V přírodě - pouze ve sloučeninách n Soli kyseliny fosforečné Biogenní prvek n Získává se z: n Apatit Ca 3(PO 4)2. Ca. X 2 kde X=F, Cl n Fosforit Ca 3(PO 4)2. Ca(OH)2 – stavba kostí, zubů, různých bílkovin a DNA

Apatit Ca 3(PO 4)2. Ca. X 2 kde X=F, Cl Fosforit Ca 3(PO 4)2. Ca(OH)2

Vlastnosti n n Nekov V přírodě pouze sloučeniny – P+5, ale i P-3, P+3 a P+4

Bílý fosfor Tvořen molekulami P 4 -> vysoká reaktivita n Měkký, nažloutlý, jedovatý, na vzduchu samovznětlivý, ve tmě páry fosforeskují (dochází k oxidaci par vzdušným kyslíkem, při které vydává světlo), uchovávání pod vodou, nerozpustný ve vodě, rozpustný v sirouhlíku, velmi reaktivní

Červený fosfor Vzniká zahříváním bílého fosforu na 250°C (tato změna probíhá i za normálních podmínek, ale pomalu) § Na vzduchu stálý, není rozpustný v rozpouštědlech, není jedovatý, s většinou prvků reaguje za vyšších teplot

Světle červený fosfor Vzniká varem bílého P s PBr 3 n Rozpustný v roztocích hydroxidů, má vrstevnatou strukturu, výskyt ve čtyřech modifikacích (např. fialový P)

Černý fosfor Vzniká zahříváním červeného P pod tlakem za teploty přes 400°C nebo zahříváním bílého P za teploty 200°C n Velmi stálý, připomíná spíše kovy fyzikálními vlastnostmi, má kovový lesk, dobrý vodič, ze všech modifikací fosforu nejstálejší

Příprava Redukce kysličníku fosforečného P 2 O 5 uhlím za vysoké teploty: P 2 O 5 + 5 CO + 2 P

Výroba 2 Ca 3(PO 4)2 + 6 Si. O 2 + 10 C P 4 + 6 Ca. Si. O 3 + 10 CO Pelletierova metoda – dnes téměř nepoužívané 1) Ca 3(PO 4)2 + 2 H 2 SO 4 + 4 H 2 O 2 Ca. SO 4. 2 H 2 O + Ca(H 2 PO 4)2 2) 3 Ca(H 2 PO 4)2 + 10 C Ca 3(PO 4)2 + 10 CO + 4 P + 6 H 2 O
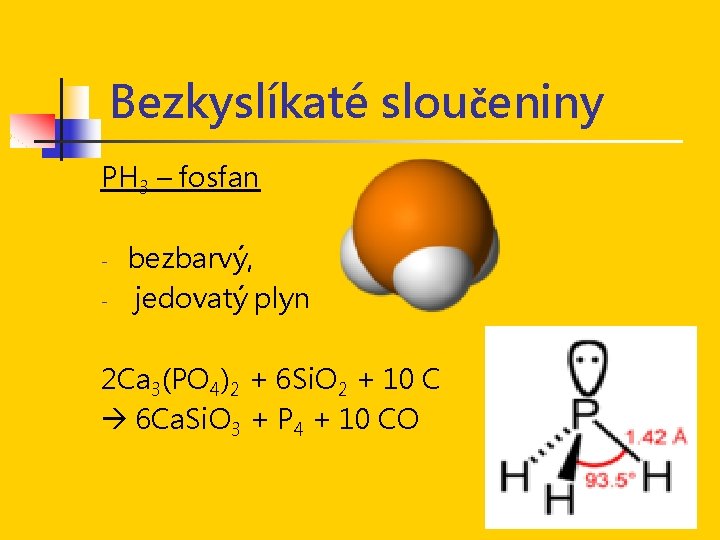
Bezkyslíkaté sloučeniny PH 3 – fosfan - bezbarvý, jedovatý plyn 2 Ca 3(PO 4)2 + 6 Si. O 2 + 10 C 6 Ca. Si. O 3 + P 4 + 10 CO
Kyslíkaté sloučeniny 1) OXIDY P 4 O 6 dimer-oxid fosforitý Bílá krystalická látka, vzniká nedokonalým spalováním fosforu P 4 O 10 dimer-oxid fosforečný Bílý, podobný sněhu, vzniká spalováním fosforu za přístupu vzduchu

2) KYSELINY H 3 PO 2 kyselina fosforná - jednosytná kyselina H 3 PO 3 kyselina trihydrogenfosforitá - dvojsytná kyselina HPO 3 kyselina fosforečná H 3 PO 4 kyselina trihydrogenfosforečná - středně silná kyselina, jedna ze základních surovin chemického průmyslu

3) SOLI KYSELINY TRIHYDROGENFOSFOREČNÉ KH 2 PO 4 dihydrogenfosforečnan draselný - hnojivo (NH 4)2 HPO 4 hydrogenfosforečnan amonný - hnojivo, impregnace tkanin Ca 3(PO 4)2 fosforečnan vápenatý - výroba hnojiv (superfosfátů)

Poznámky a zajímavosti Jeden z nejrozšířenějších minerálů v těle 85 % v kostech a zubech 15 % v měkkých tkáních a krvi
- Slides: 17