FORMULACIN Y NOMENCLATURA QUMICA INORGNICA FORMULACIN La frmula











- Slides: 27

FORMULACIÓN Y NOMENCLATURA QUÍMICA INORGÁNICA

FORMULACIÓN Ø La fórmula química expresa la composición y proporción de moléculas y compuestos de los compuestos químicos mediante símbolos químicos y subíndices Ø El Nº de compuestos químicos conocidos es superior a 13 millones!!!

SUSTANCIAS SIMPLES

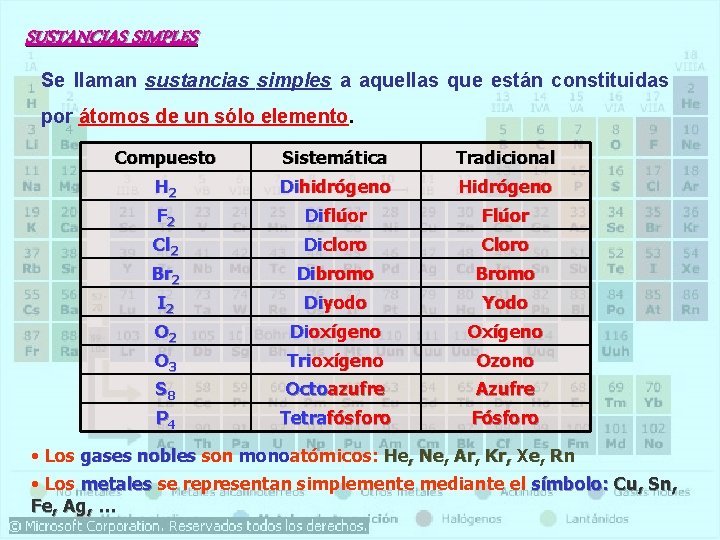
SUSTANCIAS SIMPLES Se llaman sustancias simples a aquellas que están constituidas por átomos de un sólo elemento. Compuesto Sistemática Tradicional H 2 Dihidrógeno Hidrógeno F 2 Diflúor Flúor Cl 2 Dicloro Cloro Br 2 Dibromo Bromo I 2 Diyodo Yodo O 2 Dioxígeno O 3 Trioxígeno Ozono S 8 Octoazufre Azufre P 4 Tetrafósforo Fósforo • Los gases nobles son monoatómicos: He, Ne, Ar, Kr, Xe, Rn • Los metales se representan simplemente mediante el símbolo: Cu, Sn, Fe, Ag, …

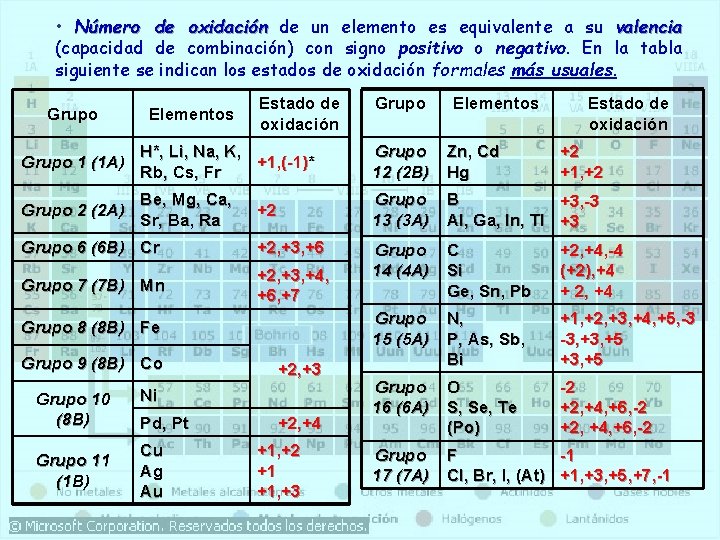
• Número de oxidación de un elemento es equivalente a su valencia (capacidad de combinación) con signo positivo o negativo. En la tabla siguiente se indican los estados de oxidación formales más usuales. Grupo Elementos Estado de oxidación Grupo 1 (1 A) H*, Li, Na, K, +1, (-1)* Rb, Cs, Fr Grupo 12 (2 B) Zn, Cd Hg Grupo 2 (2 A) Be, Mg, Ca, Sr, Ba, Ra Grupo 13 (3 A) B +3, -3 Al, Ga, In, Tl +3 Grupo 14 (4 A) C Si Ge, Sn, Pb +2, +4, -4 (+2), +4 + 2, +4 Grupo 15 (5 A) N, P, As, Sb, Bi +1, +2, +3, +4, +5, -3 -3, +5 +3, +5 Grupo 16 (6 A) O S, Se, Te (Po) -2 +2, +4, +6, -2 Grupo 17 (7 A) F -1 Cl, Br, I, (At) +1, +3, +5, +7, -1 +2 Grupo 6 (6 B) Cr +2, +3, +6 Grupo 7 (7 B) Mn +2, +3, +4, +6, +7 Grupo 8 (8 B) Fe Grupo 9 (8 B) Co Grupo 10 (8 B) Grupo 11 (1 B) +2, +3 Ni Pd, Pt Cu Ag Au +2, +4 +1, +2 +1 +1, +3 +2 +1, +2

COMPUESTOS BINARIOS

ÓXIDOS

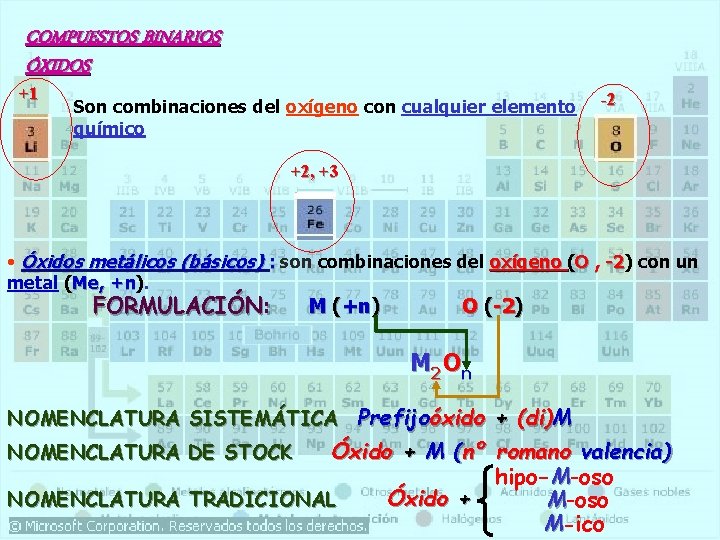
COMPUESTOS BINARIOS ÓXIDOS +1 Son combinaciones del oxígeno con cualquier elemento químico -2 +2, +3 • Óxidos metálicos (básicos) : son combinaciones del oxígeno (O , -2) -2 con un metal (Me, +n). +n FORMULACIÓN: M (+n) O (-2) M 2 On NOMENCLATURA SISTEMÁTICA Prefijoóxido + (di)M Óxido + M (nº romano valencia) hipo-M-oso NOMENCLATURA TRADICIONAL Óxido + M-oso M-ico NOMENCLATURA DE STOCK

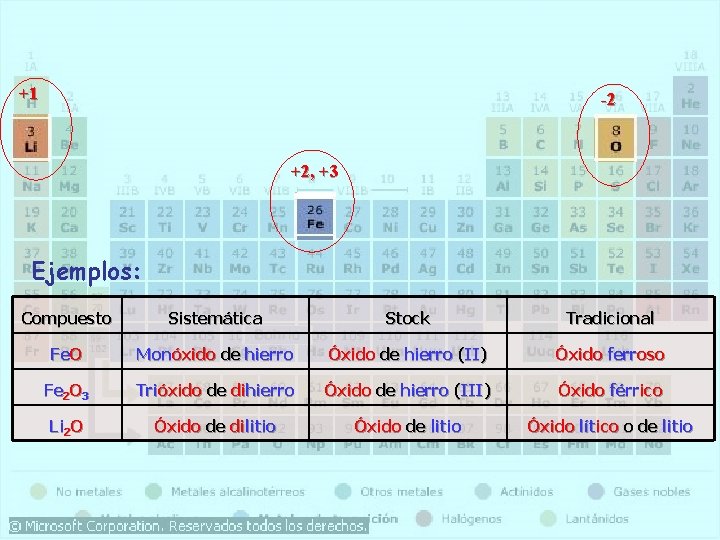
+1 -2 +2, +3 Ejemplos: Compuesto Sistemática Stock Tradicional Fe. O Monóxido de hierro Óxido de hierro (II) Óxido ferroso Fe 2 O 3 Trióxido de dihierro Óxido de hierro (III) Óxido férrico Li 2 O Óxido de dilitio Óxido de litio Óxido lítico o de litio

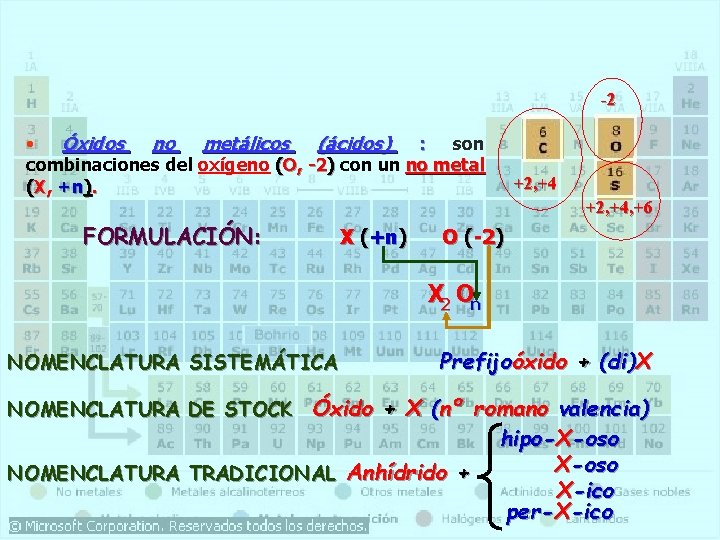
-2 • Óxidos no metálicos (ácidos) : son combinaciones del oxígeno (O, -2) con un no metal (X, +n). FORMULACIÓN: X (+n) +2, +4, +6 O (-2) X 2 On NOMENCLATURA SISTEMÁTICA Prefijoóxido + (di)X NOMENCLATURA DE STOCK Óxido + X (nº romano valencia) NOMENCLATURA TRADICIONAL Anhídrido + hipo-X-oso X-ico per-X-ico

-2 +2, +4, +6 Ejemplos: Compuesto Sistemática Stock Tradicional SO Monóxido de azufre Óxido de azufre (II) Anhídrido hiposulfuroso SO 2 Dióxido de azufre Óxido de azufre (IV) Anhídrido sulfuroso SO 3 Trióxido de azufre Óxido de azufre (VI) Anhídrido sulfúrico CO Monóxido de carbono Óxido de carbono (II) Anhídrido carbonoso CO 2 Dióxido de carbono Óxido de carbono (IV) Anhídrido carbónico

HIDRUROS

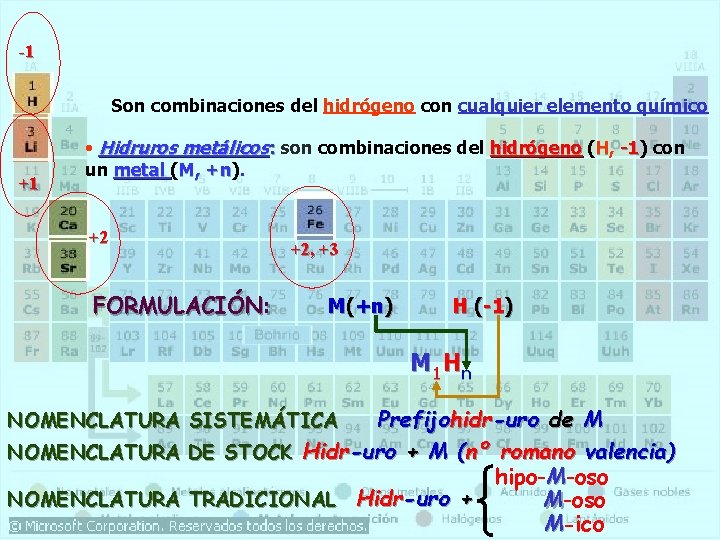
-1 Son combinaciones del hidrógeno con cualquier elemento químico +1 • Hidruros metálicos: son combinaciones del hidrógeno (H, -1) -1 con un metal (M, +n). +n +2 FORMULACIÓN: +2, +3 M(+n) H (-1) M 1 Hn Prefijohidr-uro de M NOMENCLATURA DE STOCK Hidr-uro + M (nº romano valencia) hipo-M-oso NOMENCLATURA TRADICIONAL Hidr-uro + M-oso M-ico NOMENCLATURA SISTEMÁTICA

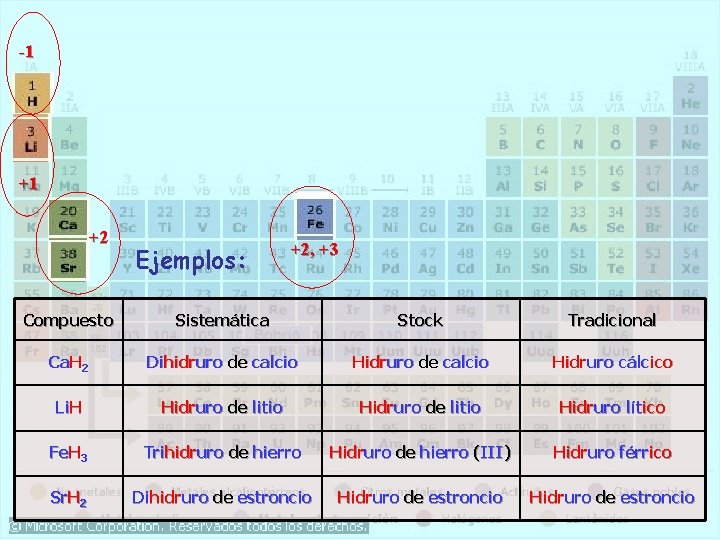
-1 +1 +2 Ejemplos: +2, +3 Compuesto Sistemática Stock Tradicional Ca. H 2 Dihidruro de calcio Hidruro cálcico Li. H Hidruro de litio Hidruro lítico Fe. H 3 Trihidruro de hierro Hidruro de hierro (III) Hidruro férrico Sr. H 2 Dihidruro de estroncio Hidruro de estroncio

+1 • Haluros de hidrógeno (hidruros no metálicos I): son combinaciones de un no metal (X, -n) -n de los grupos VIA (16) y VIIA (17) con el hidrógeno (H, +1). +1 FORMULACIÓN: H (+1) NOMENCLATURA DE STOCK -2 X(-n) Hn X NOMENCLATURA SISTEMÁTICA -1 1 X-uro de prefijohidrógeno X-uro de hidrógeno (no se usa) NOMENCLATURA TRADICIONAL Ácido + X-hídrico

+1 -1 -2 Ejemplos: Comp. Sistemática Stock Tradicional HF Fluoruro de hidrógeno Ácido fluorhídrico HCl Cloruro de hidrógeno Ácido clorhídrico H 2 S Sulfuro de dihidrógeno Sulfuro de hidrógeno Ácido sulfhídrico H 2 Se Seleniuro de dihidrógeno Seleniuro de hidrógeno Ácido selenhídrico

-3 -4 -3 +1 • Hidruros volátiles (hidruros no metálicos II): son combinaciones del hidrógeno (H, -1) -1 con un no metal (X, +n) +n de los grupos IIIA (13), IVA (14) y VA (15). FORMULACIÓN: X (+n) H (-1) X 1 H n NOMENCLATURA SISTEMÁTICA Prefijohidr-uro de X NOMENCLATURA DE STOCK Hidr-uro de X (nº romano valencia) NOMENCLATURA TRADICIONAL Nombres propios admitidos

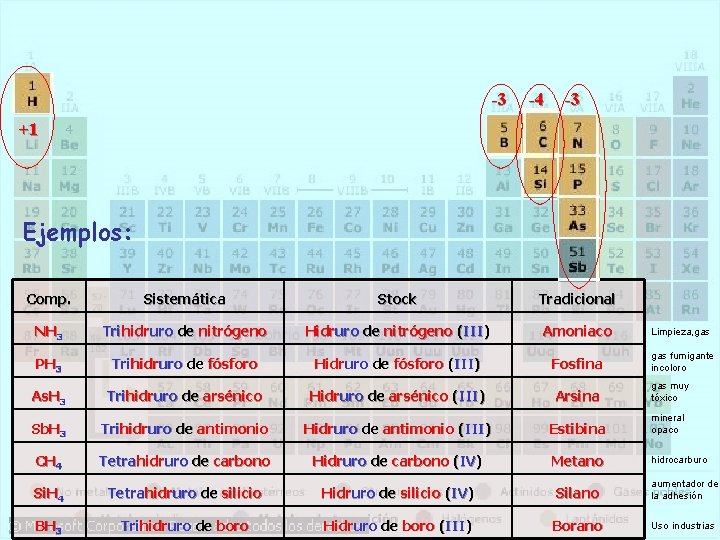
-3 -4 -3 +1 Ejemplos: Comp. Sistemática Stock Tradicional NH 3 Trihidruro de nitrógeno Hidruro de nitrógeno (III) Amoniaco Limpieza, gas PH 3 Trihidruro de fósforo Hidruro de fósforo (III) Fosfina gas fumigante incoloro As. H 3 Trihidruro de arsénico Hidruro de arsénico (III) Arsina gas muy tóxico Sb. H 3 Trihidruro de antimonio Hidruro de antimonio (III) Estibina mineral opaco CH 4 Tetrahidruro de carbono Hidruro de carbono (IV) Metano hidrocarburo Si. H 4 Tetrahidruro de silicio Hidruro de silicio (IV) Silano aumentador de la adhesión BH 3 Trihidruro de boro Hidruro de boro (III) Borano Uso industrias

SALES BINARIAS

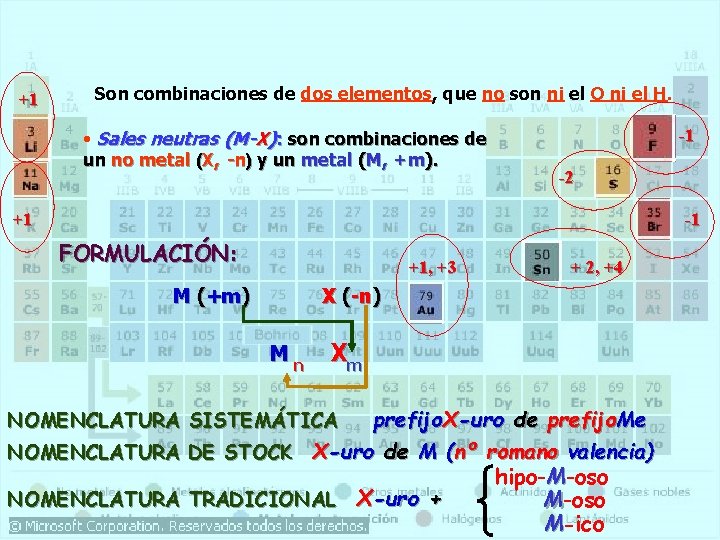
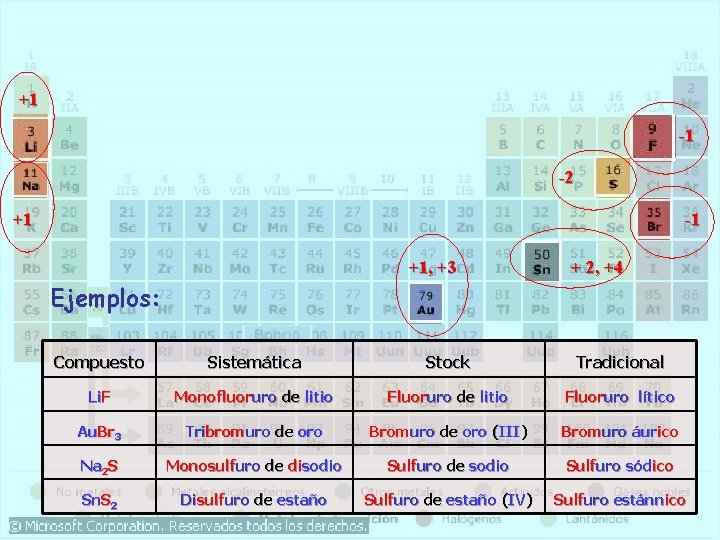
+1 Son combinaciones de dos elementos, que no son ni el O ni el H. • Sales neutras (M-X): son combinaciones de un no metal (X, -n) y un metal (M, +m). -1 -2 +1 -1 FORMULACIÓN: +1, +3 M (+m) + 2, +4 X (-n) Mn Xm prefijo. X-uro de prefijo. Me NOMENCLATURA DE STOCK X-uro de M (nº romano valencia) hipo-M-oso NOMENCLATURA TRADICIONAL X-uro + M-oso M-ico NOMENCLATURA SISTEMÁTICA

+1 -1 -2 +1 -1 +1, +3 + 2, +4 Ejemplos: Compuesto Sistemática Stock Tradicional Li. F Monofluoruro de litio Fluoruro lítico Au. Br 3 Tribromuro de oro Bromuro de oro (III) Bromuro áurico Na 2 S Monosulfuro de disodio Sulfuro de sodio Sulfuro sódico Sn. S 2 Disulfuro de estaño Sulfuro de estaño (IV) Sulfuro estánnico

COMPUESTOS TERNARIOS

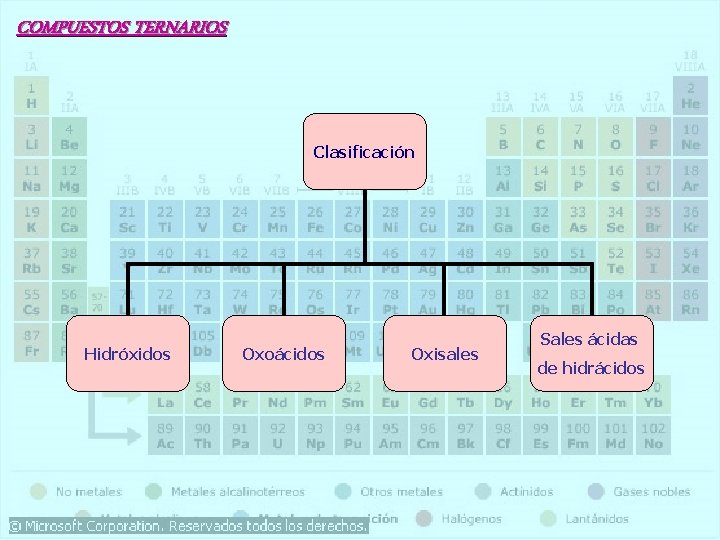
COMPUESTOS TERNARIOS Clasificación Hidróxidos Oxoácidos Oxisales Sales ácidas de hidrácidos

HIDRÓXIDOS

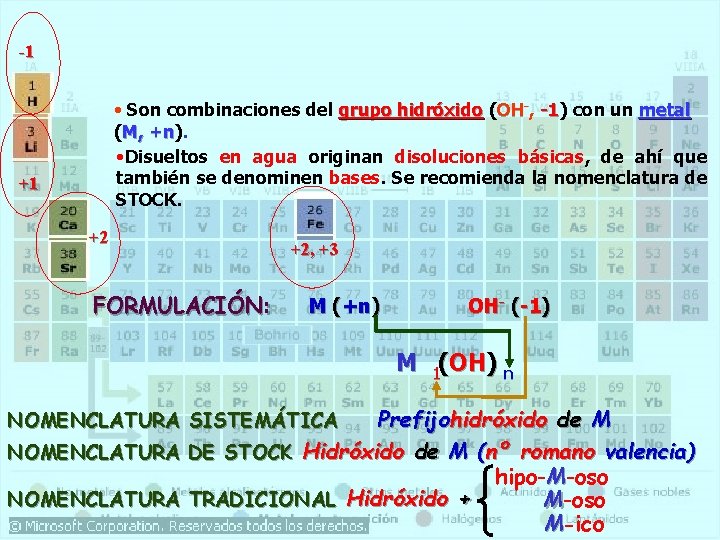
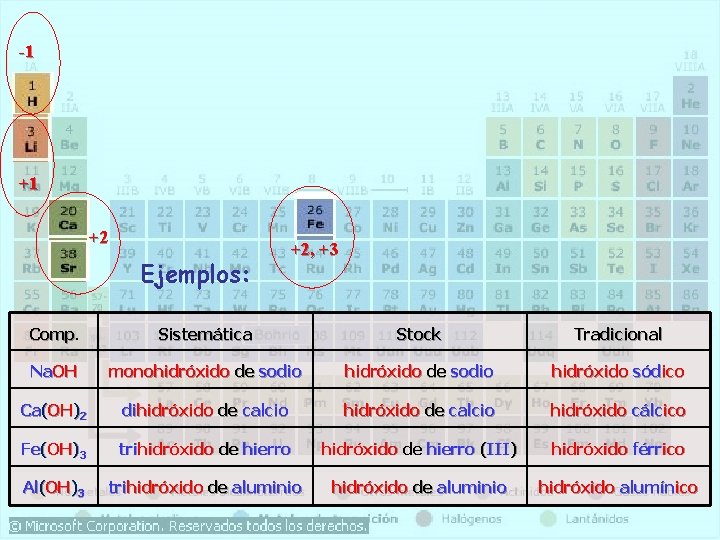
-1 • Son combinaciones del grupo hidróxido (OH-, -1) -1 con un metal (M, +n). +n • Disueltos en agua originan disoluciones básicas, de ahí que también se denominen bases. Se recomienda la nomenclatura de STOCK. +1 +2 FORMULACIÓN: +2, +3 M (+n) OH- (-1) M 1(OH) n Prefijohidróxido de M NOMENCLATURA DE STOCK Hidróxido de M (nº romano valencia) hipo-M-oso NOMENCLATURA TRADICIONAL Hidróxido + M-oso M-ico NOMENCLATURA SISTEMÁTICA

-1 +1 +2 Ejemplos: +2, +3 Comp. Sistemática Stock Tradicional Na. OH monohidróxido de sodio hidróxido sódico Ca(OH)2 dihidróxido de calcio hidróxido cálcico Fe(OH)3 trihidróxido de hierro (III) hidróxido férrico Al(OH)3 trihidróxido de aluminio hidróxido alumínico

EJERCICIOS Ø http: //www. alonsoformula. com/inorganica/osformulas_1. htm Ø http: //www. alonsoformula. com/inorganica/osnomes_1. htm Ø http: //www. alonsoformula. com/inorganica/osformulas_2. htm Ø http: //www. alonsoformula. com/inorganica/osnomes_2. htm
 Matriz de analisis de involucrados
Matriz de analisis de involucrados Nomenclatura
Nomenclatura Hidruro de potasio
Hidruro de potasio Formulacin
Formulacin Oxoacidos
Oxoacidos Formulacin
Formulacin Qumica
Qumica Postprecipitación
Postprecipitación Qumica
Qumica Qumica
Qumica Nomenclatura das bases
Nomenclatura das bases Qumica
Qumica Ch3-ch-ch2-ch-ch3
Ch3-ch-ch2-ch-ch3 Monossacarídios
Monossacarídios Stoicheon
Stoicheon Qumica
Qumica Qual a sentença verdadeira
Qual a sentença verdadeira Qumica
Qumica Haleto de alquila
Haleto de alquila Química orgânica resumo
Química orgânica resumo Homogneo
Homogneo Qumica
Qumica Philippe spitaleri kaufmann
Philippe spitaleri kaufmann Notação de lewis
Notação de lewis Qumica
Qumica Qumica
Qumica Qumica
Qumica Unip engenharia de produção
Unip engenharia de produção