Formation sur Les prlvements lidentification la stabilisation le

Formation sur « Les prélèvements, l’identification, la stabilisation, le transport… des spécimens biologiques Et les analyses de biologie délocalisées ADBD» 10 juin 2015 Josée Morin t. m. Assistante chef technologiste médicale et responsable qualité du laboratoire du CSSS du Val-Saint-François

Prélèvement sanguin L’obtention d’un spécimen de qualité est à la base de tout résultat d’analyse fiable. Toutes procédures inadéquates relatives: au prélèvement Ø à l’identification Ø à la manipulation Ø au transport des spécimens Ø peuvent entraîner des résultats erronés


1. L’identification de l’usager Ø La responsabilité de l’identification de l’usager incombe à la personne qui effectue le prélèvement Ø Par une double identification selon la directive reliée à la double identification du client (DSI-024) Ø Ø Nom et prénom Date de naissance RAMQ Photo (à la porte de la chambre ou dans FADM)
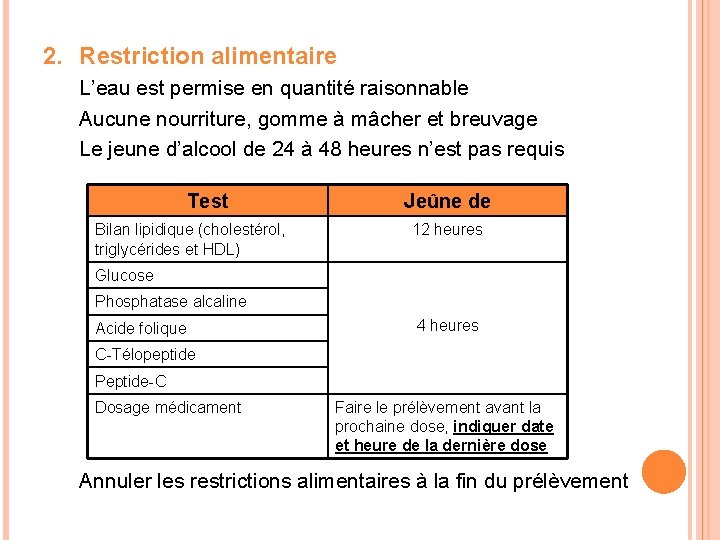
2. Restriction alimentaire L’eau est permise en quantité raisonnable Aucune nourriture, gomme à mâcher et breuvage Le jeune d’alcool de 24 à 48 heures n’est pas requis Test Bilan lipidique (cholestérol, triglycérides et HDL) Jeûne de 12 heures Glucose Phosphatase alcaline Acide folique 4 heures C-Télopeptide Peptide-C Dosage médicament Faire le prélèvement avant la prochaine dose, indiquer date et heure de la dernière dose Annuler les restrictions alimentaires à la fin du prélèvement

3. Précaution importante tourniquet (garrot) Ø L’application prolongée (+ de 1 minute) Ø Mouvement répétitif d’ouverture et fermeture de la main Cause: Ø Ø Hémoconcentration Une variation de +/- 8 à 10 % du résultat (Exemple: K, ALT, CK, Bilirubine, LDH, GGT)
4. Importance de laisser sécher l’alcool Cause: Hémolyse Ø Sensation de brûlure pour le patient Ø

5. Minimum de traumatisme L’exécution d’un prélèvement de qualité est primordiale. Il doit être effectué avec un minimum de traumatisme afin d’éviter: Ø l’activation de la coagulation et des plaquettes Ø l’hémolyse

COMMENT CORRIGER UN COLLAPSUS ? Ø Ø Ø Relever l’aiguille pour abaisser le biseau afin de permettre à la membrane de la veine de se décoller du biseau ; Tirer la peau vers le bas ou vers le haut ; Remettre le garrot pour augmenter la pression interne de la veine ; Enlever le garrot (si la peau devient blanche) ; Changer le tube (matériel défectueux) ; Retirer et remettre le tube, parfois l’aiguille décolle de la veine ;

Bientôt sur l’intranet Espace clinique 6. Liste des tests P: LaboPrélèvement PRE-9535. 16 Liste des test ordre alphabétique Version E_1. Lecture seule (ctrl + F pour recherche rapide).
LISTES DES TESTS DU LABORATOIRE DUC HUS Ø www. chus. qc. ca e Laboratoir ses y l a An

7. Ordre de prélèvement des tubes 1 2 3 4 5 6 7 8 9 10

8. Raison du tube bleu en premier Ø C’est afin de préserver l’intégrité de l’échantillon pour l’épreuve de coagulation que l’on prélève celui-ci au début du processus de prélèvement. Ø Cause : Il y a libération de thromboplastine tissulaire et activation du processus de coagulation.

9. Recommandation spéciale: coagulation Pour une demande d'analyses destinées à la coagulation de routine, (PT (INR) et PTT) le premier tube prélevé peut être utilisé; cependant, la ponction devrait être franche et l’écoulement de sang régulier durant tout le prélèvement du tube. Par contre, pour des analyses spécialisées de coagulation (p. ex. : dosage de facteurs), il est recommandé d’éliminer les cinq (5) premiers millilitres (ml) de sang avant de prélever le tube de coagulation. Attention : Lorsqu’une unité de prélèvement à ailettes (papillons) est utilisée pour la ponction veineuse et que le premier tube prélevé est destiné à la coagulation, un tube de rejet devrait être prélevé en premier pour vider l’espace d’air de la tubulure de l’unité de prélèvement et assurer un ratio sang/anticoagulant optimal. Le tube de rejet utilisé doit être un tube sans additif (blanc) ou un tube pour épreuve de coagulation (bleu) car les autres tubes contiennent un activateur de coagulation qui pourrait interférer lors de l’analyse.

9. Recommandation spéciale: électrolytes Ne pas prélever un tube destiné à l’analyse des électrolytes immédiatement après un tube contenant du citrate de sodium. Lorsqu’un tube destiné à l’analyse des électrolytes est prélevé immédiatement après un tube contenant du citrate de sodium, un tube de rejet (sans additif : tube blanc) est prélevé entre les deux.

10. Ratio sang/anticoagulant Ø La qualité et la stabilité du spécimen sont directement liées au respect du ratio adéquat de sang/anticoagulant dans le tube de prélèvement Ø Un volume de remplissage minimal de 90 % permet d’obtenir des résultats fiables dans la majeure partie des situations. (sauf le tube bleu qui doit être à 100%) Ø Lorsque le tube est moins bien rempli, les temps des tests de coagulation ont tendance à augmenter en raison de la plus grande proportion d’anticoagulant dans l’échantillon

10. Ratio sang/anticoagulant

11. Mélange des tubes Ø Le mélange des tubes contenant un anticoagulant ou un activateur de caillot doit se faire immédiatement après le prélèvement, doucement, et par retournements successifs complets, de 5 fois pour les tubes contenant un activateur de caillot (tubes or, rouge) et de 8 à 10 fois pour les tubes contenant d’autres additifs (tubes lavande, bleu, vert, rose, gris et jaune)
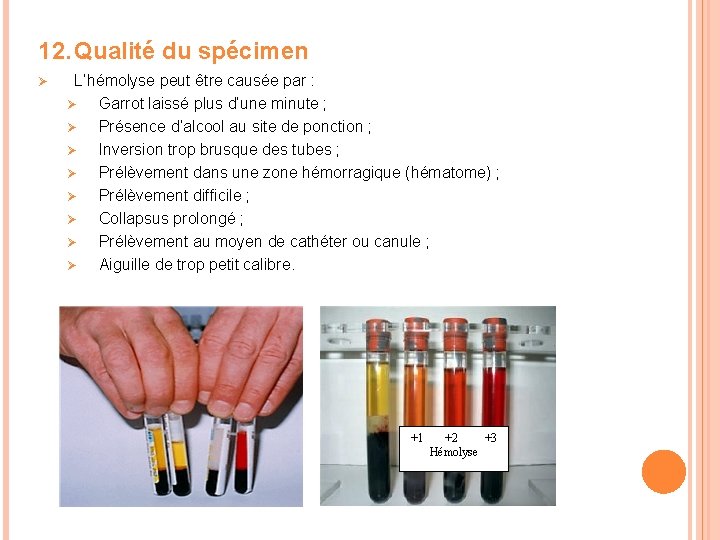
12. Qualité du spécimen Ø L’hémolyse peut être causée par : Ø Garrot laissé plus d’une minute ; Ø Présence d’alcool au site de ponction ; Ø Inversion trop brusque des tubes ; Ø Prélèvement dans une zone hémorragique (hématome) ; Ø Prélèvement difficile ; Ø Collapsus prolongé ; Ø Prélèvement au moyen de cathéter ou canule ; Ø Aiguille de trop petit calibre. +1 +2 +3 Hémolyse

13. Disposition du matériel Ø Ø Jeter l’aiguille dans un contenant rigide pour déchets piquants, tranchants, cassables. Ne pas remettre l’aiguille dans sa gaine Ces contenants doivent être placés de façon sécuritaire.

2. Prélèvement autre que sanguin 1. Urinaires Ø Analyse Délai de conservation: Ø Ø Ø 2 heures To pièce 6 heures au froid mais microscopie non valable Microalbumine Délai de conservation: Ø 72 heures au froid

1. Urinaires Ø Culture Délai de conservation: Ø 24 heures au froid

1. Urinaires Ø Urines de 24 heures Important de recueillir toutes les urines durant la période de 24 heures. Ø Diète à suivre pour: Ø Ø 5 -HIAA VMA Hydroxyproline

1. Urinaires Ø Cytologie Ø Ø Ne pas utiliser la première urine du matin, car elle est trop concentrée et elle contient des cellules dégénérées qui peuvent nuire à l’analyse. Chlamydia et gono 1 à 2 heures depuis la dernière miction Ø Recueillir les premiers 10 à 50 ml Ø

2. Selles Ø Recherche de sang (FIT test/RSosi) Conservation au froid Ø Une petite quantité de selles suffit Ø
2. Selles Ø Culture 24 heures d’intervalle entre les 2 échantillons. Ø Ne pas dépasser la flèche tracée sur l’étiquette. Ø Agiter vigoureusement. Ø Conservation au froid. Ø

2. Selles Ø Parasites 24 heures d’intervalle entre les 2 échantillons. Ø Ne pas dépasser la ligne tracée sur l’étiquette. Ø Agiter vigoureusement. Ø Conservation température pièce. Ø

2. Selles Ø C. difficile 1 seul spécimen requis. Ø Conservation au froid. Ø

3. Expectorations. 24 heures d’intervalle entre les 2 échantillons. Ø Échantillon recueilli le matin. Ø Rincer la bouche à l’eau avant la collecte. Ø Conservation au froid. Ø

3. Identification des: prescriptions, formulaires et échantillons 1. Politique sur les critères d’acceptabilité des prescriptions et des échantillons Ø Échantillons Ø Tous les échantillons doivent comporter : Ø une double identification de l’usager Ø Ø Nom, prénom Date de naissance / RAMQ / #dossier du VSF Initiales du préleveur Date et heure du prélèvement RAMQ
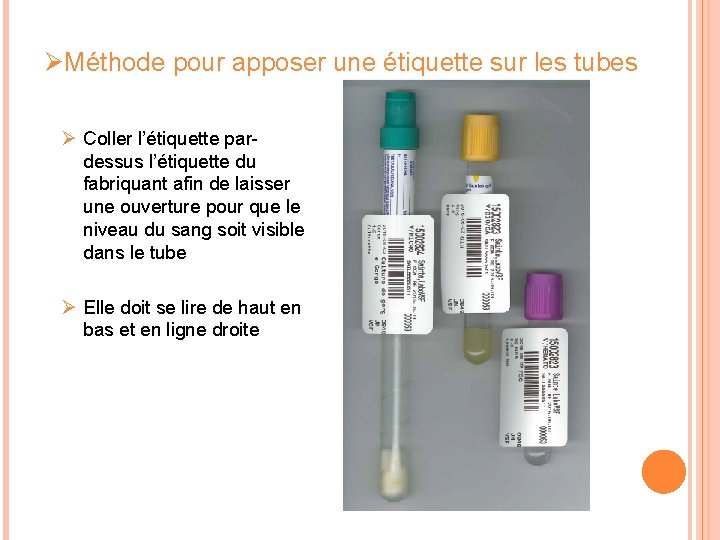
ØMéthode pour apposer une étiquette sur les tubes Ø Coller l’étiquette pardessus l’étiquette du fabriquant afin de laisser une ouverture pour que le niveau du sang soit visible dans le tube Ø Elle doit se lire de haut en bas et en ligne droite

FORMULAIRE OBLIGATOIRE Ø Certaine analyse demande qu’un formulaire soit rempli Ø Banque de sang: Ø Ø Groupe sanguin + Rh Recherche d’anticorps (Coombs indirect) Coombs direct Compatibilité (pour transfusion) Cytologie Ø Pathologie Ø Génétique Ø Analyse fait hors Québec Ø
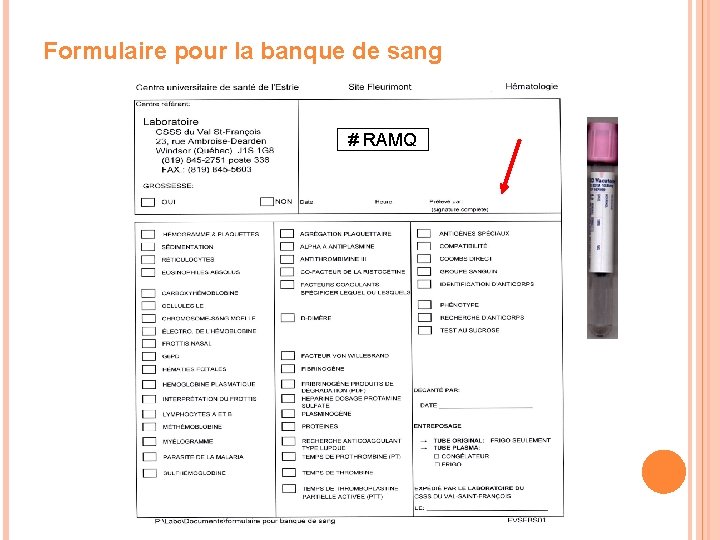
Formulaire pour la banque de sang # RAMQ

#RAMQ
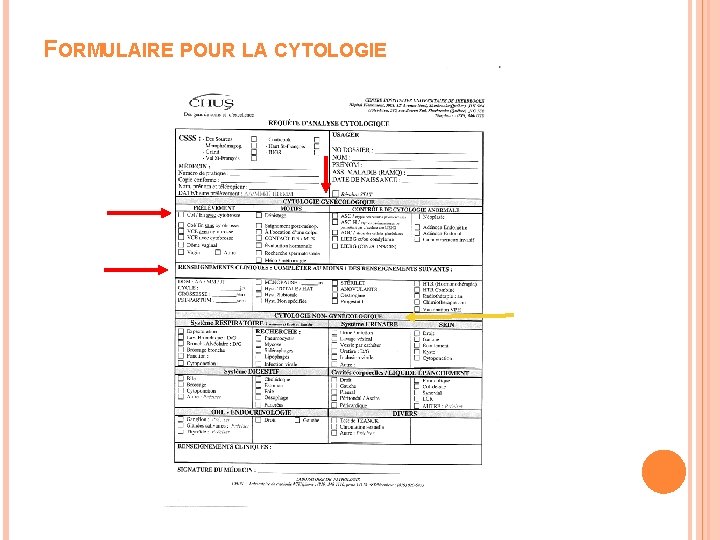
FORMULAIRE POUR LA CYTOLOGIE

F ORMULAIRE POUR LA PATHOLOGIE

FORMULAIRE POUR LA GÉNÉTIQUE

FORMULAIRE POUR TEST HORS PROVINCE

2. Politique sur les échantillons unique Un formulaire d’attestation devra être complété si l’identification d’un échantillon unique est nonconforme. Ø Exemple d’échantillon unique : Ø Ø Liquide synovial Lithiase urinaire Urine sus-pubienne Échantillon pour cytologie et pathologie

3. Procédure de rejet des échantillons Ø Voici quelques critères vérifiées: Ø Ø Ø Conditions de transport Délais de conservation Abri de la lumière Ratio / anticoagulant Identification échantillon

4. Stabilisation et transport des échantillons 1. Procédure d’emballage, de transport et de réception de « spécimen humain exempté » par transport routier Ø L’intégrité et la qualité du spécimen doivent être maintenues durant toutes ces étapes à partir du prélèvement jusqu’à la réception au laboratoire.

Ø Après le prélèvement veineux et après avoir mélangé chaque tube par retournements successifs complets au moment du prélèvement : Ø Placer les tubes en position verticale dans un support. Ø Observer les directives spéciales de conservation Exemples : Ø Réfrigérer ou conserver à température pièce Ø Centrifuger les tubes OR pour hébergement Richmond et pour Valcourt c’est l’infirmière au SIC qui s’occupe de la centrifugation Ø Préserver de la lumière
Ø Stabilisation Ø Centrifugation des tubes jaunes: attendre ½ heure après le prélèvement avant de centrifuger
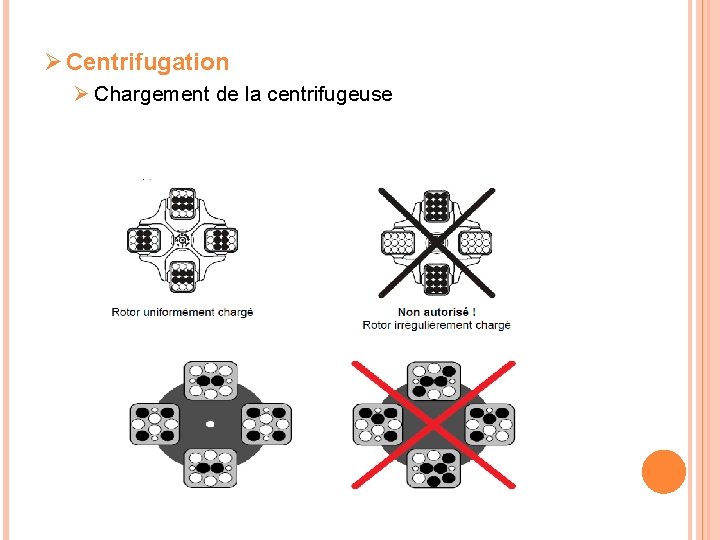
Ø Centrifugation Ø Chargement de la centrifugeuse
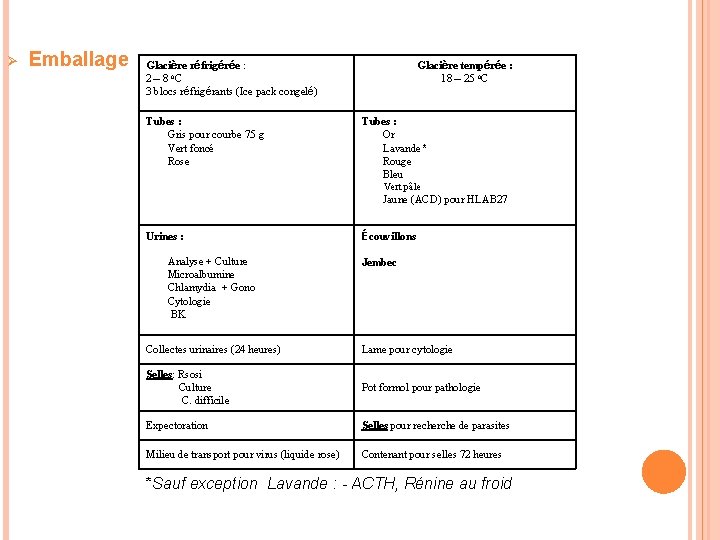
Ø Emballage Glacière réfrigérée : 2 – 8 o. C 3 blocs réfrigérants (Ice pack congelé) Tubes : Gris pour courbe 75 g Vert foncé Rose Glacière tempérée : 18 – 25 o. C Tubes : Or Lavande* Rouge Bleu Vert pâle Jaune (ACD) pour HLAB 27 Urines : Analyse + Culture Microalbumine Chlamydia + Gono Cytologie BK Écouvillons Jembec Collectes urinaires (24 heures) Lame pour cytologie Selles: Rsosi Culture C. difficile Pot formol pour pathologie Expectoration Selles pour recherche de parasites Milieu de transport pour virus (liquide rose) Contenant pour selles 72 heures *Sauf exception Lavande : - ACTH, Rénine au froid

Ø Transport Ø Ø Ø Tube en position verticale Mettre portoir des tubes dans un sac de plastique avec papier absorbant Tube ne doit pas être en contact direct avec les blocs réfrigérants Bien visser les pots d’urines Spécimen humain exempté doit être apposé sur les glacières

Ø Spécimen pour le CHUS en provenance de Richmond et Valcourt Ø Bien identifier la glacière lorsqu’il y a des tubes que nous devons envoyer le jour même au CHUS et nous téléphoner au poste 55290 Ø Exemple: ØSpécimen pour la microbiologie (culture plaie…. ) ØCompatibilité (cross match) pour transfusion ØPost exposition (personne source et exposé) ØStat pour les tests fait au CHUS

2. Procédure sur le transport des spécimens à l’intérieur d’une même installation Les échantillons doivent être transportés dans les plus brefs délais, dans le respect des exigences de transport et de conservation édictés par le laboratoire serveur pour les analyses concernées. Ø Placer les spécimens dans un sac de plastique en position verticale avec un papier absorbant Ø

3. Délai de conservation de transport pour les spécimens biologiques Ø Délai de conservation spécimen sanguin Durée conservation Tube couleur avant centrifugation Rouge sans additif 2 heures Bleu 4 heures Rouge avec additif 2 heures Or + Vert pâle 2 heures Vert foncé 1 heures Rose 4 heures Lavande 6 heures Gris 24 heures Jaune (ACD) 24 heures après centrifugation N/A 24 heures N/A
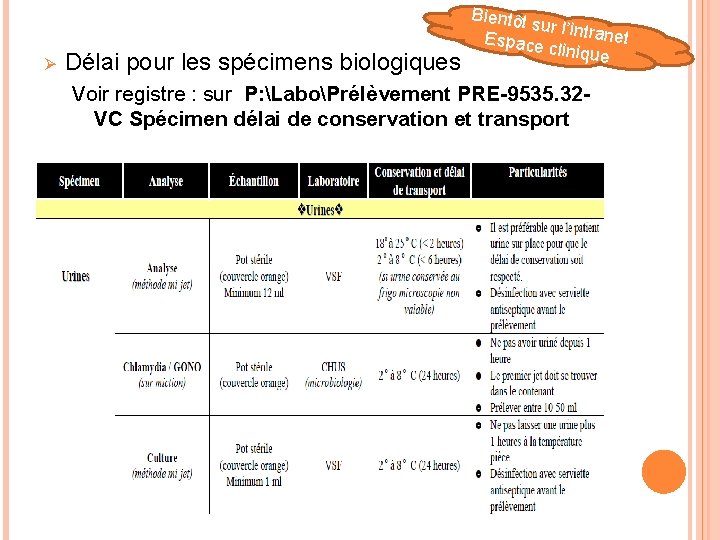
Ø Délai pour les spécimens biologiques Bientôt sur l’intr anet Espace clinique Voir registre : sur P: LaboPrélèvement PRE-9535. 32 VC Spécimen délai de conservation et transport

5. ADBD (Analyse de biologie délocalisée) Ø Rôle de l’utilisateur d’une ADBD Ø Respecte les règles des politiques et des procédures Ø S’assure qu’il n’y a pas de lacune dans l’application de la procédure d’utilisation Ø Assiste aux sessions de mises à jour et recertification Ø Voit à l’entretien de son appareil en se référant à l’aide mémoire Ø Rapporte toutes les difficultés de fonctionnement ou d’utilisation rencontrées à un superutilisateur ou en son absence à son supérieur immédiat

Analyse des urines par bandelettes réactives

1. Analyse des urines par bandelettes réactives Ø Bien mélanger l’urine doucement pour éviter les bulles Vérifier la date d’expiration de la bandelette Refermer le flacon immédiatement après avoir pris une bandelette Ne pas toucher aux zones réactives de couleur sur la bandelette Tremper la bandelette dans l’urine. Assurez-vous d’immerger toutes les zones réactives Retirer aussitôt……. . Ø Ø Ø

Ø Égoutter la bandelette en la secouant sur le rebord du contenant ou sur un papier à mains pour enlever l’excès d’urine (ne jamais essuyer ni tamponner la bandelette) Ø Commencer le minutage Ø Lire chacune des zones réactives au moment approprié tel qu’indiqué sur le flacon Ø Ne pas lire les résultats avant les temps recommandés ou plus de 2 minutes après avoir trempé la bandelette dans l’urine
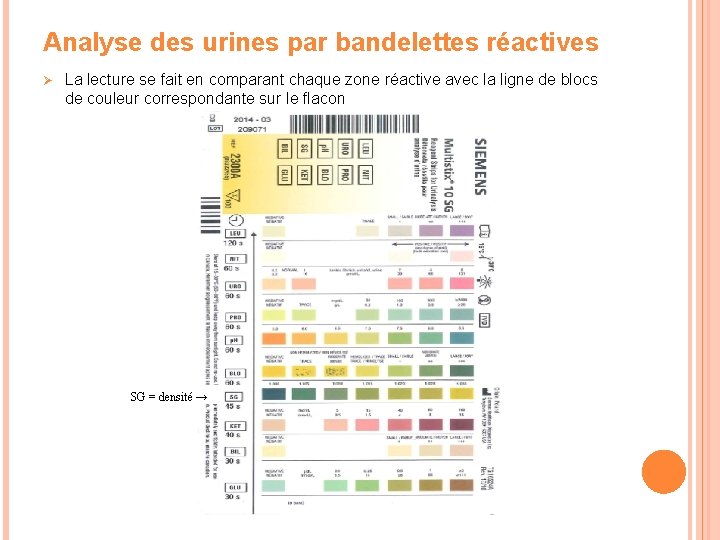
Analyse des urines par bandelettes réactives Ø La lecture se fait en comparant chaque zone réactive avec la ligne de blocs de couleur correspondante sur le flacon SG = densité →


Ø Une copie du formulaire résultat Multistix doit être envoyé au laboratoire car les résultats seront retranscrits dans le système informatique du laboratoire (SIL) avec mention que c’est une ADBD Ø CONTRÔLE DE QUALITÉ Ø Une fois par mois, chaque département fait parvenir au laboratoire 2 bâtonnets dans un contenant approprié et bien identifié avec l’étiquette suivante
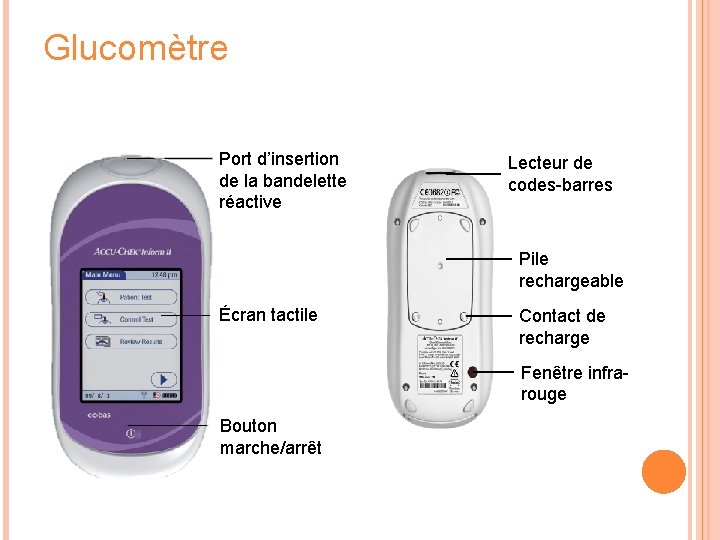
Glucomètre Port d’insertion de la bandelette réactive Lecteur de codes-barres Pile rechargeable Écran tactile Contact de recharge Fenêtre infrarouge Bouton marche/arrêt

Glucomètre Ø Obtention d’un échantillon de sang capillaire Ø Porter des gants Ø Nettoyer le site de la ponction capillaire avec de l’eau chaude (si alcool utilisé, laisser sécher à l’air complètement) Ø Essuyer la première goutte Ø Prendre la deuxième goutte pour faire l’analyse
Ø Carte identification (CIP) Ø Toujours avoir sa carte d’indentification Ø Possibilité d’inscrire votre #CIP avec le clavier du glucomètre (4 lettres et 4 chiffres)

Ø Registre d’utilisation de la carte « patient inconnu » Ø Si la carte « patient inconnu » qui est dans le coffret est utilisée vous devez remplir le formulaire: registre d’utilisation de la carte « patient inconnu »

Ø Contrôle de qualité Ø Les contrôles de qualité doivent être fait lorsque l’appareil indique de les faires car si pas fait impossible d’utiliser le glucomètre Ø Les contrôles sont programmés pour être fait à tous les 24 heures

Ø Socle

- Slides: 64