Formation laborantin danalyse mdicale Exploration biochimique de la

Formation laborantin d’analyse médicale Exploration biochimique de la corticosurrénale Présenté par: Dr. DOUKHI

Plan du cours 1 - Généralités 2 - Les glucocorticoïdes 3 - Les minéralocorticoïdes 4 - Les androgènes surrénaliens
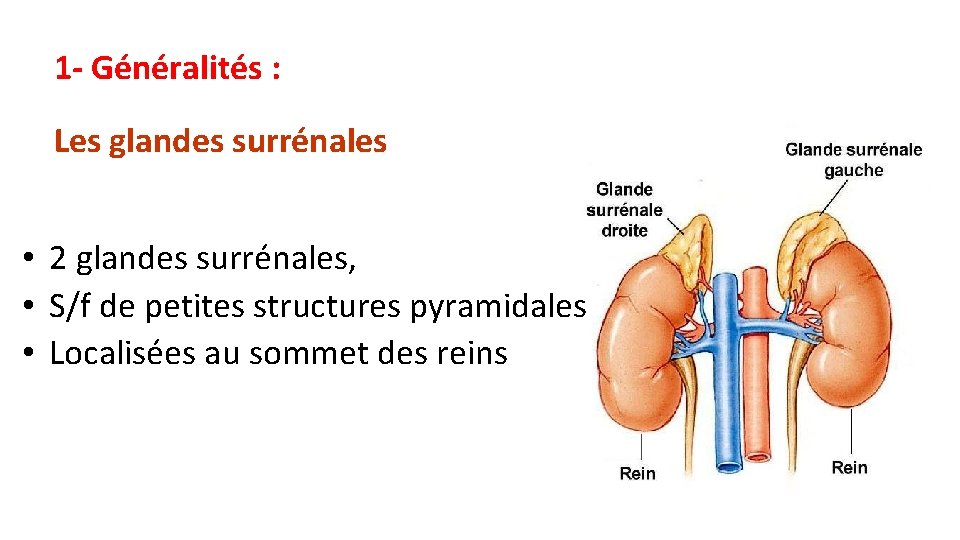
1 - Généralités : Les glandes surrénales • 2 glandes surrénales, • S/f de petites structures pyramidales • Localisées au sommet des reins

Structure de la glande surrénale • Zone périphérique dérivé du mésoderme jaunâtre ferme: • cortex surrénalien, ou "corticosurrénale " , • produit des stéroïdes (androgènes, minéralocorticoïdes et glucocorticoïdes ) • Zone centrale dérivée du neuro ectoderme (des crêtes neurales rougeâtre, très vascularisée : • "médullosurrénale ", • produit des catécholamines.
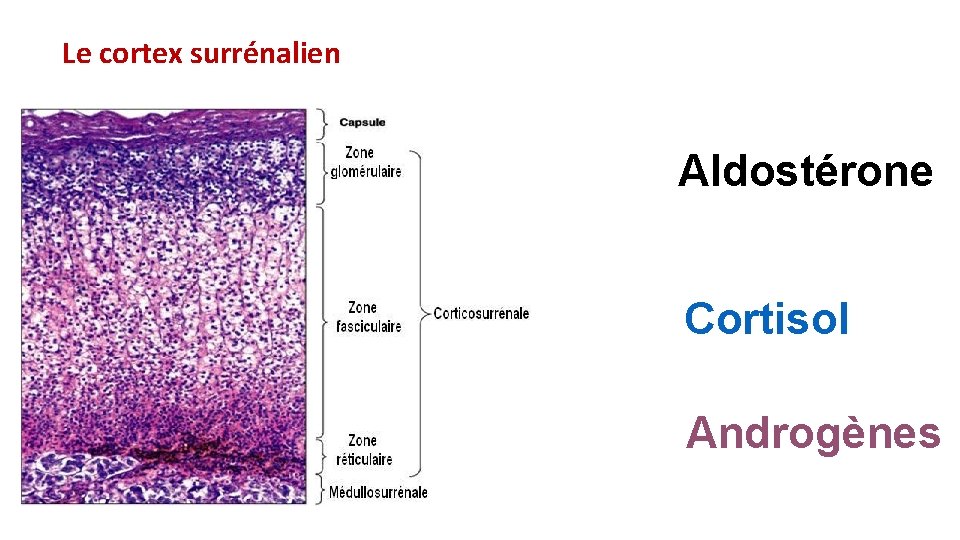
Le cortex surrénalien Aldostérone Cortisol Androgènes

• hormones stéroïdes = Dérivent du noyau stérane • Précurseur: cholestérol • Dans le sang: s/f libres ou liées à des protéines de transport • La fraction libre: la forme bio active. • Interagissent avec des récepteurs intracellulaires. • Indispensables à la vie : Assurent 2 grandes fonctions: • Reproduction : • Femme: Estrogènes et Progestérone • Homme: testostérone (Androgènes). • Régulation : • Régulation minérale (aldostérone) • Régulation glucidique (glucocorticoïdes)
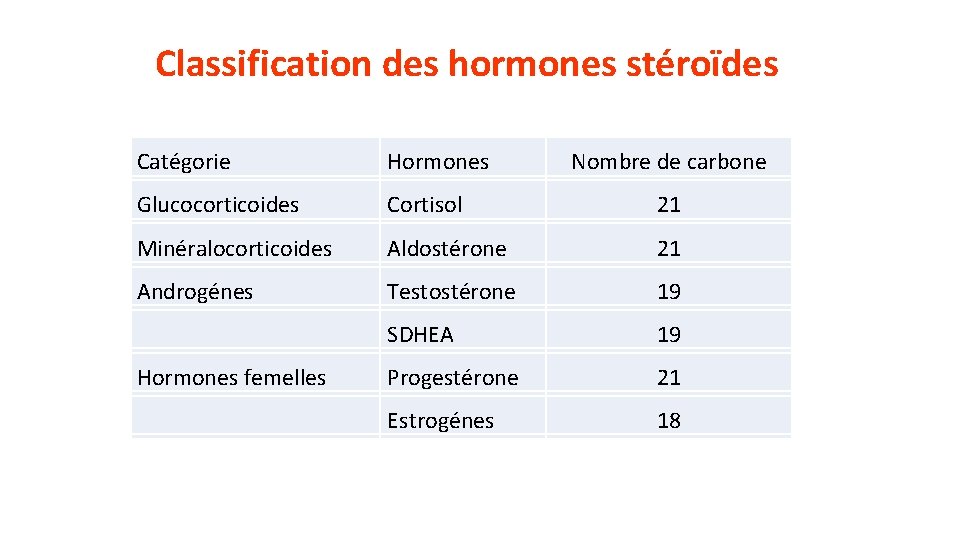
Classification des hormones stéroïdes Catégorie Hormones Glucocorticoides Cortisol 21 Minéralocorticoides Aldostérone 21 Androgénes Testostérone 19 SDHEA 19 Progestérone 21 Estrogénes 18 Hormones femelles Nombre de carbone
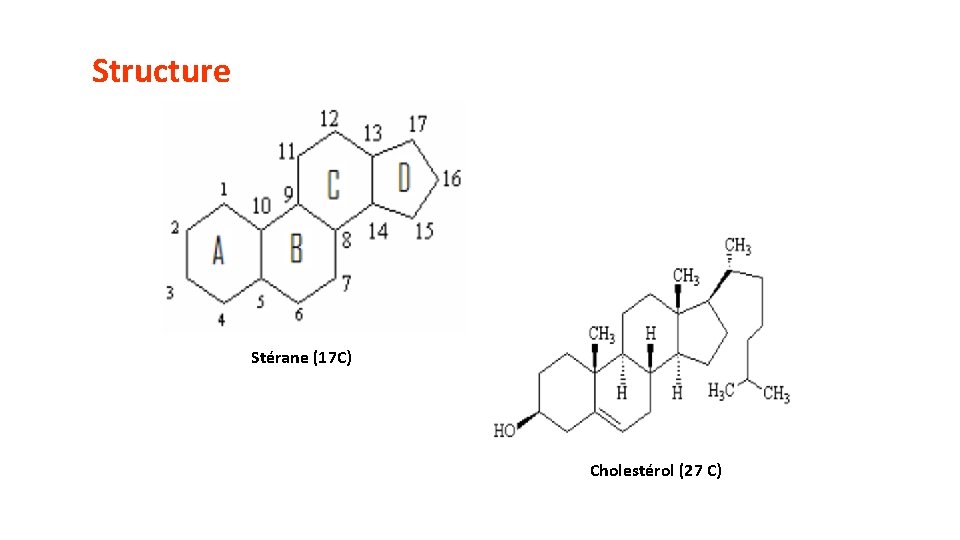
Structure Stérane (17 C) Cholestérol (27 C)
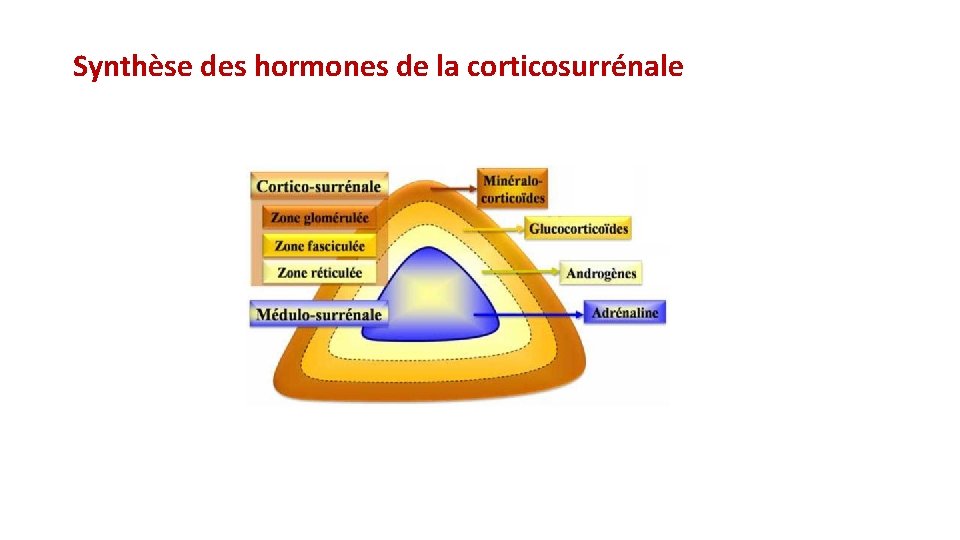
Synthèse des hormones de la corticosurrénale
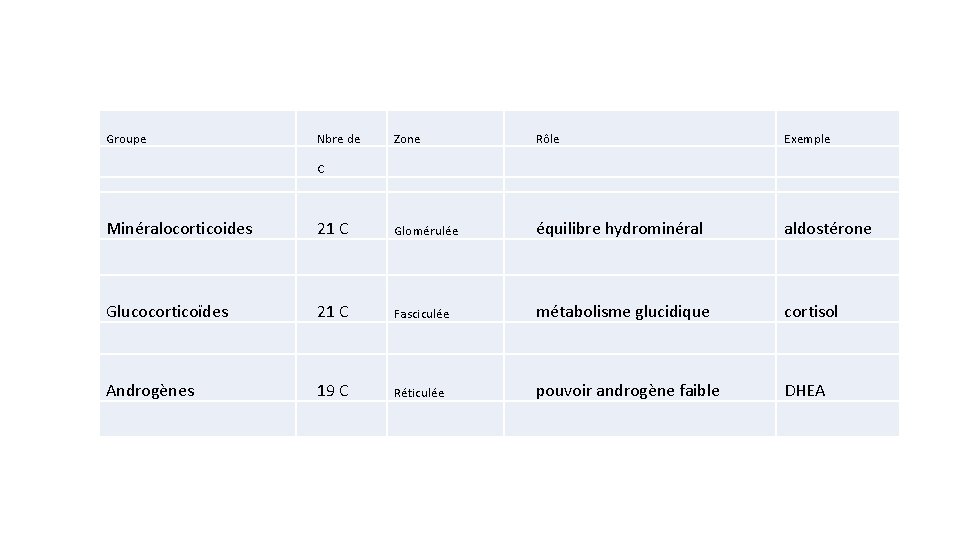
Groupe Nbre de Zone Rôle Exemple C Minéralocorticoides 21 C Glomérulée équilibre hydrominéral aldostérone Glucocorticoïdes 21 C Fasciculée métabolisme glucidique cortisol Androgènes 19 C Réticulée pouvoir androgène faible DHEA
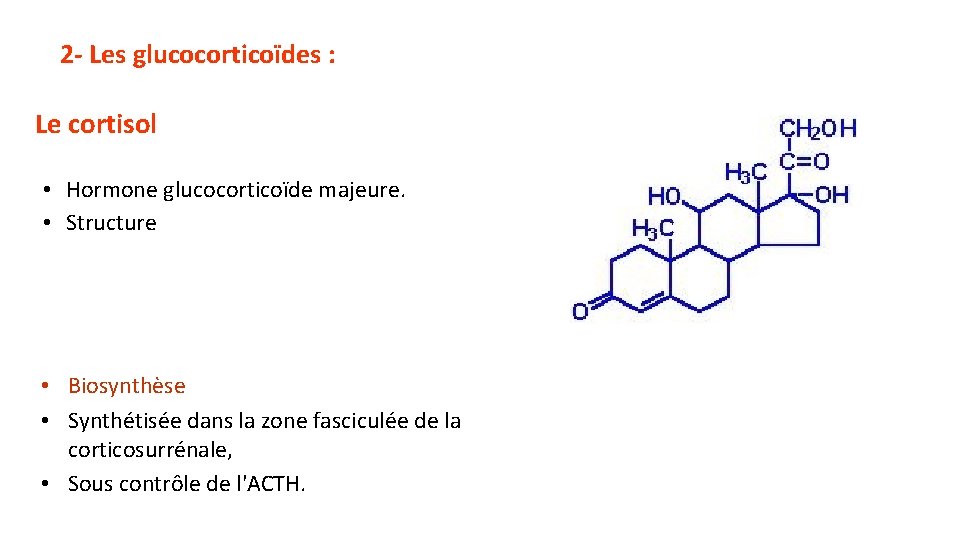
2 - Les glucocorticoïdes : Le cortisol • Hormone glucocorticoïde majeure. • Structure • Biosynthèse • Synthétisée dans la zone fasciculée de la corticosurrénale, • Sous contrôle de l'ACTH.
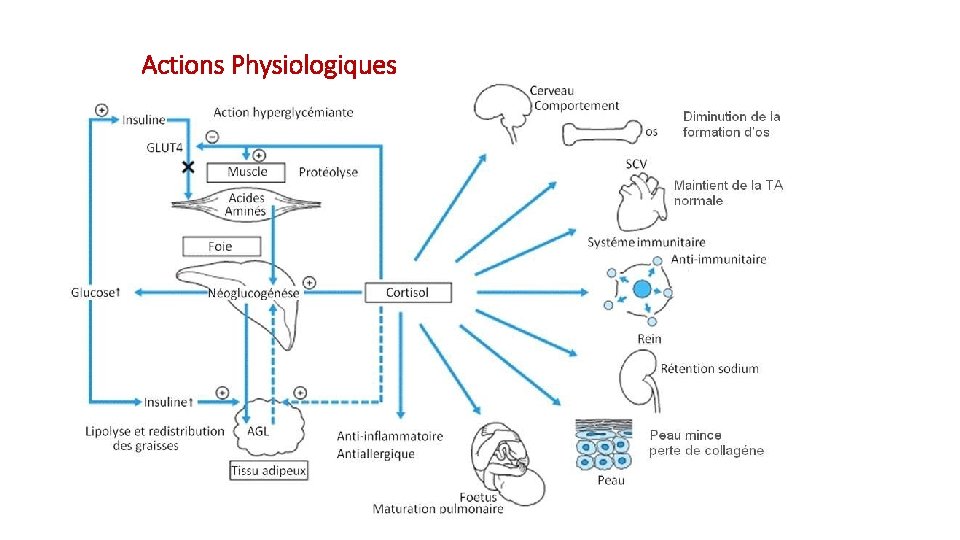
Actions Physiologiques
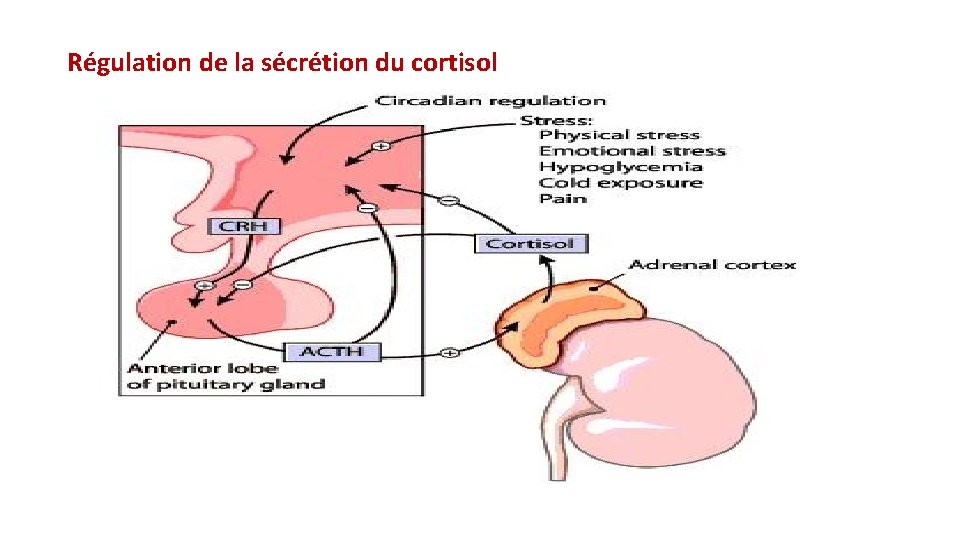
Régulation de la sécrétion du cortisol

ACTH • Adreno-Cortico-Tropic_Hormone, Hormone adrénocorticotrope ou corticotropine • Provient du clivage de la pro-opio-mélano-corticotrophine (POMC) précurseur de 266 aa (a-MSH et b-LPH). • Hormone hypophysaire contrôlant la sécrétion de cortisol • Peptide de 39 AA, secrété par les cellules corticotropes antéhypophysaires • Secrété de façon pulsatile (le taux sanguin varie) à l’origine du rythme circadien du cortisol (environ 40 pulses par 24 H) • Contrôle l'activité de la corticosurrénale sauf la zone glomérulée. • [C] max entre 6 et 9 H; minimum entre 23 et 24 H
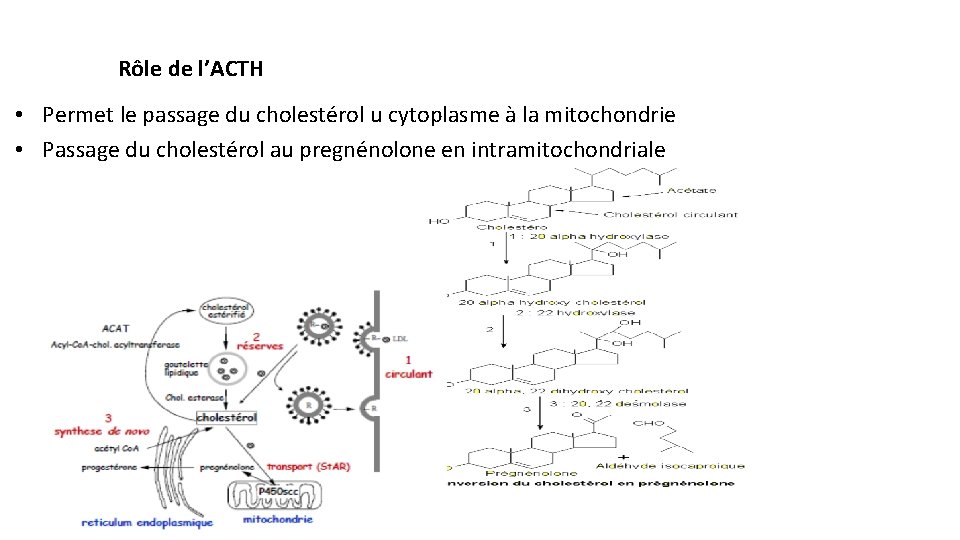
Rôle de l’ACTH • Permet le passage du cholestérol u cytoplasme à la mitochondrie • Passage du cholestérol au pregnénolone en intramitochondriale
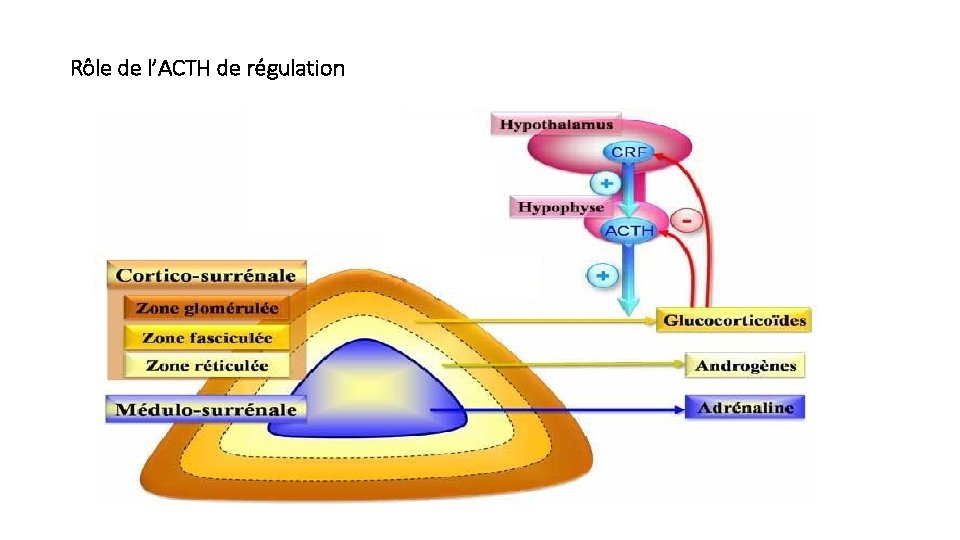
Rôle de l’ACTH de régulation

DOSAGE BIOLOGIQUE

DOSAGES STATIQUES Prélèvement sanguin • Prélèvement de sang veineux (au pli du coude) sur tube sec ou avec un anticoagulant • Effectué de préférence le matin (la sécrétion est maximale entre 7 et 8 h le matin), après un repos avec minimum de stress et d'effort physique. • L'heure du prélèvement doit être indiquée. • Prélèvement rapidement traité et congelé si dosage différé.

1 -Cortisol sanguin • 1 - Sécrétion • 25 mg de cortisol sont sécrétés/j par brèves décharges • 2 - La cortisolémie subit des variations nycthémérales • Maximal à 7 -8 Heures du matin. • Minimal vers minuit. • Ce rythme circadien se reproduit toutes les 24 H plus ou moins 1 Heure. 3 - Concentration du cortisol sanguin ou Cortisol sérique ou Cortisolémie (Valeurs normales) : = 50 - 200 µg/l ou 250 à 800 nmol/l.

RQ : Cortisol plasmatique • Valeur limitée d’un dosage isolé (stress, variations nycthémérales) • Si possible, faire des mesures au cours du cycle à : 8 H, 12 H, 16 H, 20 H, et 24 H • Pour démontrer le rythme circadien de sécrétion, 2 prélèvements sanguins sont réalisés : 1 vers 8 h et 1 à 16 h. • Classiquement, la cortisolémie vespérale = 25 % de la cortisolémie matinale. • Concentrations dépendantes de la concentration de la transcortine

2 - cortisol salivaire • La concentration de cortisol y est étroitement corrélée à la cortisolémie libre plasmatique (diffusion libre dans les cellules des glandes salivaires , absence d’albumine ou de transcorite )

Le cortisol libre urinaire CLU (FCU) Moins de 1 % des métabolites urinaires du cortisol CLU reflète la fraction active plasmatique CLU des 24 H corrélée à la quantité de cortisol bioactif ayant circulé durant le nycthémère 50 à 150 µg/24 h En cas d’ hypercorticisme la protéine porteuse du cortisol (transcortine) est saturée et donc le clu s’accroit de manière exponentielle par rapport à la cortisolemie

Conditions : ▪ Rapporté à la surface corporelle chez l’enfant ▪ Effectuer le recueille des urines des 24 h ▪ Mesure de la créatinémie pour valider le recueil urinaire des 24 h ▪ Mesure du clu par HPLC n’est pas réalisé en pratique courante ▪ Modérément élevée si diurèse excessive, stress ▪ ininterprétable en cas d’insuffisance rénale

ACTH : Prélèvement : Eviter le stress Sang veineux recueilli sur EDTA. Décanter immédiatement et mettre dans la glace, ou placer le tube dans la glace (30’). En raison du rythme diurne, le prélèvement se fait entre 8 h et 10 h du matin. Un prélèvement entre 16 h et 18 h permettra de mieux distinguer les patients atteints de la maladie de cushing des individus normaux.

Facteurs modifiants les résultats du Cortisol • Stress ( dépression ) : augmentation • Ethylisme : augmentation • Insuffisance rénale : diminution par fuite de CBG • Hyperthyroïdie : augmentation par augmentation de la synthèse de CBG • La grossesse : même effet • Certains médicaments
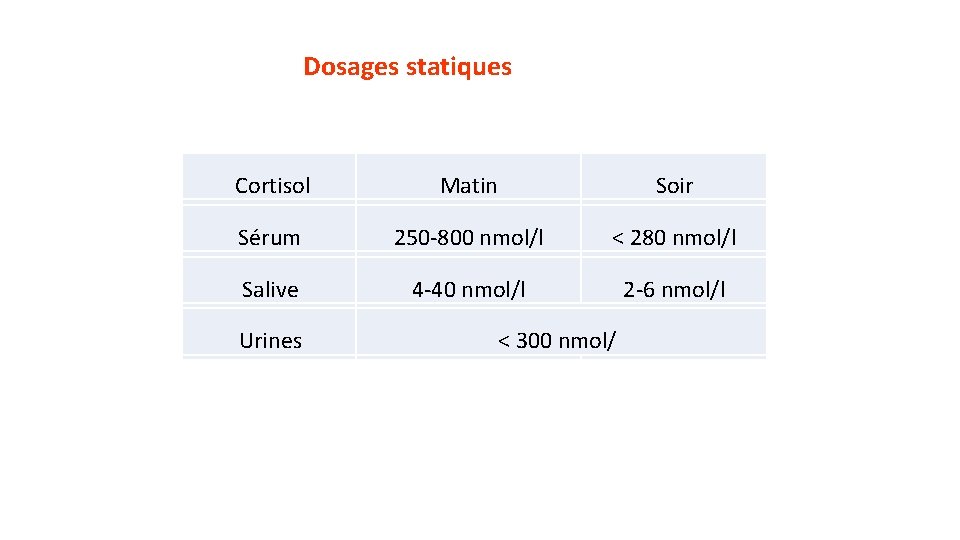
Dosages statiques Cortisol Matin Soir Sérum 250 -800 nmol/l < 280 nmol/l Salive 4 -40 nmol/l 2 -6 nmol/l Urines < 300 nmol/
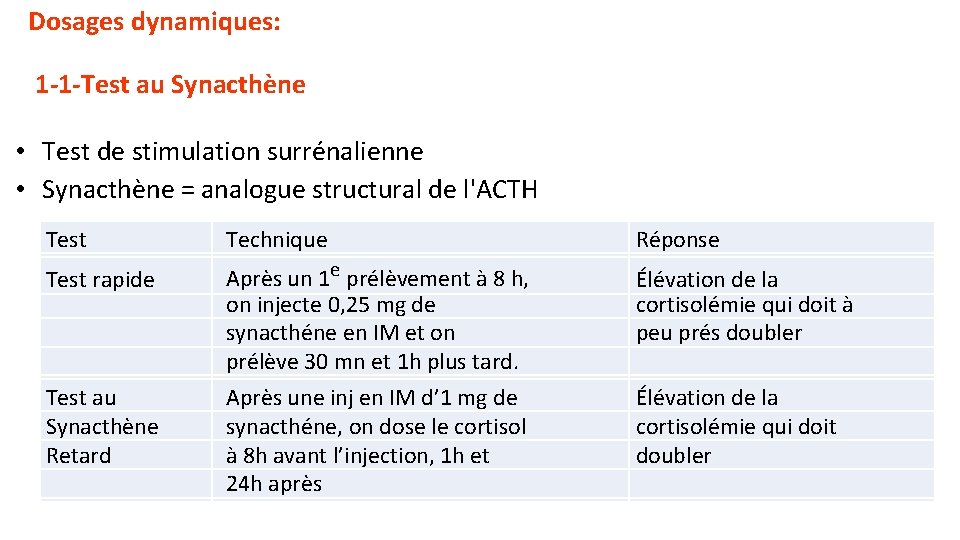
Dosages dynamiques: 1 -1 -Test au Synacthène • Test de stimulation surrénalienne • Synacthène = analogue structural de l'ACTH Test Technique Réponse Test rapide Après un 1 e prélèvement à 8 h, on injecte 0, 25 mg de synacthéne en IM et on prélève 30 mn et 1 h plus tard. Après une inj en IM d’ 1 mg de synacthéne, on dose le cortisol à 8 h avant l’injection, 1 h et 24 h après Élévation de la cortisolémie qui doit à peu prés doubler Test au Synacthène Retard Élévation de la cortisolémie qui doit doubler

Dosages dynamiques: Test à la métopirone • Test de stimulation de l’axe corticotrope, permet d’évaluer l’intégrité de l’axe hypothalamohypophysaire: test dangereux • Principe : – Blocage de la 11 b-hydroxylase – Diminution de la sécrétion de cortisol (pas de rétrocontrôle) – stimulation du CRF et de l’ACTH – Augmentation des produits en amont du site de blocage: 11 désoxycortisol ( composé S), 17 a OH P 4
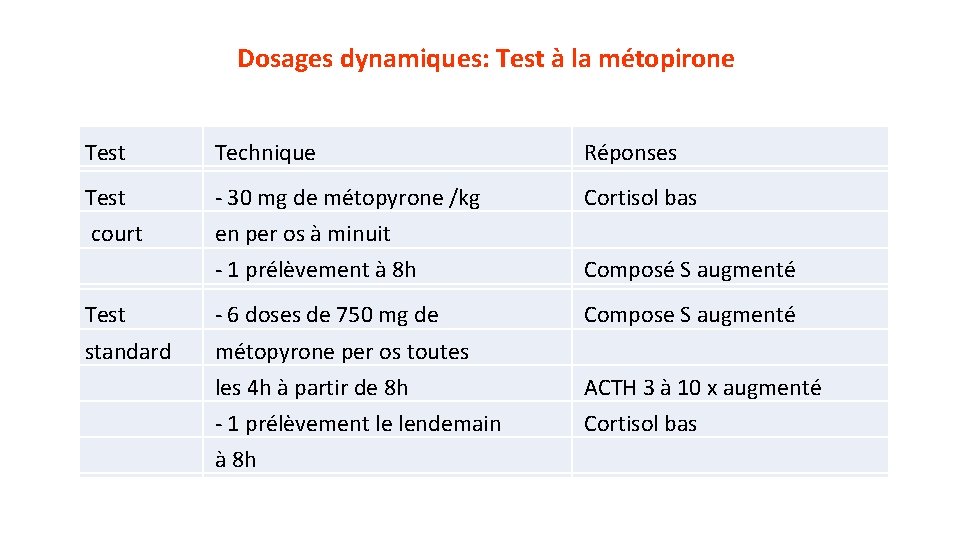
Dosages dynamiques: Test à la métopirone Test Technique Réponses Test - 30 mg de métopyrone /kg Cortisol bas court en per os à minuit - 1 prélèvement à 8 h Composé S augmenté Test - 6 doses de 750 mg de Compose S augmenté standard métopyrone per os toutes les 4 h à partir de 8 h ACTH 3 à 10 x augmenté - 1 prélèvement le lendemain Cortisol bas à 8 h

Dosages dynamiques: Autres tests Test Technique Réponse Test à l'insuline - 0, 1 UI en IV d’insuline ordinaire/ kg (5 UI/m 2) à 8 h - prélèvement à – 15’, 0’, 15’, 30’, 60’, 90’ et 120’ ACTH et cortisol augmentés à la suite de l’hypoglycémie Test à l'ADH -inj de 10 U à 8 h en IM -prélèvements à -15’, 0’, 15’, 30’, 60’ et 90’ ACTH et cortisol augmentés Test au CRH - inj IV 100 mg de CRH - prélèvements à – 15’, 0’, 15’, 30’, 60’, 90’ et 120’ ACTH et cortisol augmentés

Test de freinage: Test à la dexaméthasone • Principe: utilisation d’un corticoïde • qui freine l’axe hypothalamo-hypophysaire • ne croise pas dans le dosage du cortisol (Ex : Dexaméthasone Glucocorticoïde de synthèse ) • dose minimale discriminante pour freiner l’ACTH et ainsi le cortisol (test court 1 mg, ) ⇒ diagnostic du syndrome de Cushing • doses pharmacologiques pour diagnostic étiologique du syndrome de Cushing • Résultat: Diminution de l'ACTH et du cortisol.

Test de freinage: Test à la dexaméthazone Test Technique: dosage du cortisol et ACTH Réponse normale: Diminution du cortisol

Pathologies : • A – Les hypercorticismes • 1 - L'hypercorticisme primaire ou hypercorticisme ACTH-indépendant : Le syndrome de Cushing • 2 - Hypercorticisme secondaire ou hypercorticisme ACTH-dépendant : La maladie de Cushing • 3 - Les hypercorticismes tertiaires • B - Les Hypocorticismes • 1 - Hypocorticisme primaire • 1 -1 - l’insuffisance surrénale lente (ISL) ou chronique: Maladie d'Addison • 1 -2 - Hypocorticisme génétique • 2 - Hypocorticisme secondaire
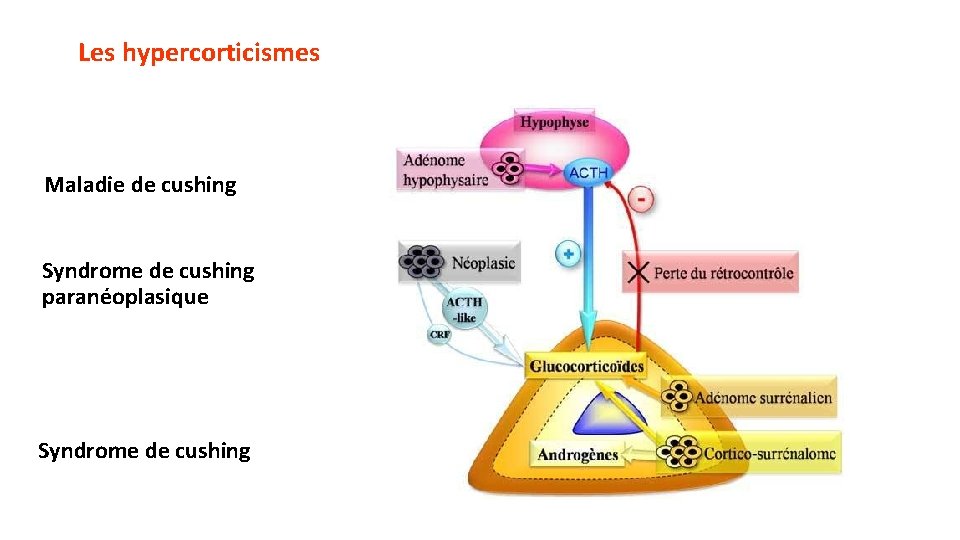
Les hypercorticismes Maladie de cushing Syndrome de cushing paranéoplasique Syndrome de cushing

Le syndrome de Cushing • Définition: • Hypersécrétion de cortisol par les corticosurrénales • Hypercorticisme primaire ou hypercorticisme ACTH-indépendant • Syndrome de Cushing = clinique + Anomalies biologiques • Inhibition de CRH et d'ACTH par rétrocontrôle négatif • Parfois associé avec hypersécrétion d'androgènes ou plus rarement d'aldostérone. • Les femmes plus touchées que les hommes (9/10)

• Causes: • Tumeurs bénignes des surrénales = adénomes • ne sécrètent que du cortisol • Tumeurs malignes = corticosurrénalomes sécrètent cortisol et androgènes

Clinique • Obésité facio-tronculaire • Visage arrondi • Accumulation de graisse au cou • bosse de bison ou buffalo neck. • Vergetures, etc. • Ecchymoses

Mise en évidence biologique de l'hypercorticisme • Dosages non hormonaux: • FNS: • Polynucléose neutrophile • Lymphopénie • Oesinopénie • Alcalose Hypokaliémique • Hyperglycémie • Hypercalciurie • Dyslipidémie: Hypercholestérolémie et hypertriglycéridémie

Mise en évidence biologique de l'hypercorticisme • Dosages hormonaux statiques: • Cortisol à 8 h élevé (fraction libre). • ACTH diminuée. • CRH diminué. • Rupture du rythme circadien ( valeurs 8 H = 16 H ) • Cortisolémie à minuit augmentée. • CLU augmenté ( 4 X la limite sup de la normale). • 17 OH stéroides élevés.
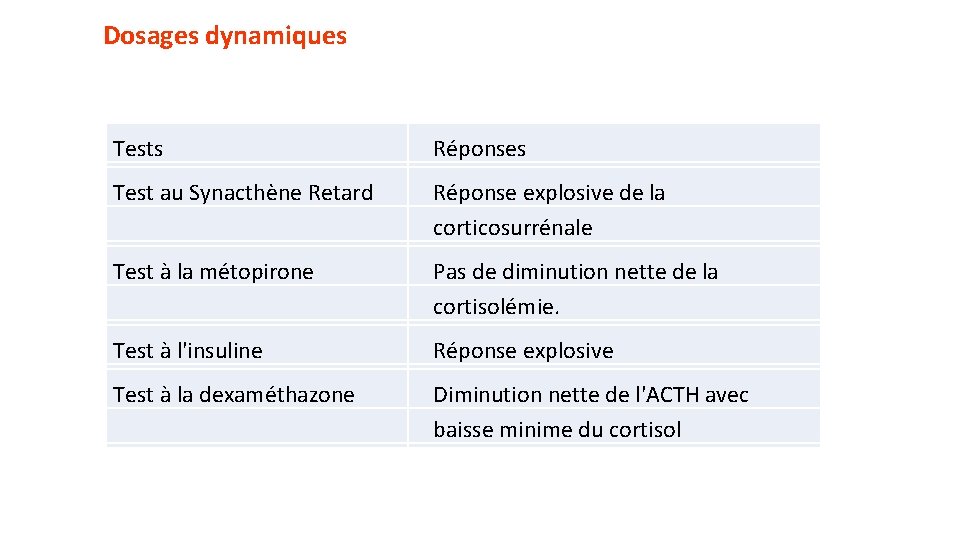
Dosages dynamiques Tests Réponses Test au Synacthène Retard Réponse explosive de la corticosurrénale Test à la métopirone Pas de diminution nette de la cortisolémie. Test à l'insuline Réponse explosive Test à la dexaméthazone Diminution nette de l'ACTH avec baisse minime du cortisol

Hypercorticisme secondaire • Hypercorticisme ACTH-dépendant: • Hyperplasie bilatérale des surrénales suite à une sécrétion excessive et inappropriée d'ACTH. • Cliniques • Mêmes signes d'hypercorticisme décrits • + Mélanodermie : due à la sécrétion de MSH (Mélanotropin Stimulating Hormon) stimule la production de mélanine et qui accompagne celle de l'ACTH

Hypercorticisme secondaire • 1 - L'ACTH d'origine eutopique (cellules corticotropes hypophysaires) • La Maladie de Cushing = adénomes corticotropes (micro-adénomes : 90 %). • Vu chez les femmes jeunes dans 80% des cas. • 2 - L'ACTH est d'origine ectopique (rare), • Syndrome de Cushing paranéoplasique (SCPN). • Produite par une tumeur non hypophysaire: • Tumeurs Neuro Endocrines (TNE) développés à partir des cellules neuroendocrines présentes dans de nombreux organes. • Siège variable mais bronchique ( 50%)

Biologie: • Dosages statiques : • Cortisol élevé (fraction libre). • ACTH élevée • CRH diminué. • Rupture du rythme circadien • CLU est augmenté • b - Dosages dynamiques : Tests Réponses Test au Synacthène Retard Réponse explosive de la corticosurrénale Test à la métopirone Réponse explosive de l’ACTH dans la M C Réponse négative de l’ACTH dans les SCPN Test au CRH Réponse explosive Test à l'ADH Réponse explosive

Les hypercorticismes tertiaires • L’atteinte de l'hypothalamus peut exister mais n'a pas été mise en évidence encore. • Une sécrétion ectopique exclusive de CRH à l'origine de l’ hypercorticisme est possible.

Les Hypocorticismes • Définition: • Ensemble des manifestations clinico-biologiques dues à la diminution du cortisol • Résultat: Déficit surrénalien • Réponse de l'hypophyse • Sécrétion de l'ACTH: Stimule la surrénale. • Sécrétion de MSH (de mélanine) = • Mélanodermie = teinte bronzée de la peau

Hypocorticisme primaire • L’insuffisance surrénale lente (ISL) ou chronique: Maladie d'Addison • Due à une destruction de 85 à 90 % du tissu surrénalien: • Rétraction corticale : maladie auto-immune avec auto-anticorps antisurrénale parfois associée à d'autres maladies auto-immunes (thyroïdite, anémie de Biermer); • la tuberculose. • Autres causes (destruction des corticosurrénales): métastases de cancers, syphilis, hémochromatose, amylose, ablation traumatique ou chirurgicale des glandes surrénales. . . • Si cause non retrouvée: Maladie d’Addison "idiopathique".

Hypocorticisme primaire • Clinique: • Asthénie profonde • Hypotension artérielle • Mélanodermie • Biologie: • Ionogramme sanguin: • Hyponatrémie • hypochlorémie • Hyperkaliémie • Anémie • Hypoglycémie • Urée augmentée
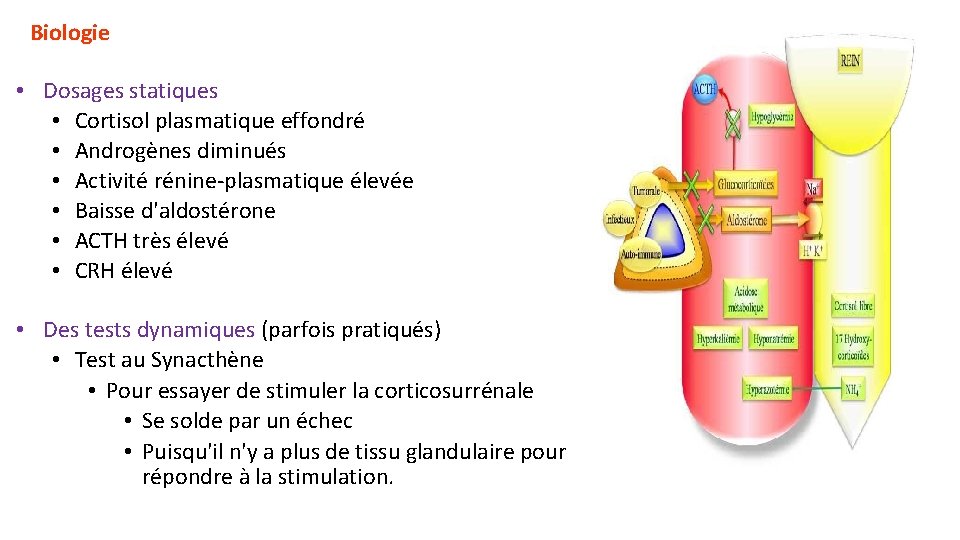
Biologie • Dosages statiques • Cortisol plasmatique effondré • Androgènes diminués • Activité rénine-plasmatique élevée • Baisse d'aldostérone • ACTH très élevé • CRH élevé • Des tests dynamiques (parfois pratiqués) • Test au Synacthène • Pour essayer de stimuler la corticosurrénale • Se solde par un échec • Puisqu'il n'y a plus de tissu glandulaire pour répondre à la stimulation.

Hypocorticisme secondaire : • Insuffisances surrénales secondaires : • Causes: Destruction des neurones à ACTH • Consécutives à une corticothérapie (cortisoniques antiinflammatoires) mettant par rétro-contrôle négatif la surrénale au repos et se révélant à l'arrêt du traitement; • Liées à des lésions de l'hypophyse (panhypopituitarisme) où c'est l'absence d'ACTH qui provoque la mise au repos de la corticosurrénale. • Liées à des affections touchant indirectement l'axe hypothalamohypophyso-surrénalien (anémies prolongées, diarrhées chroniques, myxœdème. . . )
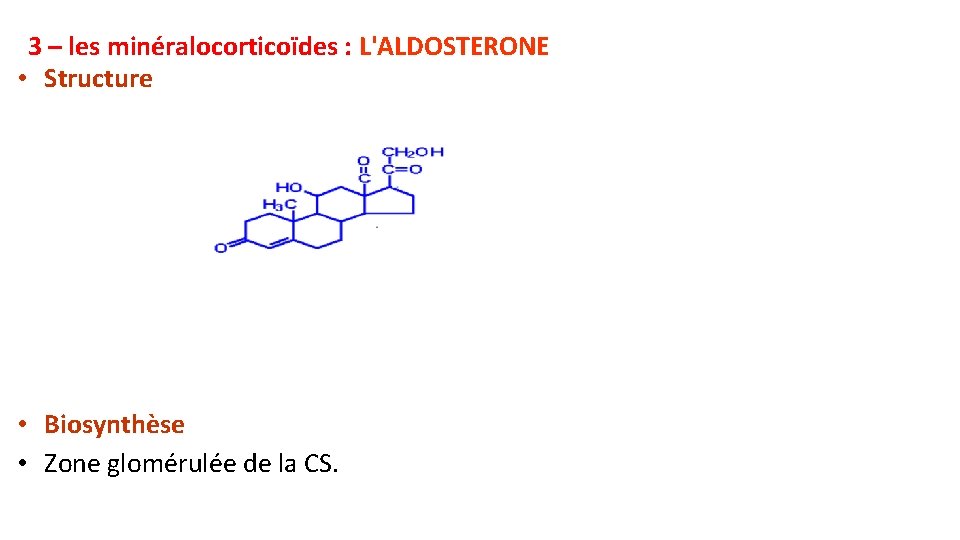
3 – les minéralocorticoïdes : L'ALDOSTERONE • Structure • Biosynthèse • Zone glomérulée de la CS.

Actions physiologiques • Action au niveau du rein (sur les parties terminales du néphron), de l'intestin et sur le côlon. • = Permet d’ajuster l'excrétion du sodium et du potassium en permettant: • la réabsorption du Na+ et l’élimination du K+. • Action sur la volémie. • Participe au maintient de la pression artérielle par réabsorption d'eau / Na+ au niveau du rein. • Rôle dans l'équilibre acido-basique.
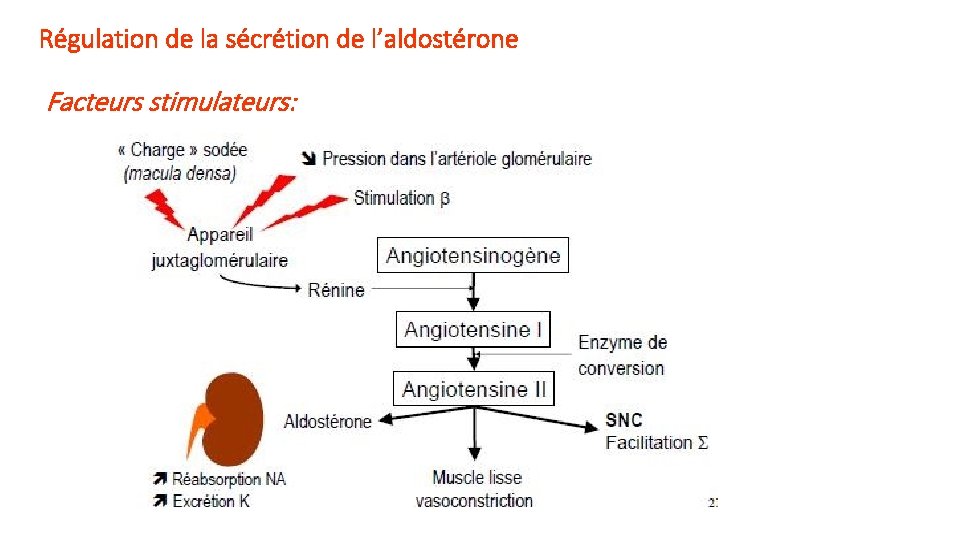
Régulation de la sécrétion de l’aldostérone Facteurs stimulateurs:

Régulation de la sécrétion de l’aldostérone Facteurs stimulateurs: • 2 - La kaliémie : Stimuli spécifique • L'aldostérone varie dans le même sens que la kaliémie. • La volémie: Baisse de la volémie = S+ l'aldostérone. • 3 - L'ACTH • Stimule les enzymes de la biosynthèse • Augmente la sécrétion de l'aldostérone jusqu'à un certain seuil limite qui ne peut être dépassé • Noter: • La libération de l'aldostérone est stimulée par : • Hyponatrémie. • Hyperkaliémie. • Hypovolémie. • Le cortisol et les œstrogènes S+ la synthèse de l'angiotensinogène.

Régulation de la sécrétion de l’aldostérone Facteurs inhibiteurs: • L'ANP (Atrial Natriuretic Peptide) • Hormone d'origine cardiaque (oreillette gauche) • Inhibe la libération d'aldostérone et de rénine • Favorise l'élimination du Na+. • La progestérone et la 17 - alpha (OH) P 4 • Inhibiteurs compétitifs de l'aldostérone • peuvent se fixer sur ses récepteurs et les bloquer

Biologie • Dosages non hormonaux • Ionogramme sanguin et urinaire et les gaz du sang. • Dosages hormonaux • Angiotensinogéne • Aldostéronémie • Activité rénine plasmatique • Rénine active • Rénine totale • Prorénine • Aldostérone urinaire • Aldostéronurie p. HI.
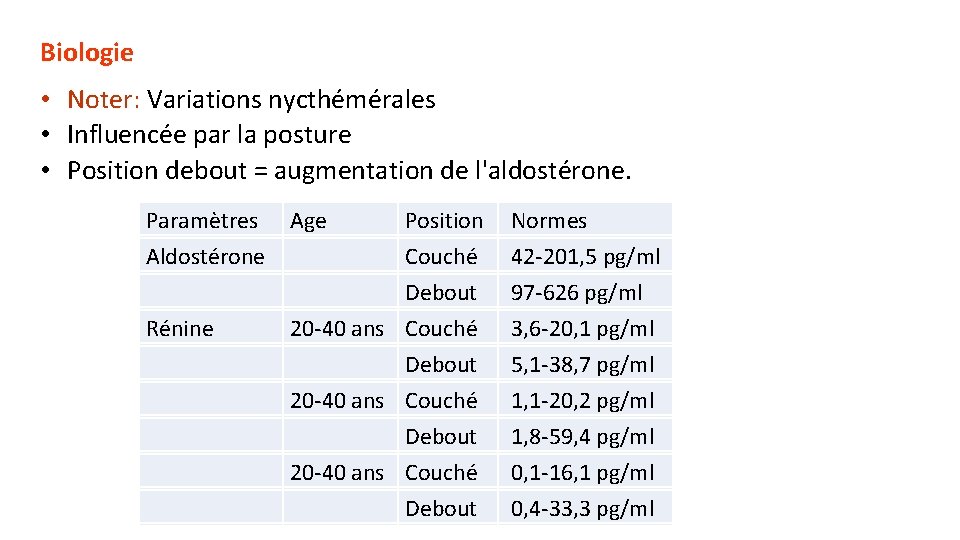
Biologie • Noter: Variations nycthémérales • Influencée par la posture • Position debout = augmentation de l'aldostérone. Paramètres Aldostérone Rénine Age Position Couché Debout 20 -40 ans Couché Debout Normes 42 -201, 5 pg/ml 97 -626 pg/ml 3, 6 -20, 1 pg/ml 5, 1 -38, 7 pg/ml 20 -40 ans Couché Debout 1, 1 -20, 2 pg/ml 1, 8 -59, 4 pg/ml 20 -40 ans Couché Debout 0, 1 -16, 1 pg/ml 0, 4 -33, 3 pg/ml

Tests dynamiques • Test d’orthostatisme • Mesures de le rénine et de l’aldostérone , • le matin, après 2 H de décubitus puis après 1 H d’orthostatisme • Activité rénine stimulée → ↗ de la rénine et de l’aldostérone • Perfusion salée • Etude de la variation de l’aldostérone au cours d’une expansion volémique • Perfusion de 2 L de sérum physiologique en 4 H → Dosage de l’aldostérone à t=0 et à la fin de la perfusion • ↘ Aldostérone • Test au Captopril (1 mg/kg) • inhibition de l’enzyme de conversion ↘ Aldostérone →↗ activité rénine

PATHOLOGIE • 1) Les hyperaldostéronismes: • a) Les hyperaldostéronismes primaires: le syndrome de CONN. • b) Les hyperaldostéronismes secondaires • 2) Les hypoaldostéronismes: • a) Les hypoaldostéronismes Primaires. • b) Les hypoaldostéronismes secondaires.

Les hyperaldostéronismes primaires: le syndrome de CONN. • Définition: hypersécrétion primitive d'aldostérone • Causes: • Tumeur bénigne de la cortico-surrénale (adénome de Conn) dans 80% des cas • Hyperplasie bilatérale des surrénales. • Clinique: • La femme est plus touchée que l'homme • Vers 30 à 50 ans. Hypertension artérielle permanente
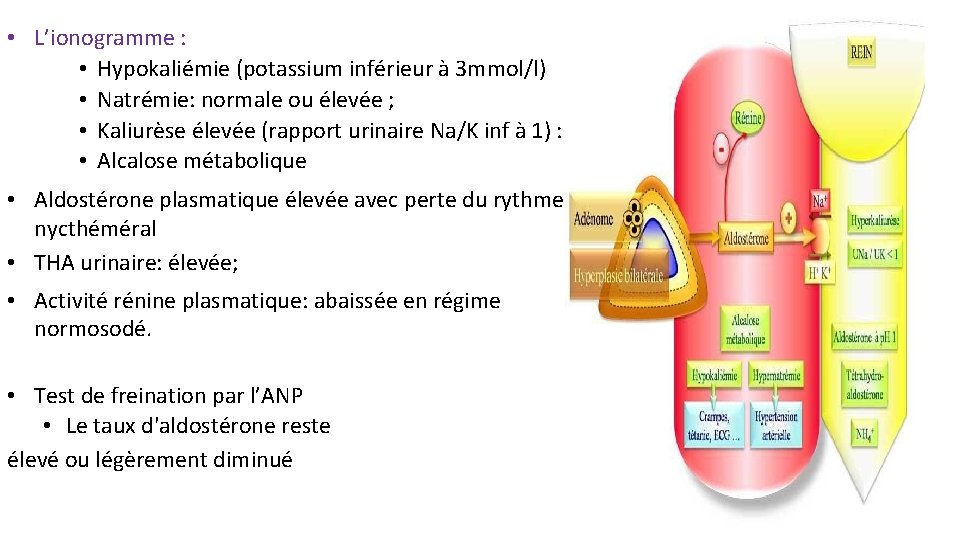
• L’ionogramme : • Hypokaliémie (potassium inférieur à 3 mmol/l) • Natrémie: normale ou élevée ; • Kaliurèse élevée (rapport urinaire Na/K inf à 1) : • Alcalose métabolique • Aldostérone plasmatique élevée avec perte du rythme nycthéméral • THA urinaire: élevée; • Activité rénine plasmatique: abaissée en régime normosodé. • Test de freination par l’ANP • Le taux d'aldostérone reste élevé ou légèrement diminué

Les Hyperaldostéronismes secondaires • Production tumorale de rénine. • Hypovolémie. • Hyponatrémie (dans les fistules digestives). • Hyperproduction d'angiotensinogène secondaire à la prise d’œstrogènes • L'activité natriurètique des progestatifs = élévation de la rénine qui S+ l'aldostéro • Trouble de libération de l'ANP. Différences entre Iaire et IIaire
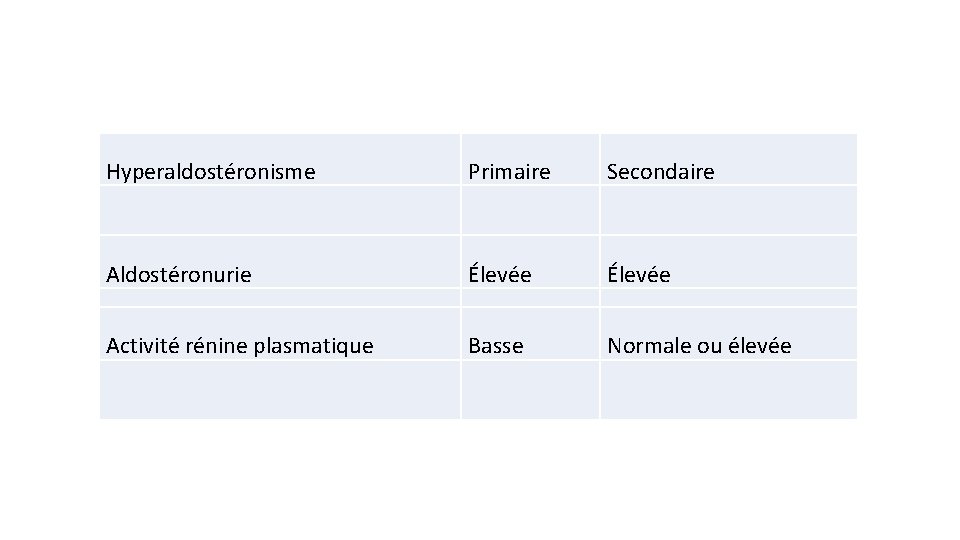
Hyperaldostéronisme Primaire Secondaire Aldostéronurie Élevée Activité rénine plasmatique Basse Normale ou élevée

Les hypoaldostéronismes • Primaires • Causes: • Insuffisance surrénalienne chronique, tuberculose souvent associée à un hypocorticisme primaire et à une hypoandrogénie. • Génétique (bloc enzymatique par déficit génétique) total ou partiel; + syndrome de perte de sels glt isolé. • Biologie : • Hyponatrémie avec Hyperkaliémie • Hypernatriurie avec Hypokaliurie • Aldostéronémie basse • Activité rénine plasmatique augmentée • Secondaires sont dues à un hyporéninisme par: • Atteinte rénale ou Insuffisance hépatique sévère; absence d'angiotensinogène

4 - Les androgènes surrénaliens • Les androgènes sont des hormones de nature stéroïdes qui provoquent l’apparition des caractères sexuels masculin. • Synthétisés chez l’homme et chez la femme. • Lieux de synthèse: • La corticosurrénale: la couche réticulée • Certains androgènes sont sécrété à la fois par la corticosurrénale et par les gonades : DHA, androstènedione. • D'autres ne sont sécrétés que par la corticosurrénale : le SDHEA. • Les androgènes surrénaliens sont sécrétés sous l’influence de l’ACTH mais ne participent pas au rétrocontrôle hypophysaire. • Les gonadotrophines n’ont aucun effet sur la sécrétion des androgènes surrénaliens.

• Exploration : - Etude de l’imprégnation androgénique sur les récepteurs : pilosité, organes génitaux externes, libido. Dosage sanguin du DHEAS (spécifique de la production surrénale) et également de la DHEA, de l’androstenedione, de la testostérone Dasages urinaires des 17 CS (homme : 9 – 17 mg/24 h, femme : 5 – 14 mg/24 h). • Pathologies : A. Hypofonctionnements corticosurrénaliens : Définition : affection s’accompagnant d’un défaut progressif ou brutal de sécrétion des hormones corticosurrénales (minéralocorticoïdes, glucocorticoïdes, androgènes) et accessoirement médullosurrénales. Cette insuffisance peut être : - Primitivement surrénale : complète, réalisant la maladie d’Addison, ou dissociée - Secondaire à une insuffisance antéhypophysaire ou à une corticothérapie prolongée. Les insuffisances corticosurrénaliennes s’expriment selon deux modalités : Lentes OU Aiguës

• B. Hyperfonctionnements corticosurrénaliens : • �Hypercorticismes purs : syndrome de Cushing : Définit l’ensemble des signes cliniques qui surviennent à la suite d’une sécrétion chronique excessive des concentrations de cortisol circulant et la perte de ses variations nycthémérales quelle qu’en soit l’étiologie. . Signes cliniques : obésité tronculaire, faciès lunaire, vergetures, ecchymoses, hypertension et intolérance au glucose. Diagnostic biologique : Caractère excessif de la sécrétion de cortisol Rupture du rythme circadien Perte de rétrocontrôle des corticoïdes exogènes sur la sécrétion • Physiopathologie : - Hypersécrétion d’hormones glucocorticoïdes - 4 causes : �Deux causes sont ACTH-dépendantes : induction d’hypercortisolisme par hypersécrétion d’ACTH. - Adénome hypophysaire corticotrope (maladie de Cushing) : hyperplasies bilatérales des surrénales d’origine hypothalamo-hypophysaire. - Hypersécrétion ectopique d’ACTH-like (syndrome paranéoplasique) �Deux causes sont ACTH-indépendant et entraînant un hypercortisolisme par sécrétion directe de cortisol : - Adénome bénin d’une surrénale - Corticosurrénalome malin
- Slides: 66