Fmtan anyagvizsglat 1 1 Az anyagot az ember

Fémtan, anyagvizsgálat 1 1

Az anyagot az ember nyeri ki a természetből és alakítja olyanná, ami az igényeknek leginkább megfelel. 2
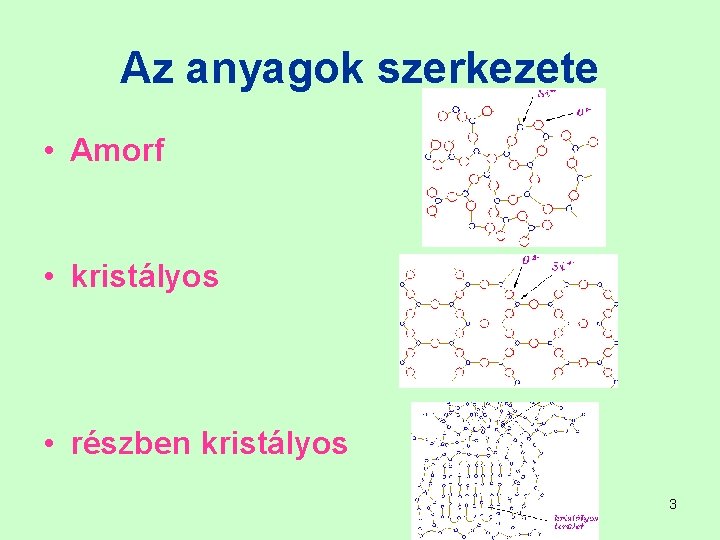
Az anyagok szerkezete • Amorf • kristályos • részben kristályos 3

Fémek Fkristályos szerkezetűek, Fkiváló hő-és elektromos vezetők Ffémes fényűek Fképlékenyen alakíthatók Fterhelhetőséggel, szilárdsággal rendelkeznek 4

Kerámiák F szerkezetük rövid távon rendezett F rossz hő-és elektromos vezetők F nagy a villamos ellenállásuk, az ellenállás a hőmérséklet növelésével általában csökken F nagy hőállósággal rendelkeznek F kis a hősokkállóság F kemények, ridegek 5

Kompozitok • Az előző csoportok felhasználásával Fszemcsés Ftekercselt, Flaminált, Fszálerősített, tervezett felépítésű anyagok. • Tulajdonságaik jelentősen függnek az alkotók tulajdonságaitól, és a kompozit szerkezetétől. 6

Kötésfajták • Elsődleges vagy primér kötés – ionos – kovalens – fémes • Másodlagos, gyenge – molekulaközi Van der Waals – hidrogénkötés 7
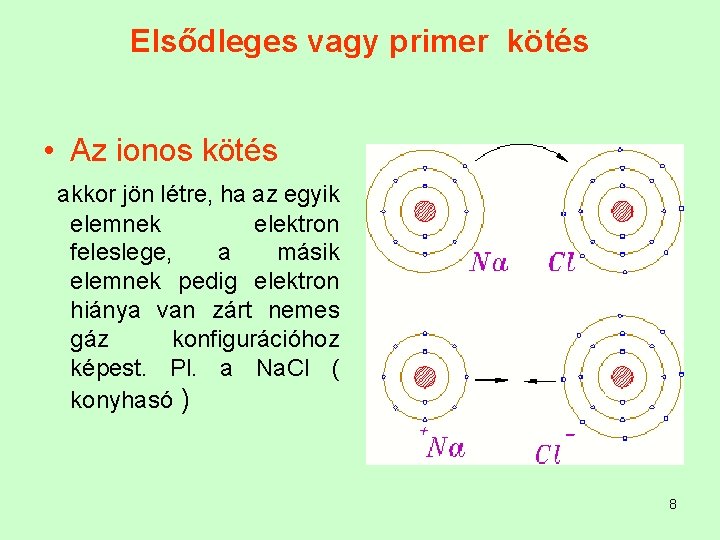
Elsődleges vagy primer kötés • Az ionos kötés akkor jön létre, ha az egyik elemnek elektron feleslege, a másik elemnek pedig elektron hiánya van zárt nemes gáz konfigurációhoz képest. Pl. a Na. Cl ( konyhasó ) 8
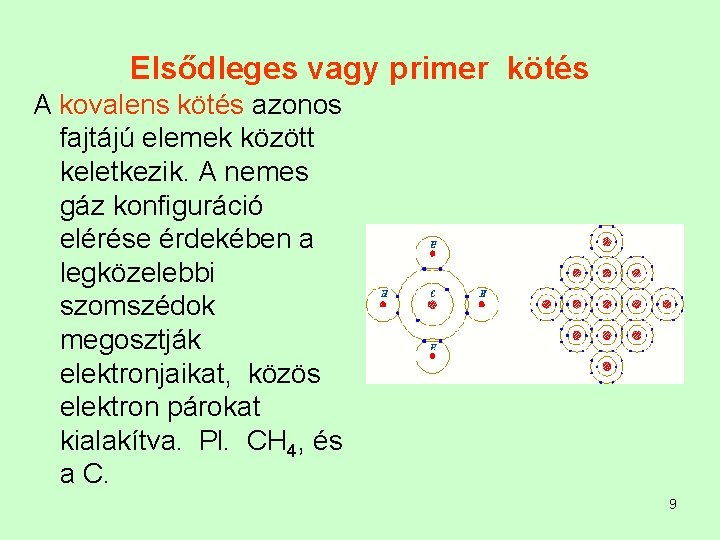
Elsődleges vagy primer kötés A kovalens kötés azonos fajtájú elemek között keletkezik. A nemes gáz konfiguráció elérése érdekében a legközelebbi szomszédok megosztják elektronjaikat, közös elektron párokat kialakítva. Pl. CH 4, és a C. 9
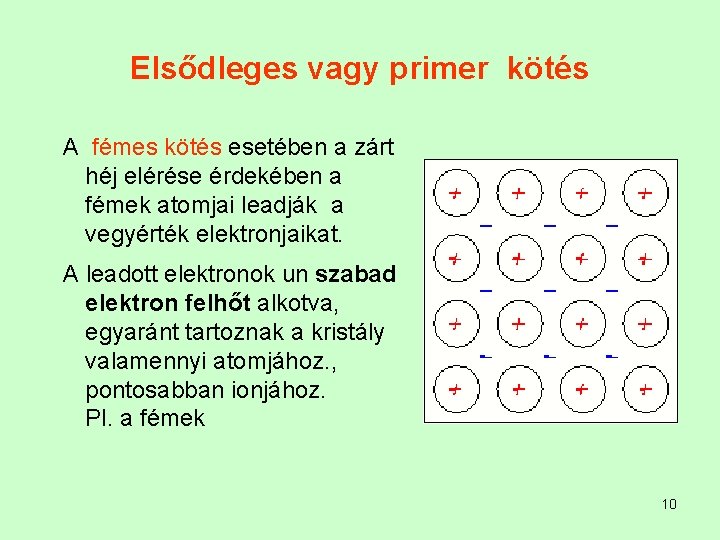
Elsődleges vagy primer kötés A fémes kötés esetében a zárt héj elérése érdekében a fémek atomjai leadják a vegyérték elektronjaikat. A leadott elektronok un szabad elektron felhőt alkotva, egyaránt tartoznak a kristály valamennyi atomjához. , pontosabban ionjához. Pl. a fémek 10
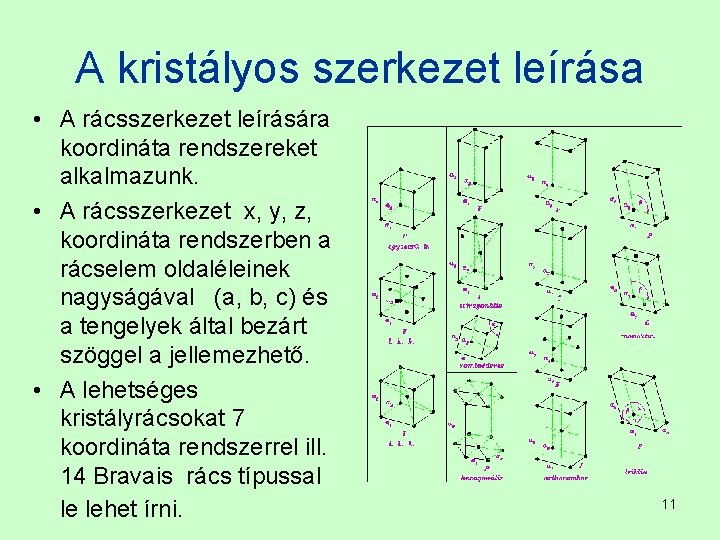
A kristályos szerkezet leírása • A rácsszerkezet leírására koordináta rendszereket alkalmazunk. • A rácsszerkezet x, y, z, koordináta rendszerben a rácselem oldaléleinek nagyságával (a, b, c) és a tengelyek által bezárt szöggel a jellemezhető. • A lehetséges kristályrácsokat 7 koordináta rendszerrel ill. 14 Bravais rács típussal le lehet írni. 11

Kristályos szerkezet • A kristályos szerkezetben az atomok szabályos geometriai rendben helyezkednek el. • Azt a legkisebb - több atomból álló szabályos idomot, melynek ismételgetésével a rácsszerkezet leírható a rácselemnek , vagy elemi cellának nevezzük. 12

Köbös vagy szabályos rendszer • • Egyszerű vagy primitív (Po) Térközepes Lapközepes gyémántrács 13

Térközepes köbös rácsszerkezet 14
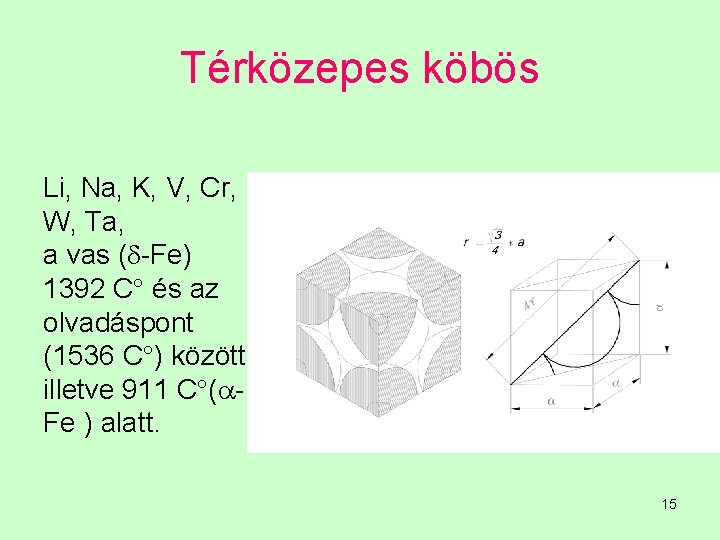
Térközepes köbös Li, Na, K, V, Cr, W, Ta, a vas ( -Fe) 1392 C és az olvadáspont (1536 C ) között illetve 911 C ( Fe ) alatt. 15

Lapközepes köbös rácsszerkezet 16
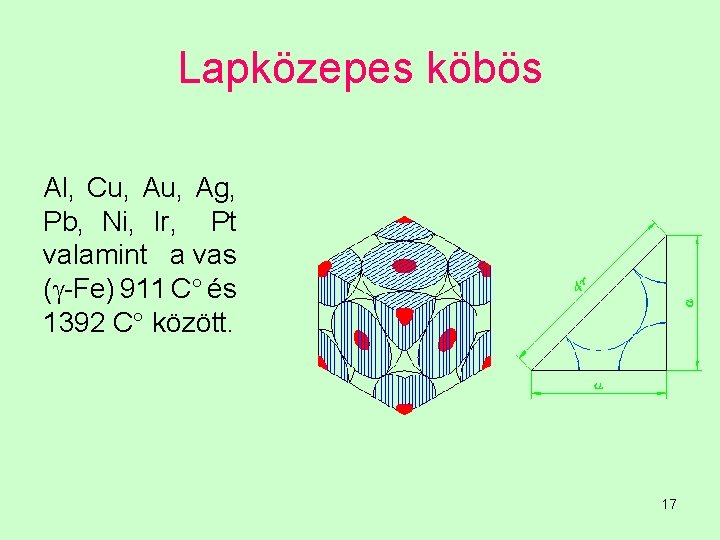
Lapközepes köbös Al, Cu, Ag, Pb, Ni, Ir, Pt valamint a vas ( -Fe) 911 C és 1392 C között. 17
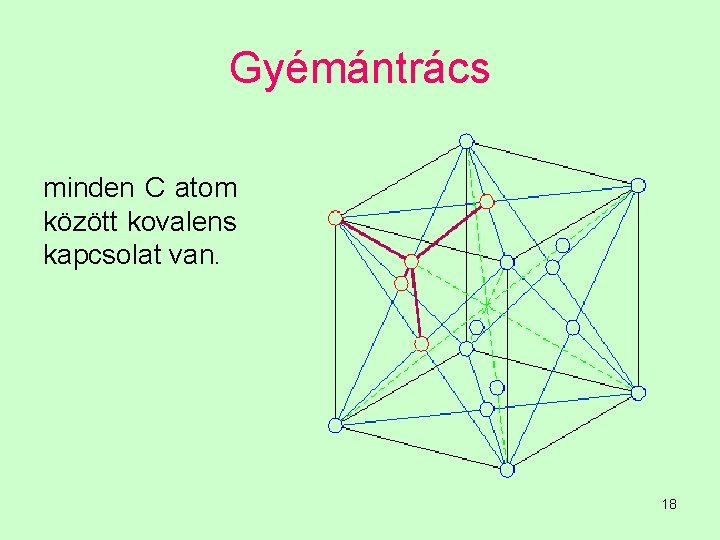
Gyémántrács minden C atom között kovalens kapcsolat van. 18

Hexagonális rácsszerkezet 19
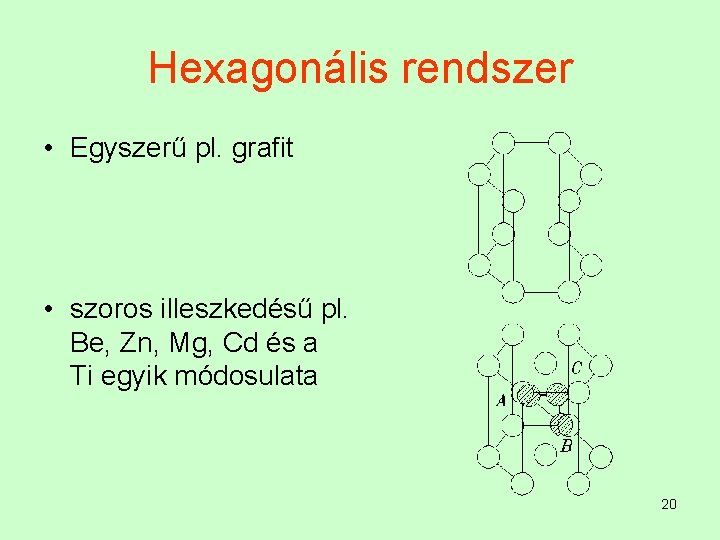
Hexagonális rendszer • Egyszerű pl. grafit • szoros illeszkedésű pl. Be, Zn, Mg, Cd és a Ti egyik módosulata 20

Kristályosodás A kristályos szerkezet rácselemekből épül fel, melynek alakja változatosésjellegzetes. Az ionos és kovalens kötéssel rendelkező anyagok, az ásványok, kerámiák kristályainak külső alakja formatartó, magán viseli a rácstípus jellegzetességeit. Ezek az egyedülálló kristályok az egykristályok. 21

Fémkristályok, krisztallitok • A fémek esetében csak speciális hűtési módszerrel tudunk egykristályokat kialakítani. Bármely fémdarabot megnézve azon a kristályosság nem fedezhető fel. • Ezek a krisztallitok 22

Olvadék dermedése az olvadékban az atomok összekapcsolódásával kristálycsirák képződnek. A kristályosodás során a meglévő csirákhoz további atomok kapcsolódnak, a csirák növekedni kezdenek. Növekedés közben a szomszédos, szabályos lapokkal határolt kristályok egymásba érve akadályozzák egymást, így szabálytalan határfelületekkel határolt szemcsék un. krisztallitok keletkeznek. 23

Olvadék dermedése 24

Kristályosodás A kristályosodás, a krisztallitok jellege és mérete a kristályosodási képességtől, vagy csiraképződéstől, és a kristályok növekedésének sebességétől függ. Mindkét tényezőt befolyásolja az olvadásponthoz képesti túlhűtés mértéke. 25
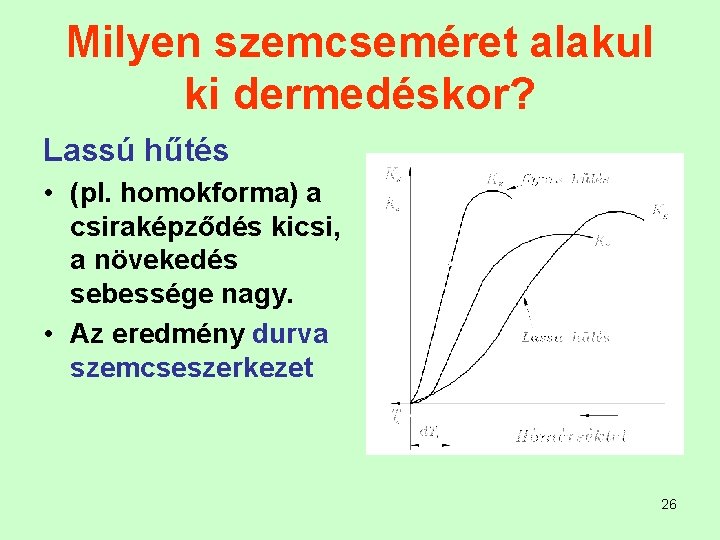
Milyen szemcseméret alakul ki dermedéskor? Lassú hűtés • (pl. homokforma) a csiraképződés kicsi, a növekedés sebessége nagy. • Az eredmény durva szemcseszerkezet 26

Milyen szemcseméret alakul ki dermedéskor? Gyors hűtés • (pl. fémforma, kokilla) a csiraképződés nagy, a növekedés sebessége nagy. • Az eredmény finom szemcseszerkezet 27

28
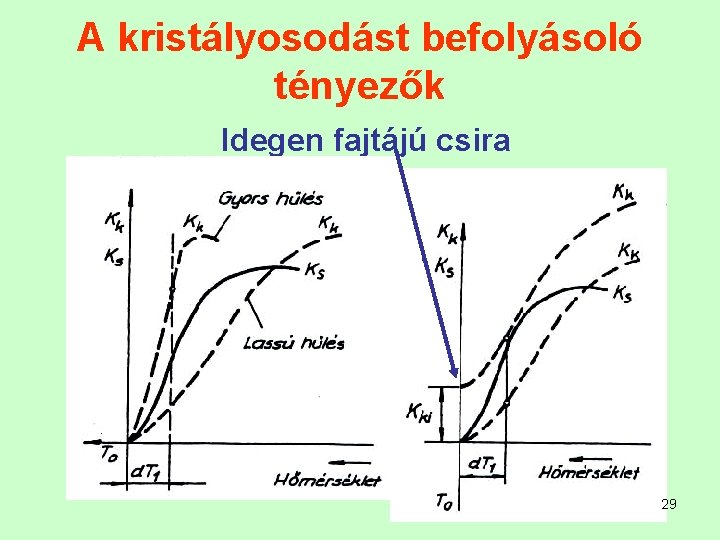
A kristályosodást befolyásoló tényezők Idegen fajtájú csira 29
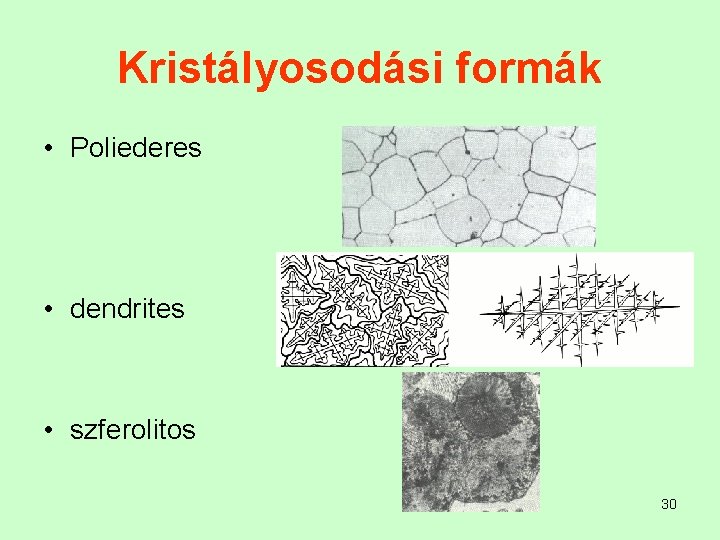
Kristályosodási formák • Poliederes • dendrites • szferolitos 30

Diffúzió A fémekben lejátszódó diffúzió alatt az atomoknak a szilárd fémben való mozgását értjük, mely koncentráció változást idéz elő. Hajtóerő a koncentráció ill. a szabadenergia különbség 31

A színfémek és ötvözetek termikus viselkedése Alapfogalmak 32

Színfémek és ötvözetek • Színfém • ötvözet= olyan , legalább látszatra egynemű, fémes természetű elegy, amelyet két vagy több fém összeolvasztása, vagy egymásban való oldása utján nyerünk. FAlapfém Fötvöző Fszennyező 33

Az ötvözetek szerkezete, fázisai • színfém, • szilárdoldat • vegyület Ezek a kristályos fázisok előfordulhatnak önállóan, mint egy fázisú szövetelemek, de alkothatnak egymással kétfázisú heterogén szövetelemeket is (eutektikum, eutektoid) 34
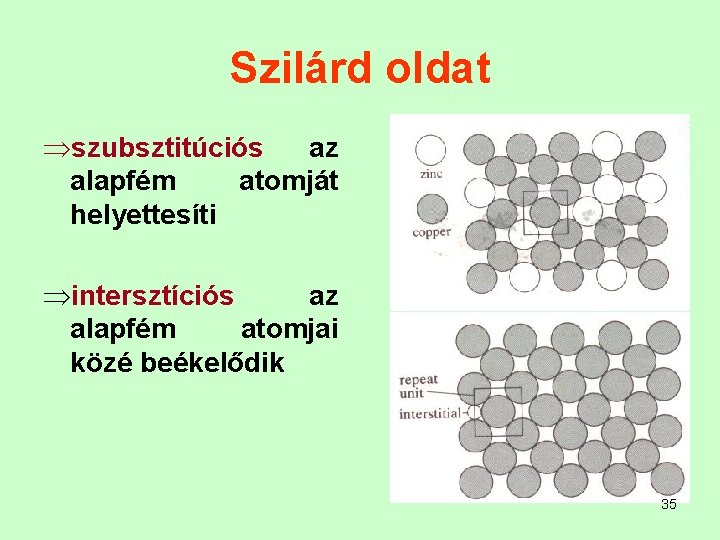
Szilárd oldat Þszubsztitúciós az alapfém atomját helyettesíti Þintersztíciós az alapfém atomjai közé beékelődik 35

Az oldódás lehet: • Korlátlan, ha: (csak szubsztitúciós) - azonos a rácsszerkezet - atomátmérőben 14 - 15 % -nál nem nagyobb az eltérés - azonos a vegyérték • Korlátozott ( csak meghatározott százalékig) a b 36

Fémvegyület • Ionvegyületek pl. Na. Cl, Ca. F 2 , Zn. S • elektronvegyület pl. Cu. Zn, Cu 5 Zn 8, Cu. Zn 3 vagy Ag. Zn, Cu 5 Si • intersztíciós vegyület pl. A 4 B, A 2 B, AB vagy AB 2 lehet vagy ilyen pl. a Fe 3 C, Mn 7 C 3 37

Az ötvözet alkotó nem oldják egymást Ha az ötvözet alkotói nem oldják egymást szilárd állapotban az ötvözetrendszerben megjelenik az eutektikum 38

A fémek és ötvözeteik egyensúlya Vizsgálatainkat az anyagnak a külvilágtól elkülönített részén az un. rendszerben végezzük. A rendszer az anyagnak a külvilágtól megfigyelés céljából elkülönített része. – Homogén vagy egyfázisú – heterogén vagy többfázisú • A rendszer homogén, önálló határoló felületekkel elkülöníthető része a fázis. Jele: F 39
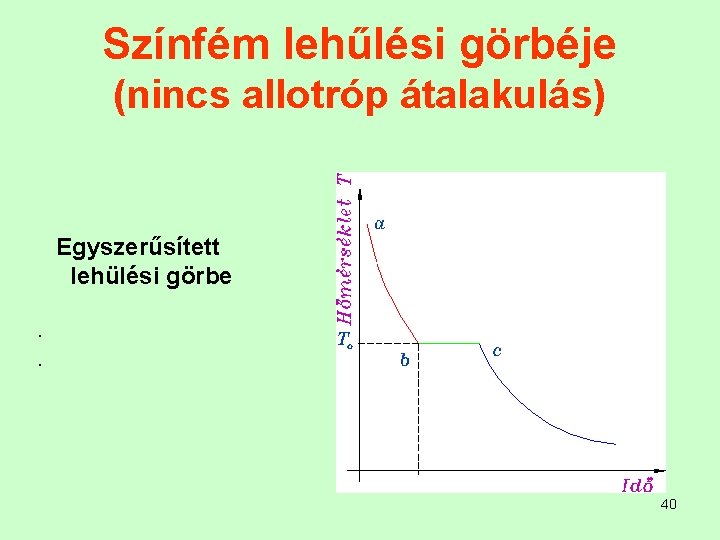
Színfém lehűlési görbéje (nincs allotróp átalakulás) Egyszerűsített lehülési görbe. . 40
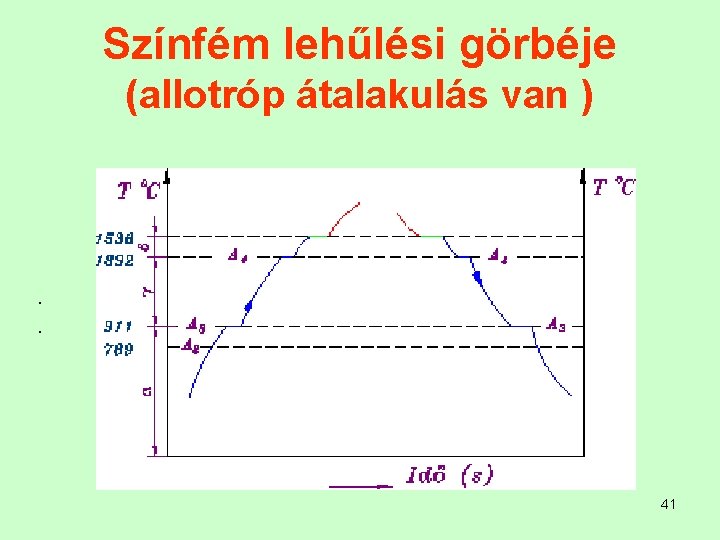
Színfém lehűlési görbéje (allotróp átalakulás van ) . . 41
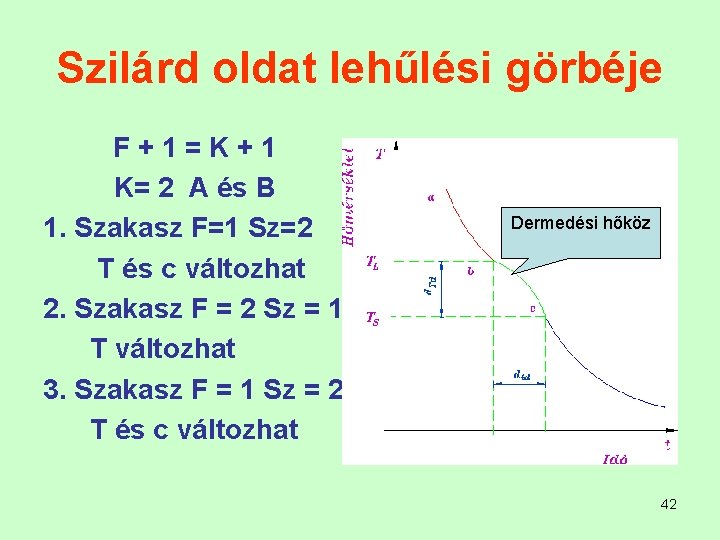
Szilárd oldat lehűlési görbéje F+1=K+1 K= 2 A és B 1. Szakasz F=1 Sz=2 T és c változhat 2. Szakasz F = 2 Sz = 1 T változhat 3. Szakasz F = 1 Sz = 2 T és c változhat Dermedési hőköz 42

Vegyület lehűlési görbéje A vegyületek (Am. Bn) keletkezhet un. nyílt maximummal, azaz egy állandó hőmérsékleten dermed és olvad a vegyület, ami a színfémmel azonos lehűlési görbét eredményez. • A vegyület peritektikus képződése azt jelenti, hogy a vegyület egy állandó hőmérsékleten egy nagyobb olvadás-dermedéspontú szilárdfázisból és egy meghatározott összetételű olvadék fázisból keletkezik. A lehűlési görbe ebben az esetben is vízszintes, mert a folyamatban F = 3 , SZ = 0 és így T = állandó. 43
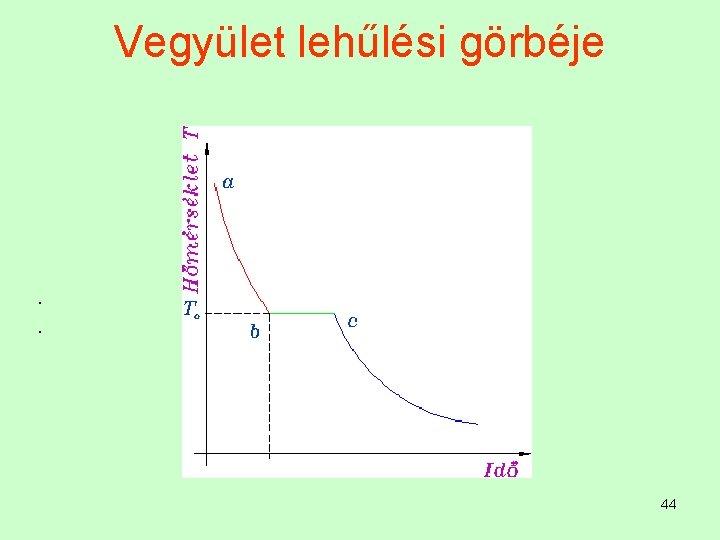
Vegyület lehűlési görbéje . . 44

Kétalkotós egyensúlyi diagramok A fémek és ötvözeteik viselkedésének vizsgálata a lehűlési görbék segítségével megtehető. Ha azonban két fém minden lehetséges összetételét akarjuk tanulmányozni, olyan diagramot kell felvennünk, ahol az összes lehetséges lehűlési görbe jellemzőit fel tudjuk tüntetni. Az ilyen diagramot egyensúlyi diagramnak vagy állapot ábrának nevezzük. 45

Kétalkotós egyensúlyi diagramok Az egyensúlyi diagram vízszintes tengelyén az A és B alkotó összes lehetséges koncentrációi vannak feltüntetve. Ez az alapvonal koncentráció egyenes - hossza 100 % nak felel meg. A vonal egyik vég pontja a tiszta A (100 % A) , a másik vég pontja a tiszta B (100 % B) alkotónak felel meg. A közbenső pontok, A-tól B felé haladva a két alkotó %-át mutatják. A függőleges 46 tengelyre a hőmérsékletet visszük fel.
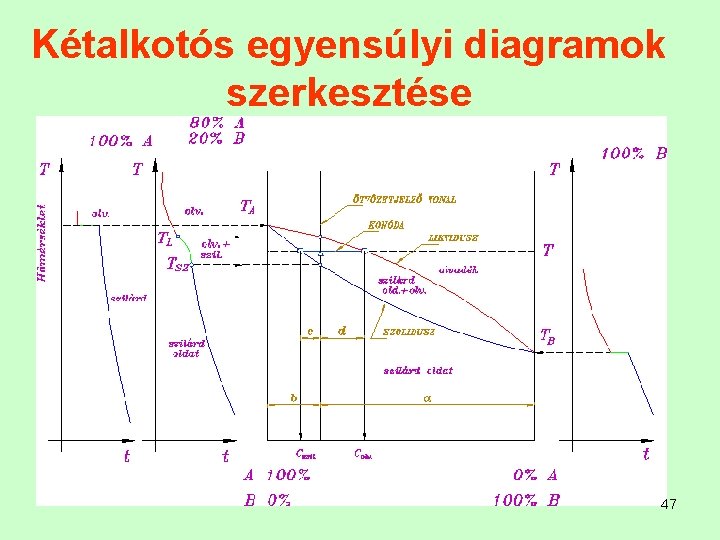
Kétalkotós egyensúlyi diagramok szerkesztése. . 47

Az egyensúlyi diagramok értelmezése adott ötvözetben és adott hőmérsékleten az alábbi kérdéseket kell megválaszolni az egyensúlyi diagramok segítségével: - milyen fázis, vagy fázisok találhatók - milyen az adott fázis, vagy fázisok összetétele, koncentrációja - mennyi a fázis, vagy fázisok mennyisége 48
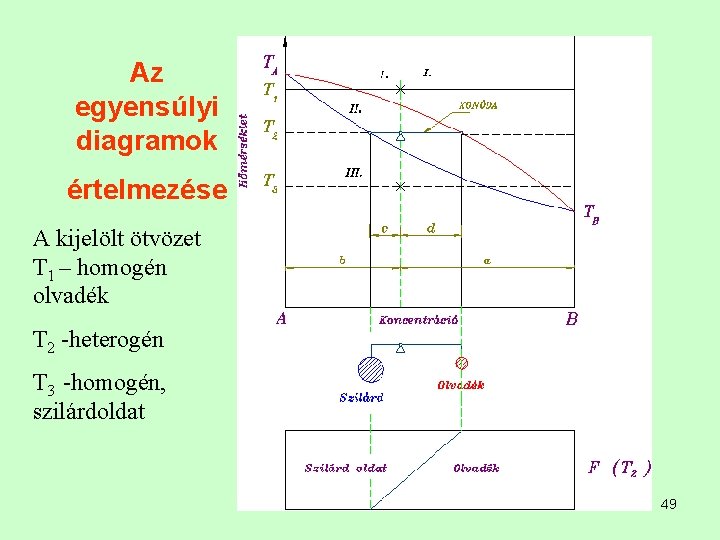
Az egyensúlyi diagramok értelmezése A kijelölt ötvözet T 1 – homogén olvadék T 2 -heterogén T 3 -homogén, szilárdoldat 49

Heterogén, kétfázisú területben Az ötvözetet a hőmérséklet jelző izotermának a likvidusz és szolidusz vonallal határolt részén az un konóda jellemzi. Két végpontja a két fázist mutatja. 50
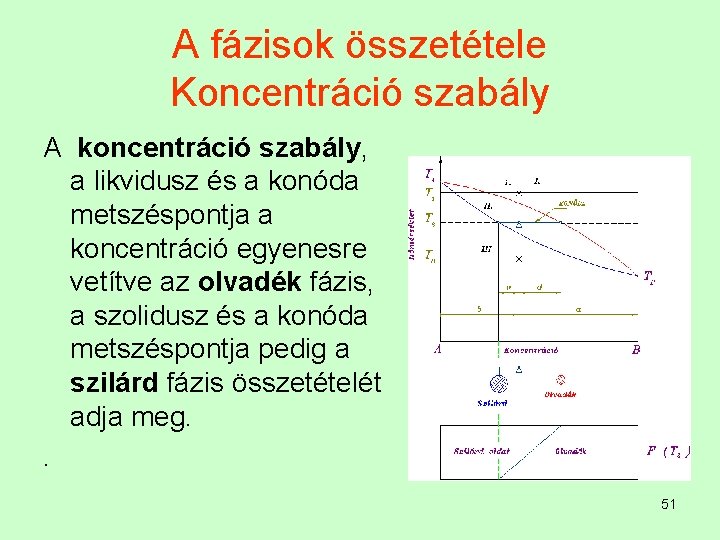
A fázisok összetétele Koncentráció szabály A koncentráció szabály, a likvidusz és a konóda metszéspontja a koncentráció egyenesre vetítve az olvadék fázis, a szolidusz és a konóda metszéspontja pedig a szilárd fázis összetételét adja meg. . 51

A fázisok mennyisége Emelőszabály Az ötvözet fázisainak mennyiségét határozhatjuk meg vele 52
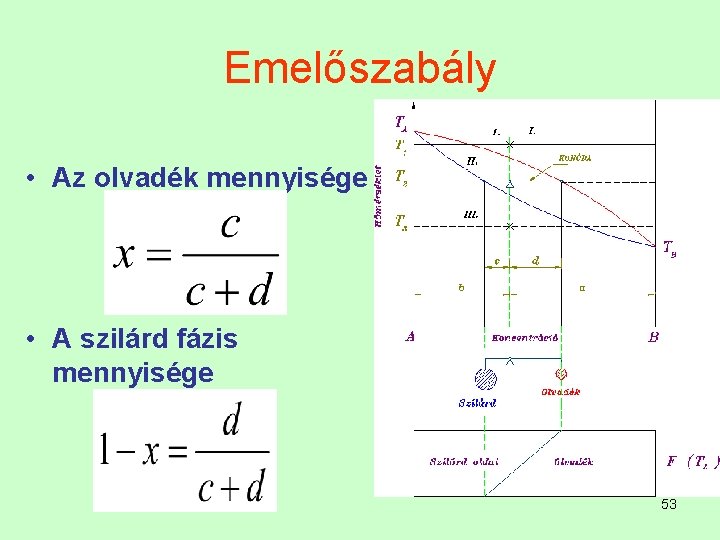
Emelőszabály • Az olvadék mennyisége • A szilárd fázis mennyisége 53

A fázisok mennyiségének meghatározása szerkesztéssel A fázisok mennyiségét a számítás módszeren kívül grafikusan is meghatározhatjuk a fázis diagram segítségével. A fázis diagramot az egyensúlyi diagram alá rajzoljuk , úgy, hogy az egyik oldala megegyezik a koncentráció egyenessel, és szintén a koncentrációt mutatja, másik, rövidebb oldala pedig az ötvözet fázisainak mennyiségét mutatja %-ban. 54
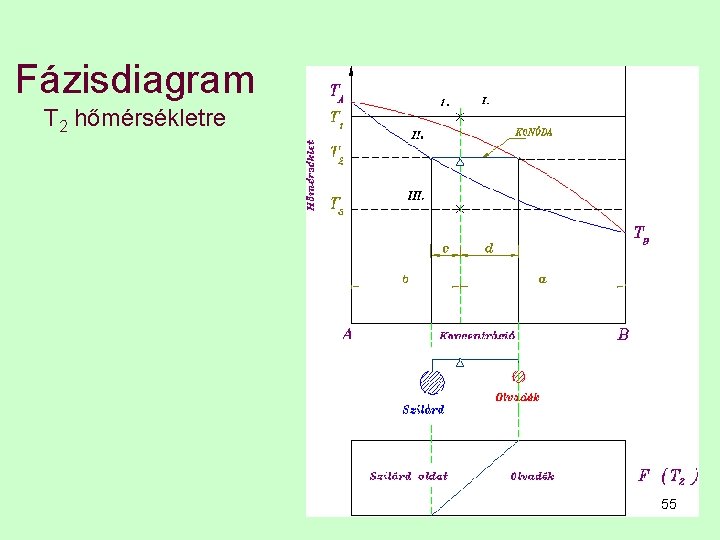
Fázisdiagram T 2 hőmérsékletre 55
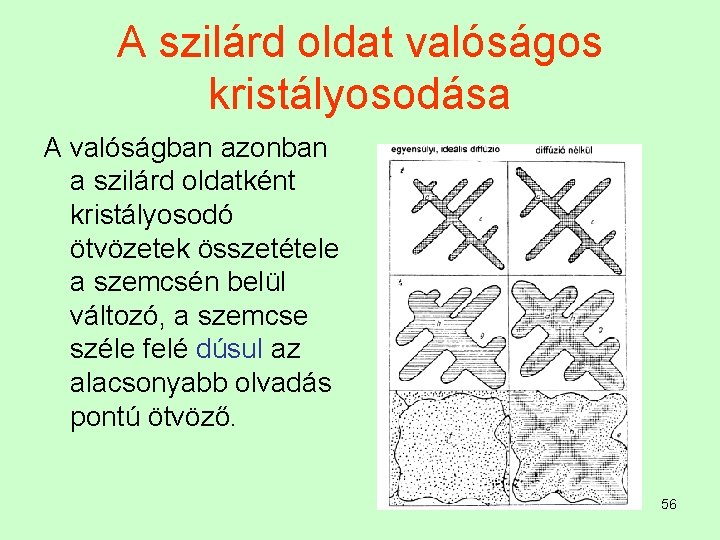
A szilárd oldat valóságos kristályosodása A valóságban azonban a szilárd oldatként kristályosodó ötvözetek összetétele a szemcsén belül változó, a szemcse széle felé dúsul az alacsonyabb olvadás pontú ötvöző. 56

Szilárd oldat Diffúziós izzítás nélkül után diffúziós izzítás 57
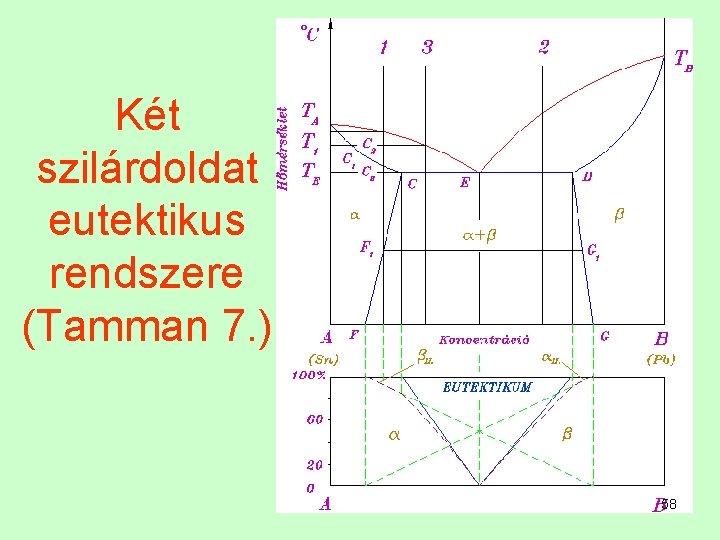
Két szilárdoldat eutektikus rendszere (Tamman 7. ) 58

Eutektikum képződés Az eutektikum két likvidusz metszéspontjának megfelelő összetételnél képződik, állandó hőmérsékleten. Általános egyenlete: olvadék szilárd 1 + szilárd 2 59
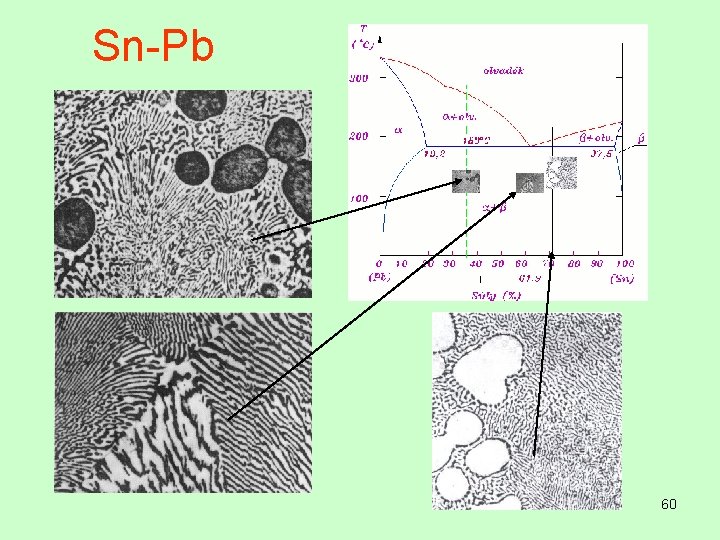
Sn-Pb 60
- Slides: 60