Fluorowce W tabeli przedstawiono temperatury topnienia i wrzenia

Fluorowce
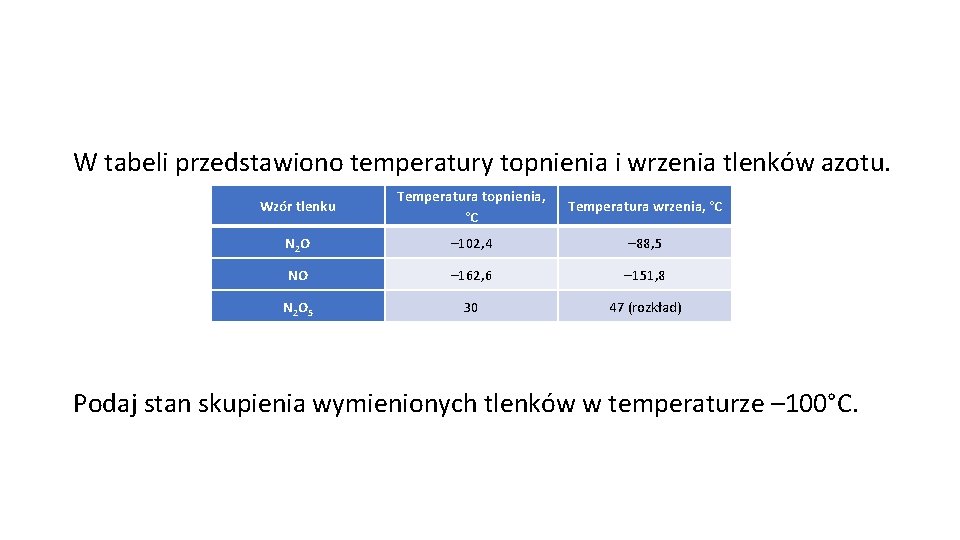
W tabeli przedstawiono temperatury topnienia i wrzenia tlenków azotu. Wzór tlenku Temperatura topnienia, °C Temperatura wrzenia, °C N 2 O – 102, 4 – 88, 5 NO – 162, 6 – 151, 8 N 2 O 5 30 47 (rozkład) Podaj stan skupienia wymienionych tlenków w temperaturze – 100°C.
• Maksymalny stopień utl. • Minimalny st. Utl.

• Rozpuszczalność w wodzie: • Rozpuszczalność w rozp. organicznych

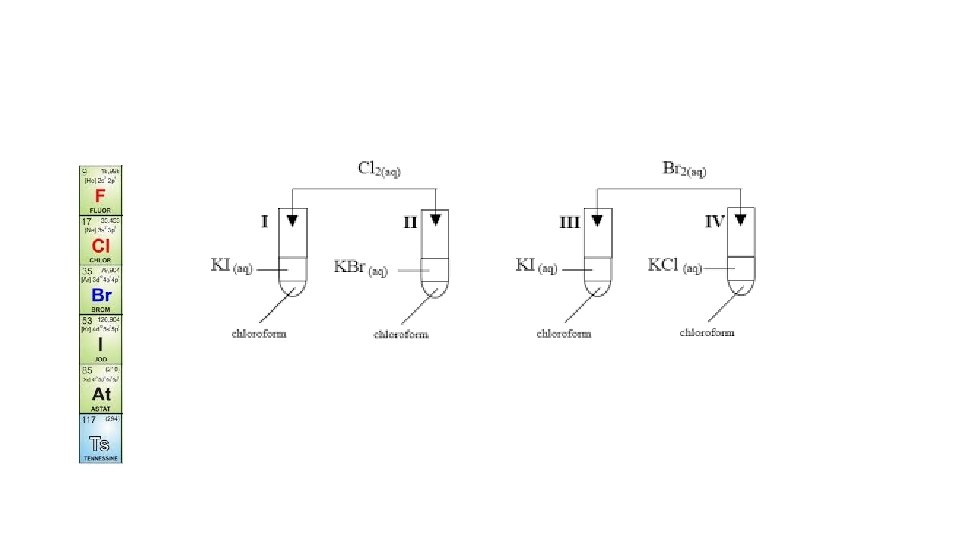
Porównanie aktywności fluorowców https: //www. youtube. com/watch? v=y. Mzy. AXTH_Ok
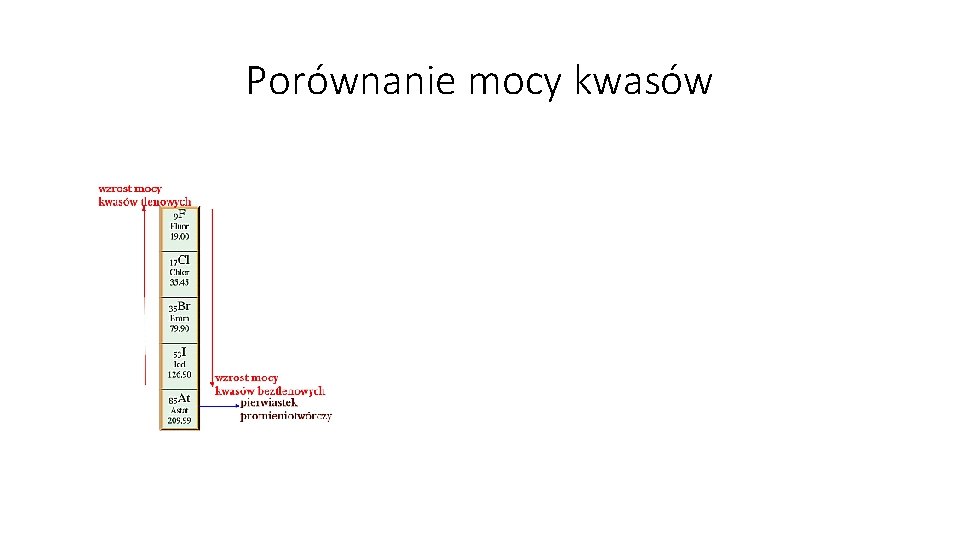
Porównanie mocy kwasów

Fluor • Zawsze na –I stopniu utlenienia! • Trawienie szkła – powstaje fluorek krzemu

Chlor +7 Cl 2 O 7 , HCl. O 4 +6 Cl. O 3 , Cl 2 O 6 +5 HCl. O 3 +4 Cl. O 2 +3 Cl 2 O 3, HCl. O 2 +1 Cl 2 O, HCl. O 0 Cl 2 -1 Cl-, HCl, Na. Cl…

Brom i jod
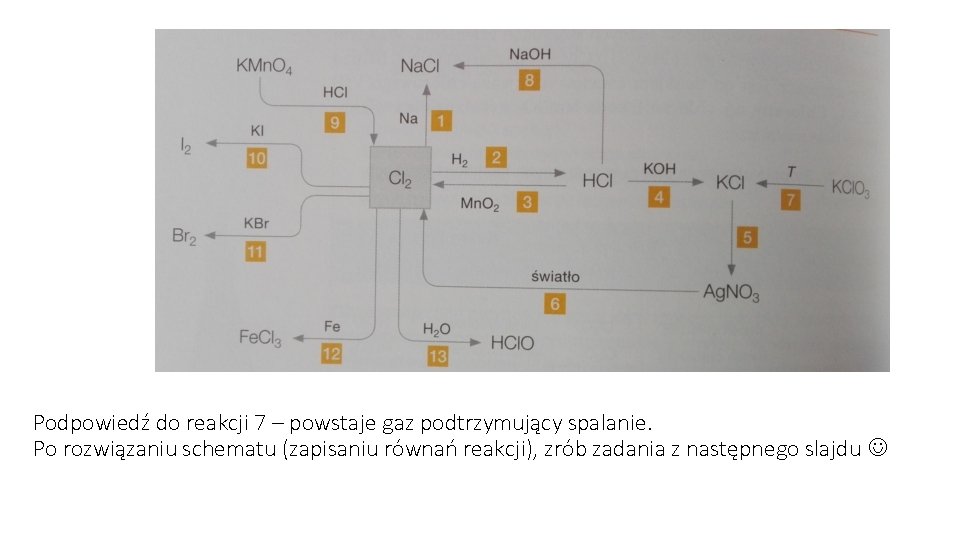
Podpowiedź do reakcji 7 – powstaje gaz podtrzymujący spalanie. Po rozwiązaniu schematu (zapisaniu równań reakcji), zrób zadania z następnego slajdu

1) Podaj numery reakcji chemicznych, które umożliwiają porównanie aktywności chemicznej fluorowców. 2) Wskaż numery reakcji, w których chlor pełni funkcję reduktora 3) Narysuj schemat i podaj przewidywane obserwacje do doświadczenia nr 7, w którym otrzymasz m. in. gaz powodujący rozpalenie rozżarzonego łuczywa. 4) Atomy dwóch fluorowców różnią się o 18 protonów w jądrze atomowym. Fluorowiec X reaguje z solą potasową fluorowca Y. Ustal jakie to pierwiastki chemiczne 5) Podaj wzór tlenku chloru, którego gęstość w warunkach normalnych wynosi 3, 01 g/dm 3 6) Wskaż substancje, które nie będą reagowały ze sobą. Odpowiedź uzasadnij. a) KI i Cl 2 b) KBr i Cl 2 c) KF i HI d) HBr i HCl

Co to za pierwiastek? Lp. Właściwości 1. 2. 3. Czerwonobrunatna lotna ciecz Pary mają duszący zapach drażniący błony śluzowe Tworzy cząsteczki dwuatomowe Wodny roztwór wykorzystuje się do wykrywania charakteru nienasyconego związków organicznych Ciało stałe Tworzy trzy odmiany alotropowe, z których jedna przewodzi prąd elektryczny Mało reaktywny chemicznie w temperaturze pokojowej Zielonkawożółty gaz Silnie trujący (użyty przez Niemców w bitwie pod Ypres) Bardzo reaktywny chemicznie Środek dezynfekcyjny do odkażania wody Nazwa pierwiastk a

Chlor tworzy tlenki, w których przyjmuje różne stopnie utlenienia. Tlenek, w którym chlor występuje na najwyższym stopniu utlenienia, otrzymuje się w reakcji odwodnienia (dehydratacji) kwasu chlorowego zawierającego chlor na tym samym stopniu utlenienia. Napisz równanie reakcji otrzymywania tego tlenku powyższą metodą.

W jednej probówce znajduje się wodny roztwór chlorku potasu, a w drugiej – wodny roztwór bromku potasu. Którego odczynnika – Br 2(aq) czy Cl 2(aq) – należy użyć, aby rozróżnić te roztwory? Podaj wzór chemiczny wybranego odczynnika oraz przewidywane obserwacje. Napisz w formie cząsteczkowej równanie reakcji, będącej podstawą rozróżnienia tych roztworów.

1. Chlor to żółtozielony gaz o charakterystycznym duszącym zapachu i o gęstości większej od gęstości powietrza. P F 2. Produktem reakcji żelaza z chlorem jest sól, w której żelazo występuje na II stopniu utlenienia. P F 3. Chlor otrzymany w reakcji 0, 6 mola tlenku manganu(IV) ze stężonym kwasem solnym reaguje z 0, 4 mola glinu. P F
- Slides: 16