FLORIN VIU Substane simple cu utilizri practice Substane

FLORIN VIU Substanţe simple cu utilizări practice Substanţe compuse cu utilizări practice Substanțe simple și compuse cu utilizări practice Auxiliar didactic pentru elevii clasei a VIII-a FĂLTICENI 2018 OUT

SISTEMUL PERIODIC AL ELEMENTELOR NIVEL ENERGETIC Perio ada Strat 2 L GRUPE PRINCIPALE IA (1) GRUPE PRINCIPALE 1 K II A (2) III A (13) IV A (14) VA (15) VI A (16) VII A (17) VIII A (18) GRUPE SECUNDARE 3 M III B (3) 4 N 5 O 6 P 57 - 71 Lantanid e 7 Q 89 - 103 Actinide IVB (4) VB (5) VI B (6) VII B (7) VIII B (8) VIII B (9) VIII B (10) IB (11) II B (12) 104 105 106 107 108 109 110 111 112 Rf Db Sg Bh Hs Mt Ds Rg Cn 114 Fl 116 Lv 57 - 71 Lantanid e 89 - 103 Actinide Back
Click pe momentul lecției Generalităţi Stare naturală Obţinerea industrială Obţinerea în laborator Proprietăţi fizice În aer sau în oxigen? Proprietăţi chimice Utilizări Rebus OXIGENUL Descoperă… Back
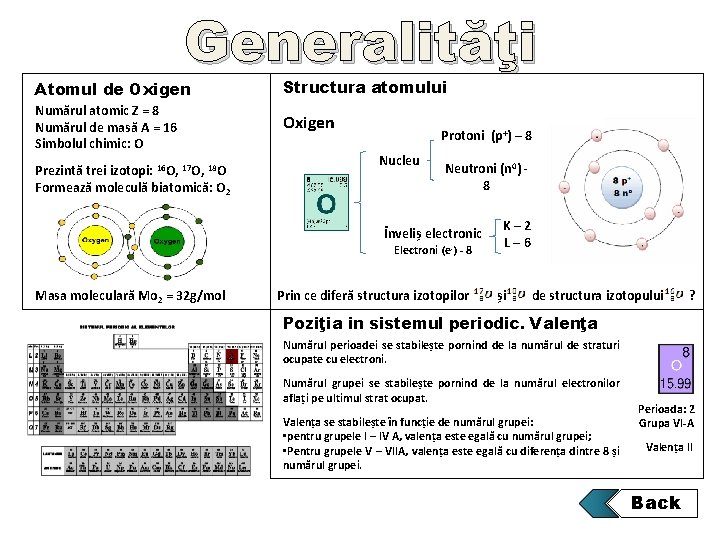
Generalităţi Atomul de Oxigen Structura atomului Numărul atomic Z = 8 Numărul de masă A = 16 Simbolul chimic: O Oxigen Prezintă trei izotopi: 16 O, 17 O, 18 O Formează moleculă biatomică: O 2 Protoni (p+) – 8 Nucleu Neutroni (n 0) 8 Înveliș electronic Electroni (e-) - 8 Masa moleculară Mo 2 = 32 g/mol Prin ce diferă structura izotopilor K– 2 L– 6 și de structura izotopului ? Poziţia in sistemul periodic. Valenţa Numărul perioadei se stabilește pornind de la numărul de straturi ocupate cu electroni. Numărul grupei se stabilește pornind de la numărul electronilor aflați pe ultimul strat ocupat. Valența se stabilește în funcție de numărul grupei: • pentru grupele I – IV A, valența este egală cu numărul grupei; • Pentru grupele V – VIIA, valența este egală cu diferența dintre 8 și numărul grupei. Perioada: 2 Grupa VI-A Valența II Back

Stare naturală ÎN STARE LIBERĂ În atmosferă: oxigenul se găsește sub două forme alotropice: oxigenul molecular (O 2) și ozonul (O 3). • Oxigenul molecular se află în atmosferă în procent de 21%; • Ozonul se găsește în cantități foarte mici în păturile superioare ale atmosferei (stratul de ozon). ÎN COMPUȘI ORGANICI • În compuși hidroxilici: alcool etilic, fenol; • În acizi organici: acidul acetic, acid citric; • În aminoacizi și proteine; • În lipide; • În zaharuri: glucoză, fructoză, zaharoză etc. RĂSP NDIREA OXIGENULUI ÎN SCOARŢA TERESTRĂ ÎN COMPUȘI MINERALI • În apă; • În oxizi – compuși ai nemetalelor și metalelor cu oxigenul: CO 2, SO 2, Ca. O, Fe 2 O 3; • În oxiacizi: HNO 3, H 2 SO 4, H 3 PO 4; • În hidroxizi: Na. OH, Ca(OH)2, Cu(OH)2; • În sărurile oxiacizilor: nitraţi (NH 4 NO 3), carbonaţi (Ca. CO 3, Cu. CO 3), sulfaţi (Cu. SO 4), fosfaţi (Ca 3(PO 4)2), silicaţi ş. a. Back
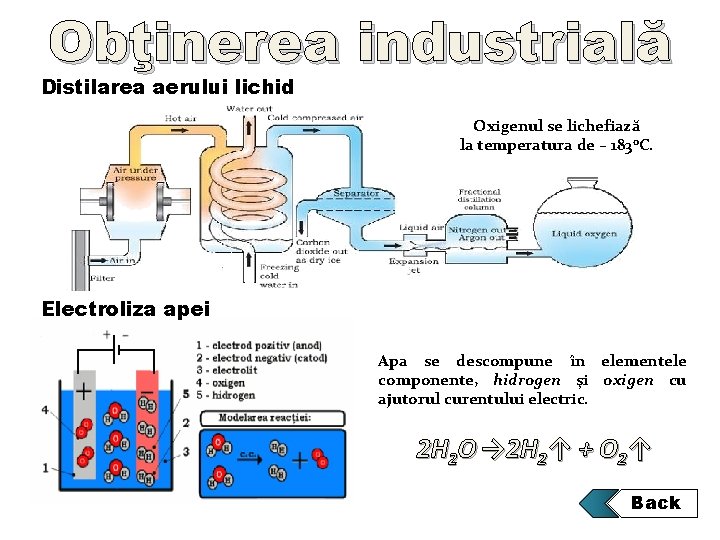
Obţinerea industrială Distilarea aerului lichid Oxigenul se lichefiază la temperatura de – 183 o. C. Electroliza apei Apa se descompune în elementele componente, hidrogen şi oxigen cu ajutorul curentului electric. 2 H 2 O → 2 H 2↑ + O 2↑ Back

Obţinerea în laborator AȘCHII DE BRAD KCl. O 3 H 2 O 2 Mn. O 2 E 1 – Descompunerea cloratului de potasiu MOD DE LUCRU: 1. Ia o eprubetă din stativ (click pe prima eprubetă din stativ) 2. Introdu în eprubetă o cantitate de clorat de potasiu, KCl. O 3, apoi dioxid de mangan, Mn. O 2 (click pe etichetele recipientelor cu reactivi) 3. Încălzește eprubeta (click pe SURSĂ DE FOC), apoi verifică natura gazului rezultat cu o așchie de brad cu punct incandescent (click pe eticheta AȘCHII DE BRAD). Ce observi? Aşchia de brad se aprinde, semn că din reacţie rezultă oxigen. Se mai obţine şi clorura de potasiu. Dioxidul de mangan joacă rol de catalizator. 2 KCl. O 3 → 2 KCl + 3 O 2↑ E 2 – Descompunerea apei oxigenate MOD DE LUCRU: 1. Ia o eprubetă din stativ (click pe prima eprubetă liberă din stânga) 2. Adaugă în eprubetă apă oxigenată, H 2 O 2 și dioxid de mangan (click pe etichetele recipientelor cu reactivi) 3. Verifică natura gazului rezultat cu o așchie de brad cu punct incandescent (Click pe eticheta AȘCHII DE BRAD). Ce se observă? Aşchia de brad se aprinde, semn că din reacţie rezultă oxigen. Celălalt produs rezultat este apa. Dioxidul de mangan joacă rol de catalizator. SURSĂ DE FOC 2 H 2 O 2 → 2 H 2 O + O 2↑ Back

Proprietăţi fizice Prezența oxigenului în atmosfera Terrei a dus la apariția și diversificarea vieții • Oxigenul este un gaz incolor, inodor, insipid; • Prezintă o densitate de 1, 1 ori mare decât cea a aerului; • Se lichefiază foarte greu la o temperatură de -183 °C; în stare lichidă prezintă culoarea albastru închis; • Solubilitate scăzută în apă. Aceasta permite vieţuitoarelor acvatice să trăiască; Oxidări si arderi Sunt reacțiile substanțelor cu oxigenul: • Oxidări vii sau arderi - reacția are loc în timp scurt, dezvoltându-se căldură și lumină(ex. arderea unei lumânări) • Oxidări lente – reacția are loc în timp îndelungat, fără creșterea temperaturii (de exemplu ruginirea fierului, oxidările din organismele vii) Back
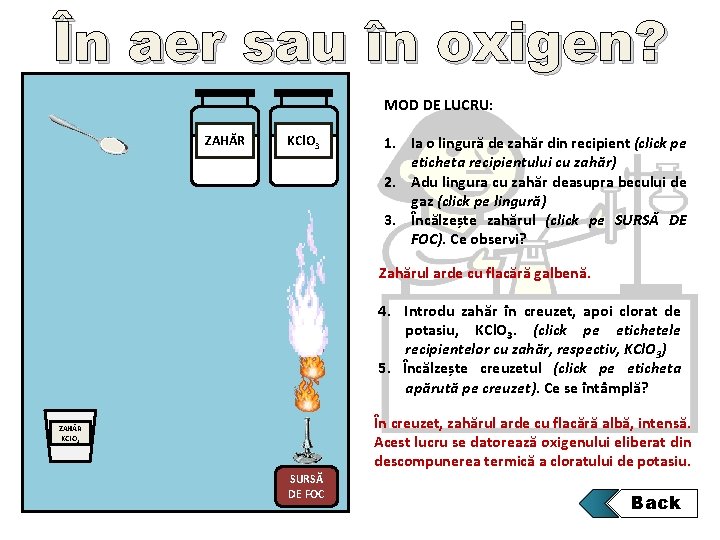
În aer sau în oxigen? MOD DE LUCRU: ZAHĂR KCl. O 3 1. Ia o lingură de zahăr din recipient (click pe eticheta recipientului cu zahăr) 2. Adu lingura cu zahăr deasupra becului de gaz (click pe lingură) 3. Încălzește zahărul (click pe SURSĂ DE FOC). Ce observi? Zahărul arde cu flacără galbenă. 4. Introdu zahăr în creuzet, apoi clorat de potasiu, KCl. O 3. (click pe etichetele recipientelor cu zahăr, respectiv, KCl. O 3) 5. Încălzește creuzetul (click pe eticheta apărută pe creuzet). Ce se întâmplă? În creuzet, zahărul arde cu flacără albă, intensă. Acest lucru se datorează oxigenului eliberat din descompunerea termică a cloratului de potasiu. ZAHĂR KCl. O 3 SURSĂ DE FOC Back

Reacţia magneziului cu oxigenul Reacţia aluminiului cu oxigenul Proprietăţi chimice Reacţia fierului cu oxigenul Reacţia carbonului cu oxigenul Reacţia sulfului cu oxigenul Back
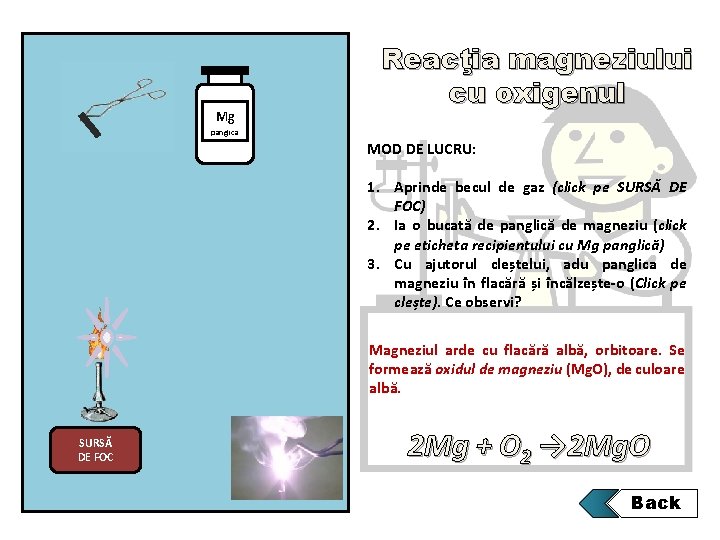
Mg Reacţia magneziului cu oxigenul panglica MOD DE LUCRU: 1. Aprinde becul de gaz (click pe SURSĂ DE FOC) 2. Ia o bucată de panglică de magneziu (click pe eticheta recipientului cu Mg panglică) 3. Cu ajutorul cleștelui, adu panglica de magneziu în flacără și încălzește-o (Click pe clește). Ce observi? Magneziul arde cu flacără albă, orbitoare. Se formează oxidul de magneziu (Mg. O), de culoare albă. SURSĂ DE FOC 2 Mg + O 2 → 2 Mg. O Back

H 2 O 2 Reacţia aluminiului cu oxigenul Al pulbere MOD DE LUCRU: 1. 2. 3. 4. 5. Aprinde becul de gaz (click pe SURSĂ DE FOC) Introdu apă oxigenată, H 2 O 2 în cilindrul cu nisip (click pe eticheta recipientului cu H 2 O 2). Ai obținut astfel, o sursă de oxigen. Adaugă pulbere de aluminiu în lingura de ars (click pe eticheta recipientului cu Al) Încălzește lingura de ars (click pe coada lingurii de ars) Introdu lingura de ars în cilindrul cu oxigen (Click pe coada lingurii de ars). Ce se întâmplă? Pulberea de aluminiu se aprinde în oxigen și arde cu scântei albe, obținându-se oxid de aluminiu, Al 2 O 3. 4 Al + 3 O 2→ 2 Al 2 O 3 SURSĂ DE FOC Back

H 2 O 2 Reacţia fierului cu oxigenul Fe pilitură MOD DE LUCRU: 1. 2. 3. 4. 5. Aprinde becul de gaz (click pe SURSĂ DE FOC) Introdu apă oxigenată, H 2 O 2 în cilindrul cu nisip (click pe eticheta recipientului cu H 2 O 2). Ai obținut astfel, o sursă de oxigen. Adaugă pilitură de fier în lingura de ars (click pe eticheta recipientului cu Fe) Încălzește lingura de ars (click pe coada lingurii de ars) Introdu lingura de ars în cilindrul cu oxigen (Click pe coada lingurii de ars). Ce se întâmplă? Pulberea de aluminiu se aprinde în oxigen și arde cu scântei galbene, obținându-se oxid de fier, Fe 3 O 4. 3 Fe + 2 O 2→Fe 3 O 4 SURSĂ DE FOC Back
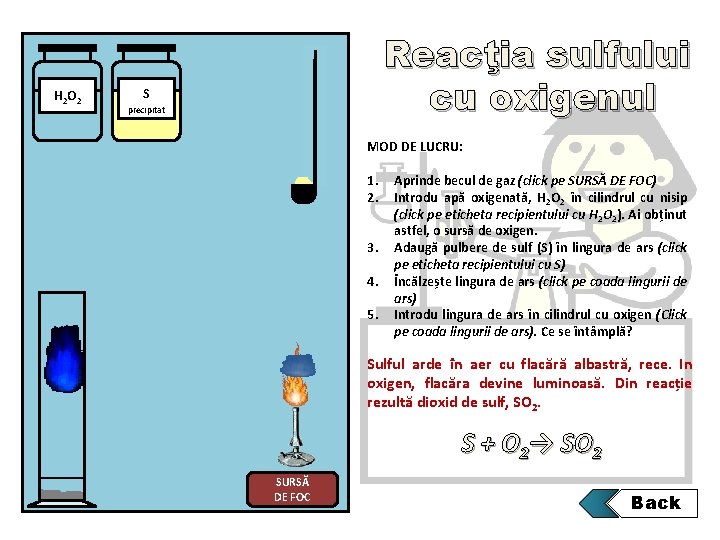
H 2 O 2 Reacţia sulfului cu oxigenul S precipitat MOD DE LUCRU: 1. 2. 3. 4. 5. Aprinde becul de gaz (click pe SURSĂ DE FOC) Introdu apă oxigenată, H 2 O 2 în cilindrul cu nisip (click pe eticheta recipientului cu H 2 O 2). Ai obținut astfel, o sursă de oxigen. Adaugă pulbere de sulf (S) în lingura de ars (click pe eticheta recipientului cu S) Încălzește lingura de ars (click pe coada lingurii de ars) Introdu lingura de ars în cilindrul cu oxigen (Click pe coada lingurii de ars). Ce se întâmplă? Sulful arde în aer cu flacără albastră, rece. In oxigen, flacăra devine luminoasă. Din reacție rezultă dioxid de sulf, SO 2. S + O 2→ SO 2 SURSĂ DE FOC Back
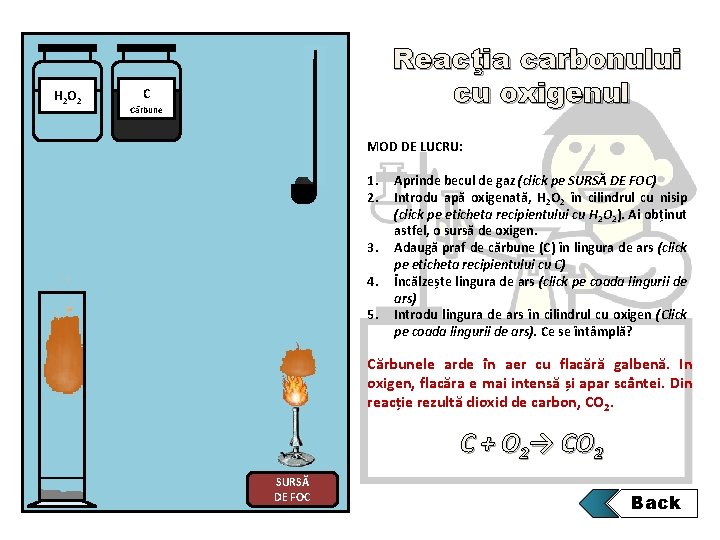
H 2 O 2 Reacţia carbonului cu oxigenul C Cărbune MOD DE LUCRU: 1. 2. 3. 4. 5. Aprinde becul de gaz (click pe SURSĂ DE FOC) Introdu apă oxigenată, H 2 O 2 în cilindrul cu nisip (click pe eticheta recipientului cu H 2 O 2). Ai obținut astfel, o sursă de oxigen. Adaugă praf de cărbune (C) în lingura de ars (click pe eticheta recipientului cu C) Încălzește lingura de ars (click pe coada lingurii de ars) Introdu lingura de ars în cilindrul cu oxigen (Click pe coada lingurii de ars). Ce se întâmplă? Cărbunele arde în aer cu flacără galbenă. In oxigen, flacăra e mai intensă și apar scântei. Din reacție rezultă dioxid de carbon, CO 2. C + O 2→ CO 2 SURSĂ DE FOC Back

Utilizări medicină Obținerea explozibililor Motoare Butelii pentru scafandri, aviatori, astronauți, mineri Sinteza acizilor Obținerea fontei și oțelului Sudarea și tăierea metalelor Albirea țesăturilor Back
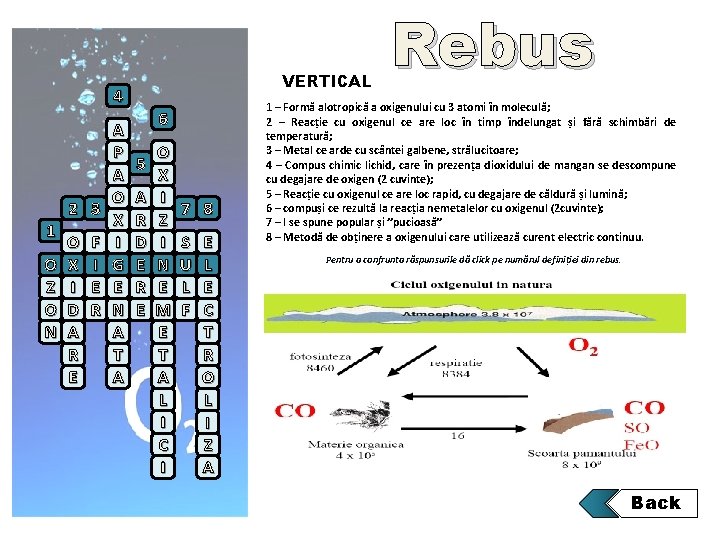
VERTICAL 4 1 O Z O N 2 3 O X I D A R E F I E R A P A O X I G E N A T A 6 5 A R D E R E O X I Z I N E M E T A L I C I 7 8 S U L F E L E C T R O L I Z A Rebus 1 – Formă alotropică a oxigenului cu 3 atomi în moleculă; 2 – Reacție cu oxigenul ce are loc în timp îndelungat și fără schimbări de temperatură; 3 – Metal ce arde cu scântei galbene, strălucitoare; 4 – Compus chimic lichid, care în prezența dioxidului de mangan se descompune cu degajare de oxigen (2 cuvinte); 5 – Reacție cu oxigenul ce are loc rapid, cu degajare de căldură și lumină; 6 – compuși ce rezultă la reacția nemetalelor cu oxigenul (2 cuvinte); 7 – I se spune popular și ”pucioasă” 8 – Metodă de obținere a oxigenului care utilizează curent electric continuu. Pentru a confrunta răspunsurile dă click pe numărul definiției din rebus. Back

Descoperă… Răspunde la cele şapte întrebări şi află cine a descoperit oxigenul 1. Numărul de neutroni conţinuţi de izotopul 17 O este: GREŞIT! a) 10 CORECT! b) 9 GREŞIT! c) 8 2. Procentul de oxigen dioxidul de carbon este: a) GREŞIT! 47, 15 CORECT! b) 72, 72 GREŞIT! c) 80, 00 3. Nu se obţine oxigen din descompunerea: a) CORECT! Cu. CO 3 b) GREŞIT! KCl. O 3 GREŞIT! c) H 2 O 2 4. Temperatura de lichefiere a oxigenului este: a) GREŞIT! -100 o. C b) GREŞIT! 183 o. C c) CORECT! -183 o. C J 5. Se obţine un oxid metalic la arderea: CORECT! a) Mg GREŞIT! b) C GREŞIT! c) S P R O S I E E S P H T L E Y 6. La arderea a 0, 4 moli. Al, numărul de moli de Al 2 O 3 obţinut este: GREŞIT! a) 0, 1 CORECT! b) 0, 2 GREŞIT! c) 0, 4 7. Concentraţia soluţiei obţinută din produsul arderii a 4, 8 g Mg şi 50 g. H 2 O este: GREŞIT! a) 32% GREŞIT! b) 18% CORECT! c) 25% Teolog, filozof natural, educator şi teoretician englez, a izolat oxigenul în formă gazoasă în anul 1774 Back

Click pe momentul lecției Generalităţi Stare naturală Proprietăţi fizice Proprietăţi chimice Utilizări Descoperă… Diagramă CARBONUL Back
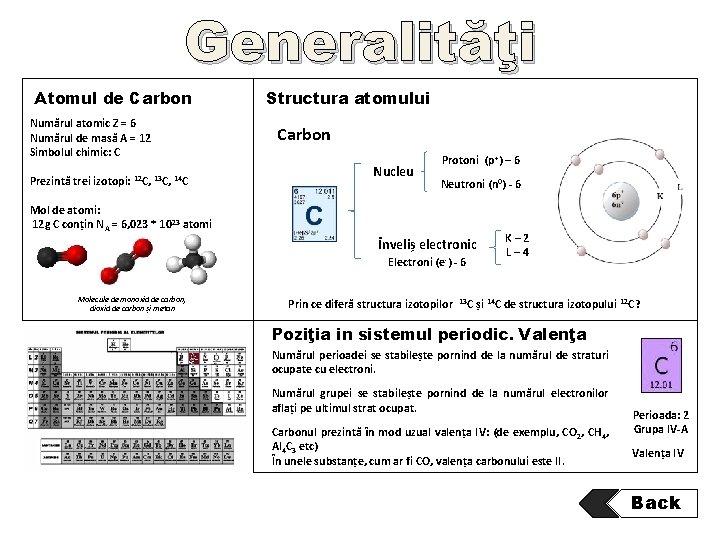
Generalităţi Atomul de Carbon Numărul atomic Z = 6 Numărul de masă A = 12 Simbolul chimic: C Prezintă trei izotopi: 12 C, 13 C, 14 C Structura atomului Carbon Nucleu Protoni (p+) – 6 Neutroni (n 0) - 6 Mol de atomi: 12 g C conțin N A = 6, 023 * 10 23 atomi Înveliș electronic Electroni (e-) - 6 Molecule de monoxid de carbon, dioxid de carbon și metan Prin ce diferă structura izotopilor 13 C K– 2 L– 4 și 14 C de structura izotopului 12 C? Poziţia in sistemul periodic. Valenţa Numărul perioadei se stabilește pornind de la numărul de straturi ocupate cu electroni. Numărul grupei se stabilește pornind de la numărul electronilor aflați pe ultimul strat ocupat. Carbonul prezintă în mod uzual valența IV: (de exemplu, CO 2, CH 4, Al 4 C 3 etc) În unele substanțe, cum ar fi CO, valența carbonului este II. Perioada: 2 Grupa IV-A Valența IV Back

Stare naturală În stare liberă Carbonul se găsește în natură sub două forme cristalizate: diamantul și grafitul. Alte două forme cristalizate ale carbonului au fost realizate în laboratoare: fulerenele și nanotuburile. Fulerenele se găsesc și în natură, în materialul numit Shungit. În combinaţii • În compușii cu oxigenul: monoxid de carbon (CO), dioxid de carbon(CO 2); • În compuși cu nemetalele: tetraclorură de carbon (CCl 4), carbura de siliciu (Si. C); • în compuși cu metalele: carbură de aluminiu (Al 4 C 3), carbură de calciu (Ca. C 2); • în carbonați: carbonatul de calciu, carbonatul de cupru; • în bicarbonați: bicarbonatul de sodiu (Na. HCO 3), bicarbonatul de amoniu (NH 4 HCO 3); • în hidrocarburi: metanul (CH 4), acetilenă (C 2 H 2); • în toți derivații hidrocarburilor: alcool etilic, acid acetic, zahăr etc. Sub formă amorfă, carbonul este întâlnit în cărbunii de pământ. Conținutul de carbon al acestora crește în ordinea: turbă, lignit, cărbune brun, huilă, antracit. Back
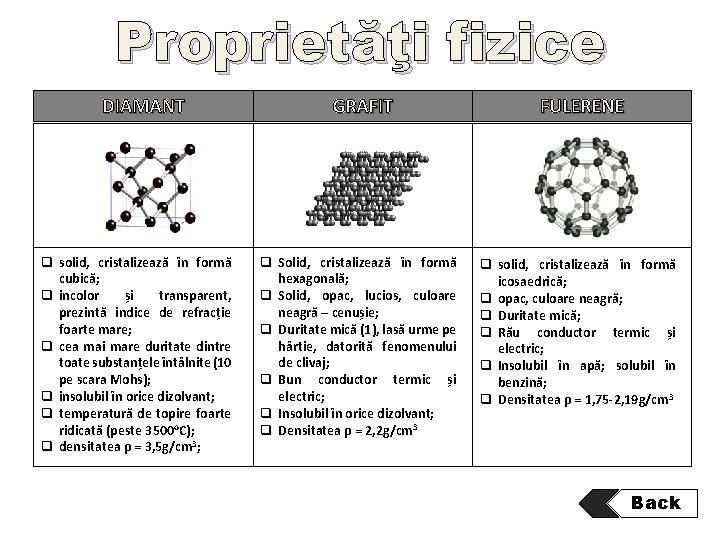
Proprietăţi fizice DIAMANT q solid, cristalizează în formă cubică; q incolor și transparent, prezintă indice de refracție foarte mare; q cea mai mare duritate dintre toate substanțele întâlnite (10 pe scara Mohs); q insolubil în orice dizolvant; q temperatură de topire foarte ridicată (peste 3500 o. C); q densitatea ρ = 3, 5 g/cm 3; GRAFIT q Solid, cristalizează în formă hexagonală; q Solid, opac, lucios, culoare neagră – cenușie; q Duritate mică (1), lasă urme pe hârtie, datorită fenomenului de clivaj; q Bun conductor termic și electric; q Insolubil în orice dizolvant; q Densitatea ρ = 2, 2 g/cm 3 FULERENE q solid, cristalizează în formă icosaedrică; q opac, culoare neagră; q Duritate mică; q Rău conductor termic și electric; q Insolubil în apă; solubil în benzină; q Densitatea ρ = 1, 75 -2, 19 g/cm 3 Back

Proprietăți chimice Reacţia carbonului cu oxigenul Reacţia carbonului cu oxidul de cupru Alte proprietăţi chimice Back
H 2 O 2 Reacţia carbonului cu oxigenul C Cărbune MOD DE LUCRU: 1. 2. 3. 4. 5. Aprinde becul de gaz (click pe SURSĂ DE FOC) Introdu apă oxigenată, H 2 O 2 în cilindrul cu nisip (click pe eticheta recipientului cu H 2 O 2). Ai obținut astfel, o sursă de oxigen. Adaugă praf de cărbune (C) în lingura de ars (click pe eticheta recipientului cu C) Încălzește lingura de ars (click pe coada lingurii de ars) Introdu lingura de ars în cilindrul cu oxigen (Click pe coada lingurii de ars). Ce se întâmplă? Cărbunele arde în aer cu flacără galbenă. In oxigen, flacăra e mai intensă și apar scântei. Din reacție rezultă dioxid de carbon, CO 2. C + O 2→ CO 2 SURSĂ DE FOC Back

iulunobrac aiţcae. R urpuc ed ludixo uc : URCUL ED DOM Ou. C , urpuc ed dixo iș C , enubrăc ed farp udortn. I. 1 roletneipicer atehcite ep kcilc( ăcim ateburpe nî )ivitcaer uc nî )HOa. N( uidos ed dixordih ed eițulos ăguad. A. 2 irutăcip avetâc iș ăguada iopa , eram ateburpe iulutneipicer atehcite ep kcilc( ănielatflonef ed. )ănielatflonef vitcepser HOa. N uc ED ĂSRUS ep kcilc( zag ed luceb iopa ednirp. A. 3 aec nî ra. D ? ăcim ateburpe nî ivresbo e. C. )COF ? eram ludixo uc ăzaenoițcaer elenubrăc , ăcim ateburpe nÎ. urpuc iș nobrac ed dixoid es-udnâmrof , urpuc ed u. C 2 + ↑ 2 OC →Ou. C 2 + C eceraoed , ăzaeroloced es aițulos , eram ateburpe nÎ. atsaeca nid uidos ed ludixordih uc ăzaenoițcaer 2 OC O 2 H + 3 OC 2 a. N→HOa. N 2 + 2 OC kca. B
Alte proprietăţi chimice ale carbonului Reacţia cu hidrogenul Carbonul se combină cu hidrogenul și formează, în funcție de condițiile de reacție, metan sau alte hidrocarburi. Metanul se obține la temperatura de 1100 o. C și în prezența nichelului C + 2 H 2 → CH 4 Reactia cu apa Are loc la temperaturi înalte. Se obține gazul de apă (format din monoxid de carbon și hidrogen) H 2 O(g) + C →CO + H 2 Back
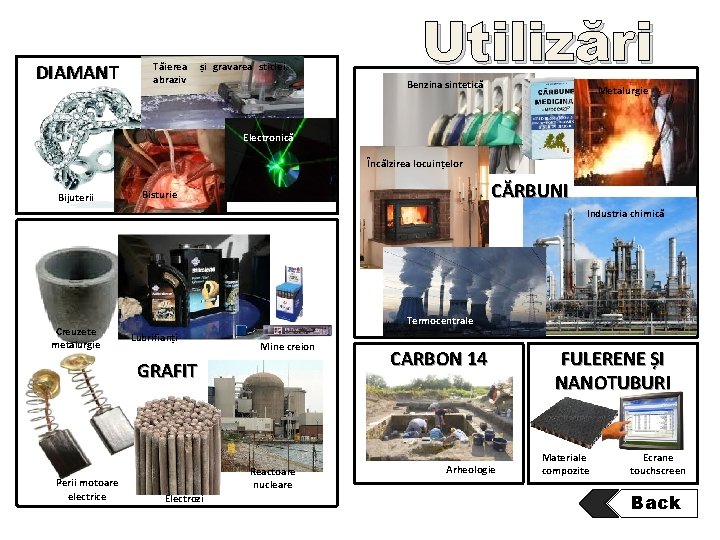
DIAMANT Tăierea abraziv și gravarea sticlei, Utilizări Benzina sintetică Metalurgie Electronică Încălzirea locuințelor Bijuterii CĂRBUNI Bisturie Industria chimică Creuzete metalurgie Termocentrale Lubrifianți Mine creion GRAFIT Perii motoare electrice Electrozi Reactoare nucleare CARBON 14 Arheologie FULERENE ȘI NANOTUBURI Materiale compozite Ecrane touchscreen Back
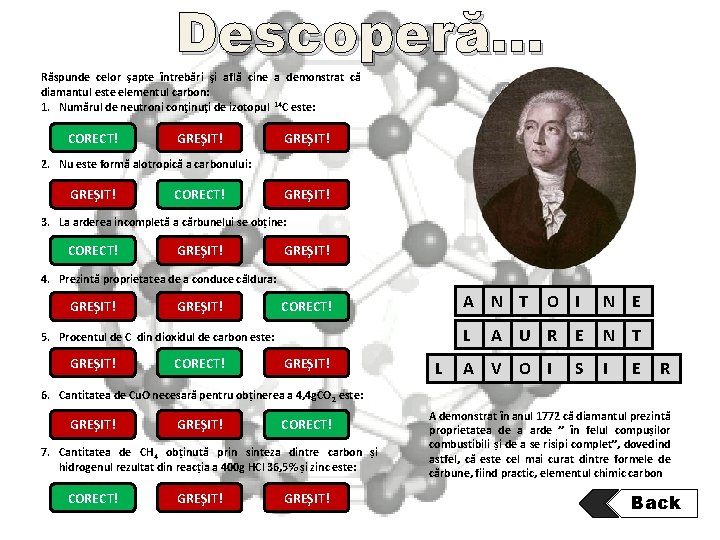
Descoperă… Răspunde celor şapte întrebări şi află cine a demonstrat că diamantul este elementul carbon: 1. Numărul de neutroni conţinuţi de izotopul 14 C este: CORECT! a) 8 GREŞIT! b) 7 GREŞIT! c) 6 2. Nu este formă alotropică a carbonului: a)GREŞIT! Diamant b) CORECT! Carbid c) GREŞIT! Grafit 3. La arderea incompletă a cărbunelui se obține: CORECT! a) CO GREŞIT! b) CO 2 GREŞIT! c) CH 4 4. Prezintă proprietatea de a conduce căldura: a)Cărbuni GREŞIT! b) GREŞIT! Diamant A N T CORECT! c)Grafit L 5. Procentul de C din dioxidul de carbon este: a) GREŞIT! 42, 85 CORECT! b) 27, 27 GREŞIT! c) 20, 00 L O I N E A U R E N T A V O I S I E R 6. Cantitatea de Cu. O necesară pentru obținerea a 4, 4 g. CO 2 este: GREŞIT! a) 8 g GREŞIT! b) 1, 6 g CORECT! c) 16 g 7. Cantitatea de CH 4 obținută prin sinteza dintre carbon și hidrogenul rezultat din reacția a 400 g HCl 36, 5% și zinc este: CORECT! a) 16 g GREŞIT! b) 1, 6 g GREŞIT! c) 8 g A demonstrat în anul 1772 că diamantul prezintă proprietatea de a arde ” în felul compușilor combustibili și de a se risipi complet”, dovedind astfel, că este cel mai curat dintre formele de cărbune, fiind practic, elementul chimic carbon. Back

Diagramă A U E P L N S C O T I N O B T I A R C N G I T 00 58 02 01 03 57 56 55 54 53 52 51 50 49 48 47 46 45 44 43 42 41 40 39 38 37 36 35 34 33 32 31 30 29 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 13 12 11 10 09 08 07 06 05 04 03 02 01 59 00 L N A STOP JOC! START E T C A R M J E E D H A T C V U D G L B B R U N P I B F O V B U U N E M F R S N A M A I T E B D L F R U N A N O T T I F A R U B G D H A E D T H U R I L J C Stările alotropice ale carbonului și cărbunii de pământ și-au uitat numele! Ajută-le să și le găsească, căutându-le pe diagramă. Numele sunt puse pe orizontală, pe verticală și pe diagonale și pot fi dispuse și de la coadă spre cap. Apăsând pe prima literă a unui nume din diagramă, vei găsi numele căutate! Apasă butonul START pentru a începe jocul. Ai trei minute pentru a descoperi cele nouă denumiri! SUCCES! Diamant Nanotuburi Cărbune brun Grafit Turbă Huilă Fulerene Lignit Antracit Back
Click pe momentul lecției Generalităţi Stare naturală Obţinere Proprietăţi fizice Proprietăţi chimice Utilizări Aplicaţii Descoperă… FIERUL Back

Generalităţi Atomul de fier Numărul atomic Z = 26 Numărul de masă A = 56 Simbolul chimic: Fe Structura atomului Fier Nucleu Protoni (p+) – 26 Neutroni (n 0) - 30 Mol de atomi: 56 g Fe conțin NA = 6, 023 * 1023 atomi Înveliș electronic Electroni (e-) - 26 K– 2 L– 8 M – 14 N-2 Fierul prezintă patru izotopi naturali. În ordinea abundenței relative, aceștia sunt: 56 Fe, 54 Fe, 57 Fe și 58 Fe. De asemenea, se cunosc alți 10 izotopi sintetici ai fierului. Poziția in sistemul periodic. Valența Numărul perioadei se stabilește pornind de la numărul de straturi ocupate cu electroni. Fierul este poziționat în grupa secundară VIII B, deoarece completează cu electroni penultimul strat (M) Prezintă în mod uzual valența II (Fe. Cl 2, Fe. SO 4) sau III (Fe 2 O 3, Fe. Cl 3, Fe(OH)3) Perioada: 4 Grupa a VIII-a B Valențe: II, III Back

Stare naturală ÎN STARE LIBERĂ RĂSP NDIREA FIERULUI ÎN TOATE STRATURILE P M NTULUI Meteoriți Bucată de fier cu puritatea 99, 7% RĂSP NDIREA FIERULUI ÎN SCOARȚĂ Deși e doar al patrulea ca răspândire în scoarța terestră, cu un procent de 4, 3%, totuși fierul este cel mai răspândit în toate straturile Pământului, procentul fiind de 35%. Oare de ce? Hemoglobina – compus care se găsește în globulele roșii ale sângelui, cu rol în transportul gazelor respiratorii – este un compus din care fierul este nelipsit. ÎN COMPUȘI Se găsește în minereuri, cei mai importanți fiind: § hematitul - Fe 2 O 3 § magnetitul - Fe 3 O 4 § pirita – Fe. S 2 § calcopirita Cu. Fe. S 2 § siderit – Fe. CO 3 § limonit – Fe 2 O 3. H 2 O Back

Obținere În stare pură, fierul nu prezintă interes industrial datorită proprietății sale de a se sparge ușor (casant). Se folosesc pe scară largă aliajele sale cu carbonul: fonta și oțelul. Aceste aliaje se obțin în cuptoare înalte, numite furnale. Fonta prezintă un procent de 2, 1 – 5%C. Se obține din reducerea oxizilor de fier cu monoxid de carbon, utilizându-se ca materii prime minereuri de fier, cocs, fondanți și aer. Oțelul prezintă un procent de C cuprins între 0, 04 și 1, 9%. Se obține prin reducerea carbonului din fontă, utilizându-se ca materii prime fonta, fierul vechi, varul și aerul. Pentru obținerea de oțeluri cu calități superioare, la fabricarea acestora se adaugă metale diferite, pentru a îmbunătăți proprietățile aliajelor rezultate. FURNAL DE FONTĂ Back

Proprietăţi fizice În stare pură, fierul prezintă următoarele proprietăți fizice: • Culoarea cenușie, luciu metalic caracteristic; • Prezintă duritate mică (4 pe scara Mohs); • Densitate mare (7, 8 g/cm 3); • Temperatură de topire ridicată (1538 o. C); • Bun conductor termic și electric; • Maleabil (se trage în foi); • Ductil (se trage în fire); • Casant (se sparge ușor); • Prezintă proprietăți magnetice. Linii de câmp ale unui magnet, puse în evidență cu ajutorul piliturii de fier Maleabilitate Ductilitate Back

Proprietăţi chimice Reacţia fierului cu sulfatul de cupru Reacţia fierului cu oxigenul Reacţia fierului cu sulful Reacţia fierului cu acizii Back

H 2 O 2 Reacţia fierului cu oxigenul Fe pilitură MOD DE LUCRU: 1. 2. 3. 4. 5. Aprinde becul de gaz (click pe SURSĂ DE FOC) Introdu apă oxigenată, H 2 O 2 în cilindrul cu nisip (click pe eticheta recipientului cu H 2 O 2). Ai obținut astfel, o sursă de oxigen. Adaugă pilitură de fier în lingura de ars (click pe eticheta recipientului cu Fe) Încălzește lingura de ars (click pe coada lingurii de ars) Introdu lingura de ars în cilindrul cu oxigen (Click pe coada lingurii de ars). Ce se întâmplă? Pulberea de aluminiu se aprinde în oxigen și arde cu scântei galbene, obținându-se oxid de fier, Fe 3 O 4. 3 Fe + 2 O 2→Fe 3 O 4 SURSĂ DE FOC Back

Fe S pilitură Reacția fierului cu sulful MOD DE LUCRU: 1. Aprinde becul de gaz (click pe SURSĂ DE FOC) 2. Pune pe sita de azbest pulbere de sulf (click pe eticheta recipientului cu S) apoi pilitură de fier (click pe eticheta recipientului cu Fe) 3. Încălzește bagheta în flacără (click pe baghetă) 4. Introdu bagheta în amestecul de Fe și S (Click pe baghetă). Ce se întâmplă? Are loc o reacţie cu degajare de căldură şi lumină. Substanţa nou obţinută se numeşte sulfură de fier (Fe. S) și are culoarea neagră. SURSĂ DE FOC Fe + S → Fe. S Back
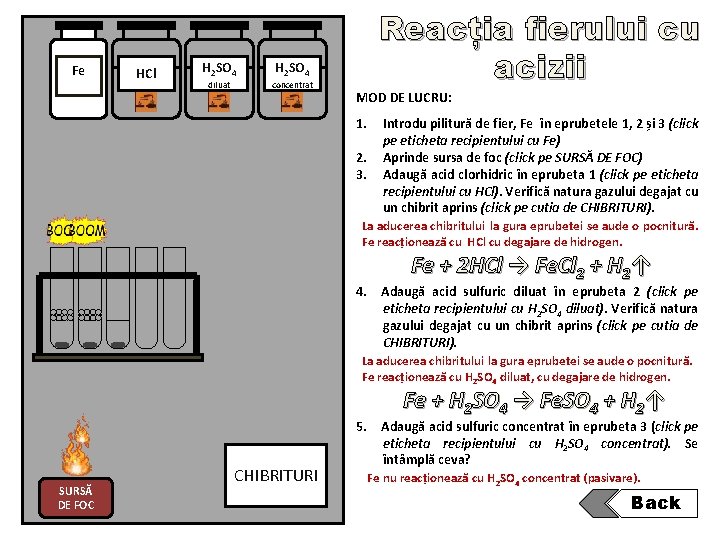
Fe HCl H 2 SO 4 diluat concentrat Reacția fierului cu acizii MOD DE LUCRU: 1. 2. 3. Introdu pilitură de fier, Fe în eprubetele 1, 2 și 3 (click pe eticheta recipientului cu Fe) Aprinde sursa de foc (click pe SURSĂ DE FOC) Adaugă acid clorhidric în eprubeta 1 (click pe eticheta recipientului cu HCl). Verifică natura gazului degajat cu un chibrit aprins (click pe cutia de CHIBRITURI). La aducerea chibritului la gura eprubetei se aude o pocnitură. Fe reacționează cu HCl cu degajare de hidrogen. 4. Fe + 2 HCl → Fe. Cl 2 + H 2↑ Adaugă acid sulfuric diluat în eprubeta 2 (click pe eticheta recipientului cu H 2 SO 4 diluat). Verifică natura gazului degajat cu un chibrit aprins (click pe cutia de CHIBRITURI). La aducerea chibritului la gura eprubetei se aude o pocnitură. Fe reacționează cu H 2 SO 4 diluat, cu degajare de hidrogen. 5. SURSĂ DE FOC CHIBRITURI Fe + H 2 SO 4 → Fe. SO 4 + H 2↑ Adaugă acid sulfuric concentrat în eprubeta 3 (click pe eticheta recipientului cu H 2 SO 4 concentrat). Se întâmplă ceva? Fe nu reacționează cu H 2 SO 4 concentrat (pasivare). Back

uc iulureif aiţcae. R urpuc ed lutaflus : URCUL ED DOM ed ălutaps o ăpa uc lurahap nî udortn. I. 1 atehcite ep kcilc( 4 OSu. C , urpuc ed taflus. )4 OSu. C uc iulutneipicer eițulos uc lurahap nî reif ed luiuc udortn. I. 2 ăpud ivresbo e. C. )iuc ep kcilc( 4 OSu. C ed ? pmit nu ed citaişor tarts nu uc tirepoca a-s luiu. C. )u. C( urpuc ăca. D. eraoluc al sihcsed a-s 4 OSu. C ed aiţulo. S av es aiţulos , eraunitnoc nî luiuc eniţ mov iulutaflus iirămrof ătirotad , edrev nî aroloc. )4 OSe. F( reif ed ↓u. C + 4 OSe. F→ 4 OSu. C + e. F Back
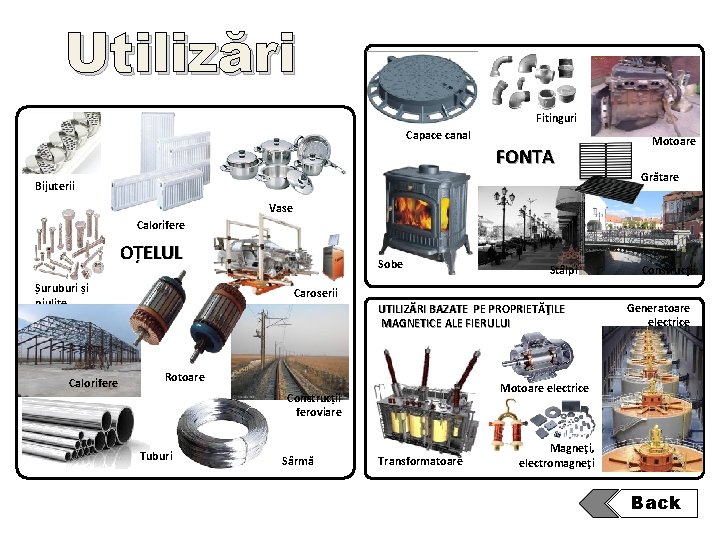
Utilizări Fitinguri Capace canal FONTA Motoare Grătare Bijuterii Vase Calorifere OȚELUL Șuruburi și piulițe Calorifere Sobe Stâlpi Construcții Caroserii UTILIZĂRI BAZATE PE PROPRIETĂŢILE MAGNETICE ALE FIERULUI Rotoare Motoare electrice Construcții feroviare Tuburi Sârmă Generatoare electrice Transformatoare Magneţi, electromagneţi Back

Aplicații 1. Completează cu cuvintele potrivite: siderit răspândit hematit meteoriți pirita magnetit patru limonit După aluminiu, fierul este cel mai ________ metal din scoarța terestră și ocupă locul ______ între elementele chimice. În stare liberă, fierul se găsește în _________. În scoarța terestră se găsește sub formă de compuși în următoarele minereuri: _______ (Fe 2 O 3), _________ (Fe 3 O 4), _________(Fe. S 2), ________ (Fe. CO 3), _________ (Fe 2 O 3. H 2 O) 2. Rebus 1 F U 2 O Ţ 3 L A M I N A 4 M A G N E T I 5 H E M A T R E R C I N A L L E E T 1 – Cuptor înalt pentru obţinerea fontei 2 – Aliaj al fierului cu 0, 04 – 1, 5%C Proprietatea metalelor de a fi trase în foi 4 – proprietăţi ale pe baza cărora, pilitura de fier se poate separa dintr-un amestec pe care aceasta îl formează cu sulful 5 – Minereu de fier cu formula Fe 2 O 3 Combinatul siderurgic Arcelor Mittal Galaţi Back

Răspunde la cele şapte întrebări şi descoperă un monument ciudat… Descoperă… 1. Nu se găsește în natură izotopul: GREŞIT! a) 54 Fe GREŞIT! b) 56 Fe CORECT! c) 60 Fe 2. Procentul de fier din Fe 2 O 3 este: a) CORECT! 70, 00% b) GREŞIT! 52, 33% c)GREŞIT! 72, 41% 3. Fierul se găsește alături de cupru în: a)CORECT! Calcopirita b) GREŞIT! Pirita c) GREŞIT! Siderit 4. La reacția a 0, 5 moli Fe cu HCl, se degajă: GREŞIT! a)2 g. H 2 CORECT! b)1 g. H 2 c)reacția nu are GREŞIT! loc 5. 0, 1 moli Fe reacționează cu: a) 98 g. H SO 2 4 CORECT! 10% b) reacția nu are GREŞIT! loc c) 9, 8 g H 2 SO 4 GREŞIT! 10% 6. Care din următoarele proprietăți ale Fe sunt utilizate la fabricarea transformatoarelor? a)GREŞIT! ductilitatea b) proprietățile CORECT! magnetice c) maleabilitatea GREŞIT! 7. Cantitatea de fontă cu 4%C obținută din 994 kg siderit este: a) GREŞIT! 560 kg GREŞIT! b) 500 g CORECT! c) 500 kg C O L O A N A F I E D R E D D L H I E N I Înaltă de șase metri și grea de șase tone are o vechime de peste 1500 de ani. Cu toate acestea, ea nu a fost atacată de rugină, datorită compoziției sale chimice: 99, 72%Fe și 0, 28%C, fără nici o altă impuritate. Back

Click pe momentul lecției Generalităţi Stare naturală Obţinerea industrială Obţinerea în laborator Proprietăţi fizice Proprietăţi chimice Utilizări Descoperă… CUPRUL Diagramă Back

Generalităţi Atomul de cupru Structura atomului Numărul atomic Z = 29 Numărul de masă A = 64 Simbolul chimic: Cu Cupru Mol de atomi: 64 g Cu conțin NA = 6, 023 * 1023 atomi Nucleu Protoni (p+) – 29 Neutroni (n 0) - 35 Înveliș electronic Electroni (e-) - 29 K– 2 L– 8 M – 18 N-1 Cuprul prezintă 29 izotopi. Dintre aceștia, doar izotopii 63 Cu și 65 Cu sunt stabili, toți ceilalți fiind radioactivi Poziția în sistemul periodic. Valența Numărul perioadei se stabilește pornind de la numărul de straturi ocupate cu electroni. Cuprul este poziționat în grupa secundară I B, deoarece completează cu electroni penultimul strat (M) Prezintă în mod uzual valența I (Cu. Cl) sau II (Cu. Cl 2, Cu. SO 4, Cu(OH)2) Perioada: 4 Grupa I B Valențe: I, II Back

Stare naturală Cuprul se găsește atât în stare nativă, cât și în combinații chimice, cum ar fi: o Calcopirită - Cu. Fe. S 2 ; o Calcozină - Cu 2 S; o Cuprit - Cu 2 O; o Malachit - Cu. CO 3*Cu(OH)2; o Azurit - 2 Cu. CO 3*Cu(OH)2. Compuși în care se găsește cuprul: o Clorură de cupru (II) - Cu. Cl 2; o Oxid de cupru (II) - Cu. O; o Carbonat de cupru, - Cu. CO 3; o Sulfat de cupru, - Cu. SO 4; Cariera de la Roșia Poieni – cel mai mare zăcământ de cupru din România Mina Chuquicamata (Chile), este cea mai mare mină de cupru din lume. Având 850 de metri adâncime, Chuqui este a doua cea mai adâncă mină din lume. De aici s-au extras 29 de milioane de tone de cupru în 2007 și chiar dacă aceasta este exploatată intens de 90 de ani, rămâne una din cele mai mari resurse de cupru din lume. Back

Obţinerea industrială Minereurile conțin de obicei 2 -4%Cu, rareori peste 7%. De aceea, înainte de procedeul de obținere a metalului, este necesară o prăjire parțială, cu aer insuficient. Se obține o zgură formată din sulfură de fier și de cupru, numită mată cuproasă. 2 Cu 2 S + 3 O 2 = 2 Cu 2 O + 2 SO 2 Oxidul cupros este transformat în cupru impur prin încălzire: 2 Cu 2 O = 4 Cu + O 2 Cuprul obținut în această reacție are puritatea de 95 -98%; Îndepărtarea impurităților se face într-un cuptor cu flacără, sau prin cuprul electrolitic (prin electroliză), obținându-se cupru de puritate aproape maximă, 99, 9%. Back

Obţinerea în laborator : URCUL ED DOM ed ălutaps o ăpa uc lurahap nî udortn. I. 1 atehcite ep kcilc( 4 OSu. C , urpuc ed taflus. )4 OSu. C uc iulutneipicer eițulos uc lurahap nî reif ed luiuc udortn. I. 2 ăpud ivresbo e. C. )iuc ep kcilc( 4 OSu. C ed ? pmit nu ed citaişor tarts nu uc tirepoca a-s luiu. C. )u. C( urpuc ăca. D. eraoluc al sihcsed a-s 4 OSu. C ed aiţulo. S av es aiţulos , eraunitnoc nî luiuc eniţ mov iulutaflus iirămrof ătirotad , edrev nî aroloc. )4 OSe. F( reif ed ↓u. C + 4 OSe. F→ 4 OSu. C + e. F Back

Proprietăţi fizice o o o o Stare de agregare solidă; Culoare brun – roşiatică, prezintă luciu metalic; este unul dintre cele trei metale care nu prezintă culoarea gri sau argintiu (alături de aur – galben și osmiu - albastru); Densitate mare (ρ = 8, 96 g/cm 3 ); Duritate mică (3 pe scara Mohs); Foarte bun conducător termic şi electric; Maleabil şi ductil; Temperatură de topire mare (1083 o. C); Formează aliaje (cele mai cunoscute fiind alama și bronzul) Obiecte din alamă (stânga) și bronz (dreapta) Tablă și sârmă de cupru Cuprul a fost primul metal folosit de către om la confecționarea uneltelor (perioada eneolitică). Odată cu obținerea bronzului, s-a renunțat la cupru, din cauza durității mici a acestuia. Metale colorate: Osmiu(albastru), Aur(galben), și Cupru(brun roșcat) Back

Proprietăți chimice Reacţia cuprului cu acizii Reacţia cuprului cu nitratul de argint Reacția cuprului cu oxigenul Back

iulurpuc aițcae. R iizica uc : URCUL ED DOM ep kcilc( eteburpe icnic elec nî urpuc ed ereblup udortn. I )urpu. C uc iulutneipicer atehcite dica , l. CH , cirdihrolc dica udortni 4 iș 2 , 1 eleteburpe nÎ kcilc( taulid 3 ONH cirtin dica vitcepser taulid , 4 OS 2 H , ciruflus ? ălpmâtnî es e. C )ivitcaer uc roletneipicer eletehcite ep . 1. 2 ludica iș taulid ciruflus ludica , cirdihrolc ludic. A. lurpuc ăcata un taulid cirtin ep kcilc( tartnecnoc ciruflus dica ăguada 3 ateburpe nÎ ? ălpmâtnî es e. C. )cnoc 4 OS 2 H uc iulutneipicer atehcite . 3 ep iopa , COF ED ĂSRUS ep kcilc( ateburpe iopa etșezlăcnÎ ? ivresbo e. C. )ăteburpe . 4 . ecer al lurpuc ăcata un tartnecnoc ciruflus ludic. A ed erajaged ărăf eițcaer o col era , erizlăcnî a. L ed dixoid , urpuc ed taflus ăzaemrof e. S . negordih. ăpa iș flus O 2 H 2 + ↑ 2 OS + 4 OSu. C → 4 OS 2 H 2 + u. C atehcite ep kcilc( tartnecnoc cirtin dica ăguada 5 ateburpe nÎ ? ălpmâtnî es e. C. )cnoc 3 ONH uc iulutneipicer . 5 ed erajaged ărăf eițcaer o col era , erizlăcnî a. L ed dixo , urpuc ed tatoza ăzaemrof e. S . negordih. ăpa iș toza O 2 H 4 + ↑ON 2 + 2)3 ON(u. C 3 → 3 ONH 8 + u. C 3 kca. B

Ag. NO 3 Reacția cu nitratul de argint : URCUL ED DOM taflus ed ălutaps o ăpa uc lurahap nî udortn. I. 1 atehcite ep kcilc( 3 ONg. A , tnigra ed tartin ed. )3 ONg. A uc iulutneipicer uc lurahap nî urpuc ed auaets udortn. I. 2 ivresbo e. C. )aets ep kcilc( 3 ONg. A ed eițulos ? pmit nu ăpud tnigra ed tarts nu uc tirepoca a-s auaet. S. )g. A( urtsabla nî aeraoluc tabmihcs a-iș aiţulo. S. 2)3 ON(u. C , urpuc ed iulutartin ătirotad ↓g. A 2 + 2)3 ON(u. C → 3 ONg. A 2 + u. C Back

iulurpuc aițcae. R lunegixo uc : URCUL ED DOM ĂSRUS ep kcilc( zag ed luceb ednirp. A. 1 )COF ED atehcite ep kcilc( urpuc ed ăţucălp o a. I. 2 )u. C ed eţucălp uc iulutneipicer ed amrâs uda , iuletșelc lurotuja u. C. 3 ep kcil. C( o-etșezlăcnî iș ărăcalf nî urpuc ? ivresbo e. C. )etșelc ăzaeroloc urpuc ed ațucălp , ărăcalf nî ăsudortn. I. urpuc ed ludixo ăzaemrof e. S. edrev nî arăcalf Ou. C 2 = 2 O + u. C 2 kca. B

Utilizări Statui Tablă Radiatoare pentru mașini Vase de aramă Site Țevi, tuburi Monezi Circuite integrate Statui Cabluri și conductor i electrici Robineți Alambicuri Back
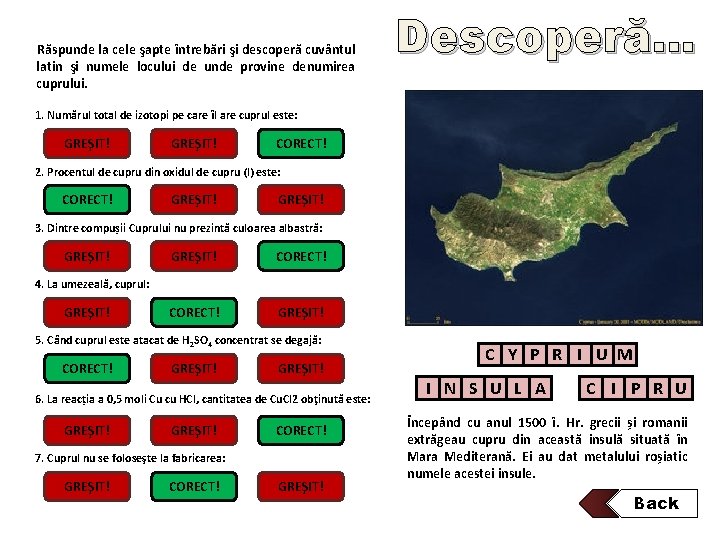
Răspunde la cele şapte întrebări şi descoperă cuvântul latin şi numele locului de unde provine denumirea cuprului. Descoperă… 1. Numărul total de izotopi pe care îl are cuprul este: GREŞIT! a) 2 GREŞIT! b) 27 CORECT! c) 29 2. Procentul de cupru din oxidul de cupru (I) este: CORECT! a) 88, 88 GREŞIT! b) 80 GREŞIT! c) 66, 67 3. Dintre compușii Cuprului nu prezintă culoarea albastră: a)GREŞIT! Cu(NO 3)2 b) GREŞIT! Cu. SO 4 CORECT! c) Cu. CO 3 b) coclește CORECT! c. GREŞIT! ) pasivează 4. La umezeală, cuprul: a)GREŞIT! ruginește 5. Când cuprul este atacat de H 2 SO 4 concentrat se degajă: CORECT! a) SO 2 GREŞIT! b) H 2 c) reacția nu GREŞIT! are loc 6. La reacția a 0, 5 moli Cu cu HCl, cantitatea de Cu. Cl 2 obţinută este: a) GREŞIT! 67, 5 g GREŞIT! b) 135 g c) Reacţia nu CORECT! are loc 7. Cuprul nu se foloseşte la fabricarea: a)GREŞIT! bronzului CORECT! b) fontei c)GREŞIT! alamei C Y P R I U M I N S U L A C I P R U Începând cu anul 1500 î. Hr. grecii și romanii extrăgeau cupru din această insulă situată în Mara Mediterană. Ei au dat metalului roșiatic numele acestei insule. Back

Diagramă Analizează literele înscrise în diagramă și găsește numele a cinci compuși ai cuprului și a două aliaje. Pentru a confirma apasă pe prima literă a denumirii C A L C O Z I N A L D C O L C Z U R I T H M C A D M H N C P E O S C C STOP START JOC! B A T E R M V C L T I H C A L A M R N C U P R I C M C N B F S A T E C L R A T I R I S T O C P O C L 00 58 02 01 03 57 56 55 54 53 52 51 50 49 48 47 46 45 44 43 42 41 40 39 38 37 36 35 34 33 32 31 30 29 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 13 12 11 10 09 08 07 06 05 04 03 02 01 59 00 Calcopirita Calcozină Malachit Azurit Cuprit R A C Bronz Alama Apasă butonul START pentru a începe jocul. Ai trei minute pentru a descoperi cele șapte denumiri! Back
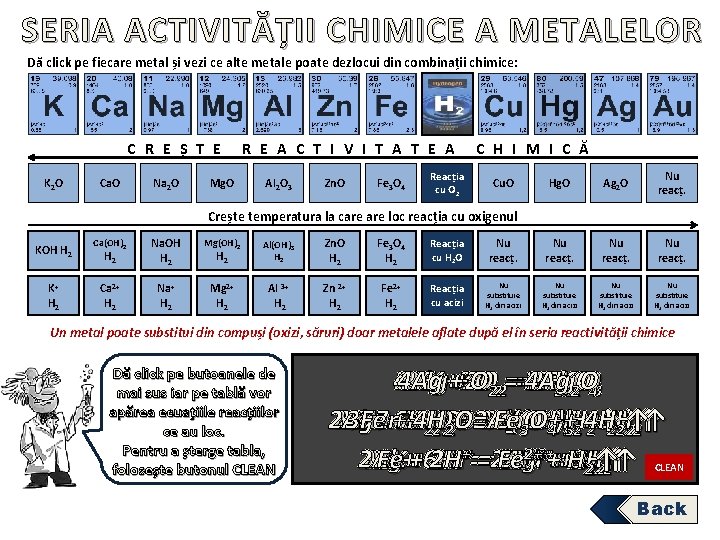
SERIA ACTIVITĂȚII CHIMICE A METALELOR Dă click pe fiecare metal și vezi ce alte metale poate dezlocui din combinații chimice: C R E Ș T E K 2 O Ca. O Na 2 O Mg. O R E A C T I V I T A T E A Al 2 O 3 Zn. O Fe 3 O 4 Reacția cu O 2 C H I M I C Ă Cu. O Hg. O Ag 2 O Nu reacț. Crește temperatura la care loc reacția cu oxigenul KOH H 2 K+ H 2 Ca(OH)2 H 2 Na. OH H 2 Mg(OH)2 H 2 Al(OH)3 H 2 Zn. O H 2 Fe 3 O 4 H 2 Reacția cu H 2 O Nu reacț. Ca 2+ H 2 Na+ H 2 Mg 2+ H 2 Al 3+ H 2 Zn 2+ H 2 Fe 2+ H 2 Reacția cu acizi Nu substituie H 2 din acizi Un metal poate substitui din compuși (oxizi, săruri) doar metalele aflate după el în seria reactivității chimice Dă click pe butoanele de mai sus iar pe tablă vor apărea ecuațiile reacțiilor ce au loc. Pentru a șterge tabla, folosește butonul CLEAN 4 Al 2 Mg 4 Na 4 Ag 3 Fe 2 Hg 2 Ca 2 Cu 2 Zn 4 K++++3 O 2 O O O 2222===4 Ag 2 K 2 Na 2 Al 2 Ca. O 2 Mg. O 2 Zn. O 2 Cu. O 2 Hg. O Fe 23 O O 43 2 O 2 Al Mg 2 Na Ca 3 Fe 2 K+Zn ++6 H +2 H 4 H O= O= 2 Al(OH) =Mg(OH) Ca(OH) Fe Zn. O 2 KOH 2 Na. OH +2++4 H H H 3 H H ↑ +2 H O= +↑ H 2↑ ↑ 2 H 2 O= 222 O 3 O 4+ 2+ 3 H 2+ 2 22↑ 2+ 3+ +2+ ++ 2 Al Mg Na Ca Zn Fe 2 K+++6 H 2 H 2 H++++===2 Al 2 Na Ca Mg Zn Fe 2 K 2+ ++++H H 3 H HH 222↑ ↑ 2↑ 2↑ 2↑ CLEAN Back
Click pe momentul lecției Definiţie, clasificare Denumirea Metode obţinere Proprietăţi fizice Proprietăţi chimice Utilizări Aplicaţii Identifică oxizii OXIZI Back

Definiţie, clasificare OXIZII sunt compuși ai nemetalelor și metalelor cu oxigenul Oxizii se clasifică în: Oxizi acizi (nemetalici) – conțin atomi (nemetalici) ai unor nemetale și oxigen, de exemplu, oxizi ai carbonului (CO; CO 2), siliciului (Si. O 2), oxizi ai azotului(N 2 O, NO, N 2 O 3, NO 2, N 2 O 5), ai sulfului (SO 2) etc. Oxizi bazici (metalici) – conțin atomi ai unor metale și oxigen, de exemplu: oxizi ai metalelor alcaline (Na 2 O, K 2 O), oxizi ai metalelor alcalino-pământoase (Ca. O, Mg. O, Ba. O), oxizi ai metalelor din blocul p (Al 2 O 3, Pb. O 2), oxizi ai metalelor tranziționale (Fe 2 O 3, Fe. O, Cu 2 O, Cu. O, Mn. O 2 ) etc. Formula generală a oxizilor nemetalici E 2 O x E – nemetal X – valența nemetalului Formula generală a oxizilor metalici M 2 O x M – metal X – valența metalului Back
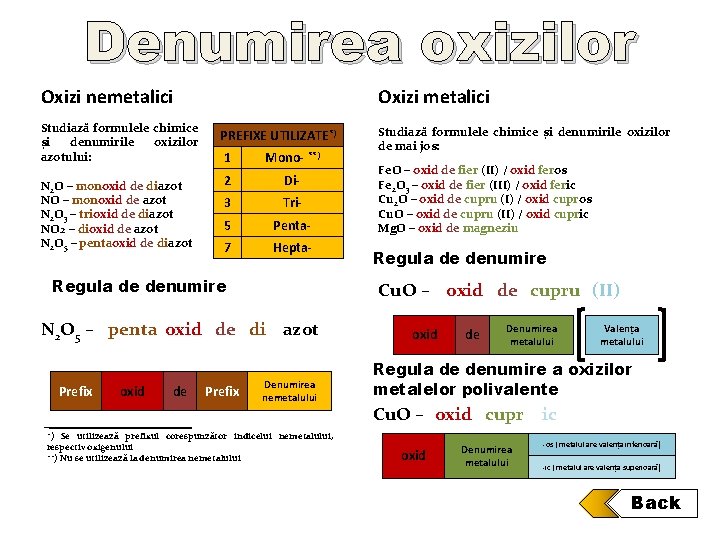
Denumirea oxizilor Oxizi nemetalici Studiază formulele chimice și denumirile oxizilor azotului: N 2 O – monoxid de diazot NO – monoxid de azot N 2 O 3 – trioxid de diazot NO 2 – dioxid de azot N 2 O 5 – pentaoxid de diazot Oxizi metalici PREFIXE UTILIZATE*) 1 Mono- **) 2 Di- 3 Tri- 5 Penta- 7 Hepta- Regula de denumire oxid de Prefix Fe. O – oxid de fier (II) / oxid feros Fe 2 O 3 – oxid de fier (III) / oxid feric Cu 2 O – oxid de cupru (I) / oxid cupros Cu. O – oxid de cupru (II) / oxid cupric Mg. O – oxid de magneziu Regula de denumire Cu. O – oxid de cupru (II) N 2 O 5 – penta oxid de di azot Prefix Studiază formulele chimice și denumirile oxizilor de mai jos: Denumirea nemetalului *) Se utilizează prefixul corespunzător indicelui nemetalului, respectiv oxigenului **) Nu se utilizează la denumirea nemetalului oxid de Denumirea metalului Valența metalului Regula de denumire a oxizilor metalelor polivalente Cu. O – oxid cupr ic oxid Denumirea metalului -os ( metalul are valența inferioară) -ic ( metalul are valența superioară) Back
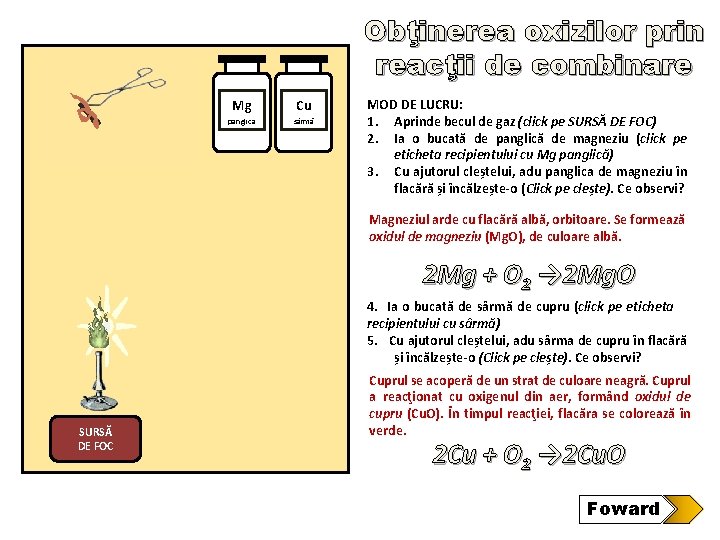
Obţinerea oxizilor prin reacţii de combinare Mg Cu panglica sârmă MOD DE LUCRU: 1. Aprinde becul de gaz (click pe SURSĂ DE FOC) 2. Ia o bucată de panglică de magneziu (click pe eticheta recipientului cu Mg panglică) 3. Cu ajutorul cleștelui, adu panglica de magneziu în flacără și încălzește-o (Click pe clește). Ce observi? Magneziul arde cu flacără albă, orbitoare. Se formează oxidul de magneziu (Mg. O), de culoare albă. 2 Mg + O 2 → 2 Mg. O 4. Ia o bucată de sârmă de cupru (click pe eticheta recipientului cu sârmă) 5. Cu ajutorul cleștelui, adu sârma de cupru în flacără și încălzește-o (Click pe clește). Ce observi? SURSĂ DE FOC Cuprul se acoperă de un strat de culoare neagră. Cuprul a reacţionat cu oxigenul din aer, formând oxidul de cupru (Cu. O). În timpul reacţiei, flacăra se colorează în verde. 2 Cu + O 2 → 2 Cu. O Foward

Obţinerea oxizilor prin reacţii de descompunere : URCUL ED DOM amirp ep kcil. C( vitats nid ăteburpe o a. I. 1 )agnâts nid ăteburpe tanobrac ed ălutaps o ăteburpe nî udortn. I. 2 atehcite ep kcilc( 3 OCu. C , urpuc ed )3 OCu. C uc iulutneipicer ED ĂSRUS ep kcilc( zag ed luceb etșenro. P. 3 ? ivresbo e. C. )COF eraoluc ed ăuon ăţnatsbus o erapa , pmit niţup ăpu. D. )Ou. C( urpuc ed ludixo – ărgaen arug al l-uda iș lutirbihc iopa ednirp. A. 4 es e. C. )tirbihc ep kcilc( ieteburpe ? ălpmâtnî – tatluzer sudorp tlaliulec ătirotad snits a-s lutirbih. C eniţertnî un erac zag – )2 OC( nobrac ed ludixoid. aeredra ↑ 2 OC + Ou. C→ 3 OCu. C Back

Proprietăţi fizice Starea de agregare La temperaturi obișnuite, majoritatea oxizilor sunt: • gazoși (CO 2, SO 2, NO 2) • Solizi (Ca. O, P 2 O 5, Si. O 2) Culoarea • Incolori (CO 2, Si. O 2); • Colorați (Ca. O – alb, Cu. O – negru, Hg. O – roșu, Cr 2 O 3 – verde, Pb 3 O 4 – portocaliu, Pb. O – galben ș. a. ) Un oxid special – cuarțul • unele varietăți sunt transparente, refractă lumina; • luciu sticlos pe fețele prismei, gras pe suprafața de spărtură; • duritate mare (7 pe scara Mohs) • punct de topire ridicat (1713 o. C) • prezintă proprietăți piezoelectrice. Back

Proprietăţi chimice Reacţia oxizilor acizi cu apa Reacţia oxizilor bazici cu acizii Reacţia oxizilor bazici cu apa Reacţia oxizilor acizi cu bazele Back
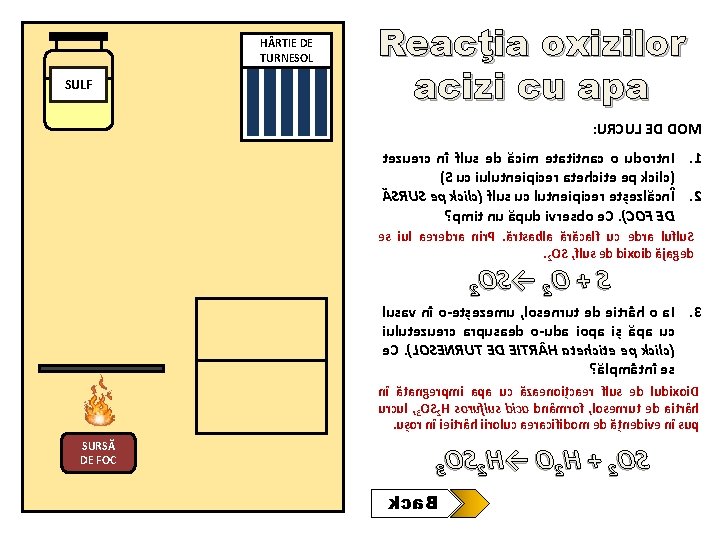
H RTIE DE TURNESOL SULF Reacţia oxizilor acizi cu apa : URCUL ED DOM tezuerc nî flus ed ăcim etatitnac o udortn. I. 1 )S uc iulutneipicer atehcite ep kcilc( ĂSRUS ep kcilc( flus uc lutneipicer etșezlăcnÎ. 2 ? pmit nu ăpud ivresbo e. C. )COF ED es iul aeredra nir. P. ărtsabla ărăcalf uc edra luflu. S. 2 OS , flus ed dixoid ăjaged 2 OS→ 2 O + S lusav nî o-etșezemu , losenrut ed eitrâh o a. I. 3 iulutezuerc arpusaed o-uda iopa iș ăpa uc e. C. )LOSENRUT ED EITR H atehcite ep kcilc( ? ălpmâtnî es nî ătangerpmi apa uc ăzaenoițcaer flus ed ludixoi. D urcul , 3 OS 2 H soruflus dica dnâmrof , losenrut ed aitrâh. ușor nî ieitrâh iiroluc aeracifidom ed ățnedive nî sup SURSĂ DE FOC 3 OS 2 H→ O 2 H + 2 OS kca. B
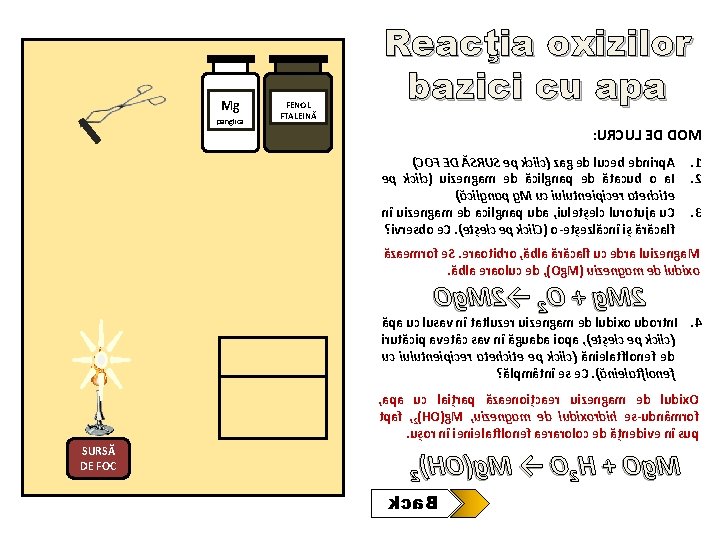
Mg panglica FENOL FTALEINĂ Reacţia oxizilor bazici cu apa : URCUL ED DOM )COF ED ĂSRUS ep kcilc( zag ed luceb ednirp. A ep kcilc( uizengam ed ăcilgnap ed ătacub o a. I )ăcilgnap g. M uc iulutneipicer atehcite nî uizengam ed acilgnap uda , iuletșelc lurotuja u. C ? ivresbo e. C. )etșelc ep kcil. C( o-etșezlăcnî iș ărăcalf . 1. 2. 3 ăzaemrof e. S. eraotibro , ăbla ărăcalf uc edra luizenga. M. ăbla eraoluc ed , )Og. M( uizengam ed ludixo Og. M 2→ 2 O + g. M 2 ăpa uc lusav nî tatluzer uizengam ed ludixo udortn. I. 4 irutăcip avetâc sav nî ăguada iopa , )etșelc ep kcilc( uc iulutneipicer atehcite ep kcilc( ănielatflonef ed ? ălpmâtnî es e. C. )ănielatflonef , apa uc laițrap ăzaenoițcaer uizengam ed ludix. O tpaf , 2)HO(g. M , uizengam ed ludixordih es-udnâmrof. ușor nî ienielatflonef aeraroloc ed ățnedive nî sup SURSĂ DE FOC 2)HO(g. M → O 2 H + Og. M kca. B

rolizixo aiţcae. R elezab uc izica : URCUL ED DOM ateburpe nî 3 OCu. C , urpuc ed tanobrac udortn. I )3 OCu. C uc iulutneipicer atehcite ep kcilc( ăcim nî )HOa. N( uidos ed dixordih ed eițulos ăguad. A irutăcip avetâc iș ăguada iopa , eram ateburpe iulutneipicer atehcite ep kcilc( ănielatflonef ed. )ănielatflonef vitcepser HOa. N uc ED ĂSRUS ep kcilc( zag ed luceb iopa ednirp. A aec nî ra. D ? ăcim ateburpe nî ivresbo e. C. )COF ? eram . 1. 2 . 3 ed dixo nî enupmocsed es 3 OCu. C , ăcim ateburpe nÎ. 2 OC , nobrac ed dixoid iș Ou. C , urpuc ↑ 2 OC + Ou. C→ 3 OCu. C eceraoed , ăzaeroloced es aițulos , eram ateburpe nÎ. atsaeca nid uidos ed ludixordih uc ăzaenoițcaer 2 OC O 2 H + 3 OC 2 a. N→HOa. N 2 + 2 OC kca. B
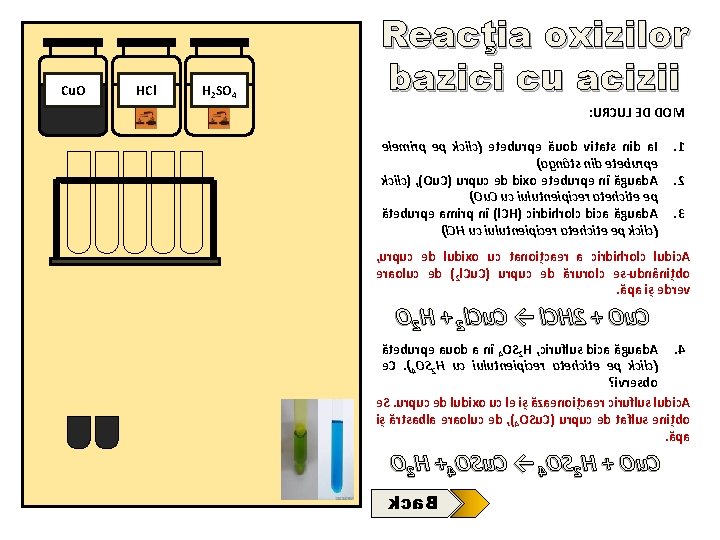
Cu. O HCl H 2 SO 4 Reacţia oxizilor bazici cu acizii : URCUL ED DOM elemirp ep kcilc( eteburpe ăuod vitats nid a. I )agnâts nid eteburpe kcilc( , )Ou. C( urpuc ed dixo eteburpe nî ăguad. A )Ou. C uc iulutneipicer atehcite ep ăteburpe amirp nî )l. CH( cirdihrolc dica ăguad. A )l. CH uc iulutneipicer atehcite ep kcilc( . 1. 2. 3 , urpuc ed ludixo uc tanoițcaer a cirdihrolc ludic. A eraoluc ed )2 l. Cu. C( urpuc ed ărurolc es-udnânițbo. ăpa iș edrev O 2 H + 2 l. Cu. C → l. CH 2 + Ou. C ăteburpe auod a nî 4 OS 2 H , ciruflus dica ăguad. A. 4 e. C. )4 OS 2 H uc iulutneipicer atehcite ep kcilc( ? ivresbo e. S. urpuc ed ludixo uc le iș ăzaenoițcaer ciruflus ludic. A iș ărtsabla eraoluc ed , )4 OSu. C( urpuc ed taflus enițbo. ăpa O 2 H +4 OSu. C → 4 OS 2 H + Ou. C kca. B
Utilizări Zăpadă carbonică Catalizatori Pigmenți Utilizări generale Materii prime pentru substanțe Abrazive pe bază de Al 2 O 3 Pietre semiprețioase Stingătoare Tratarea unor boli (mofete) Substanță criogenă CO 2 Sifoane Băuturi carbogazoase Decoloranți Sticlă de cuarț Metalurgie Văruire pomi SO 2 Dezinfectanți Refractometre Materiale construcții Si. O 2 Ceasuri electronice Ind. Sticlei Rafinarea petrolului Compuși ai Si Acid sulfuric Rafinarea zahărului Ca. O Agricultură Materiale construcții Back
Aplicaţii Denumiți și clasificați următorii oxizi, ale căror formule chimice sunt: CO 2 Dioxid de carbon Oxid acid Fe 2 O 3 Oxid de fier (III) Oxid bazic SO 2 Dioxid de sulf Oxid acid CO Monoxid de carbon Oxid acid Fe. O Oxid de fier (II) Oxid bazic Al 2 O 3 Oxid de aluminiu Oxid bazic Na 2 O Oxid de sodiu Oxid bazic P 2 O 5 Pentaoxid de fosfor Oxid acid Ca. O Oxid de calciu Oxid bazic Back

Identifică oxizii Ca. O Var nestins H 2 O 2 (30%) Perhidrol Răspunde la întrebările de mai jos și află denumirile uzuale oxizilor din imagini! CO 2 solid Zăpadă carbonică Fe 2 O 3 Hematit Întrebarea 8 Întrebarea 5 Întrebarea 1. Întrebarea 2. Întrebarea 6 Întrebarea 7 Întrebarea 3 Întrebarea 4 Compusul rezultat în urma reacției La descompunerea oxidului de mercur, Formula generală a oxizilor metalici Dioxidul de azot, NO Cantitatea necesară de Ca(OH) La reacția Cu. O cu H 2 SO 2 prezintă 4, soluția finală 2 Nu este oxid metalic: La descompunerea Cu. CO dintre SO starea de agregare a metalului rezultat 2 și apă, colorează hârtia de 3 se obțin: este: culoarea: necesară reacției cu 0, 3 moli CO va avea culoarea: 2 este: turnesol în: este: Al 2 O 3 Corindon Mn. O 2 Piroluzit Si. O 2 Nisip, Cuarț Pb. O Litargă a) Dioxid a) Cu și a) brun a) lichidă CORECT! GREȘIT! a) verde a) 44, 4 g a)roșu a)E 2 Ox de siliciu roșcat CO 2 b) Dioxid b) Cu. O și b) albastră b)albastru b) incolor CORECT! b) solidă CORECT GREȘIT! b) M b) 22, 2 g O de plumb CO 22 x Back

Click pe momentul lecției Clasificare, denumire Definiţie Stare naturală Obţinerea in industrie Obţinerea in laborator Proprietăţi fizice Proprietăti chimice Proprietăţi chimice generale Utilizări ACIZI Aplicaţii Descoperă… Back
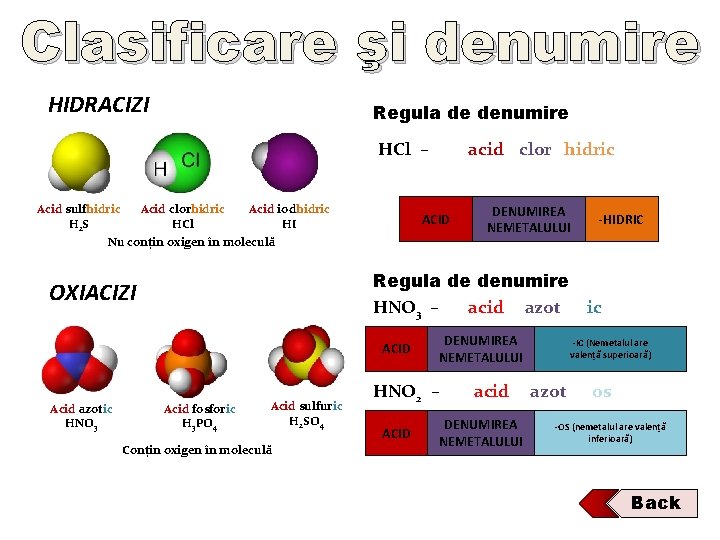
Clasificare şi denumire HIDRACIZI Regula de denumire HCl – Acid sulfhidric H 2 S Acid clorhidric HCl Acid iodhidric HI acid clor hidric ACID Nu conțin oxigen în moleculă -HIDRIC Regula de denumire HNO 3 – acid azot ic OXIACIZI ACID Acid azotic HNO 3 DENUMIREA NEMETALULUI Acid fosforic H 3 PO 4 Acid sulfuric H 2 SO 4 Conțin oxigen în moleculă DENUMIREA NEMETALULUI HNO 2 – ACID acid DENUMIREA NEMETALULUI -IC (Nemetalul are valență superioară) azot os -OS (nemetalul are valență inferioară) Back

Definiţie, forma generală ACIZII sunt compuși chimici ce conțin în moleculă unul sau mai mulți atomi de hidrogen și un radical acid FORMA GENERALĂ HIDRACIZI H X E OXIACIZI HXEOY(Y-1) E – nemetal X – valența nemetalului Back
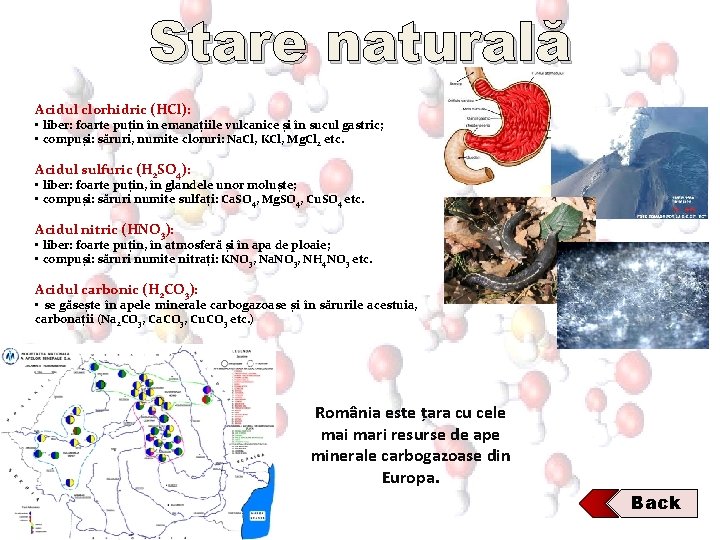
Stare naturală Acidul clorhidric (HCl): • liber: foarte puțin în emanațiile vulcanice și în sucul gastric; • compuși: săruri, numite cloruri: Na. Cl, KCl, Mg. Cl 2 etc. Acidul sulfuric (H 2 SO 4): • liber: foarte puțin, în glandele unor moluște; • compuși: săruri numite sulfați: Ca. SO 4, Mg. SO 4, Cu. SO 4 etc. Acidul nitric (HNO 3): • liber: foarte puțin, în atmosferă și în apa de ploaie; • compuși: săruri numite nitrați: KNO 3, Na. NO 3, NH 4 NO 3 etc. Acidul carbonic (H 2 CO 3): • se găsește în apele minerale carbogazoase și în sărurile acestuia, carbonații (Na 2 CO 3, Ca. CO 3, Cu. CO 3 etc. ) România este țara cu cele mai mari resurse de ape minerale carbogazoase din Europa. Back

Obţinerea în industrie Obținerea industrială a HCl Acidul clorhidric se obține prin sinteză din elementele componente, prin arderea hidrogenului în atmosferă de clor. H 2 + Cl 2 → 2 HCl(g)↑ Obținerea industrială a H 2 SO 4 Pentru obținerea H 2 SO 4 se utilizează procedeul prin contact. Procesul are loc în trei etape: 1. Obținerea dioxidului de sulf prin prăjirea piritei: 4 Fe. S 2 + 11 O 2 → 2 Fe 2 O 3 + 8 SO 2↑ 2. Oxidarea dioxidului de sulf la trioxid de sulf: 2 SO 2 + O 2 → 2 SO 3↑ 3. Absorbția trioxidului de sulf în apă: SO 3 + H 2 O → H 2 SO 4 Back
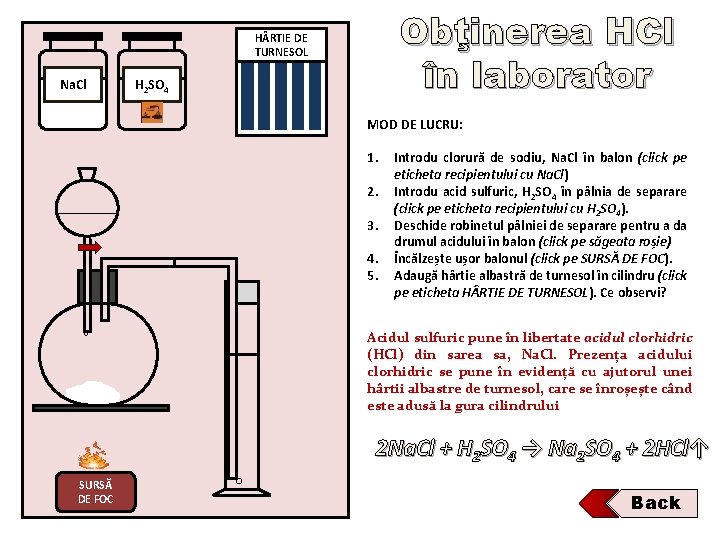
Obţinerea HCl în laborator H RTIE DE TURNESOL Na. Cl H 2 SO 4 MOD DE LUCRU: 1. 2. 3. 4. 5. Introdu clorură de sodiu, Na. Cl în balon (click pe eticheta recipientului cu Na. Cl) Introdu acid sulfuric, H 2 SO 4 în pâlnia de separare (click pe eticheta recipientului cu H 2 SO 4). Deschide robinetul pâlniei de separare pentru a da drumul acidului în balon (click pe săgeata roșie) Încălzește ușor balonul (click pe SURSĂ DE FOC). Adaugă hârtie albastră de turnesol în cilindru (click pe eticheta H RTIE DE TURNESOL). Ce observi? Acidul sulfuric pune în libertate acidul clorhidric (HCl) din sarea sa, Na. Cl. Prezența acidului clorhidric se pune în evidență cu ajutorul unei hârtii albastre de turnesol, care se înroșește când este adusă la gura cilindrului 2 Na. Cl + H 2 SO 4 → Na 2 SO 4 + 2 HCl↑ SURSĂ DE FOC Back

Proprietăţi fizice • Acizii pot fi substanțe gazoase (HCl, H 2 S), lichide (HNO 3, H 2 SO 4) sau solide (H 3 PO 4) • Toți acizii sunt solubili în apă; • Soluțiile acizilor prezintă gust acru; • Soluțiile acizilor sunt bune conducătoare de electricitate (se mai numesc și electroliți) Acizii tari sunt substanțe corozive. Ei provoacă puternice leziuni ale pielii și țesuturilor! Proprietăți fizice ale HCl • gaz incolor, miros caracteristic înțepător; • densitate mai mare decât apa; • foarte solubil în apă (soluțiile de acid clorhidric fumegă în aer). Proprietăți fizice ale H 2 SO 4 • lichid uleios, incolor, inodor; • densitate mai mare decât apa; • solubil în apă; la dizolvare se degajă căldură; • foarte avid de apă; La prepararea soluțiilor de acid sulfuric nu se toarnă niciodată apă în acid! Se va turna prin prelingere acidul în apă. Proprietăți fizice ale HNO 3 • lichid, incolor, miros înțepător; • densitate mai mare decât apa; • solubil în apă. Back

Acţiunea asupra indicatorilor Reacţia cu metalele Reacţia cu oxizi metalici Reacţia cu bazele Proprietăţi chimice generale Reacţia HCl cu Ag. NO 3 Reacţia H 2 SO 4 cu Ba. Cl 2 Reacţia HCl cu Na 2 CO 3 Back
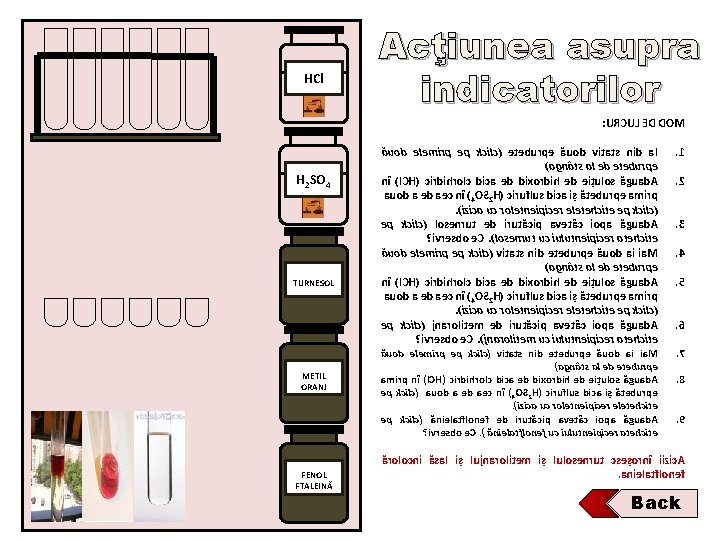
HCl Acţiunea asupra indicatorilor : URCUL ED DOM H 2 SO 4 TURNESOL METIL ORANJ FENOL FTALEINĂ ăuod elemirp ep kcilc( eteburpe ăuod vitats nid a. I )agnâts al ed eteburpe nî )l. CH( cirdihrolc dica ed dixordih ed eițulos ăguad. A auod a ed aec nî )4 OS 2 H( ciruflus dica iș ăteburpe amirp. )izica uc roletneipicer eletehcite ep kcilc( losenrut ed irutăcip avetâc iopa ăguad. A ? ivresbo e. C. )losenrut uc iulutneipicer atehcite ăuod elemirp ep kcilc( vitats nid eteburpe ăuod ai ia. M )agnâts al ed eteburpe nî )l. CH( cirdihrolc dica ed dixordih ed eițulos ăguad. A auod a ed aec nî )4 OS 2 H( ciruflus dica iș ăteburpe amirp. )izica uc roletneipicer eletehcite ep kcilc( jnarolitem ed irutăcip avetâc iopa ăguad. A ? ivresbo e. C. )jnarolitem uc iulutneipicer atehcite ăuod elemirp ep kcilc( vitats nid eteburpe ăuod ai ia. M )agnâts al ed eteburpe amirp nî )l. CH( cirdihrolc dica ed dixordih ed eițulos ăguad. A ep kcilc( auod a ed aec nî )4 OS 2 H( ciruflus dica iș ăteburpe. )izica uc roletneipicer eletehcite ep kcilc( ănielatflonef ed irutăcip avetâc iopa ăguad. A ? ivresbo e. C. ) ănielatflonef uc iulutneipicer atehcite . 1. 2. 3. 4. 5. 6. 7. 8. 9 ărolocni ăsal iș lujnarolitem iș lulosenrut cseșornî iizic. A. anielatflonef Back
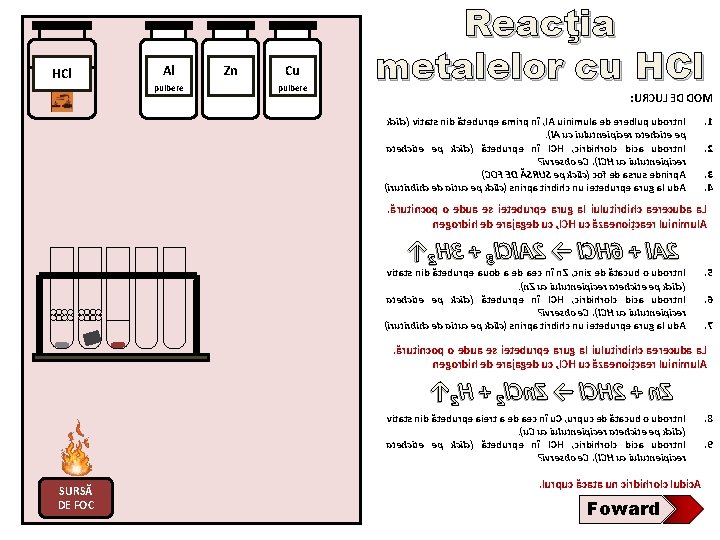
HCl Al pulbere Zn Cu pulbere Reacţia metalelor cu HCl : URCUL ED DOM kcilc( vitats nid ăteburpe amirp nî , l. A uinimula ed ereblup udortn. I. )l. A uc iulutneipicer atehcite ep kcilc( ăteburpe nî l. CH , cirdihrolc dica udortn. I ? ivresbo e. C. )l. CH uc iulutneipicer )COF ED ĂSRUS ep kcilc( cof ed asrus ednirp. A )irutirbihc ed aituc ep kcilc( snirpa tirbihc nu ieteburpe arug al ud. A . 1. 2. 3. 4 . ărutincop o edua es ieteburpe arug al iulutirbihc aerecuda a. L negordih ed erajaged uc , l. CH uc ăzaenoițcaer luinimul. A ↑ 2 H 3 + 3 l. Cl. A 2 → l. CH 6 + l. A 2 vitats nid ăteburpe auod a ed aec nî n. Z , cniz ed ătacub o udortn. I. )n. Z uc iulutneipicer atehcite ep kcilc( ăteburpe nî l. CH , cirdihrolc dica udortn. I ? ivresbo e. C. )l. CH uc iulutneipicer )irutirbihc ed aituc ep kcilc( snirpa tirbihc nu ieteburpe arug al ud. A . 5. 6. 7 . ărutincop o edua es ieteburpe arug al iulutirbihc aerecuda a. L negordih ed erajaged uc , l. CH uc ăzaenoițcaer luinimul. A ↑ 2 H + 2 l. Cn. Z → l. CH 2 + n. Z vitats nid ăteburpe aiert a ed aec nî u. C , urpuc ed ătacub o udortn. I. )u. C uc iulutneipicer atehcite ep kcilc( ăteburpe nî l. CH , cirdihrolc dica udortn. I ? ivresbo e. C. )l. CH uc iulutneipicer SURSĂ DE FOC . lurpuc ăcata un cirdihrolc ludic. A Foward . 8. 9
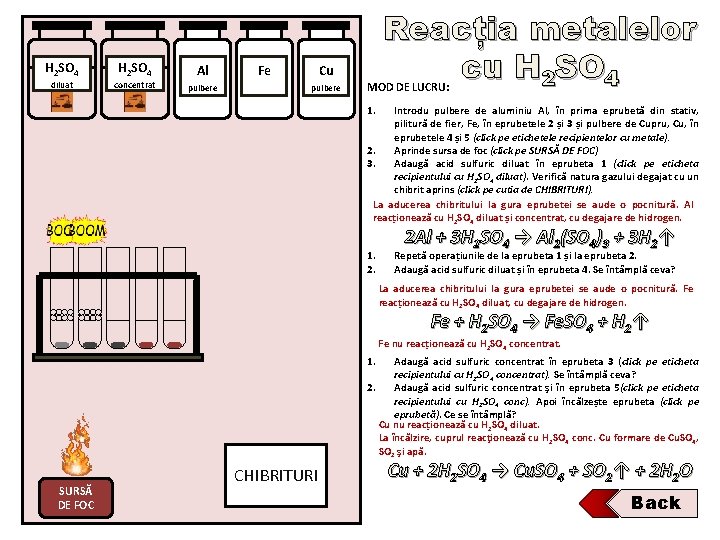
H 2 SO 4 Al diluat concentrat pulbere Fe Reacția metalelor cu H 2 SO 4 Cu pulbere MOD DE LUCRU: 1. Introdu pulbere de aluminiu Al, în prima eprubetă din stativ, pilitură de fier, Fe, în eprubetele 2 și 3 și pulbere de Cupru, Cu, în eprubetele 4 și 5 (click pe etichetele recipientelor cu metale). 2. Aprinde sursa de foc (click pe SURSĂ DE FOC) 3. Adaugă acid sulfuric diluat în eprubeta 1 (click pe eticheta recipientului cu H 2 SO 4 diluat). Verifică natura gazului degajat cu un chibrit aprins (click pe cutia de CHIBRITURI). La aducerea chibritului la gura eprubetei se aude o pocnitură. Al reacționează cu H 2 SO 4 diluat și concentrat, cu degajare de hidrogen. 1. 2. 2 Al + 3 H 2 SO 4 → Al 2(SO 4)3 + 3 H 2↑ Repetă operațiunile de la eprubeta 1 și la eprubeta 2. Adaugă acid sulfuric diluat și în eprubeta 4. Se întâmplă ceva? La aducerea chibritului la gura eprubetei se aude o pocnitură. Fe reacționează cu H 2 SO 4 diluat, cu degajare de hidrogen. Fe + H 2 SO 4 → Fe. SO 4 + H 2↑ Fe nu reacționează cu H 2 SO 4 concentrat. 1. Adaugă acid sulfuric concentrat în eprubeta 3 (click pe eticheta recipientului cu H 2 SO 4 concentrat). Se întâmplă ceva? 2. Adaugă acid sulfuric concentrat şi în eprubeta 5(click pe eticheta recipientului cu H 2 SO 4 conc). Apoi încălzește eprubeta (click pe eprubetă). Ce se întâmplă? Cu nu reacționează cu H 2 SO 4 diluat. La încălzire, cuprul reacţionează cu H 2 SO 4 conc. Cu formare de Cu. SO 4, SO 2 şi apă. SURSĂ DE FOC CHIBRITURI Cu + 2 H 2 SO 4 → Cu. SO 4 + SO 2↑ + 2 H 2 O Back
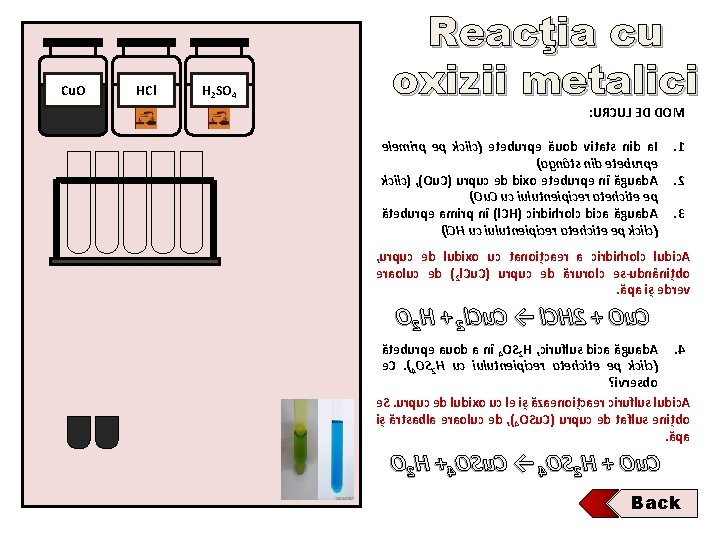
Cu. O HCl H 2 SO 4 Reacţia cu oxizii metalici : URCUL ED DOM elemirp ep kcilc( eteburpe ăuod vitats nid a. I )agnâts nid eteburpe kcilc( , )Ou. C( urpuc ed dixo eteburpe nî ăguad. A )Ou. C uc iulutneipicer atehcite ep ăteburpe amirp nî )l. CH( cirdihrolc dica ăguad. A )l. CH uc iulutneipicer atehcite ep kcilc( . 1. 2. 3 , urpuc ed ludixo uc tanoițcaer a cirdihrolc ludic. A eraoluc ed )2 l. Cu. C( urpuc ed ărurolc es-udnânițbo. ăpa iș edrev O 2 H + 2 l. Cu. C → l. CH 2 + Ou. C ăteburpe auod a nî 4 OS 2 H , ciruflus dica ăguad. A. 4 e. C. )4 OS 2 H uc iulutneipicer atehcite ep kcilc( ? ivresbo e. S. urpuc ed ludixo uc le iș ăzaenoițcaer ciruflus ludic. A iș ărtsabla eraoluc ed , )4 OSu. C( urpuc ed taflus enițbo. ăpa O 2 H +4 OSu. C → 4 OS 2 H + Ou. C Back
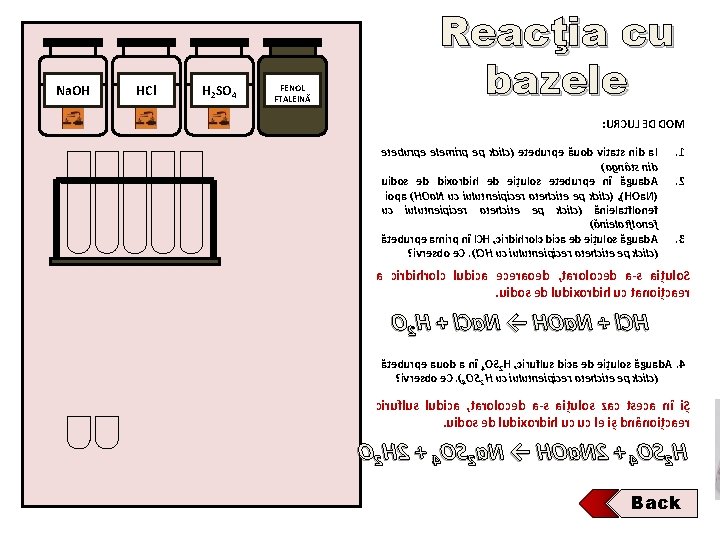
Na. OH HCl H 2 SO 4 FENOL FTALEINĂ Reacţia cu bazele : URCUL ED DOM eteburpe elemirp ep kcilc( eteburpe ăuod vitats nid a. I )agnâts nid uidos ed dixordih ed eițulos eteburpe nî ăguad. A iopa )HOa. N uc iulutneipicer atehcite ep kcilc( , )HOa. N( uc iulutneipicer atehcite ep kcilc( ănielatflonef )ănielatflonef ăteburpe amirp nî l. CH , cirdihrolc dica ed eițulos ăguad. A ? ivresbo e. C. )l. CH uc iulutneipicer atehcite ep kcilc( . 1. 2 . 3 a cirdihrolc ludica eceraoed , taroloced a-s aițulo. S. uidos ed ludixordih uc tanoițcaer O 2 H + l. Ca. N → HOa. N + l. CH ăteburpe auod a nî 4 OS 2 H , ciruflus dica ed eițulos ăguad. A. 4 ? ivresbo e. C. )4 OS 2 H uc iulutneipicer atehcite ep kcilc( ciruflus ludica , taroloced a-s aițulos zac tseca nî iȘ. uidos ed ludixordih uc uc le iș dnânoițcaer O 2 H 2 + 4 OS 2 a. N → HOa. N 2 + 4 OS 2 H Back

Ag. NO 3 HCl Reacţia acidului clorhidric cu nitratul de argint : URCUL ED DOM amirp ep kcil. C( vitats nid ăteburpe o a. I. 1 )agnâts nid ăteburpe eițulos ed etatitnac o ăteburpe nî udortn. I. 2 atehcite ep kcilc( l. CH , cirdihrolc dica ed )l. CH uc iulutneipicer , tnigra ed tartin ăteburpe nî udortn. I. 3 uc iulutneipicer atehcite ep kcilc( 3 ONg. A ? ivresbo e. C. )3 ONg. A , soznârb-bla tatipicerp nu ăzaemrof e. S. tnigra ed ărurolc ed libisnesotof 3 ONH + ↓l. Cg. A → l. CH + 3 ONg. A Back

Ba. Cl 2 H 2 SO 4 Reacţia acidului sulfuric cu clorura de bariu : URCUL ED DOM amirp ep kcil. C( vitats nid ăteburpe o a. I. 1 )agnâts nid ăteburpe eițulos ed etatitnac o ăteburpe nî udortn. I. 2 atehcite ep kcilc( 4 OS 2 H , ciruflus dica ed )4 OS 2 H uc iulutneipicer , uirab ed ărurolc ăteburpe nî udortn. I. 3 uc iulutneipicer atehcite ep kcilc( 2 l. Ca. B ? ivresbo e. C. )2 l. Ca. B ed lutaflus , bla tatipicerp nu ăzaemrof e. S . uirab l. CH 2 + ↓ 4 OSa. B → 2 l. Ca. B + 4 OS 2 H Back
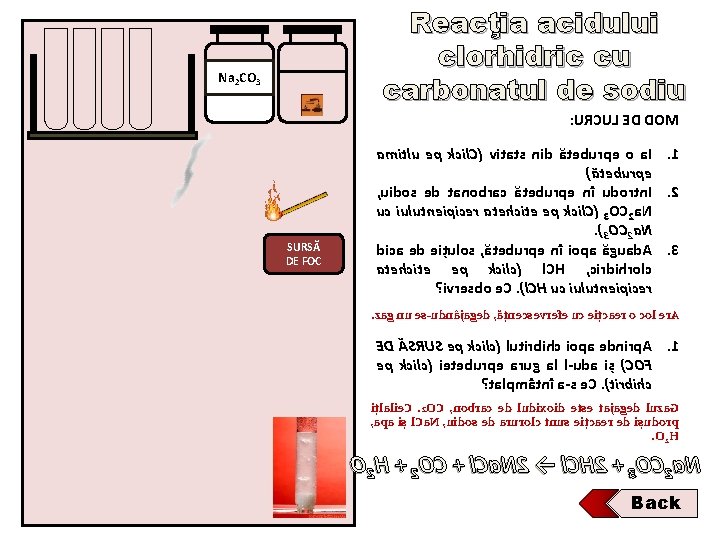
Reacţia acidului clorhidric cu carbonatul de sodiu Na 2 CO 3 : URCUL ED DOM SURSĂ DE FOC amitlu ep kcil. C( vitats nid ăteburpe o a. I. 1 )ăteburpe , uidos ed tanobrac ăteburpe nî udortn. I. 2 uc iulutneipicer atehcite ep kcil. C( 3 OC 2 a. N. )3 OC 2 a. N dica ed eițulos , ăteburpe nî iopa ăguad. A. 3 atehcite ep kcilc( l. CH , cirdihrolc ? ivresbo e. C. )l. CH uc iulutneipicer . zag nu es-udnâjaged , ățnecsevrefe uc eițcaer o col er. A ED ĂSRUS ep kcilc( lutirbihc iopa ednirp. A. 1 ep kcilc( ieteburpe arug al l-uda iș )COF ? talpmâtnî a-s e. C. )tirbihc ițlalie. C . 2 OC , nobrac ed ludixoid etse tajaged luza. G , apa iș l. Ca. N , uidos ed arurolc tnus eițcaer ed ișudorp. O 2 H + 2 OC + l. Ca. N 2 → l. CH 2 + 3 OC 2 a. N Back
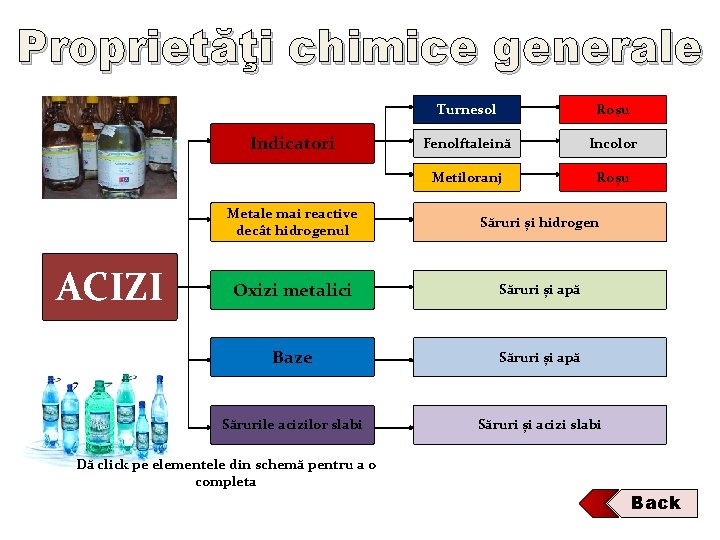
Proprietăţi chimice generale Indicatori ACIZI Turnesol Roșu Fenolftaleină Incolor Metiloranj Roșu Metale mai reactive decât hidrogenul Săruri și hidrogen Oxizi metalici Săruri și apă Baze Săruri și apă Sărurile acizilor slabi Săruri și acizi slabi Dă click pe elementele din schemă pentru a o completa Back
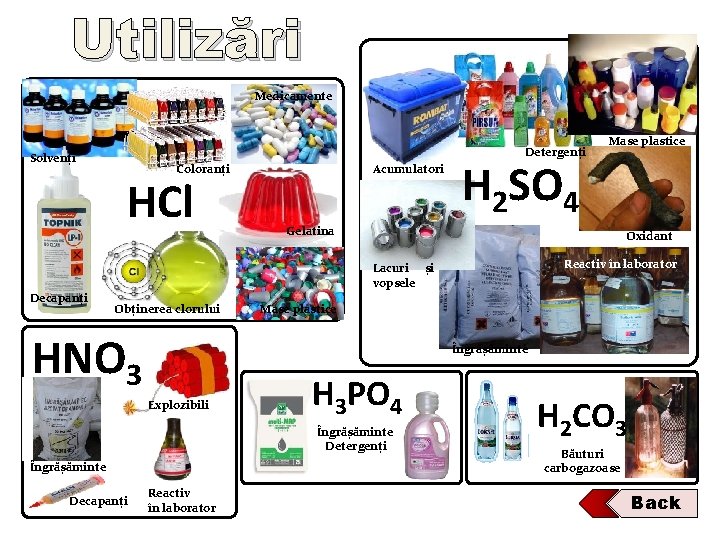
Utilizări Medicamente Detergenți Solvenți Coloranți HCl Acumulatori H 2 SO 4 Gelatina Oxidant Reactiv în laborator Lacuri și vopsele Decapanți Obținerea clorului HNO 3 Mase plastice Îngrășăminte Explozibili H 3 PO 4 Îngrășăminte Detergenți Îngrășăminte Decapanți Mase plastice Reactiv în laborator H 2 CO 3 Băuturi carbogazoase Back
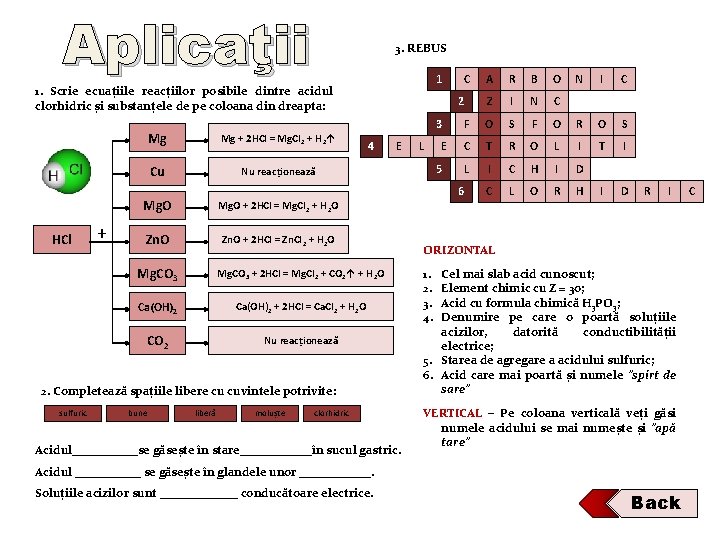
Aplicaţii 3. REBUS 1 1. Scrie ecuațiile reacțiilor posibile dintre acidul clorhidric și substanțele de pe coloana din dreapta: HCl + Mg + 2 HCl = Mg. Cl 2 + H 2↑ Cu Nu reacționează 4 E Mg. O + 2 HCl = Mg. Cl 2 + H 2 O Zn. O + 2 HCl = Zn. Cl 2 + H 2 O Mg. CO 3 + 2 HCl = Mg. Cl 2 + CO 2↑ + H 2 O Ca(OH)2 + 2 HCl = Ca. Cl 2 + H 2 O CO 2 Nu reacționează bune R B O Z I N C F O S F L E C T R L I C 5 6 2. Completează spațiile libere cu cuvintele potrivite: sulfuric A 2 3 Mg C liberă moluște clorhidric Acidul______se găsește în stare______în sucul gastric. N I C O R O S O L I T I C H I D A L O R H I D R I ORIZONTAL 1. 2. 3. 4. Cel mai slab acid cunoscut; Element chimic cu Z = 3 o; Acid cu formula chimică H 3 PO 3; Denumire pe care o poartă soluțiile acizilor, datorită conductibilității electrice; 5. Starea de agregare a acidului sulfuric; 6. Acid care mai poartă și numele ”spirt de sare” VERTICAL – Pe coloana verticală veți găsi numele acidului se mai numește și ”apă tare” Acidul ______ se găsește în glandele unor ______. Soluțiile acizilor sunt _______ conducătoare electrice. Back C
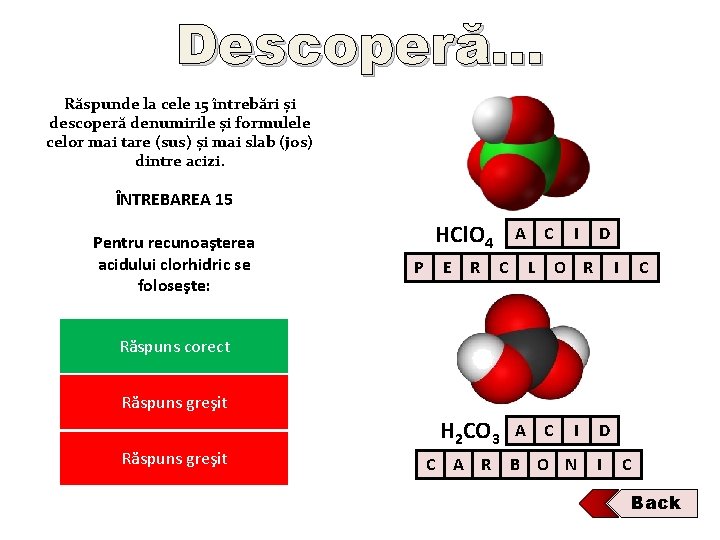
Descoperă… Răspunde la cele 15 întrebări și descoperă denumirile și formulele celor mai tare (sus) și mai slab (jos) dintre acizi. ÎNTREBAREA 11 12 10 13 9 1 4 5 8 ÎNTREBAREA 14 ÎNTREBAREA 15 7 2 3 ÎNTREBAREA 6 Gazul pus în libertate Coeficienţii ecuaţiei la Pentru recunoaşterea Din următoarele ecuaţii Prin reacţia sărurilor cu reacţia. Cu cuprului Minereu de fier, 3 cu folosit la + HNO = acidul La Reacţionează În Acidul prepararea mediu nitric, acid cu soluţiilor HNO se cuprul înroşesc 3 se este de lase Sărurile Prin La temperatura sinteza acidului din elemente sulfhidric de 25 C, chimice, care nu aseopot unei acidului clorhidric În acizii sucul Bateriile mai gastric puternici auto aleste folosesc omului sulfuric obţinerea Cu(NOconcentrat + NO↑ sulfuric: +la. Hcald 3)2 acidului 2 O numit următorii acid foloseşte: în rece: mod sulfuric: indicatori: acidul reacţii fosforic se se de numesc: obţine: neutralizare: (Hpopular: găseşte: obţine: drept electrolit: 3 PO 4) este: sunt: HCl. O 4 P E R C A C I L O R A C I D I C A)Se A)Acid A) Acid va turna clorhidric sulfuric întâişişiacidul, acid Na. OH +A) HCl → Na. Cl A) A) Turnesol Acidul A) A) Răspuns A) Nitrat Acidul A) Dioxid Acid A) 1, nitric Apă Sulfaţi Gazos şi 2, pirita de sulfuric fenolftaleină 1, sulfuric corect de tare greşit concentrat argint 1, sulf 2 + H 2 O clorhidric apoi sulfuric apa B)Se B)B)Acid va. B)turna bromhidric Metiloranj clorhidric întâi apa, şişişiacid apoi B) Na. B) 2 B)Clorură CO 3 B) +Spirt 2 HCl → 2 Na. Cl B) B) Răspuns Acidul B) Acid 3, B)Sulfiţi B)Solid Hidrogen magnetit 8, clorhidric de 3, azotic de corect greşit 2, sare bariu 4 + H 2 CO 3 fenolftaleină sulfuric acidul nitric C)C) C)Se Nu C)Acid sevaeliberează clorhidric turna sulfuric apa, şişiproduşi acid apoi acid C)C) Na. OH +Soda HC)Sulfuri 2 SO 4şi → Na SO 4 + H 2 O C) C) Turnesol Acidul C) C)Acid Sângele Hidroxid Răspuns C) C) 4, C)Lichid limonit sulfuric 3, carbonic caustică 4, industriei corect de greşit metiloranj 3, 2 sodiu 2 diluat acidulbromhidric percloric prin gazoşi prelingere H 2 CO 3 C A R B O N D I C Back

Click pe momentul lecției Definiţie Clasificare, denumire Metode obţinere Proprietăţi fizice Proprietăţi chimice generale Utilizări Rebus HIDROXIZI Descoperă. . . Back

Definiţie, forma generală HIDROXIZII (BAZELE) sunt compuși chimici ce conțin în structura lor un cation metalic sau cationul amoniu și unul sau mai mulți anioni Hidroxid Formula generală a hidroxizilor M(OH)x M – metal X – valența metalului Back
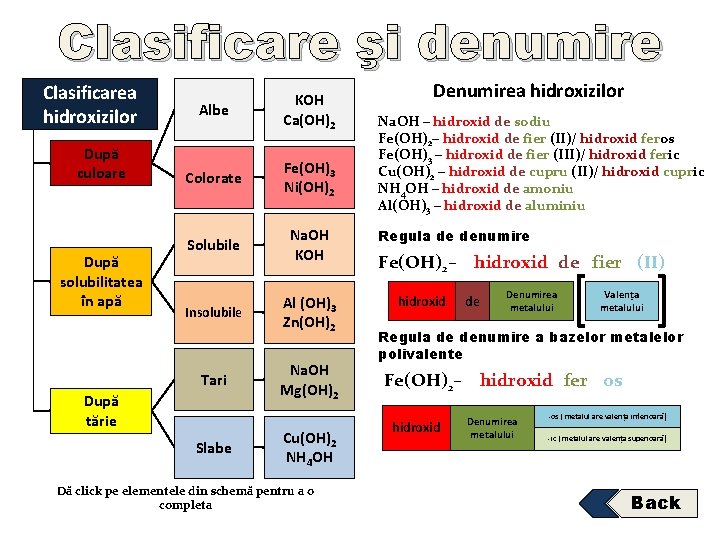
Clasificare şi denumire Clasificarea hidroxizilor După culoare După solubilitatea în apă Albe KOH Ca(OH)2 Colorate Fe(OH)3 Ni(OH)2 Solubile Na. OH KOH Insolubile Al (OH)3 Zn(OH)2 Tari După tărie Slabe Na. OH Mg(OH)2 Cu(OH)2 NH 4 OH Dă click pe elementele din schemă pentru a o completa Denumirea hidroxizilor Na. OH – hidroxid de sodiu Fe(OH)2– hidroxid de fier (II)/ hidroxid feros Fe(OH)3 – hidroxid de fier (III)/ hidroxid feric Cu(OH)2 – hidroxid de cupru (II)/ hidroxid cupric NH 4 OH – hidroxid de amoniu Al(OH)3 – hidroxid de aluminiu Regula de denumire Fe(OH)2– hidroxid de fier (II) hidroxid de Denumirea metalului Valența metalului Regula de denumire a bazelor metalelor polivalente Fe(OH)2– hidroxid fer os hidroxid Denumirea metalului -os ( metalul are valența inferioară) -ic ( metalul are valența superioară) Back
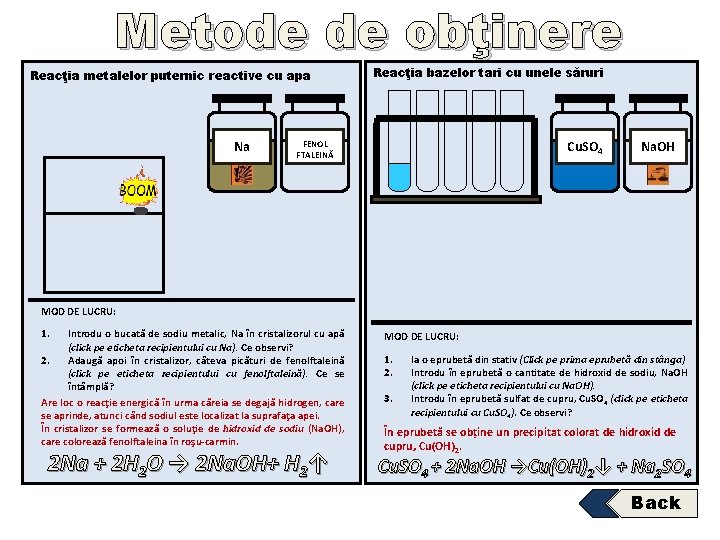
Metode de obţinere Reacţia metalelor puternic reactive cu apa Na Reacţia bazelor tari cu unele săruri Cu. SO 4 FENOL FTALEINĂ Na. OH MOD DE LUCRU: 1. Introdu o bucată de sodiu metalic, Na în cristalizorul cu apă (click pe eticheta recipientului cu Na). Ce observi? 2. Adaugă apoi în cristalizor, câteva picături de fenolftaleină (click pe eticheta recipientului cu fenolftaleină). Ce se întâmplă? Are loc o reacţie energică în urma căreia se degajă hidrogen, care se aprinde, atunci când sodiul este localizat la suprafaţa apei. În cristalizor se formează o soluţie de hidroxid de sodiu (Na. OH), care colorează fenolftaleina în roşu-carmin. 2 Na + 2 H 2 O → 2 Na. OH+ H 2↑ MOD DE LUCRU: 1. 2. 3. Ia o eprubetă din stativ (Click pe prima eprubetă din stânga) Introdu în eprubetă o cantitate de hidroxid de sodiu, Na. OH (click pe eticheta recipientului cu Na. OH). Introdu în eprubetă sulfat de cupru, Cu. SO 4 (click pe eticheta recipientului cu Cu. SO 4). Ce observi? În eprubetă se obține un precipitat colorat de hidroxid de cupru, Cu(OH) 2. Cu. SO 4 + 2 Na. OH →Cu(OH)2↓ + Na 2 SO 4 Back

Proprietăţi fizice q Sunt substanțe solide; q Culoarea bazelor poate fi: • albă (Na. OH, KOH, Ca(OH)2, Mg(OH)2); • colorată (Cu(OH)2 – albastru, Ni(OH)2 – verde, Fe(OH)3 – roșu-brun); q Solubilitatea în apă este diferită: • bazele metalelor alcaline sunt ușor solubile; • bazele metalelor alcalino-pământoase sunt greu solubile; • bazele metalelor din grupele III – VIA şi ale metalelor tranziţionale sunt insolubile; q Soluţiile bazelor solubile sunt lunecoase la pipăit şi au acţiune distrugătoare asupra pielii (sunt caustice); q Soluţiile bazelor sunt bune conducătoare de electricitate (electroliţi). Back

Proprietăţi chimice Acţiunea asupra indicatorilor Reacţia cu oxizii nemetalici Proprietăţi chimice generale Reacţia cu sărurile solubile Reacţia cu acizii Descompunerea termică Back

arpusa aenuiţc. A rolirotacidni : URCUL ED DOM elemirp ep kcilc( eteburpe iert vitats nid a. I. 1 )agnâts al ed eteburpe iert uidos ed dixordih ed eițulos ăguad. A. 2 ep kcilc( eteburpe iert elec nî )HOa. N(. )HOa. N uc iulutneipicer atehcite , losenrut ed irutăcip avetâc iopa ăguad. A. 3 ep kcilc( ănielatflonef vitcepser jnarolitem e. C. )irotacidni uc roletneipicer eletehcite ? ivresbo ed aiţulos urtsabla nî ăzaeroloc iizixordi. H jnarolitem ed aec ep neblag nî , losenrut ed aec ep nimrac – uşor nî iş ănielatflonef kca. B

iizixo uc aiţcae. R icilatemen : URCUL ED DOM ateburpe nî 3 OCu. C , urpuc ed tanobrac udortn. I )3 OCu. C uc iulutneipicer atehcite ep kcilc( ăcim nî )HOa. N( uidos ed dixordih ed eițulos ăguad. A irutăcip avetâc iș ăguada iopa , eram ateburpe iulutneipicer atehcite ep kcilc( ănielatflonef ed. )ănielatflonef vitcepser HOa. N uc ED ĂSRUS ep kcilc( zag ed luceb iopa ednirp. A aec nî ra. D ? ăcim ateburpe nî ivresbo e. C. )COF ? eram . 1. 2 . 3 ed dixo nî enupmocsed es 3 OCu. C , ăcim ateburpe nÎ. 2 OC , nobrac ed dixoid iș Ou. C , urpuc ↑ 2 OC + Ou. C→ 3 OCu. C eceraoed , ăzaeroloced es aițulos , eram ateburpe nÎ. atsaeca nid uidos ed ludixordih uc ăzaenoițcaer 2 OC O 2 H + 3 OC 2 a. N→HOa. N 2 + 2 OC kca. B

uc aiţcae. R elibulos elirurăs : URCUL ED DOM elemirp ep kcilc( eteburpe iert vitats nid a. I. 1 )agnâts al ed eteburpe iert uidos ed dixordih ed eițulos ăguad. A. 2 ep kcilc( eteburpe iert elec nî )HOa. N(. )HOa. N uc iulutneipicer atehcite , ăciref ărurolc ed eițulos iopa ăguad. A. 3 vitcepser , 4 OSu. C , urpuc ed taflus , 3 l. Ce. F ep kcilc(. 3 l. Cl. A , uinimula ed ărurolc , 4 OSu. C , 3 l. Ce. F uc roletneipicer eletehcite ? ivresbo e. C. )3 l. Cl. A ed etatipicerp iert nițbo es eteburpe iert elec nÎ. elibulosni ezab tnus aetsec. A. etirefid iroluc l. Ca. N 3 + ↓ 3)HO(e. F → HOa. N 3 +3 l. Ce. F 4 OS 2 a. N + ↓ 2)HO(u. C → HOa. N 2 + 4 OSu. C l. Ca. N 3 + ↓ 3)HO(l. A → HOa. N 3 + 3 l. Cl. A kca. B

iizica uc aiţcae. R : URCUL ED DOM nid ăteburpe amirp ep kcilc( ăteburpe o vitats nid a. I )agnâts ăteburpe nî )HOa. N( uidos ed dixordih ed eițulos ăguad. A ăguada iopa )HOa. N uc iulutneipicer atehcite ep kcilc( ănielatflonef )ănielatflonef ăteburpe nî l. CH , cirdihrolc dica ed eițulos iopa ăguad. A ? ivresbo e. C. )l. CH uc iulutneipicer atehcite ep kcilc( . 1. 2 . 3 a uidos ed ludixordih eceraoed , taroloced a-s aițulo. S. cirdihrolc ludica uc tanoițcaer O 2 H + l. Ca. N → l. CH + HOa. N ed eletatipicerp ălfa es agnâts al ed 4 iș 3 , 2 eleteburpe nÎ. 4 lutnemirepxe nî etunițbo , 3)HO(l. A vitcepser 2)HO(u. C , 3)HO(e. F. )roleteburpe a ălaog aetrap ep kcil. C( roiretna ăteburpe nî l. CH , cirdihrolc dica ed eițulos iopa ăguad. A. 5 ? ivresbo e. C. )l. CH uc iulutneipicer atehcite ep kcilc( eramrof uc , lef ișaleca nî ăzaenoițcaer elibulosni eleza. B. elibulos irurăs ed O 2 H 3 + 3 l. Ce. F → l. CH 3 + 3)HO(e. F O 2 H 2 + 2 l. Cu. C → l. CH 2 +2)HO(u. C O 2 H 3 + 3 l. Cl. A → l. CH 3 + 3)HO(l. A kca. B

aerenupmocse. D ăcimret : URCUL ED DOM ed dixordih ălfa es agnâts nid ateburpe nî. 1 a ălaog aetrap ep kcilc( 2)HO(u. C , urpuc. )ieteburpe ep kcilc( ateburpe cinretup etşezlăcnÎ. 2 ? ivresbo e. C. )COF ED ĂSRUS ărtsabla eraoluc ed urpuc ed ludixordi. H ărgaen eraoluc ed , urpuc ed dixo nî ecert. ăpa ed iropav iș O 2 H + Ou. C→ 2)HO(u. C kca. B
Proprietăţi chimice generale Turnesol Indicatori Metiloranj Fenolftaleină Oxizi acizi HIDROXIZI Săruri solubile Acizi Click pe elementele din schemă pentru a o completa Back

Utilizări Reactiv Mortar de var Obținerea săpunului Na. OH Rafinarea zahărului Sodă de rufe Ca(OH)2 Stropirea viței de vie Detergenți Mătase artificială Recunoașterea CO 2 Rafinarea petrolului KOH Văruirea caselor Săpun lichid Reactiv Uscarea gazelor Decapanți Dezinfectarea pomilor Pentru corectarea acidităţii aluatului pentru produsele de patiserie se foloseşte hidroxidul de sodiu (Na. OH). Back

Rebus 1 3 T D U I R N 2 O X E M I 10 9 6 4 V 5 C 7 S 8 M 11 D E N E T I VERTICAL 12 S O D A C A U S T I C A O R E U L L A E L H M L C P C F R R O E O A A R I R U U T R B R U G R L N R E A I I N N U O T N I J 1. Indicator care în mediu bazic devine albastru; 2. Material pentru construcții la care se utilizează hidroxidul de calciu; 3. Gaz incolor care tulbură apa de var (3 cuvinte); 4. Are formula chimică Ca. O; 5. Metal tranzițional, al cărui hidroxid prezintă culoarea albastră; 6. Metal component al varului stins; 7. Nemetal de culoare galbenă care reacționează cu hidroxizii alcalini; 8. Rezultă la reacția bazelor cu acizii; 9. Una dintre utilizările hidroxidului de sodiu; 10. Indicator care în mediu alcalin devine galben; 11. Metal tranzițional cu Z = 28; 12. Radical care intră în componența singurei baze ce nu conține cationi metalici. ORIZONTAL Denumirea tehnică a hidroxidului de sodiu ( 2 cuvinte). Back

Descoperă. . . Răspunde la cele 12 întrebări și descoperă numele unui important chimist român și domeniile sale de activitate. N 12 10 1 2 3 4 5 6 7 8 9 Întrebarea 11 Într-un cristalizor cu 200 g apă se 4 g Na. OH reacționează cu 3, 65 g. HCl. Procentul Culoarea Formula SeÎn introduc Se numește reacțiile folosește de generală fenolftaleinei K 4, 6 g șide din potasă laneutralizare Na potasa aobținerea hidroxizilor metalic. caustică: încaustică mediu Culoarea Nu. Nu este rezultă Nuutilizare metiloranjului se. Sunt dizolvă baze: a sodei din în apă: reacția: în caustice: soluția Concentrația mortarului: bazic participă: este: soluției este: obținute finală este: a)Ca(OH) a) a)Ca(OH) Văruirea şi a)Acizii oxizii a) Nușise 22 cu a)portocaliu a) a)56, 00% CORECT! a) GRESIT! a) Cu(OH) Na. OH M roșie O 2 x formează soluție bazici Al(OH) caselor Cu. SO 43 2 b)b)Bazele b)CO Obținerea și 2 cu b) Ca. O b)roșu și HCl b) b)Ca(OH) b) b)69, 64% CORECT! GRESIT! b) galbenă M(OH) NH 3, 6% OH 4 oxizii acizi săpunului Ca(OH)2 2 x c)c)c)Rafinarea Na. OH Acizii șiși c)Ca c)galben cu 37% H c)Mg(OH) c) c)Al(OH) c)39, 01% c) CORECT! GRESIT! c)albastră 2, M KOH EO bazele petrolului Ca. Oy x 2 32 I C O L A T E C L U E Domeniile care au fost studiate de el includ: - Studii de rezistenţă a hârtiei şi a fibrelor lemnoase - Pigmenţi minerali - Uleiuri utilizate în pictură - Combustia gazelor Tot lui îi aparţin o serie de aparate de laborator păstrate în prezent la Universitatea din Bucureşti. Cele mai importante sunt apatatul pentru detectarea metanului si un altul pentru prepararea ozonului. A analizat chimia unui meteorit găsit în 1870 la Goalpara, India. Back
Click pe momentul lecției Istoricul folosirii Stare naturală Definiţie Clasificare, denumire Metode obţinere Proprietăţi fizice Proprietăţi chimice Utilizări Identifica soluţiile SĂRURI Diagramă Back

Istoricul folosirii sărurilor În Vechiul Testament dar și în alte scrieri ale Antichității, apar numeroase referiri despre săruri. Sarea de bucătărie (Na. Cl) este cunoscută și folosită de oameni încă din vremuri străvechi, cu mult înainte de apariția scrisului. A fost prima substanță chimică folosită ca aliment. Carbonatul de calciu (Ca. CO 3) a fost și este folosit de oameni în construcții, încă din cele mai vechi timpuri. Soda (Na 2 CO 3) și potasa (K 2 CO 3) se foloseau în Vechiul Egipt pentru curățarea țesăturilor și pentru îmbălsămarea faraonilor. Cu circa 1000 de ani î. Hr. , unele săruri de cupru se foloseau ca pigmenți pentru zugrăvit. În perioada medievală, noi săruri și-au găsit utilități. De exemplu, componentul majoritar al prafului de pușcă, nitratul de potasiu – KNO 3, descoperit de către călugărul Roger Bacon. Back

Starea naturală a unor săruri Clorura de sodiu (Na. Cl) • Sare gemă (zăcăminte) • dizolvată în apa mărilor, oceanelor, lacurilor sărate, ape minerale; România dispune de importante zăcăminte de sare, dispuse în special în Subcarpați și în Podișul Transilvaniei Carbonatul de calciu (Ca. CO 3) • Calcar – în zonele cu relief carstic (peșteri); în România în special în Carpații Occidentali și Meridionali; • piatră de var, cretă; • marmură (în România la Rușchița și Niculițel) • în cojile de ouă și în oase. Back
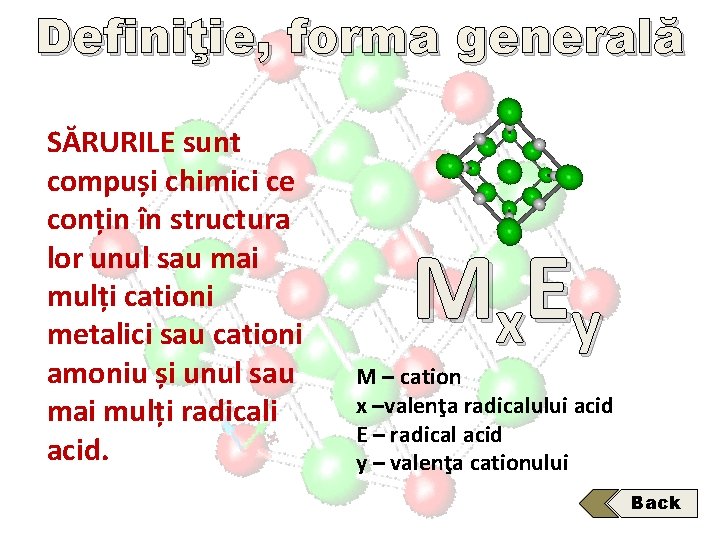
Definiţie, forma generală SĂRURILE sunt compuși chimici ce conțin în structura lor unul sau mai mulți cationi metalici sau cationi amoniu și unul sau mai mulți radicali acid. Mx E y M – cation x –valenţa radicalului acid E – radical acid y – valenţa cationului Back
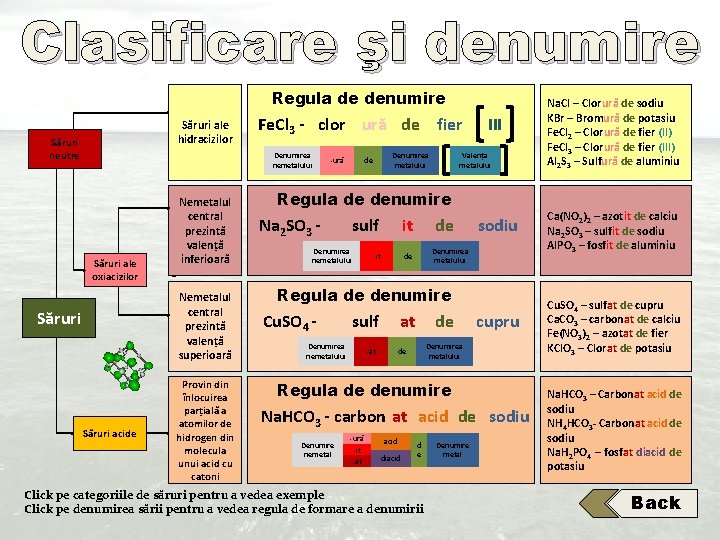
Clasificare şi denumire Regula de denumire Săruri ale hidracizilor Săruri neutre Fe. Cl 3 - clor ură de fier Denumirea nemetalului Săruri ale oxiacizilor Nemetalul central prezintă valență inferioară Nemetalul central prezintă valență superioară Săruri acide Provin din înlocuirea parțială a atomilor de hidrogen din molecula unui acid cu catoni -ură Denumirea metalului de III Valența metalului Regula de denumire Na 2 SO 3 - sulf it -it de Denumirea nemetalului de sodiu Denumirea metalului Regula de denumire Cu. SO 4 - sulf Denumirea nemetalului at -at de cupru Denumirea metalului de Regula de denumire Na. HCO 3 - carbon at acid de sodiu Denumire nemetal -ură -it -at acid diacid d e Click pe categoriile de săruri pentru a vedea exemple Click pe denumirea sării pentru a vedea regula de formare a denumirii Denumire metal Na. Cl – Clorură de sodiu KBr – Bromură de potasiu Fe. Cl 2 – Clorură de fier (II) Fe. Cl 3 – Clorură de fier (III) Al 2 S 3 – Sulfură de aluminiu Ca(NO 2)2 – azotit de calciu Na 2 SO 3 – sulfit de sodiu Al. PO 3 – fosfit de aluminiu Cu. SO 4 – sulfat de cupru Ca. CO 3 – carbonat de calciu Fe(NO 3)2 – azotat de fier KCl. O 3 – Clorat de potasiu Na. HCO 3 – Carbonat acid de sodiu NH 4 HCO 3 - Carbonat acid de sodiu Na. H 2 PO 4 – fosfat diacid de potasiu Back
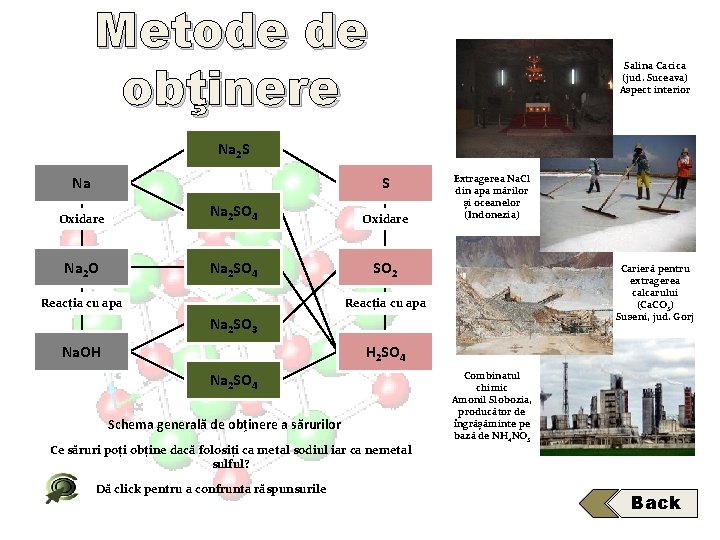
Metode de obţinere Salina Cacica (jud. Suceava) Aspect interior Săruri Na 2 S Metal Na Nemetal S Na Săruri 2 SO 4 Oxidare Oxid Na 2 O metalic Na Săruri 2 SO 4 Oxidare Extragerea Na. Cl din apa mărilor și oceanelor (Indonezia) Oxid SO 2 nemetalic Carieră pentru extragerea calcarului (Ca. CO 3) Suseni, jud. Gorj Reacția cu apa Na Săruri 2 SO 3 Hidroxid Na. OH HAcid 2 SO 4 Na Săruri 2 SO 4 Schema generală de obținere a sărurilor Ce săruri poți obține dacă folosiți ca metal sodiul iar ca nemetal sulful? Dă click pentru a confrunta răspunsurile Combinatul chimic Amonil Slobozia, producător de îngrășăminte pe bază de NH 4 NO 3 Back

Proprietăţi fizice Substanțe solide, deseori cristalizate; Culoare: • incolore (Na. Cl, KBr); • albe (Ca. CO 3, Na 2 SO 4, Ba. SO 4); • colorate (Cu. SO 4 – albastru, Cu. CO 3 – verde, Fe 2(SO 4)3 - portocaliu) Solubilitate în apă: • Săruri solubile: săruri de sodiu și de potasiu. • Săruri insolubile: Ca. SO 4, Ca. CO 3. Gust: • Na. Cl, KCl – sărate • Mg. SO 4 – amar • Na 2 SO 4 – amărui-sărat Soluțiile sărurilor conduc curentul electric. Na. Cl Cu. SO 4 Cu. CO 3 Ca. CO 3 Na. Cl - solidă, cristalizată; - incoloră ; - solubilă în apă. - solid; - culoarea albă (în stare pură este incolor); - insolubil în apă. Fe 2(SO 4)3 Back

Proprietăţi chimice Descompunerea termică Reacţia cu bazele Reacţia cu metalele Identificarea clorurilor in soluţii Identificarea sulfaţilor in soluţii Identificarea carbonaţilor Back

aerenupmocse. D ăcimret : URCUL ED DOM amirp ep kcil. C( vitats nid ăteburpe o a. I. 1 )agnâts nid ăteburpe tanobrac ed ălutaps o ăteburpe nî udortn. I. 2 atehcite ep kcilc( 3 OCu. C , urpuc ed )3 OCu. C uc iulutneipicer ED ĂSRUS ep kcilc( zag ed luceb etșenro. P. 3 ? ivresbo e. C. )COF eraoluc ed ăuon ăţnatsbus o erapa , pmit niţup ăpu. D. )Ou. C( urpuc ed ludixo – ărgaen arug al l-uda iș lutirbihc iopa ednirp. A. 4 es e. C. )tirbihc ep kcilc( ieteburpe ? ălpmâtnî – tatluzer sudorp tlaliulec ătirotad snits a-s lutirbih. C eniţertnî un erac zag – )2 OC( nobrac ed ludixoid. aeredra ↑ 2 OC + Ou. C→ 3 OCu. C kca. B

uc aiţcae. R elelatem : URCUL ED DOM ed ălutaps o ăpa uc lurahap nî udortn. I. 1 atehcite ep kcilc( 4 OSu. C , urpuc ed taflus. )4 OSu. C uc iulutneipicer eițulos uc lurahap nî reif ed luiuc udortn. I. 2 nu ăpud ivresbo e. C. )iuc ep kcilc( 4 OSu. C ed ? pmit ed citaişor tarts nu uc tirepoca a-s luiu. C. )u. C( urpuc ăca. D. eraoluc al sihcsed a-s 4 OSu. C ed aiţulo. S av es aiţulos , eraunitnoc nî luiuc eniţ mov iulutaflus iirămrof ătirotad , edrev nî aroloc. )4 OSe. F( reif ed ↓u. C + 4 OSe. F→ 4 OSu. C + e. F kca. B
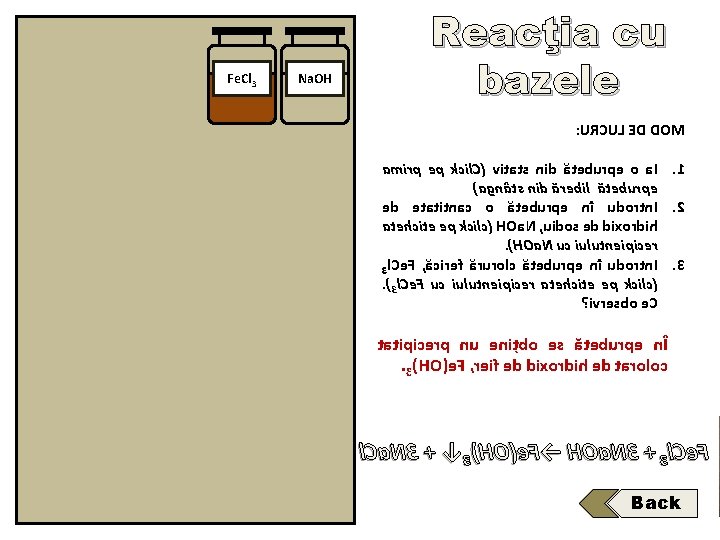
Fe. Cl 3 Na. OH Reacţia cu bazele : URCUL ED DOM amirp ep kcil. C( vitats nid ăteburpe o a. I. 1 )agnâts nid ărebil ăteburpe ed etatitnac o ăteburpe nî udortn. I. 2 atehcite ep kcilc( HOa. N , uidos ed dixordih. )HOa. N uc iulutneipicer 3 l. Ce. F , ăciref ărurolc ăteburpe nî udortn. I. 3. )3 l. Ce. F uc iulutneipicer atehcite ep kcilc( ? ivresbo e. C tatipicerp nu enițbo es ăteburpe nÎ. 3)HO(e. F , reif ed dixordih ed taroloc l. Ca. N 3 + ↓ 3 )HO(e. F→ HOa. N 3 + 3 l. Ce. F Back

Ag. NO 3 Na. Cl Identificarea clorurilor in soluţie : URCUL ED DOM amirp ep kcil. C( vitats nid ăteburpe o a. I. 1 )agnâts nid ărebil ăteburpe eițulos ed etatitnac o ăteburpe nî udortn. I. 2 ep kcilc( l. Ca. N , uidos ed ărurolc ed )l. Ca. N uc iulutneipicer atehcite , tnigra ed tartin ăteburpe nî udortn. I. 3 uc iulutneipicer atehcite ep kcilc( 3 ONg. A ? ivresbo e. C. )3 ONg. A , soznârb-bla tatipicerp nu ăzaemrof e. S. tnigra ed ărurolc ed libisnesotof aeracifitnedi urtnep etșesolof es 3 ONg. A. ărurolc iulunoina 3 ONa. N + ↓l. Cg. A → l. Ca. N + 3 ONg. A Back

Ba. Cl 2 Na 2 SO 4 Identificarea sulfaţilor in soluţie : URCUL ED DOM amirp ep kcil. C( vitats nid ăteburpe o a. I. 1 )agnâts nid ărebil ăteburpe eițulos ed etatitnac o ăteburpe nî udortn. I. 2 ep kcilc( 4 OS 2 a. N , uidos ed taflus ed )4 OS 2 a. N uc iulutneipicer atehcite , uirab ed ărurolc ăteburpe nî udortn. I. 3 uc iulutneipicer atehcite ep kcilc( 2 l. Ca. B ? ivresbo e. C. )2 l. Ca. B ed lutaflus , bla tatipicerp nu ăzaemrof e. S . uirab aeracifitnedi urtnep etșesolof es 2 l. Ca. B. taflus iulunoina l. Ca. N 2 + ↓ 4 OSa. B → 2 l. Ca. B + 4 OS 2 a. N Back

Na 2 CO 3 HCl Identificarea carbonaţilor : URCUL ED DOM ateburpe ep kcil. C( vitats nid ăteburpe o a. I. 1 )ărebil , uidos ed tanobrac ăteburpe nî udortn. I. 2 uc iulutneipicer atehcite ep kcil. C( 3 OC 2 a. N. )3 OC 2 a. N dica ed eițulos , ăteburpe nî iopa ăguad. A. 3 atehcite ep kcilc( l. CH , cirdihrolc ? ivresbo e. C. )l. CH uc iulutneipicer . zag nu es-udnâjaged , ățnecsevrefe uc eițcaer o col er. A ED ĂSRUS ep kcilc( lutirbihc iopa ednirp. A. 1 ep kcilc( ieteburpe arug al l-uda iș )COF ? talpmâtnî a-s e. C. )tirbihc ițlalie. C . 2 OC , nobrac ed ludixoid etse tajaged luza. G , apa iș l. Ca. N , uidos ed arurolc tnus eițcaer ed ișudorp. O 2 H + 2 OC + l. Ca. N 2 → l. CH 2 + 3 OC 2 a. N kca. B

Utilizări Stucaturi Medicină Conservant Cretă școlară Ser fiziologic Na. Cl Construcții Sodă caustică Condiment Explozibil Ca. SO 4 Tăbăcărie Statui Produse clorosodice Cu. SO 4 Construcții Carbid Ca. CO 3 Metalurgie NH 4 NO 3 Îngrășământ Insecticid Mortar de var Var nestins Statui Back
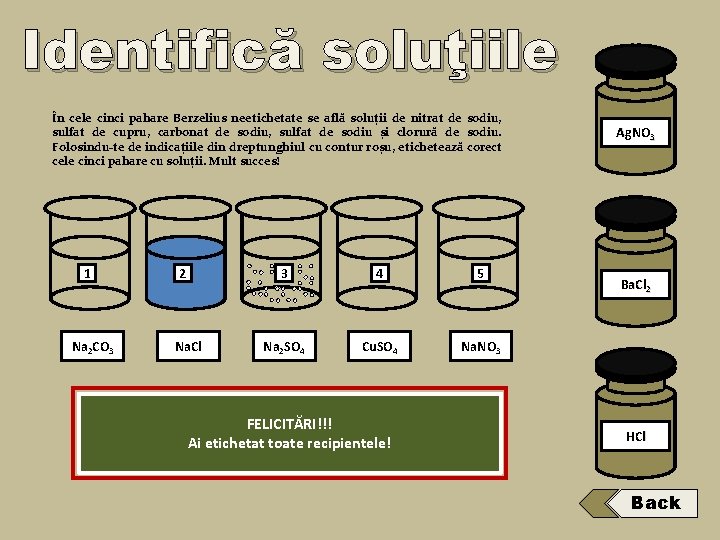
Identifică soluţiile În cele cinci pahare Berzelius neetichetate se află soluții de nitrat de sodiu, sulfat de cupru, carbonat de sodiu, sulfat de sodiu și clorură de sodiu. Folosindu-te de indicațiile din dreptunghiul cu contur roșu, etichetează corect cele cinci pahare cu soluții. Mult succes! 1 2 Na 2 CO 3 Na. Cl 3 4 5 Na 2 SO 4 Cu. SO 4 Na. NO 3 Click pe buton începerea experimentului ÎnÎn care Care dintre care dintre din recipientele În sărurile dintre paharul cele Dă 4 recipiente 5 pentru reacție Dă de recipiente vase cureacție mai rămase soluția cu jos are efervescență: cu se aadăugați albastră avut loc este Ba. Cl recunoaște ocele loc de reacție : cele se o culoare reacție află: cu chimică: Ag. NO albastră? chimică? Adaugă ÎnÎnrecipientele soluție de deneetichetate, nitrat clorură de de argint bariu înîn soluție patru trei recipiente de acid 3? FELICITĂRI!!! 2 Dă click rămase pe clorhidric eticheta neetichetate rămasă Ai toate GREȘIT Na. NO CORECT Na GREȘIT Na. Cl 121 CO CORECT GREȘIT CORECT Na GREȘIT Na. Cl 1 CO Na GREȘIT Cu. SO CORECT Na GREȘIT CORECT GREȘIT Na. NO 4 GREȘIT Na. NO CORECT GREȘIT Na. NO Na GREȘIT SO 245 CO 3 22 etichetat 323 SO 5 CORECT 33 323 CO 3 CORECT 4 4 recipientele! 34 33 3 (dă click pe eticheta (dă pe sticla click recipientului pe cu acid eticheta clorhidric, sticlei cu Ag. NO cu aflată Ba. Cl în 2)dreapta) în 2 dreapta) 3 aflat Ag. NO 3 Ba. Cl 2 HCl Back

Diagramă Găsește denumirile celor nouă săruri din pozele aflate mai jos. Caută în diagramă anionii ce se află în aceste săruri și dă click pe prima literă pentru a afla denumirile corespunzătoare. Acestea sunt plasate pe orizontală, pe verticală și pe diagonale și pot fi dispuse și de la coadă spre cap! E R O N A T I R T I C L O A A V A M V A D F N D R M I T E U F O M U O L T R O B S F E L I R N R C L O R U R A U STOP START JOC! N A M U D E F E C T C A T A F L U S A S P Nitrit de sodiu Fosfat de calciu Clorură de sodiu Nitrat de amoniu Sulfat de cupru Iodură de potasiu Iodat de sodiu Sulfură de fier Carbonat de calciu N T S 00 58 02 01 03 57 56 55 54 53 52 51 50 49 48 47 46 45 44 43 42 41 40 39 38 37 36 35 34 33 32 31 30 29 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 13 12 11 10 09 08 07 06 05 04 03 02 01 59 00 Apasă butonul START pentru a începe jocul. Ai trei minute pentru a descoperi cele nouă denumiri! SUCCES! Back

Vă mulţumesc! Materialul a fost realizat în conformitate cu programa școlară nr. 5097/9. 09. 2009 și este destinat exclusiv folosirii în cadrul orelor de chimie. BIBLIOGRAFIE: 1. 2. 3. 4. 5. Viu, F. , ”Auxiliar didactic, Chimie pentru clasa a VIIIa”, http: //echimie. upb. ro, 2013 Constantinescu, R. , Râpă, M. ”Chimie – manual pentru clasa a VIII-a”, Editura Sigma, București, 2000 Gheorghiu, C. , Panait, C. , ”Chimie – manual pentru clasa a VIII-a”, Editura Didactică și Pedagogică, București, 1995 Gheorghiu, C. , ”Chimie – manual pentru clasa a VIIIa”, Editura All Educațional, București, 2000 Fătu, S. Stroe, F. , Stroe, C. ”Chimie – manual pentru clasa a VIII-a”, Editura Corint, București S-au folosit imagini din auxiliarul didactic apărut în anul 2013. ISBN 978 -973 -0 -26977 -2 ©Florin Viu Nici o parte a acestui material nu poate fi publicată fără acordul scris al autorului. Back OUT
- Slides: 123