FISIOPATOLOGIA DEL METABOLISMO DE HIDRATOS DE CARBONO HIPOGLUCEMIAS

FISIOPATOLOGIA DEL METABOLISMO DE HIDRATOS DE CARBONO HIPOGLUCEMIAS HIPERGLUCEMIAS

Regulación de la glucemia a) Fase postprandrial: Dura 3 -4 hs tras la comida Aumenta niveles de glucemia Se eleva la insulinemia lo cual aumenta la glucogenogénesis, disminuye la glucolisis y neoglucogénesis. Del hígado sale el 50% de la glucosa que le llega. b) Fase de ayuno: A las 8 hs de haber comido disminuye la glucosa y la insulina, se elevan la hormonas contrainsulares (GH, catecolaminas, cortisol y glucagón) lo cual aumenta la glucogenolisis y la neoglucogénesis. La clínica de la hipoglucemia se debe al aumento de catecolaminas. Con glucemia inferior a 20 mg% aparece disfunción cerebral (el cerebro puede usar como energía cuerpos cetónicos pero no FFA)

Hipoglucemia Concepto - Síntomas aparecidos con glucemia inferior a 50 mg% en plasma en el hombre (40 en sangre capilar) o 40 mg% en la mujer. - Dificultad diagnóstica por: a) Síntomas poco específicos b) Umbral de glucemia para los síntomas variables c) Síntomas pueden variar en un individuo d) Puede haber sujetos normales con glucemias bajas bien toleradas ( < 45 mg% tras SOG) e) Pseudohipoglucemia por glucolisis (se tarda en analizar)

Hipoglucemias A) De ayuno - Disminución de producción de glucosa Déficit hormonas contrainsulares (GH, cortisol. . ) Déficit de sustrato: desnutrición. Hepatopatía Drogas (alcohol, propranolol; salicilatos) - Uso excesivo de glucosa * Con hiperinsulinismo Insulinoma Fármacos: Insulina exógena, sulfonilureas Sepsis (citoquinas) * Sin hiperinsulinismo Tumores extrapancreáticos B) Reactiva (postprandrial) - Idiopatica o funcional - Alimentaria: intolerancia fructosa, leucina, galactosemia - Diabetes Mellitus tipo 2 de comienzo

SINTOMAS DE HIPOGLUCEMIA a) Simpatoadrenales - Sudor, temblor, hambre, ansiedad, palpitaciones, hipertensión - Por activación adrenal, simpático y parasimpático - Preceden a los neuroglucopénicos - Puede no aparecer (hipoglucemias inadvertidas) Triada de Whipple: - Síntomas hipoglucémicos - Glucosa inferior a 45 mg/dl en plasma (para otros < 40) - Desaparecen al tomar azúcar (no específica)

SINTOMAS DE HIPOGLUCEMIA b) Neuroglucopenia - Con glucemia < 40 mg/dl (umbral variable). - Síntomas progresivos según nadir de glucemia y duración: 1). - Trastorno cognitivo Irritabilidad, confusión, cefaleas, somnolencia, visión borrosa (simula embriaguez) 2). - Descoordinación motora, espasmos tonicoclónicos convulsiones. Puede aparecer focalidad neurológica. 3). - Bradicardia, hipotermia coma y muerte Si la hipoglucemia no se trata en 20 minutos, deja secuelas irreversibles

HIPOGLUCEMIA MAS FRECUENTES A) Diabetes. Consecuencia del tratamiento (insulinas, secretagogos) Favorecida por: Error en eo tratamiento, aumento de ejercicio disminución de ingesta, alcohol, neuropatía B) Idiopatica o funcional: En mujeres jóvenes con ansiedad Sintomas adernergicos. Con frecuencia no coincide la hipoglucemia con la clínica C) Insulinoma: Tumor (adenoma) o hiperplasia productora de insulina D) Hipoglucemia tumoral: Tumores mesenquimatosos de gran tamaño (retroperitoneal. . ) Producen IGF ll
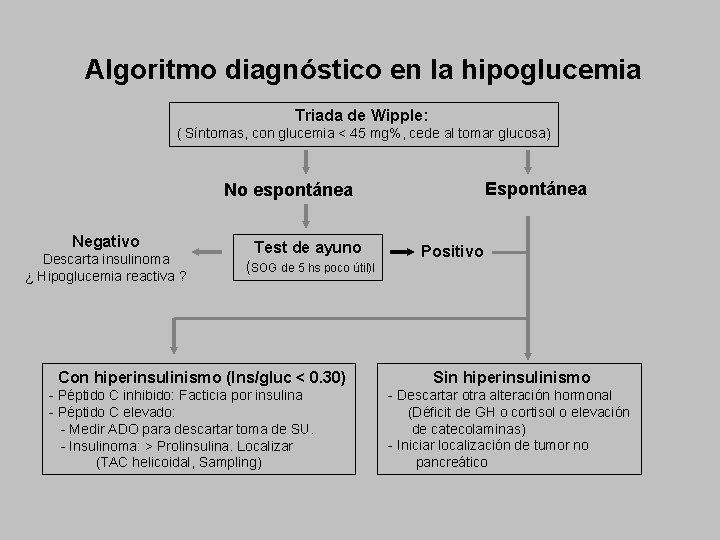
Algoritmo diagnóstico en la hipoglucemia Triada de Wipple: ( Síntomas, con glucemia < 45 mg%, cede al tomar glucosa) Espontánea No espontánea Negativo Descarta insulinoma ¿ Hipoglucemia reactiva ? Test de ayuno (SOG de 5 hs poco útil)l Con hiperinsulinismo (Ins/gluc < 0. 30) - Péptido C inhibido: Facticia por insulina - Péptido C elevado: - Medir ADO para descartar toma de SU. - Insulinoma: > Prolinsulina. Localizar (TAC helicoidal, Sampling) Positivo Sin hiperinsulinismo - Descartar otra alteración hormonal (Déficit de GH o cortisol o elevación de catecolaminas) - Iniciar localización de tumor no pancreático

Diabetes Clasificación. Etiopatogenia Clínica. Diagnóstico

Definición de diabetes Grupo de enfermedades metabólicas caracterizadas por hiperglucemia producida por defecto en la secreción y/o acción de la insulina. La hiperglucemia crónica produce daños, disfunción y fallo de varios órganos a largo plazo, fundamentalmente en los ojos, riñones, nervios, vasos y corazón El defecto en la secreción de insulina coexiste con frecuencia con defecto en su acción.

CLASIFICACION DE LA DIABETES Tipo 1: - autoinmune (LADA: desarrollo lento, en adultos) - Idiopática Tipo 2 Otros tipos - Defectos genéticos de la célula beta - Defectos genéticos en la ación de la insulina - Pancreatopatías - Endocrinopatías - Secundaria a drogas y agentes químicos - Infecciosas - Formas genéticas poco comunes - Otros síndromes genéticos asociados a la diabetes Diabetes gestacional Aparece con el embarazo y desaparece tras él
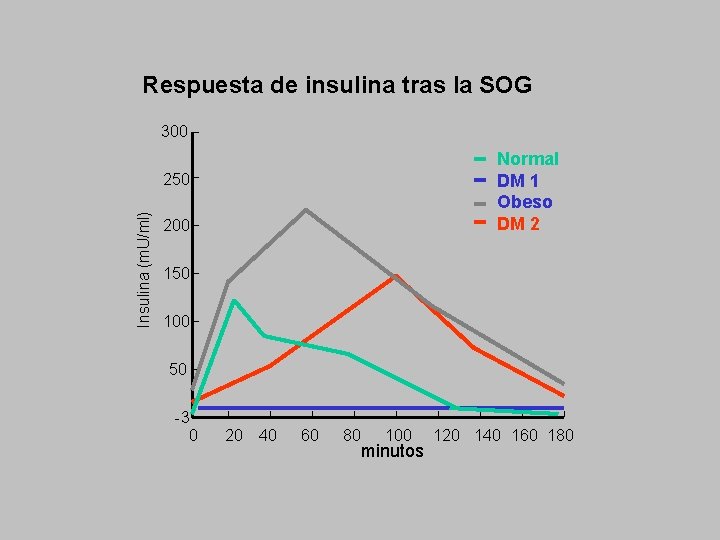
Respuesta de insulina tras la SOG 300 Normal DM 1 Obeso DM 2 Insulina (m. U/ml) 250 200 150 100 50 -3 0 20 40 60 80 100 minutos 120 140 160 180

PATOGENIA DE LA DM 1 Influencia genética: - Tendencia familiar. - Concordancia para gemelos homocigotos del 50% - Riesgo con un hermano diabético: 6. 6%, si el padre es diabetico: 2. 9% - Haplotipo Favorecedores: HLA DR 3 ( riesgo x 3), y DR 4 (riesgo x 4). Protector: HLA DR 2 DQW 8 (asociado al DR 4 contiene valina, serina o alanina en posición 57). La carga negativa le da una configuración espacial al receptor HLAll que favorecedora de la reacción inmune

Patogenia de la DM 1 Factores ambientales: Virus: a) Ratas: producen diabetes coxsackie, picornavirus. y retrovirus (produce insulitis con Acs) b) Hombre: - Se ha demostrado la infectación pancreática por virus CMV en diabéticos de reciente comienzo. - En diabéticos recientes hay Acs contra virus - Nutrición: - Lactancia artificial ( Acs antialbúmina de vaca en DM 1) - Hormonas: Mas incidencia de la diabetes en la pubertad

INMUNIDAD EN LA PATOGENIA DE LA DM 1 Inmunidad humoral: Anticuerpos (85 -90% alinicio) - ICA: Anticuerpo contra Ag plasmático de células de islotes. Inespecífico. No valor patogénico. Muy especifico y sensible - IAA: anticuerpos antiinsulina. Valor patogénico. - GADA 65: Acs contra glutámico decarboxilasa (produce GABA que actúa como neurotransmisor en la célula beta). Valor patogénico. Inmunidad celular - Aumentan linfocitos T helper y disminuyen los supresores. - Presentación patológica del HLA ll por la célula beta. - En el islote hay Infiltrado de linfocitos T y B activados, de macrófagos, de célula K y NK, depósito de inmunocomplejos y presentación de antígeno de clase ll en células capilares células beta
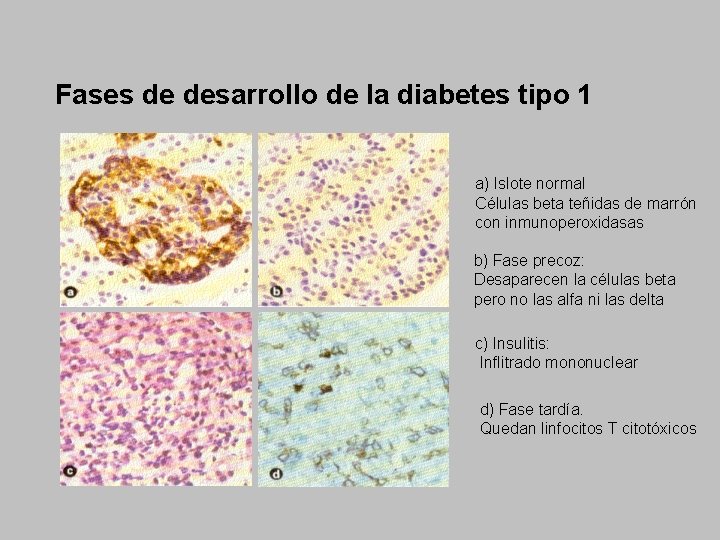
Fases de desarrollo de la diabetes tipo 1 a) Islote normal Células beta teñidas de marrón con inmunoperoxidasas b) Fase precoz: Desaparecen la células beta pero no las alfa ni las delta c) Insulitis: Inflitrado mononuclear d) Fase tardía. Quedan linfocitos T citotóxicos
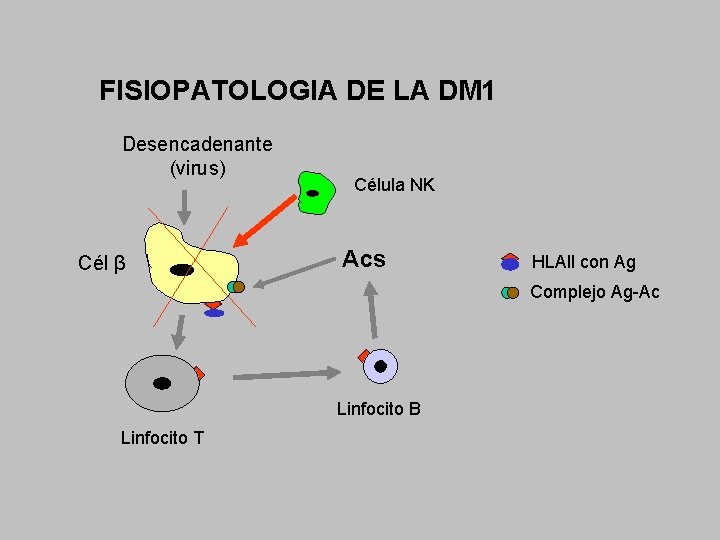
FISIOPATOLOGIA DE LA DM 1 Desencadenante (virus) Cél β Célula NK Acs HLAll con Ag Complejo Ag-Ac Linfocito B Linfocito T
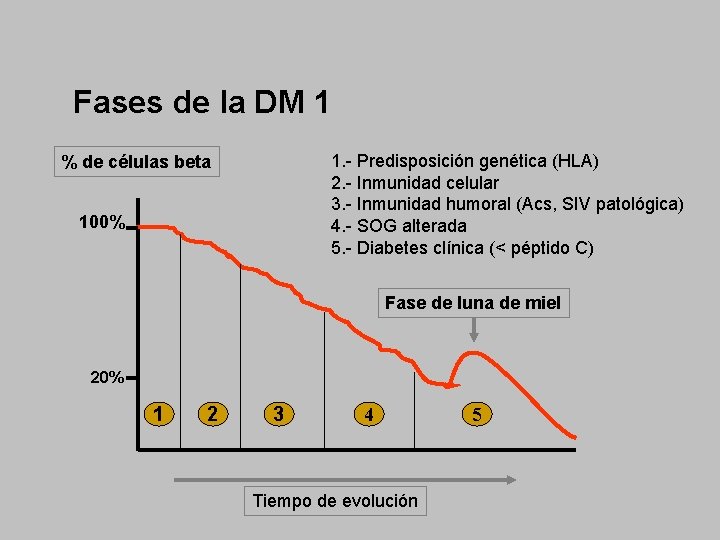
Fases de la DM 1 1. - Predisposición genética (HLA) 2. - Inmunidad celular 3. - Inmunidad humoral (Acs, SIV patológica) 4. - SOG alterada 5. - Diabetes clínica (< péptido C) % de células beta 100% Fase de luna de miel 20% 1 2 3 4 Tiempo de evolución 5

PATOGENIA DE LA DM 2 Influencia genética: Más importante que en la DM 1 Poligenica. No se conocen los genes Factores ambientales: ØObesidad abdominal: Estos adipocitos producen factores de resistencia: FFA, TNF alfa, leptina, RBP 4 y disminuyen factor protector: adiponectina Ø Sedentarismo: El ejercicio aumenta la expresión de GLUT 4 Ø La edad: Disminuye la secreción de insulina Interacción entre factores genéticos y ambientales - Hipótesis del fenotipo ahorrador (recién nacido con bajo peso, o emigrantes

PATOGENIA DE LA DM 2 1. - Resistencia a la insulina (RI) Favorecida genéticamente. Es anterior al déficit de insulina 2. - Alteración en la secreción de insulina Se suma al anterior para que aparezca la DM 2. Puede predominar el factor 1 o 2 pero la insulinemia no es suficiente para controlar la glucemia 3. - Aumento de la producción hepática de glucosa Consecuencia de los dos anteriores

PATOGENIA DE LA DM 2 Resistencia a la insulina (RI) Ø Transmisión genética Ø Favorecida por factores ambientales Ø Alteraciones detectadas: a) Menor transporte transmembrana de glucosa (menor translocación de GLUT 4) b) Menor eficiencia de glucógeno sintetasa
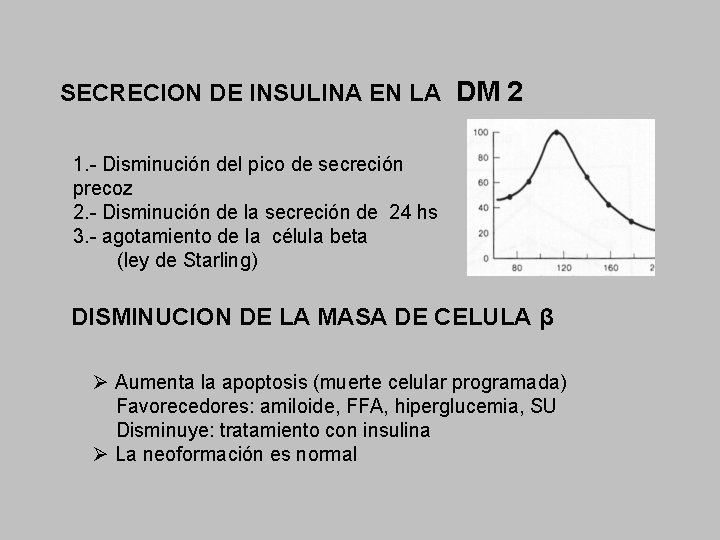
SECRECION DE INSULINA EN LA DM 2 1. - Disminución del pico de secreción precoz 2. - Disminución de la secreción de 24 hs 3. - agotamiento de la célula beta (ley de Starling) DISMINUCION DE LA MASA DE CELULA β Ø Aumenta la apoptosis (muerte celular programada) Favorecedores: amiloide, FFA, hiperglucemia, SU Disminuye: tratamiento con insulina Ø La neoformación es normal
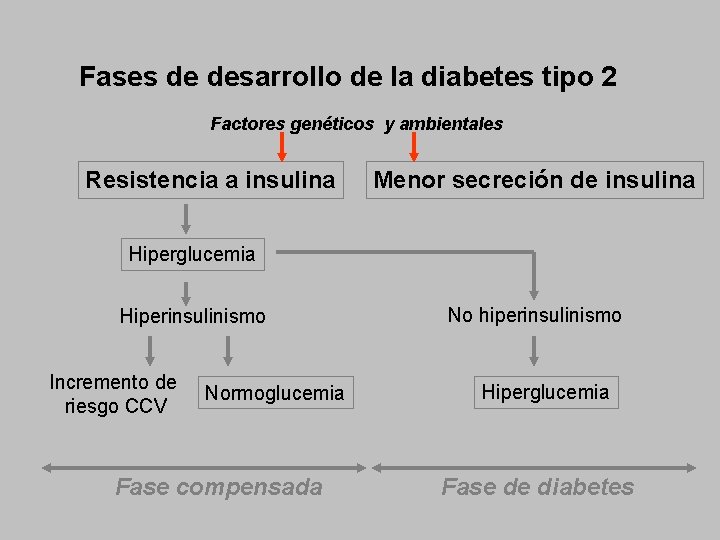
Fases de desarrollo de la diabetes tipo 2 Factores genéticos y ambientales Resistencia a insulina Menor secreción de insulina Hiperglucemia Hiperinsulinismo Incremento de riesgo CCV Normoglucemia Fase compensada No hiperinsulinismo Hiperglucemia Fase de diabetes

DIAGNOSTICO DE DM 1ª. - Glucemia plasma al azar ≥ 200 mg/dl con síntomas cardinales 2º. - Glucemia plasm. A en ayunas ≥ 126 mg/dl en más de una ocasión 3ª. - Glucemia plasma 2 hs tras SOG ≥ 200 mg/dl Glucemia capilar no vale como diagnostico, si como sospecha

Otros criterios diagnósticos en la DM ATG (alteración de la tolerancia a la glucosa) (IGT) Glucemia en plasma a las dos horas de la SOG entre 140 y 200 mg/dl AGA (alteración de la glucemia en ayunas) (IFG): Glucemia plasmática en ayunas entre 100 y 126 mg/dl Normalidad: Glucemia en plasma en ayunas menor de 100 mg/dl Realización de la SOG: (EADPG) - Con 75 grs de glucosa o 1. 75 gr/kg en niños. Extracciones basal y a las dos horas. La ADA sólo la indica en el embarazo con 100 grs ADA 2004

DIAGNOSTICO DE DIABETES EN EMBARAZO Criterios EADPG (IDF 2005) - Realizar SOG si una glucemia > 110 mg/dl (en cualquier momento). -Diabetes si glucemia basal > 126 mg/dl, , o a las 2 hs de la SOG con 75 grs > 140 mg/dl Criterios ADA (2001) - Screening en embarazadas con riesgo - Test O´Sullivan (50 grs de glucosa), entre la semana 24 y 28 , si a la hora glucemia > 140 mg/dl, hacer SOG con 100 grs. Diabetes si 2 o más valores son superiores a: Ayunas 95 mg/dl 1 h 180 mg/dl 2 hs 155 mg/dl 3 hs 140 mg/dl

Clínica de la diabetes Asintomática durante años (DM 2). Sin embargo ya tiene efectos perjudiciales CCV por producir alteración en la coagulación, lípidos, hipertensión o disfunción endotelial Cardinal: Poliuria polidipsia, polifagia, pérdida de peso. Otras: astenia, infecciones Complicaciones - Agudas: Cetoacidosis diabética. Coma hiperosmolar Coma hipoglucémico. Acidosis láctica - Crónicas: Por microangiopatía: Retinopatía y Nefropatía Neuropatía periférica y autonómica Macroangiopatía: IAM, Ulceras en pie, Claudicación intermitente
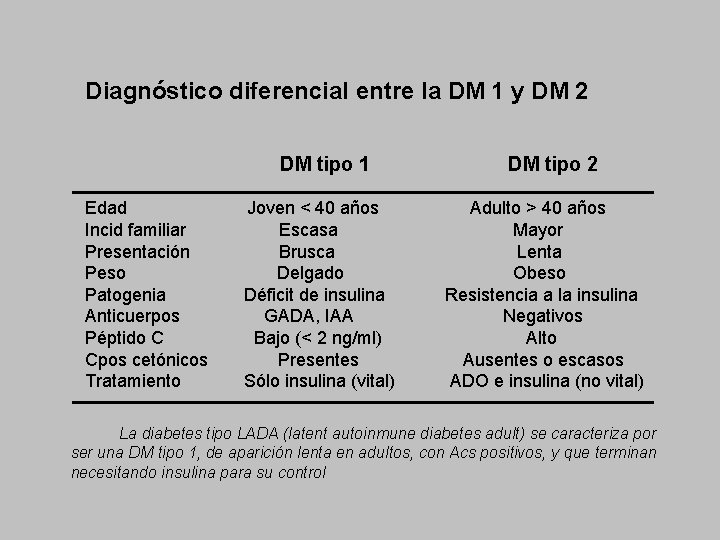
Diagnóstico diferencial entre la DM 1 y DM 2 DM tipo 1 Edad Incid familiar Presentación Peso Patogenia Anticuerpos Péptido C Cpos cetónicos Tratamiento Joven < 40 años Escasa Brusca Delgado Déficit de insulina GADA, IAA Bajo (< 2 ng/ml) Presentes Sólo insulina (vital) DM tipo 2 Adulto > 40 años Mayor Lenta Obeso Resistencia a la insulina Negativos Alto Ausentes o escasos ADO e insulina (no vital) La diabetes tipo LADA (latent autoinmune diabetes adult) se caracteriza por ser una DM tipo 1, de aparición lenta en adultos, con Acs positivos, y que terminan necesitando insulina para su control
- Slides: 28