Fisiopatologia dei globuli rossi Le anemie Parte III
Fisiopatologia dei globuli rossi Le anemie – Parte III

Anemie ipoproliferative

Anemie ipoproliferative (75% anemie) • Insufficienza midollare: the erithroid marrow has not proliferated • Cause principali: – Sideropenia lieve/moderata (+++) – Infiammazione (+++) – Danno al midollo • Infiltrazione/fibrosi • Aplasia – Ridotta stimolazione (EPO) • Soppressione da citochine infiammatorie (i. e. IL-1) • malattia metabolica (ipotiroidismo) • Insufficienza renale

Anemie ipoproliferative At least 75% of all cases of anemia are hypopproliferative in nature. A hypoproliferative anemia reflects absolute or relative marrow failure in which the eritroid marrow has not proliferated appropriately for the degree of anemia. The majority of hypoproliferative anemias are due to mild or moderate iron deficiency or inflammation. A hypoproliferative anemia can result from marrow damage, iron deficiency, or inadeguate EPO stimulation. The last may reflect impaired renal function, suppression of EPO production by inflammatory citokines suche as IL 1 , or reduced tissue needs for oxigen from metabolic disease such as hypotiroidism. Only occasionally is the marrow unable to produce red cells at a normal rate, and this is most prevalent in patients with renal failure. In general hypoproliferative anemias are characterized by normocitic, normocromic red cells, although microcitic hypochromic cells may be obsedrved with mild iron deficiency or long standing chronic inflammatory disease.

ANEMIA SIDEROPENICA -RIDOTTA SINTESI DI Hb -ERITROCITI PICCOLI MCV < 80 NORMALE ANEMIA SIDEROPENICA Hb g/dl 15, 0 7, 5 ERITROCITI / l 5. 000 4. 000 Hct 45% 28% MCV (Hct / GR) 90 3 70 3 - RIDOTTO APPORTO DI FERRO (ALIMENTI) - RIDOTTO ASSORBIMENTO DI FERRO - AUMENTATA PERDITA DI FERRO (SANGUE)

FERRO COMPOSTI “FUNZIONALI” QUASI SEMPRE EMICI* - PER LA “RESPIRAZIONE” CELLULARE (ENZIMI) - PER IL DEPOSITO DELL’ O 2 (MIOGLOBINA, MUSCOLO) - PER IL TRASPORTO E LO SCAMBIO DELL’ O 2 (EMOGLOBINA) COMPOSTI DI DEPOSITO - FERRITINA, EMOSIDERINA (SISTEMA MONOCITOMACROFAGICO, EPATOCITI) * EME: NUCLEO TETRAPIRROLICO CON UN ATOMO DI FERRO CAPACE DI LEGARE O 2

IL FERRO NELL’ORGANISMO COMPOSTI FUNZIONALI -EMICI - EMOGLOBINA 1800 - 2800 mg - MIOGLOBINA 300 - 600 mg - ENZIMI -NON EMICI - PROTEINE, ENZIMI 6 - 10 mg 2 - 4 mg COMPOSTI DI TRASPORTO - TRANSFERRINA 2 - 4 mg COMPOSTI DI DEPOSITO - FERRITINA, EMOSIDERINA 200 - 1200 mg TOTALE ~ 2300 - 4600 mg 50 mg/Kgt
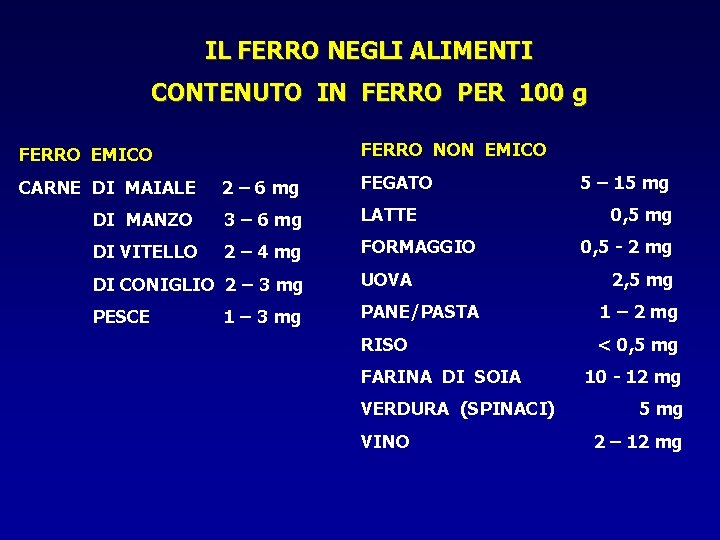
IL FERRO NEGLI ALIMENTI CONTENUTO IN FERRO PER 100 g FERRO NON EMICO FERRO EMICO CARNE DI MAIALE 2 – 6 mg FEGATO DI MANZO 3 – 6 mg LATTE DI VITELLO 2 – 4 mg FORMAGGIO 5 – 15 mg 0, 5 - 2 mg DI CONIGLIO 2 – 3 mg UOVA PESCE PANE/PASTA 1 – 2 mg RISO < 0, 5 mg 1 – 3 mg FARINA DI SOIA VERDURA (SPINACI) VINO 2, 5 mg 10 - 12 mg 5 mg 2 – 12 mg

CARENZA MARZIALE E ANEMIA SIDEROPENICA - CARENZA MARZIALE VUOL DIRE CHE NELL’ORGANISMO NON C’E’ PIU’ FERRO NEI DEPOSITI, C’E’ POCO FERRO DISPONIBILE PER LA MIOGLOBINA E GLI ENZIMI EMICI, MA C’E’ ANCORA FERRO A SUFFICIENZA PER SINTETIZZARE Hb: MANCANO CIRCA 1000 mg DI FERRO. - ANEMIA SIDEROPENICA VUOL DIRE CHE NON C’E’ PIU’ NEANCHE FERRO A SUFFICIENZA PER LA SINTESI DELL’ Hb: MANCANO PIU’ DI 1000 mg DI FERRO, IN GENERE PIU’ DI 2000.

LE CAUSE DELLA CARENZA MARZIALE - DEFICIT DI APPORTO (LATTE NON MATERNO, NON ARRICCHITO IN FERRO, DIETA POVERA) - DEFICIT DI ASSORBIMENTO (MALATTIE INFIAMMATORIE CRONICHE DEL TUBO DIGERENTE, MALASSORBIMENTI, ANTICORPI ANTI-GLIADINA) - AUMENTO PERDITE - “FISIOLOGICHE” – MESTRUAZIONI, GRAVIDANZE - PATOLOGICHE BENIGNE – METRORRAGIE, ERNIA GASTRICA IATALE, ULCERE GASTRICHE E DUODENALI, MALATTIE INFIAMMATORIE CRONICHE DELL’INTESTINO, POLIPOSI COLICA, ANGIOMI, EMORROIDI, . . . - PATOLOGICHE MALIGNE – TUMORI DEL TUBO DIGERENTE

LE CAUSE DELLA CARENZA DI FERRO -NEI PAESI “RICCHI” PREVALENTEMENTE UN ECCESSO DI PERDITA - CAUSE GINECOLOGICHE NELLE FEMMINE - CAUSE GASTROENTERICHE NEI MASCHI -NEI PAESI “POVERI” PREVALENTEMENTE UN DIFETTO DI APPPORTO E ASSORBIMENTO

CARENZA MARZIALE E ANEMIA SIDEROPENICA L’IMPORTANZA DELLE PICCOLE EMORRAGIE O PERDITE CRONICHE IN 1 ml DI SANGUE CI SONO 0, 15 g DI Hb IN 1 g DI Hb CI SONO 3, 33 mg DI FERRO IN 1 ml DI SANGUE CI SONO 0, 50 mg DI FERRO PERDERE 5 ml DI SANGUE AL GIORNO VUOL DIRE PERDERE CIRCA 2, 5 mg DI FERRO, CIOE’ PIU’ DEL DOPPIO DELLA PERDITA FISIOLOGICA

SINTOMI E SEGNI DELLA CARENZA MARZIALE E DELL’ANEMIA SIDEROPENICA - CARENZA E ANEMIA SI STABILISCONO LENTAMENTE. IL PAZIENTE “SI ABITUA AL SUO STATO”. - DEFICIT DI CONCENTRAZIONE, DI ATTENZIONE, DI MEMORIA. - FRAGILITA’ UMORALE E COMPORTAMENTALE. - FACILE STANCABILITA’. - ASTENIA, CARDIOPALMO E DISPNEA DA SFORZO. - TACHICARDIA, PALLORE. - FRAGILITA’ DEI CAPELLI E DELLE UNGHIE. - DISTROFIA MUCOSA CAVO ORALE E FARINGE (SINDROME DI PLUMMER-VINSON).

COME SI MISURA IL FERRO NELL’ORGANISMO SIDEREMIA - MISURA LA QUANTITA’ DI FERRO CHE CIRCOLA LEGATO ALLA TRANSFERRINA - MOLTO BASSA (< 30) IN CASO DI ANEMIA SIDEROPENICA - BASSA (< 80) IN CASO DI CARENZA MARZIALE - BASSA (< 80) IN CASO DI ANEMIA SECONDARIA (INTRAPPOLAMENTO DEL FERRO NEL SISTEMA MONOCITO-MACROFAGICO) - ALTA (> 150) IN CASO DI EMOCROMATOSI E EMOSIDEROSI

COME SI MISURA IL FERRO NELL’ORGANISMO TRANSFERRINEMIA MISURA LA QUANTITA’ DI PROTEINA (TRANSFERRINA) CAPACE DI LEGARE IL FERRO (TOTAL IRON BINDING CAPACITY, TIBC) - MOLTO ALTA (> 400) IN CASO DI ANEMIA SIDEROPENICA - ALTA (> 300) IN CASO DI CARENZA MARZIALE - BASSA (< 250) IN CASO DI INTRAPPOLAMENTO DEL FERRO NEL SISTEMA MONOCITO-MACROFAGICO (ANEMIE SECONDARIE) - MOLTO BASSA (< 200) IN CASO DI EMOCROMATOSI E EMOSIDEROSI

COME SI MISURA IL FERRO NELL’ORGANISMO SATURAZIONE DELLA TRANSFERRINA SIDEREMIA TRANSFERRINEMIA X 100 120 300 X 100 = 40 % - MOLTO BASSA (< 10%) IN CASO DI ANEMIA SIDEROPENICA - BASSA (< 25%) IN CASO DI CARENZA MARZIALE - ALTA (> 50%) IN CASO DI ANEMIA SECONDARIA - MOLTO ALTA (> 75%) IN CASO DI EMOCROMATOSI E EMOSIDEROSI

COME SI MISURA IL FERRO NELL’ORGANISMO FERRITINEMIA IN CONDIZIONI FISIOLOGICHE 1 g = 8 mg DI FERRO NEI DEPOSITI - MOLTO BASSA (< 10) IN CASO DI CARENZA MARZIALE E DI ANEMIA SIDEROPENICA - ALTA (> 200) IN CASO DI ANEMIA SECONDARIA* - MOLTO ALTA (> 1000) IN CASO DI EMOCROMATOSI E EMOSIDEROSI * IL DANNO TISSUTALE DA INFEZIONE, INFIAMMAZIONE E TUMORI AUMENTA LA FERRITINEMIA, INDIPENDENTEMENTE DALLA QUANTITA’ DI FERRO NEI DEPOSITI

NORMALE CARENZA MARZIALE ANEMIA SIDEROPENICA ANEMIE SECONDARIE EMOCROMATOSI E EMOSIDEROSI SIDEREMIA 80 -150 < 80 < 30 < 80 > 150 TRANSFERRINEMIA 200 -300 > 400 < 250 < 200 SATURAZIONE TRANSFERRINA 20 -40% < 20% < 10% > 50% > 75% FERRITINEMIA 50 -200 < 20 < 10 > 200 > 1000
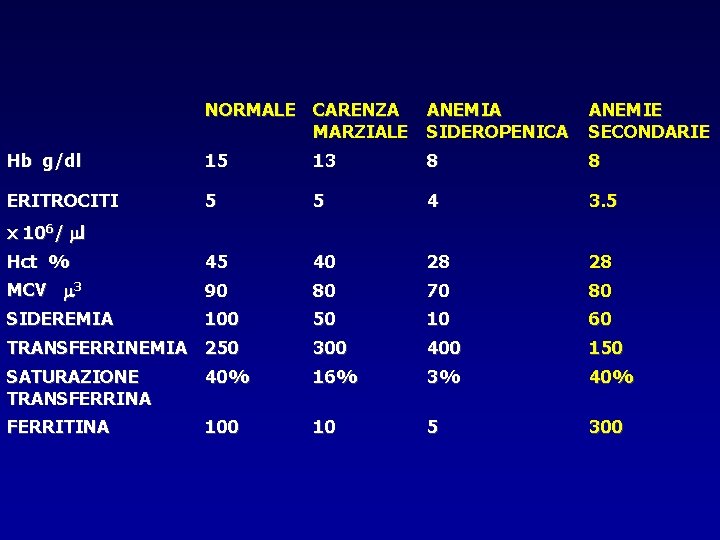
NORMALE CARENZA MARZIALE ANEMIA SIDEROPENICA ANEMIE SECONDARIE Hb g/dl 15 13 8 8 ERITROCITI 5 5 4 3. 5 Hct % 45 40 28 28 MCV 3 90 80 70 80 SIDEREMIA 100 50 10 60 TRANSFERRINEMIA 250 300 400 150 SATURAZIONE TRANSFERRINA 40% 16% 3% 40% FERRITINA 100 10 5 300 x 106/ l

LA CARENZA DI FERRO - RIDUCE LA RESISTENZA ALLE INFEZIONI? - SI – L’O 2 E’ NECESSARIO PER LE FUNZIONI MICROBICIDE - NO – IL FERRO E’ UTILE PER LA CRESCITA DEI BATTERI - INFLUENZA LE CAPACITA’ FISICHE E INTELLETTIVE, IL COMPORTAMENTO E L’UMORE? - SI, DIPENDONO DALL’ O 2 E DALLO STATO GENERALE DI SALUTE - INFLUENZA IL LAVORO CARDIACO? - SI – PERCHE’ IL CUORE DISPONE DI MENO O 2 - NO – PERCHE’ IN CORSO DI CARENZA MARZIALE GLI ERITROCITI SONO PICCOLI E DEFORMABILI, LE RESISTENZE AL FLUSSO SONO DIMINUITE E IL LAVORO CARDIACO E ’ RIDOTTO - INFLUENZA LA DURATA DELLA VITA? - ? …. . LE FEMMINE VIVONO PIU’ A LUNGO DEI MASCHI

I diversi gradi della sideropenia • II-III fase – (Hb Htc ) – Moderata anemia = stadio ipoproliferativo – Anemia severa = stadio iperproliferativo – ------> Ineffective maturation – MCHC e MCV diminuiscono. – in caso di grave anemia, danno epiteliale causato da deplezione degli enzimi che utilizzano ferro

Sideropenia
![ANEMIA DA PATOLOGIE CRONICHE [Anemia da infiammazione cronica] ANEMIA DA PATOLOGIE CRONICHE [Anemia da infiammazione cronica]](http://slidetodoc.com/presentation_image/1c977d807f620e265a2c3282e8375fdf/image-23.jpg)
ANEMIA DA PATOLOGIE CRONICHE [Anemia da infiammazione cronica]

Definizione • Anemia ipoproliferativa • Patologie croniche non-ematologiche -Infezioni -Tumori -Immunitarie -Traumatiche • In comune: risposta infiammatoria alla causa sottostante

Anemia da patologie croniche 1. Tipo di anemia più comune in pazienti ospedalizzati 2. Tipicamente da lieve a moderata (proporzionalmente al processo infiammatorio sottostante) 3. RBC: Normocitici, normocromici 4. Ipoferremia e aumento ferro nei depositi

CAUSE PREVALENTI DI ANEMIA DA MALATTIA CRONICA La prevalenza e gravità della anemia correla con lo stadio di avanzamento della patologia sottostante e con la età. Nei tumori è subordinata al tipo di terapia

FATTORI FISIOPATOLOGICI - alterata omeostasi del ferro - eritropoiesi ridotta - bassi livelli di eritropoietina

Anemia da patologie croniche • Alterato Metabolismo del Fe - serum iron concentration - normal to TIBC - transferrin saturation - iron absorption - Normal to serum ferritin - macrophage iron stores normochromic, normocytic anemia mild to moderate low reticulocyte count (underproduction) no absolute iron deficiency multifactorial

Anemia da patologie croniche Anemia of chronic disease is a normochromic, normocytic anemia that is characteristically mild (hemoglobin level, 9. 5 g per deciliter) to moderate (hemoglobin level, 8 g per deciliter). Patients with the condition have a low reticulocyte count, which indicates underproduction of red cells. The evaluation of anemia of chronic disease must also include a determination of the status of whole-body iron in order to rule out iron-deficiency anemia, usually hypochromic and microcytic. The difference between anemia of chronic disease and irondeficiency anemia thus relates to the latter as an absolute iron deficiency, whereas the pathophysiology of anemia of chronic disease is multifactorial. In both anemia of chronic disease and iron-deficiency anemia, the serum concentration of iron and transferrin saturation are reduced, reflecting absolute iron deficiency in iron-deficiency anemia and hypoferremia due to acquisition of iron by the reticuloendothelial system in anemia of chronic disease. In the case of anemia of chronic disease, the decrease in transferrin saturation is primarily a reflection of decreased levels of serum iron. In iron-deficiency anemia, transferrin saturation may be even lower because serum concentrations of the iron transporter transferrin are increased, whereas transferrin levels remain normal or are decreased in anemia of chronic disease. The search for an underlying cause of iron deficiency should include a history taking to rule out a dietary cause. Frequently, iron deficiency indicates pathological blood loss such as an increased loss of menstrual blood in women or chronic gastrointestinal bleeding in the setting of ulcerative gastrointestinal disease, inflammatory bowel disease, angiodysplasia, colon adenomas, gastrointestinal cancer, or parasitic infections. Ferritin is used as a marker of iron storage, and a level of 15 ng per milliliter is generally taken as indicating absent iron stores. For patients with anemia of chronic disease, however, ferritin levels are normal or increased, reflecting increased storage and retention of iron within the reticuloendothelial system, along with increased ferritin levels due to immune activation.
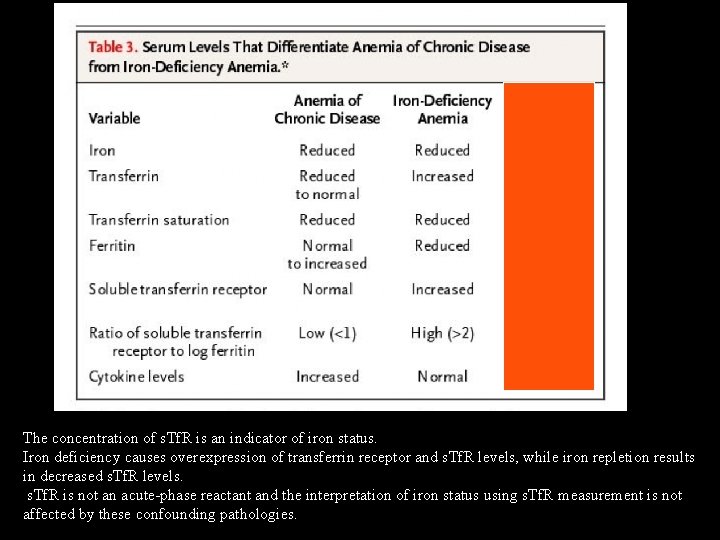
The concentration of s. Tf. R is an indicator of iron status. Iron deficiency causes overexpression of transferrin receptor and s. Tf. R levels, while iron repletion results in decreased s. Tf. R levels. s. Tf. R is not an acute-phase reactant and the interpretation of iron status using s. Tf. R measurement is not affected by these confounding pathologies.
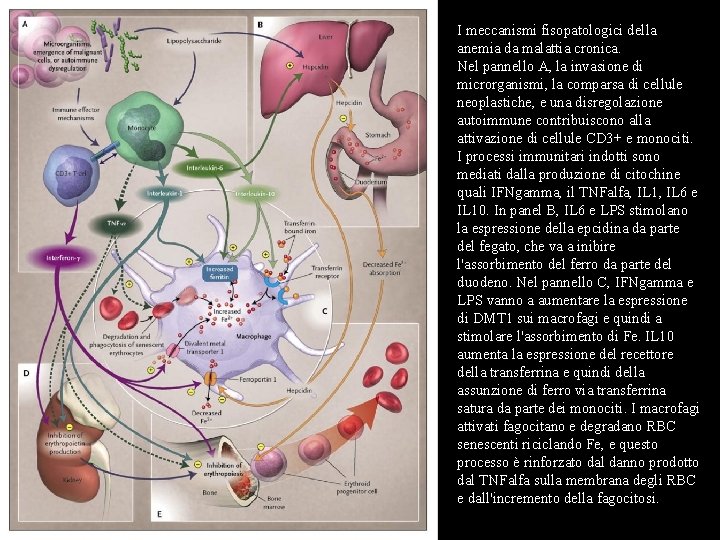
I meccanismi fisopatologici della anemia da malattia cronica. Nel pannello A, la invasione di microrganismi, la comparsa di cellule neoplastiche, e una disregolazione autoimmune contribuiscono alla attivazione di cellule CD 3+ e monociti. I processi immunitari indotti sono mediati dalla produzione di citochine quali IFNgamma, il TNFalfa, IL 1, IL 6 e IL 10. In panel B, IL 6 e LPS stimolano la espressione della epcidina da parte del fegato, che va a inibire l'assorbimento del ferro da parte del duodeno. Nel pannello C, IFNgamma e LPS vanno a aumentare la espressione di DMT 1 sui macrofagi e quindi a stimolare l'assorbimento di Fe. IL 10 aumenta la espressione del recettore della transferrina e quindi della assunzione di ferro via transferrina satura da parte dei monociti. I macrofagi attivati fagocitano e degradano RBC senescenti riciclando Fe, e questo processo è rinforzato dal danno prodotto dal TNFalfa sulla membrana degli RBC e dall'incremento della fagocitosi.
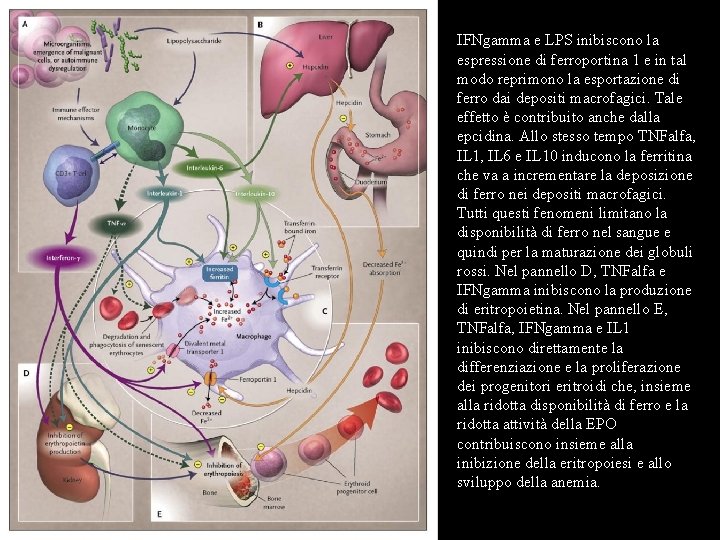
IFNgamma e LPS inibiscono la espressione di ferroportina 1 e in tal modo reprimono la esportazione di ferro dai depositi macrofagici. Tale effetto è contribuito anche dalla epcidina. Allo stesso tempo TNFalfa, IL 1, IL 6 e IL 10 inducono la ferritina che va a incrementare la deposizione di ferro nei depositi macrofagici. Tutti questi fenomeni limitano la disponibilità di ferro nel sangue e quindi per la maturazione dei globuli rossi. Nel pannello D, TNFalfa e IFNgamma inibiscono la produzione di eritropoietina. Nel pannello E, TNFalfa, IFNgamma e IL 1 inibiscono direttamente la differenziazione e la proliferazione dei progenitori eritroidi che, insieme alla ridotta disponibilità di ferro e la ridotta attività della EPO contribuiscono insieme alla inibizione della eritropoiesi e allo sviluppo della anemia.

Aplastic Anemia, myelodysplasia, e sindromi correlate a insufficienza midollare n n Anemie ipoproliferative associate a danno midollare n Aplastic anemia n Myelodysplasia (MDS) n Aplasia pura eritrocitaria n mieloftisi Ematopoiesi inefficiente provoca pancitopenia Anemia normocromica, normocitica o macrocitica Conta reticolocitaria ridotta

Aplastic anemia n n n Grave sindrome a rischio letale per assente produzione di RBC, leucociti e piastrine. Aplastic anemia insorge a tutte le età e sesso. Incidenza: 2 casi/million/anno

Aplastic anemia n n Il difetto primario consiste nella riduzione o deplezione del pool di cellule staminali precursori delle diverse linee differenziative ematologiche, conseguente pancitopenia periferica. Assenza di fattori patogenetici che provocano infiltrazione, sostituzione o soppressione del tessuto ematopoietico.

Aplastic Anemia Fisiopatologia n Patogenesi eterogenea Difetto qualitativo della cellula staminale n Micro-ambiente midollare difettivo n Difettosa produzione o funzionalità di fattori di crescita emopoietici n Immune suppression n

Aplastic Anemia Classificazione n Congenita (~ 20%) n Sindrome Congenita da insufficienza midollare • • n Fanconi Anemia Dyskeratosis Congenita Shwachman-Diamond Syndrome Amegakaryocytic Thrombocytopenia Acquisita(~ 80%) n n ~ 50% causa accertata ~ 50% idiopatica

Aplastic anemia n Congenital disorders n Fanconi’s anemia n Autosomal recessive n Increased risk for malignancies n Chromosomes are susceptible to DNA cross-linking agents n At least 8 different genetic defects n Genes play a role in response to DNA damage n the disorder usually becomes symptomatic ~ 5 years of age and is associated with progressive bone marrow hypoplasia. Congenital defects such as skin hyperpigmentation and small stature also seen in affected individuals.

Aplastic anemia n Acquired n Most cases of aplastic anemia are idiopathic and there is no history of exposure to substances known to be causative agents of the disease n Exposure to ionizing radiation – hematopoietic cells are especially susceptible to ionizing radiation. Whole body radiation of 300 -500 rads can completely wipe out the bone marrow. With sublethal doses, the bone marrow eventually recovers. n Chemical agents – include chemical agents with a benzene ring, chemotherapeutic agents, and certain insecticides. n Idiosyncratic reactions to some commonly used drugs such as chloramphenicol or quinacrine (no dose response).

Aplastic anemia n n Infections – viral and bacterial infections such as infectious mononucleosis, infectious hepatitis, cytomegalovirus infections, and miliary tuberculosis occasionally lead to aplastic anemia Immunologic disease (Transfusion associated GVHD, eosinophilic fasciitis) Pregnancy (rare) Paroxysmal nocturnal hemoglobinuria – this is a stem cell disease in which the membranes of RBCs, WBCs and platelets have an abnormality making them susceptible to complement mediated lysis.

Aplastic anemia n Lab findings n Severe pancytopenia with relative lymphocytosis (lymphocytes live a long time) n CD 34+ cells - stem cell pool < 1% n Normochromic, normocytic RBCs (may be slightly macrocytic) n Mild to moderate anisocytosis and poikilocytosis n Decreased reticulocyte count n Hypocellular bone marrow with > 70% yellow marrow (FAT)

Pure Red Cell Aplasia n Is characterized by a selective decrease in erythroid precursor cells in the bone marrow. WBCs and platlets are unaffected.

Pure Red Cell Aplasia n Congenital n Diamond-Blackfan syndrome – occurs in young children and is progressive. It is probably due to an intrinsic or regulatory defect in the committed erythroid stem cell. Acquired n n n n Transitory with viral or bacterial infections Patients with hemolytic anemias may suddenly halt erythropoiesis Thymoma and malignancy – cytotoxic antibodies to bone marrow erythroblasts or to erythropoietin are sometimes produced Connective tissue disorders with immunologic abnormalities Drugs Idiopathic

ANEMIA OF RENAL DISEASE • Failure to produce adeguately EPO • Reduction of red cell survival

ANEMIA OF HYPOMETABOLIC STATES • Endocrine deficiency – – – Testosterone estrogeni Ipotiroidismo Ipopituitarismo Addison disease Iperparatiroidismo • Protein starvation • Chronic liver disease – Excess cholesterol ----> spur cells, stomatociti (ridotta sopravvivenza)
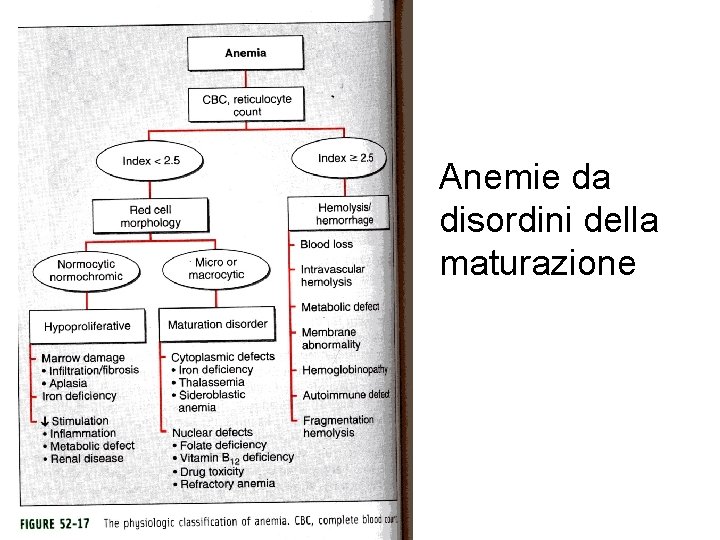
Anemie da disordini della maturazione

Disordini della maturazione The low reticulocite production index is a reflection of the ineffective erithropoiesis that results from the destruction within the marrow of the developing eritroblasts. Marrow morfology shows M/E ratio < 1: 1, diagnostic of eritroid iperplasia. • Difetti maturazione a livello citoplasmatico: Microcitosi e ipocromia da Hb – Sideropenia grave • Anemia sideropenica • Anemia sideroblastica – Talassemia • Difetti maturazione a livello nucleare: macrocitosi e sviluppo anomalo del midollo – – Deficienza di folati Def. Vitamina B 12 Tossicità da farmaci che interferiscono con metabolismo DNA Anemia refrattaria (mielodisplasia)

Anemia sideropenica e anemia sideroblastica Nel caso di anemia sideropenica se l'anemia è grave e prolungata, il midollo eritroide diventa iperplastico nonostante il deficit marziale. La anemia è caratterizzata da eritropoiesi inefficace. L’ anemia sideroblastica è conseguenza di mielodisplasia. La mancata formazione dell’eme è causata da accumulo del ferro nei mitocondri dei sideroblasti midollari che assumono la forma di sideroblasti ad anello. In ambedue i casi l’indice di produttività dei reticolociti è basso
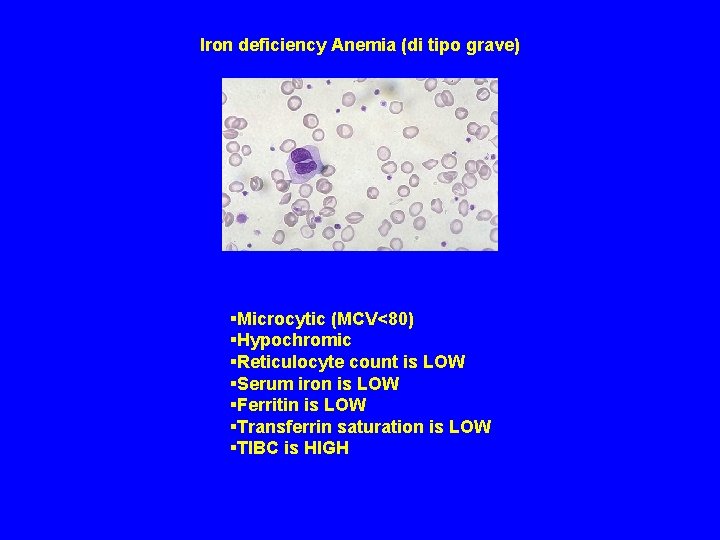
Iron deficiency Anemia (di tipo grave) §Microcytic (MCV<80) §Hypochromic §Reticulocyte count is LOW §Serum iron is LOW §Ferritin is LOW §Transferrin saturation is LOW §TIBC is HIGH

TALASSEMIE vedi slides a parte
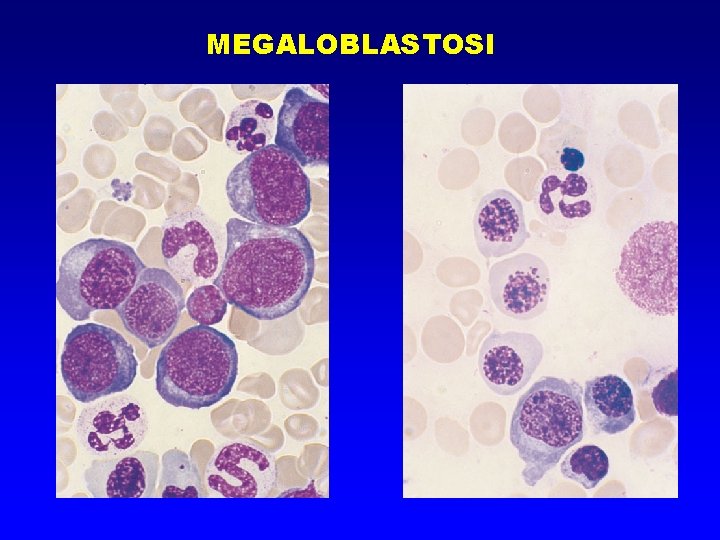
MEGALOBLASTOSI

ANEMIE difetti maturativi • Da deficit di sintesi di DNA per: – Carenza di Vitamina B 12 – Carenza di Acido folico/folati – Farmaci MEGALOBLASTOSI DEI PRECURSORI ERITROIDI • Asincronismi maturativi nucleo-citoplasmatici • Alterata divisione cellulare con frequente arresto in fase S e salto di una o più mitosi MACROCITOSI DEGLI ERITROCITI (MCV > 100 )
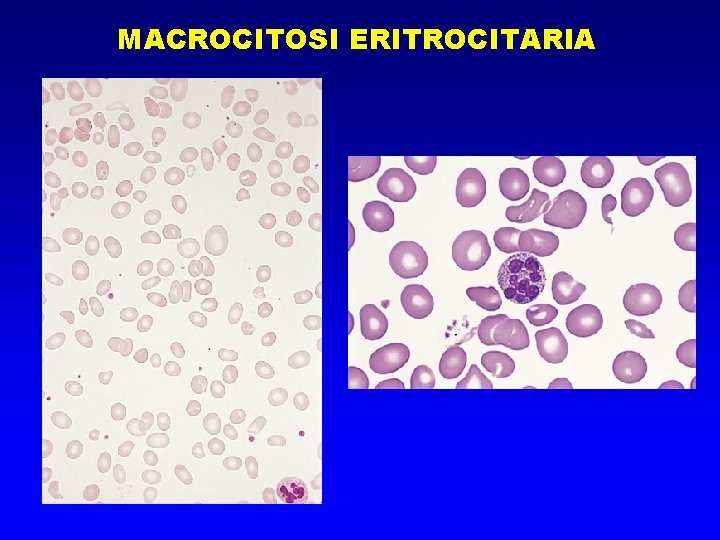
MACROCITOSI ERITROCITARIA

ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 • La Vitamina B 12 (cobalamina) è presente nel cibo (prevalentemente di origine animale quali carni, latte, uova) nelle forme coenzimaticamente attive: – Metil-cobalamina: Coenzima della METIONINA SINTETASI Metilazione della omocisteina a metionina – Adenosil-cobalamina: coenzima della L-METIL-MALONIL-COA MUTASI isomerizzazione della L metilmalonil-Co. A a Succinil Co. A
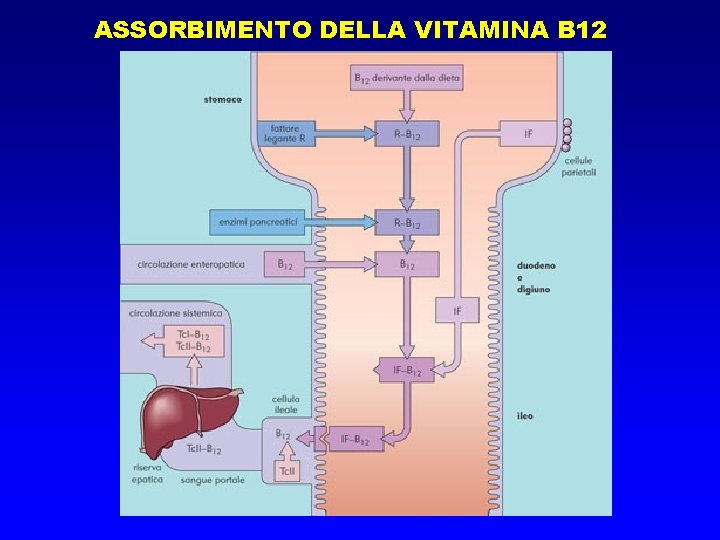
ASSORBIMENTO DELLA VITAMINA B 12

ANEMIE MEGALOBLASTICHE DA DEFICIT DI ACIDO FOLICO E FOLATI • L’acido folico e i folati sono presenti nei vegetali e nelle carni sotto forma di: – Acido pteroilmonoglutammico: assorbito direttamente nel duodeno e digiuno prossimale – Poliglutammati: convertiti intraluminalmente in acido folico (FH 4) • I folati animali (monoglutammati) sono meglio assorbiti di quelli vegetali (per lo più poliglutammati)
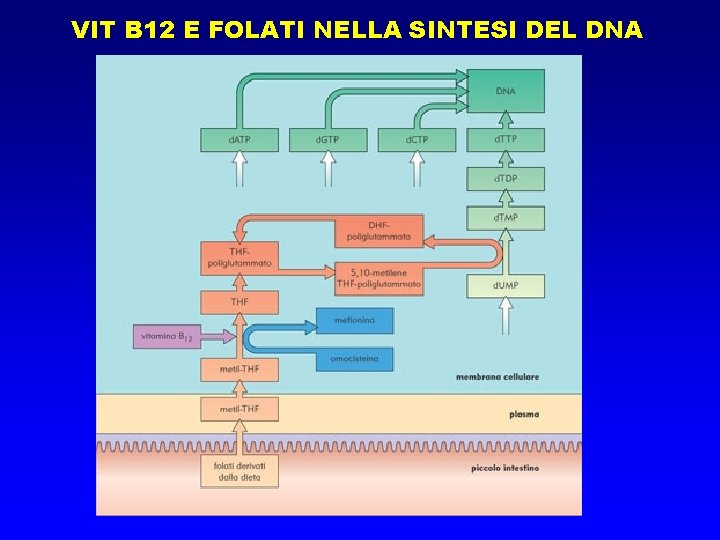
VIT B 12 E FOLATI NELLA SINTESI DEL DNA

METABOLISMO DELLA VITAMINA B 12 E DEI FOLATI VIT B 12 AC. FOLICO ALIMENTI • Vegetali • Animali +++ + +++ FABBISOGNO/DIE 2. 5 g 50 -500 g ASSORBIMENTO ileo Duodeno/digiuno prossimale Transcobalamina I/II Albumina/ 2 macroglobulina 200 -900 ng/ml 6 -20 g/L - 160 -640 g/L 2 -5 mg 5 -20 mg LEGAMI PROTEICI CONC. SIERICA CONC. ERITROCITI DEPOSITI

CAUSE DI ANEMIA MEGALOBLASTICA DEFICIT DI VITAMINA B 12 • Insufficiente apporto: dieta strettamente vegetale • Carenza di FI: – anemia perniciosa (Ab anti FI nel 60% casi, anti cell parietali stomaco nel 90% casi) – gastrectomia totale/subtotale – gastrite atrofica • Malassorbimento intestinale: – – diverticolosi del tenue parassitosi intestinale sprue tropicale ileite, fistole ileo-coliche, resezione ileale (M. di Crohn)

CAUSE DI ANEMIA MEGALOBLASTICA DEFICIT DI ACIDO FOLICO • Insufficiente apporto : ipoalimentazione, diete, alcolismo • Malassorbimento intestinale: – resezione digiunale – enteropatia da glutine – sprue tropicale – dermatite erpetiforme – linfomi intestinali • Aumentato consumo: – – gravidanza, allattamento, nati prematuri Neoplasie aumentato turnover midollare (iperplasia dell’ eritrone) malattie infiammatorie croniche • Perdita eccessiva: – Dialisi

ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 CLASSIFICAZIONE ETIOPATOGENETICA • PERNICIOSA – Predisposizione genetica – Autoimmune (Ab anti FI mucosa gastrica) • PERNICIOSIFORMI – Acquisite – Non autoimmuni QUADRI CLINICO-LABORATORISTICI SIMILI

ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 E FOLATI QUADRI CLINICI-LABORATORISTICI • Legati al difetto di sintesi del DNA: manifestazioni cliniche a carico dei tessuti in rapida proliferazione (midollo osseo, tubo digerente) • Il deficit di vitamina B 12 comporta anche sintomi neurologici

ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 E FOLATI QUADRI CLINICI • Manifestazioni gastroenteriche: glossiteipo/atrofia della lingua, aftosi, cheilite angolare, diarrea, malassorbimento • Manifestazioni neurologiche: neuropatia demielinizzante di vario grado, per lo più agli arti inferiori • Sintomi da anemia
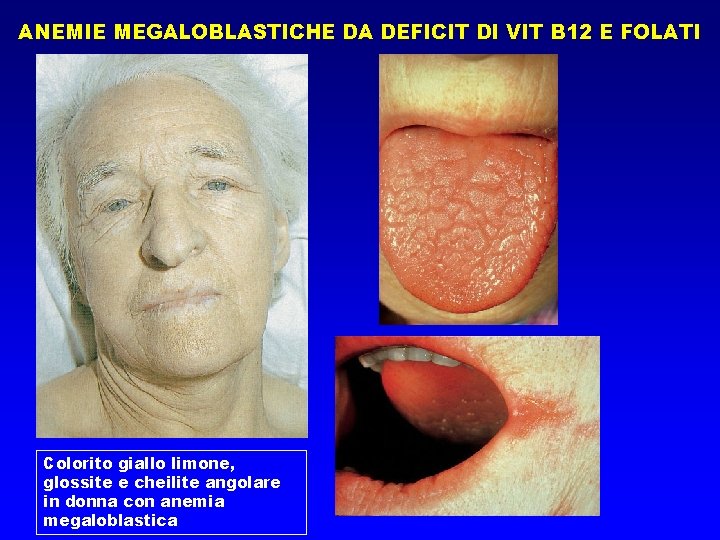
ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 E FOLATI Colorito giallo limone, glossite e cheilite angolare in donna con anemia megaloblastica
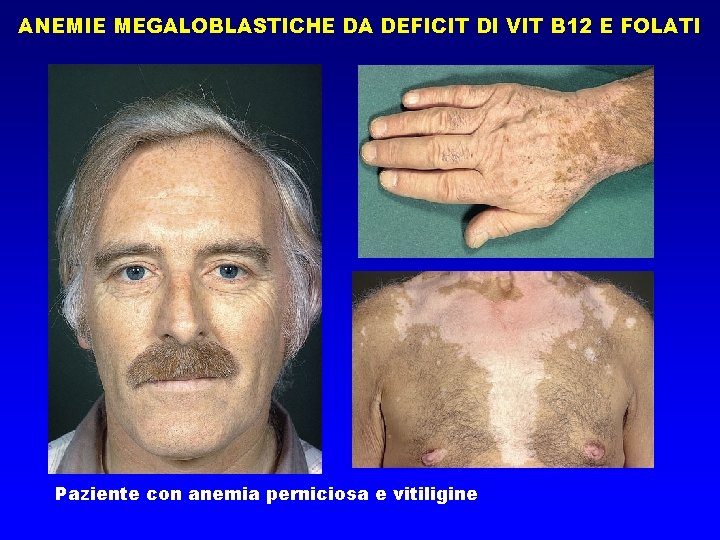
ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 E FOLATI Paziente con anemia perniciosa e vitiligine

ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 E FOLATI LABORATORIO: CARATTERIZZAZIONE DELL’ANEMIA • Anemia macrocitica • Riduzione reticolociti • All’osservazione al microscopio due segni patognomonici: – Macrovalocitosi (con anisopoichilocitosi) – Ipersegmentazione dei granulociti neutrofili • Mielobiopsia: iperplasia dell’eritropoiesi con megaloblastosi e predominanza degli eritroblasti basofili e policromatofili. MKC pseudo-iperdiploidi (ipersegmentati)
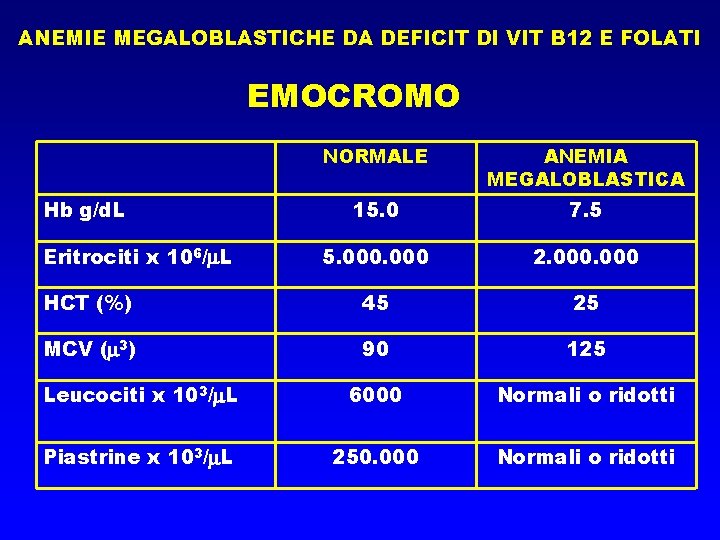
ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 E FOLATI EMOCROMO NORMALE ANEMIA MEGALOBLASTICA 15. 0 7. 5 5. 000 2. 000 HCT (%) 45 25 MCV ( 3) 90 125 Leucociti x 103/ L 6000 Normali o ridotti Piastrine x 103/ L 250. 000 Normali o ridotti Hb g/d. L Eritrociti x 106/ L

ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 E FOLATI LABORATORIO: altri parametri alterati • Possibile leucopenia e piastrinopenia • Iperbilirubinemia indiretta (bilirubina non coniugata) e aumento di LDH, espressione di aumentata eritroblastolisi endomidollare

ANEMIE MEGALOBLASTICHE DA DEFICIT DI VIT B 12 E FOLATI DIAGNOSI • Dosaggio Vit. B 12 e Folati. Carenza se: – Vit. B 12 < 100 ng/m. L – Ac. Folico < 4 µg/m. L • Sintomi e segni di laboratorio • Ricerca delle cause: – Autoanticorpi anti FI e cellule parietali gastriche – Esofagogastroduodenoscopia

Anemie megaloblastiche • Esempio meglio studiato di eritropoiesi inefficace • Eritropoietina fortemente stimolata: eritropoiesi aumentata 3 volte, produzione eritrociti inferiore alla norma • Marcata ipertrofia midollo osseo che si espande in forma funzionale alle diafisi delle ossa lunghe • Causa anemia: Maturazione abnorme e distruzione nel midollo dei precursori
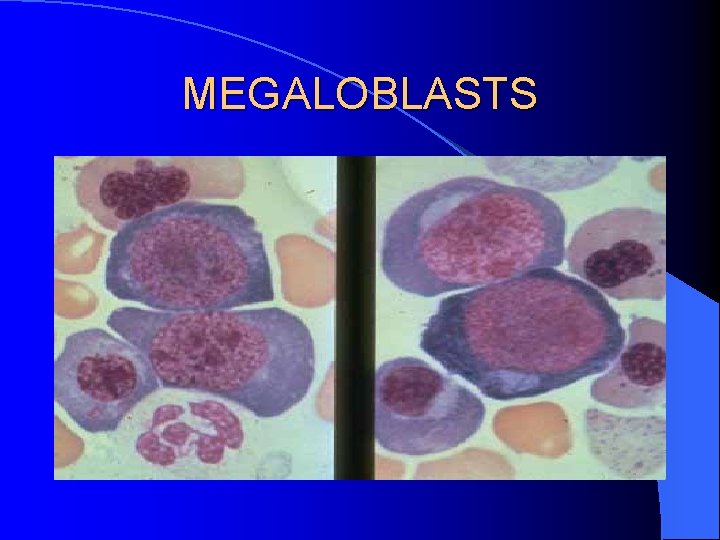
MEGALOBLASTS

Acido folico • Normal individuals have 5 -20 mg in various body stores • deficiency will occur within months IF dietary intake or intestinal absorption is curtailed
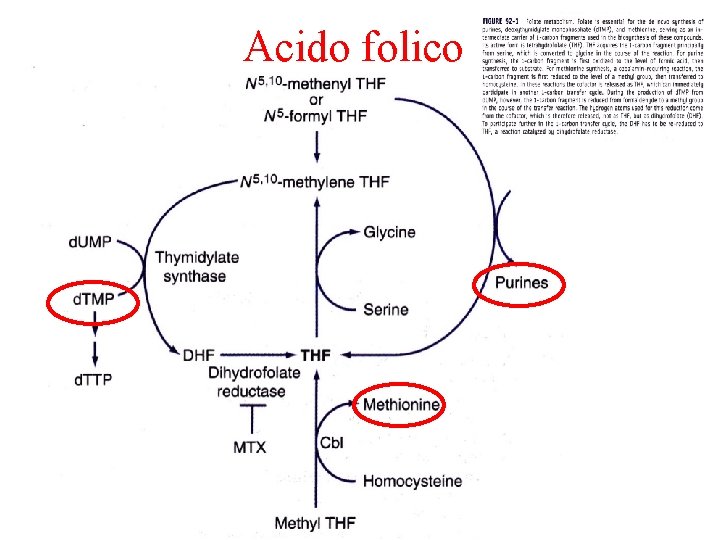
Acido folico

BIOCHEMICAL FEATURES Vitamin B 12 rich foods include organ meats as well as fortified breakfast cereals and dairy products § Normally 2 mg is stored in liver and another 2 mg elsewhere. § Minimum daily requirement. Sono richiesti circa 3 -5 ug di § vitamina B 12 al giorno. Poichè solo il 70% circa viene assorbito, la quantità di vitamina B 12 presente nella dieta giornaliera deve essere pari a 5 -7 ug. § The liver stores up to a 6 -year supply of Vitamin B 12.

BIOCHEMICAL FEATURES § § § Vitamin B 12 in foods is usually bound to protein in the methyl or 5 -deoxyadenosyl forms B 12 must first be removed from the protein by acid hydrolysis in stomach, or by trypsin digestion in intestine B 12 then combines with intrinsic factor, secreted by stomach, which carries it to the ileum for absorption Tc. II is the acceptor for newly adsorbed B 12 Most circulating B 12 is bound to Tc. I

BIOCHEMICAL FEATURES l l § § Vitamin B 12 is an essential cofactor for two enzymes: methionine synthase and methylmalonyl-Co. A synthase When methionine synthase reaction is impaired (B 12 deficiency) ---> folate metabolism is deranged The B 12 dependent methionine synthesis reaction appears to be the only major pathway by which N 5 -methyl THF can return to the THF pool This leads to a build up of N 5 methyl. THF and a deficiency of THF derivatives for purine and d. TMP biosynthesis All of the folate is “trapped” as the N 5 methyl. THF Megaloblastic anemia is thought to reflect this defect

Biochemistry of Neurological Symptoms I disturbi neurologici da deficienza da vitamina B 12 sono dovuti ad accumulo di propionil Co. A. § Per la sintesi degli acidi grassi, anzichè essere impiegato il succinil Co. A (donatore di 2 atomi di C), viene impiegato il propionil Co. A (donatore di 3 atomi di C). § L'utilizzo di questi acidi grassi nelle membrane delle fibre nervose (mielina), ne comporta la destabilizzazione (demielinizzazione). §

MEGALOBLASTIC ANEMIA • • LDH elevated (90%) Serum Fe normal or elevated Serum B 12 or folate low Marrow classic megaloblastic changes

COBALAMIN DEFICIENCY Manifestations • Both brain and spinal cord • Brain: – Dementia – Psychological disturbances – degenerazione a chiazza sostanza bianca cervello (pazzia megaloblastica, alterazioni gusto e olfatto, difetti vista, atassia, paraplegia • Spinal cord: – Demyelinating disease – lesioni degenerative del midollo spinale • Colore pelle giallo limone (aumento bilirubina non coniugata) + splenomegalia (1/3) • Neurologic disease stabilized with treatment, but usually not reversed • Treatment with folate does nothing for neurologic disease

Pathophysiologic Mechanism l Majority of Vit B 12 deficiency due to inadequate absorption of vitamin – Intrinsic factor antibody assay – Gastric parietal cell antibody assay – Schilling Test
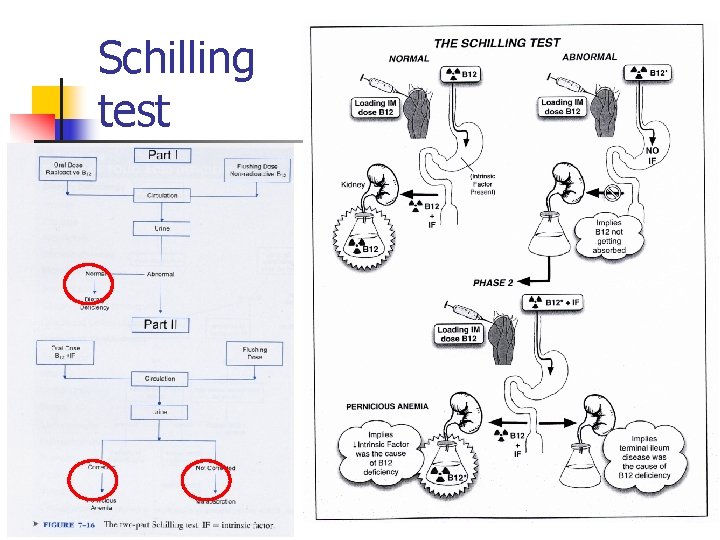
Schilling test

Mancanza di fattore intrinseco (prodotto nell’area gastrica) • Congenita (autosomico recessivo) • Acquisita – Gastrectomie – Anemia perniciosa addisoniana (+++ comune) • atrofia mucosa gastrica • fattori genetici (Scandinavia, gruppo A) + immunitari (autoanticorpi contro componenti citoplasmatici delle cellule parietali, 90%, anti fattore intrinseco nel siero, saliva e succo gastrico, 57%: prevengono legame con vitamina oppure assorbimento attraverso ileo) • Assenza di produzione di acido cloridrico e pepsina

cause di malassorbimento

- Slides: 84