FISIOLOGA RENAL Concentracin de la orina Equilibrio AcidoBsico

FISIOLOGÍA RENAL (Concentración de la orina, Equilibrio Acido-Básico) ycx Dpto. de Ciencias Biológicas y Fisiológicas Laboratorio de Transporte de Oxígeno

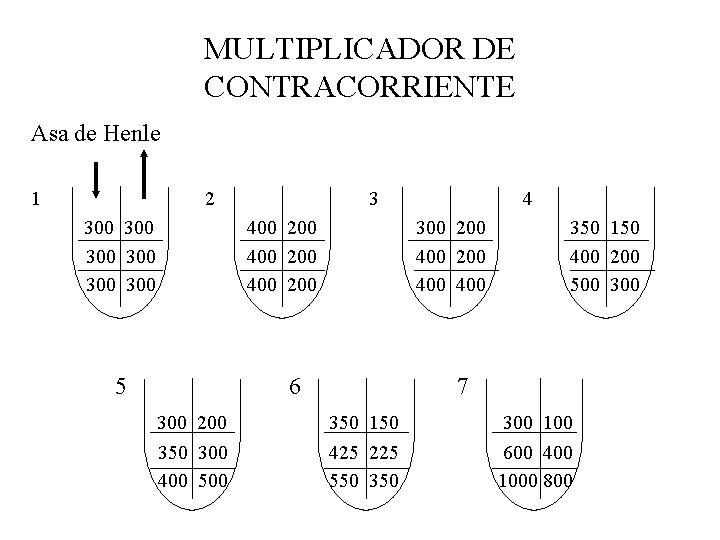
MULTIPLICADOR DE CONTRACORRIENTE Asa de Henle 1 2 300 300 300 3 400 200 5 300 200 400 400 6 300 200 350 300 400 500 4 350 150 400 200 500 300 7 350 150 425 225 550 300 100 600 400 1000 800

MULTIPLICADOR DE CONTRACORRIENTE Ø Las bombas en la porción ascendente gruesa mueven Na+ y Cl - activamente hacia el intersticio, aumentan su osmolaridad hasta 400 m. Osm/Kg y esto se equilibra con el líquido isotónico en la rama ascendente. Ø No obstante, continua fluyendo líquido isotónico hacia el interior de esta última y el líquido hipotónico sale de la rama ascendente gruesa. Ø La operación continua de las bombas hace que el líquido que abandona la rama sea aún más hipotónico, mientras que se acumula hipertonicidad en el ápice del asa

LA ÚREA Ø Se concentra en la parte superior del tubo colector (médula externa), impermeable a la urea. Ø Se reabsorbe en la parte inferior del tubo colector (médula interna). (Estos cambios son controlados por ADH) Ø Se recicla en la médula interna donde se añade al gradiente osmótico.
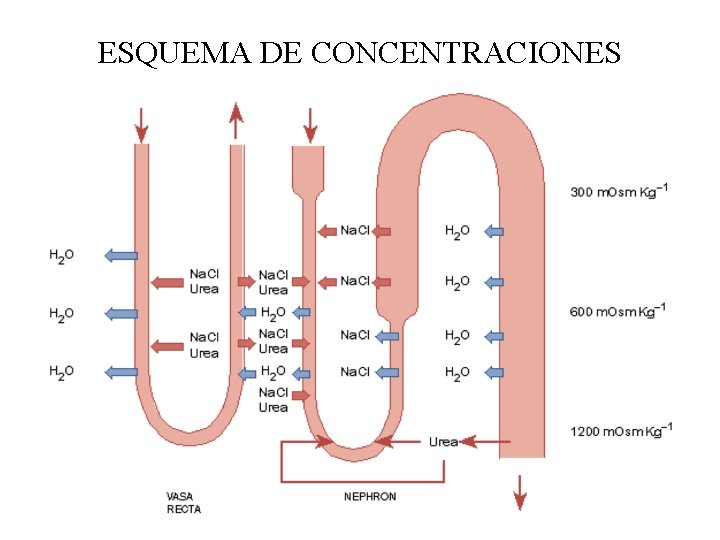
ESQUEMA DE CONCENTRACIONES


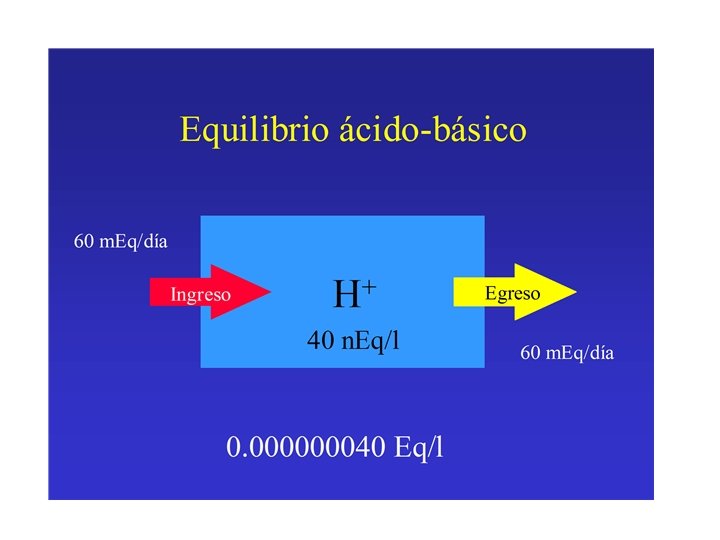




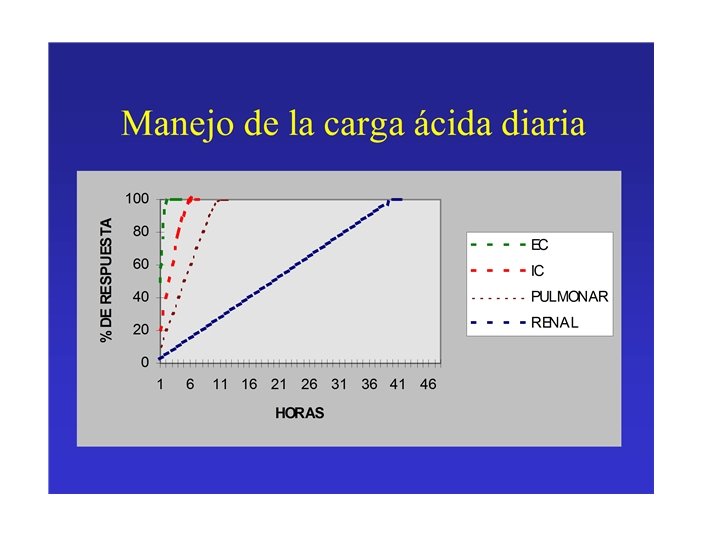

ECUACIÓN DE HENDERSON-HASSELBACH Ø Para hallar p. H: 1. - K H 2 CO 3 = [H+]. [HCO 3 -] [H 2 CO 3] H 2 CO 3 CO 2 2. - K H 2 CO 3 = [H+]. [HCO 3 -] [CO 2] p. H = - log H+ 3. - log K = log [H+] + log [HCO 3 -] [CO 2] - log K = - log [H+] + log [HCO 3 -] [CO 2] 4. - p. H = 6. 1 + log 24 nmol/L 0. 03 x 40 mm. Hg p. H = 7. 4

ECUACIÓN DE HENDERSON-HASSELBACH Ø Para hallar PCO 2: 1. - p. H = p. K + log [HCO 3 -] [H 2 CO 3] 2. - [H+] = K´. [H 2 CO 3] [HCO 3 -] K´. PCO 2 [HCO 3 -] 3. - K´ para CO 2 = 8 x 10 -7 mmol/L HCO 34. - K´ = 800 nmol/L x 0. 03 mmol/L. mm. Hg = 24
![ECUACIÓN DE HENDERSON-HASSELBACH 5. - [H+] = 24 x 40 = 40 nmol/L 24 ECUACIÓN DE HENDERSON-HASSELBACH 5. - [H+] = 24 x 40 = 40 nmol/L 24](http://slidetodoc.com/presentation_image_h/7a6bc158fa262d0322f688b6938c9c46/image-18.jpg)
ECUACIÓN DE HENDERSON-HASSELBACH 5. - [H+] = 24 x 40 = 40 nmol/L 24 6. - [HCO 3 -] = 24 x PCO 2 = 24 x 40 = 24 mmol/L [H+] 40 7. - PCO 2 = [H+]. [HCO 3 -] = 40 x 24 = 40 mm. Hg 24 24

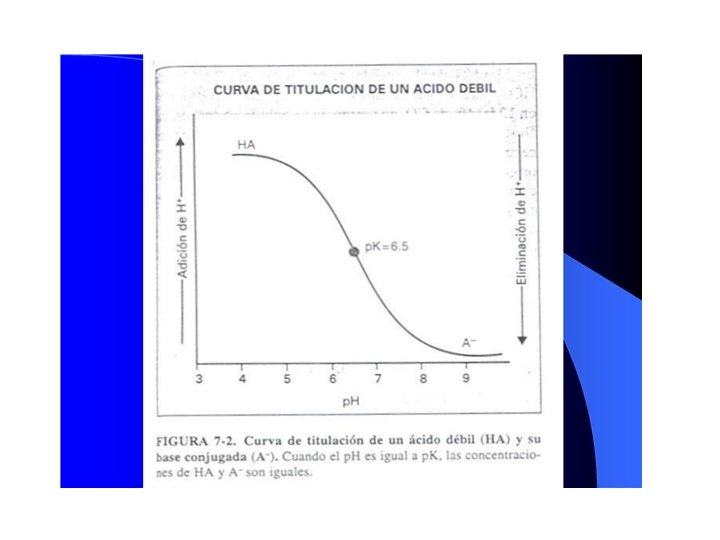
Amortiguación Principios de amortiguación - Amortiguador es una mezcla de un ácido débil con su base conjugada (o viceversa). - Una solución amortiguada resiste cambios de p. H. - Los líquidos del cuerpo contienen gran variedad de amortiguadores que representan una primera defensa importante contra los cambios de p. H.

Amortiguación Ecuación de Henderson-Hasselbalch - Se emplea para calcular el p. H de una solución amortiguada. p. H = p. K + log [A-] / [HA] Donde: [A-] = forma base del amortiguador (meq/L) [HA] = forma ácida del amortiguador (meq/L)

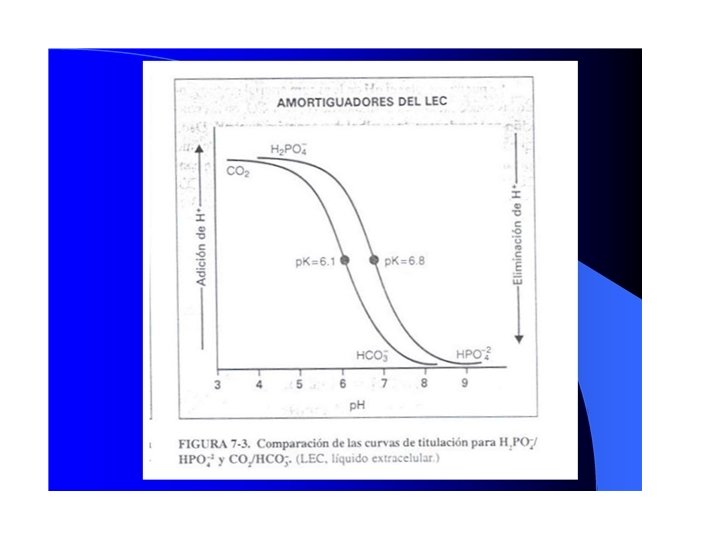
Amortiguadores del LEC Amortiguador HCO 3/CO 2 • Se utiliza como la primera línea de defensa cuando el cuerpo pierde o gana H+. • Características: a) la concentración de la forma HCO 3 es alta (24 meq/L). b) el p. K es 6. 1, bastante próximo al p. H del LEC. c) el CO 2 es volátil y se puede espirar por los pulmones.

Amortiguadores del LIC • Los fosfatos orgánicos del LIC incluyen ATP, ADP, AMP, glucosa-1 -fosfato y 2, 3 difosfoglicerato (p. K = 6. 0 a 7. 5). • Las proteínas intracelulares sirven como amortiguadores por su abundante contenido de grupos –COOH/COO- o –NH 3/NH 2. • El amortiguador intracelular más significativo es la hemglobina (p. K de la oxihemoglobina = 6. 7 y de la desoxihemoglobina 7. 9).

REGULACIÓN DEL EQUILIBRIO ÁCIDO BÁSICO SI NO HAY COMPENSACIÓN Ø Se añaden 12 m. M/L de H+ al LEC. PCO 2 = 40 mm. Hg. HCO 3= 24 m. M/L. H 2 CO 3 = 1. 2 m. M/L. Ø 12 m. M H+ + 12 m. M HCO 3 - 12 m. M H 2 CO 3 Ø 24 m. M HCO 3 - - 12 m. M = 12 m. M HCO 3Ø 1. 2 m. M H 2 CO 3 + 12 m. M = 13. 2 m. M H 2 CO 3 Ø p. H = 6. 1 + log 12 m. M HCO 3 - p. H = 6. 06 MORTAL!!! 13. 2 m. M H 2 CO 3

REGULACIÓN DEL EQUILIBRIO ÁCIDO BÁSICO CON COMPENSACIÓN RESPIRATORIA HIPERVENTILACIÓN Ø PCO 2 baja de 40 mm. Hg a 24 mm. Hg. Ø H 2 CO 3 CO 2 y CO 2 = PCO 2 x CO 2 = 24 x 0. 03 Ø p. H = 6. 1 + log 12 m. M HCO 30. 72 p. H = 7. 32 OK!!!


CAMBIOS ACIDO-BASICOS ACIDOSIS RESPIRAT. - p. H < 7. 4 - PCO 2 arterial - [H 2 CO 3] - HCO 3 - + H+ y p. H - secreción H+ - reabsorción de HCO 3 - [HCO 3 -] - p. H (Bronquios, asma, neumonía) ACIDOSIS METABÓLICA - p. H < 7. 4 - [HCO 3 -] - H+ - A- H+ + C+HCO 3 A-C+ +H 2 CO 3 = CO 2+H 2 O - [H 2 CO 3] - [CO 2] - p. H (Enfermedades renales, diarrea)

CAMBIOS ACIDOS-BASICOS ALCALOSIS RESPIRAT - p. H > 7. 4 - PCO 2 H 2 CO 3 - HCO 3 - + H+ y p. H - la secreción de H+ - reabsorción de HCO 3 - excreción de HCO 3 - [HCO 3 -] - p. H (Hiperventilación, altura, histeria) ALCALOSIS METABÓLICA - p. H > 7. 4 - [HCO 3 -] (por de H+ ) - la ventilación - H 2 CO 3 - [CO ] 2 - p. H (Vómitos, pérdida de HCl, TFG)

![BRECHA ANIÓNICA BA = [Na+] - ([Cl-] + [HCO 3 -]) Valores normales: 8 BRECHA ANIÓNICA BA = [Na+] - ([Cl-] + [HCO 3 -]) Valores normales: 8](http://slidetodoc.com/presentation_image_h/7a6bc158fa262d0322f688b6938c9c46/image-31.jpg)
BRECHA ANIÓNICA BA = [Na+] - ([Cl-] + [HCO 3 -]) Valores normales: 8 - 16 meq / L La [Na+] > ([Cl-] + [HCO 3 -]), la diferencia es la BA (proteínas plasmáticas, fosfatos, sulfatos) Cuando el HCO 3 - disminuye, puede ser reemplazado por otros aniones para mantener la electronegatividad y BA . La BA también aumenta por el aumento del catabolismo de grasas.
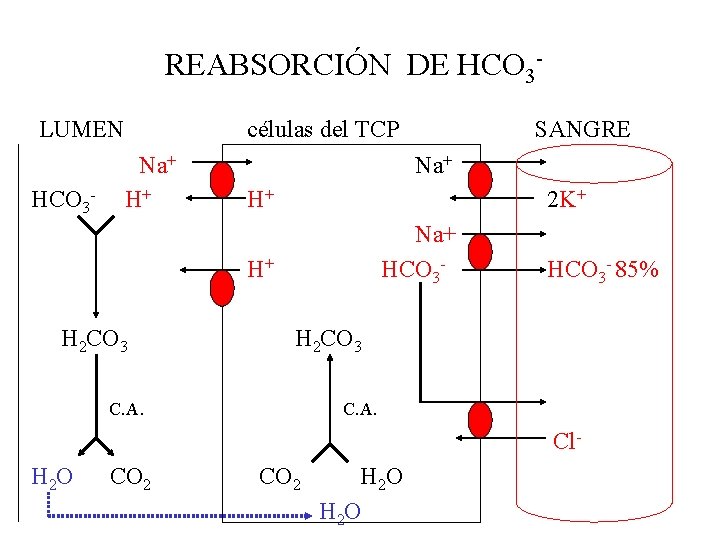
REABSORCIÓN DE HCO 3 LUMEN HCO 3 - células del TCP Na+ H+ 2 K+ Na+ HCO 3 - H+ H 2 CO 3 SANGRE HCO 3 - 85% H 2 CO 3 C. A. Cl. H 2 O CO 2 H 2 O
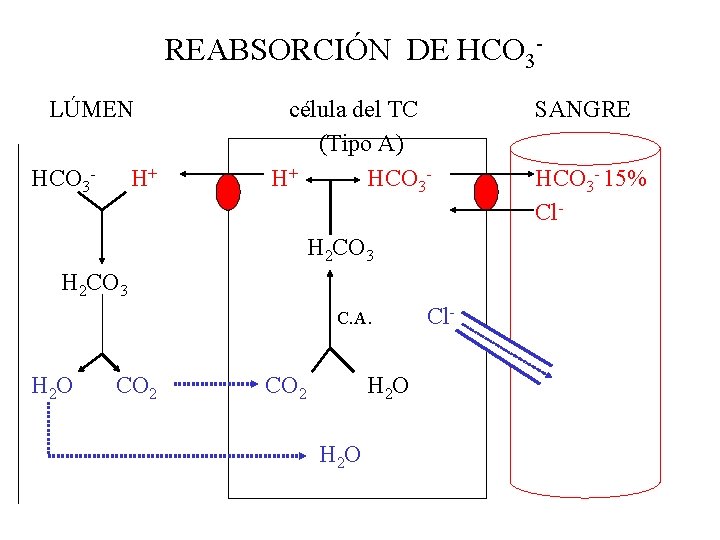
REABSORCIÓN DE HCO 3 LÚMEN HCO 3 - H+ célula del TC (Tipo A) H+ HCO 3 H 2 CO 3 C. A. H 2 O CO 2 H 2 O Cl- SANGRE HCO 3 - 15% Cl-

MECANISMOS DE ELIMINACIÓN DE H+ 1) Como protones libres: A la máxima concentración urinaria sólo se eliminan 0. 1 meq H+ /día. 2) Unidos al tampón fosfato: HPO 4 -2 / H 2 PO 4 A p. H = 7. 4, 10 - 30 meq H+ / día 7. 4 = 6. 8 + log [Na 2 HPO 4] / [Na. H 2 PO 4] (se excreta en la orina) 3) Unidos al tampón NH 3/NH 4+ 20 - 50 meq / día El NH 3 se sintetiza a partir de la desaminación de la glutamina. NH 3 + H+ ==> NH 4+ (se elimina como sal)
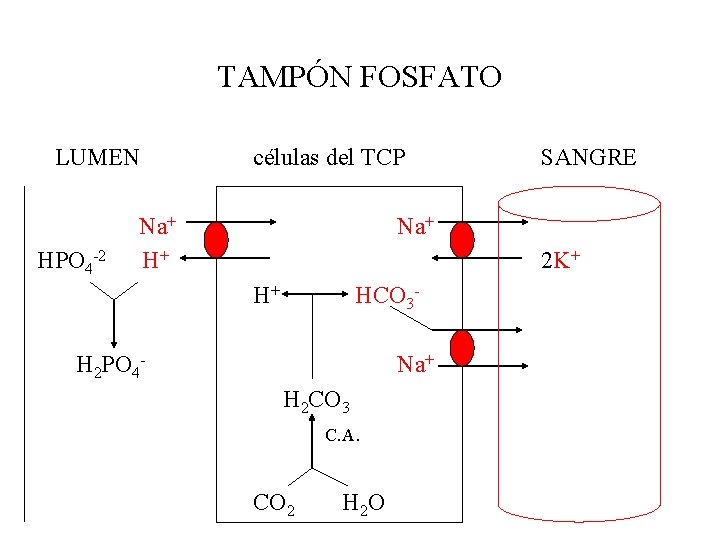
TAMPÓN FOSFATO LUMEN HPO 4 -2 células del TCP Na+ H+ SANGRE Na+ 2 K+ H+ HCO 3 - H 2 PO 4 - Na+ H 2 CO 3 C. A. CO 2 H 2 O
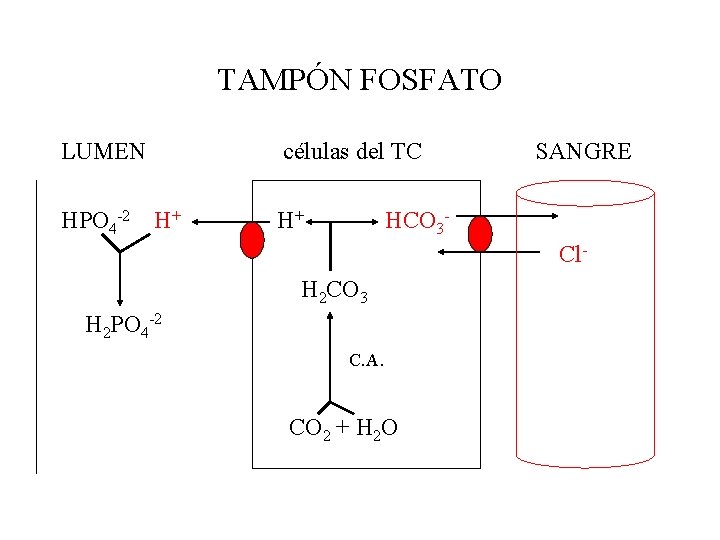
TAMPÓN FOSFATO LUMEN HPO 4 -2 células del TC H+ H+ SANGRE HCO 3 Cl- H 2 CO 3 H 2 PO 4 -2 C. A. CO 2 + H 2 O
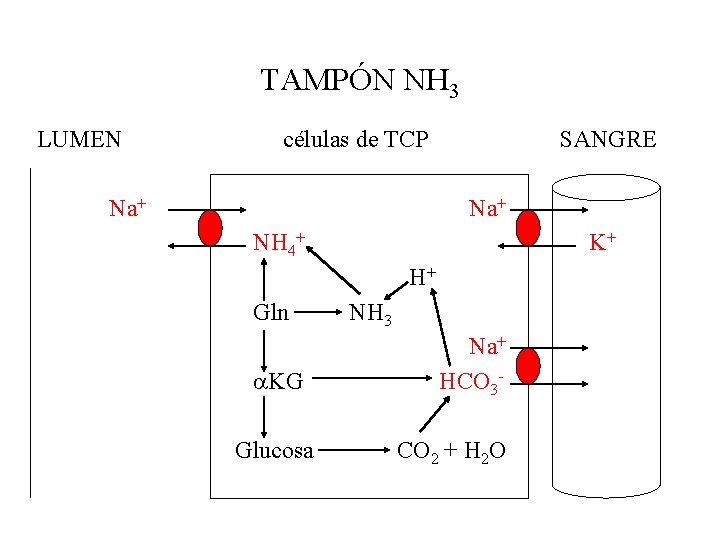
TAMPÓN NH 3 LUMEN células de TCP Na+ SANGRE Na+ NH 4+ K+ H+ Gln KG Glucosa NH 3 Na+ HCO 3 CO 2 + H 2 O
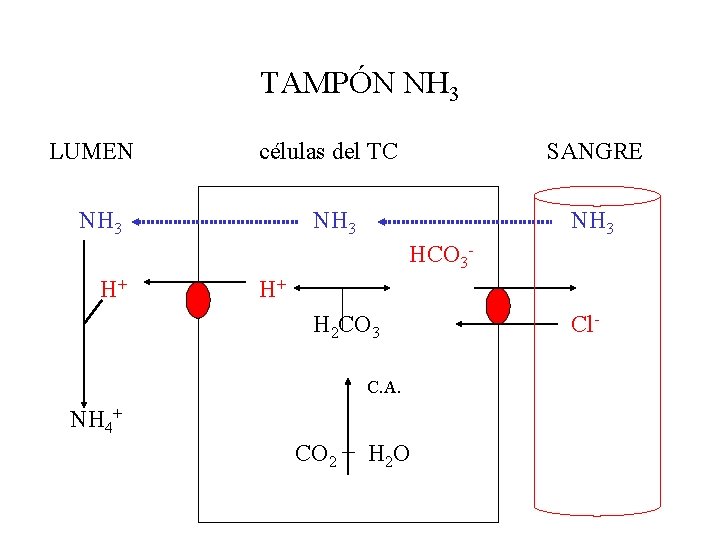
TAMPÓN NH 3 LUMEN células del TC SANGRE NH 3 HCO 3 H+ H+ H 2 CO 3 C. A. NH 4+ CO 2 + H 2 O Cl-
- Slides: 38