Fe 3 Combinazione di semireazioni di riduzione E

Fe 3+ Combinazione di semireazioni di riduzione E =? (aq) + 3 e Fe(s) DG 0 = -z. FDE 0 0 - E 0 = -0, 44 V Fe 2+(aq) + 2 e- Fe(s) Fe 3+(aq) + 1 e- Fe 2+ (aq) E 0 = 0, 771 V Fe 3+(aq) + 3 e- Fe(s) E 0 non è la somma dei due E 0 DG 0 = - 2 x F x -0, 44 V Fe 2+(aq) + 2 e- Fe(s) Fe 3+(aq) + 1 e- Fe 2+ (aq) DG 0 = -1 x F x 0, 771 V Fe 3+(aq) + 3 e- Fe(s) DG 0 = 0, 880 x F - 0, 771 x F =0, 109 x F DG 0 = -z. FE 0(Fe 3+/Fe) 0, 109 F = -3 x F x E 0(Fe 3+/Fe) da cui E 0(Fe 3+/Fe) = -0, 0363 V

Reazioni di dismutazione: i potenziali redox ci dicono se una specie puo’ dismutare 3 Cr 2+ 2 Cr 3+ + Cr 2 Cu+ Cu 2+ + Cu La reazione di dismutazione è favorita quando la somma algebrica dei DG 0 delle semireazioni di riduzione e ossidazione è minore di zero DG 0 = -z. FDE 0 DG 0 (Cr 3+/Cr 2+) = -(-0. 41)F = 0. 42 x F DG 0 (Cr 2+/Cr) = -2(-0. 91)F = 1. 82 x F DG 0 > 0 DG 0 (Cu 2+/Cu+) = -(0. 16)F = -0. 16 x F DG 0 (Cr+/Cu) = -(0. 52)F = -0. 52 x F DG 0 < 0
![Celle a concentrazione [Cu 2+] = 1. 0 x 10 -1 [Cu 2+] = Celle a concentrazione [Cu 2+] = 1. 0 x 10 -1 [Cu 2+] =](http://slidetodoc.com/presentation_image_h/b93d57abeb5309d92d73d00a83010dba/image-3.jpg)
Celle a concentrazione [Cu 2+] = 1. 0 x 10 -1 [Cu 2+] = 1. 0 x 10 -2 Elettrodi di rame Nella semicella meno concentrata (anodo) avviene l’ossidazione: Cu Cu 2+ + 2 e. Nella semicella più concentrata (catodo) avviene la riduzione: Cu 2+ + 2 e. La f. e. m. DE = DE 0 In una pila a concentrazione la variazione spontanea si verifica sempre nella direzione in cui la soluzione piu’ concentrata si diluisce ed quella piu’ diluita aumenta di concentrazione. Cu – 0. 059/2 log 1 x 10 -2 1 x 10 -1 = 0 + 0. 059/2 = 0. 030 V La pila eroga correte fino a che la conc. di Cu 2+ è uguale nelle due semicelle

Celle a concentrazione Pt|H 2(1 bar)|H+(x M)|| H+(1 M)|H 2(1 bar)|Pt In una pila a concentrazione la variazione spontanea si verifica sempre nella direzione in cui la soluzione piu’ concentrata si diluisce ed quella piu’ diluita aumenta di concentrazione. In questa pila le reazioni in gioco sono: Catodo (riduzione): 2 H+ (1 M) + 2 e- H 2(1 bar) Anodo (ossidazione): H 2(1 bar) 2 H+ (x M) + 2 e. Totale reazione: 2 H+ (1 M) 2 H+ (x M)

Celle a concentrazione Pt|H 2(1 bar)|H+(x M)|| H+(1 M)|H 2(1 bar)|Pt L’equazione di Nernst per la reazione della pila è: DE =DE 0 - 0. 0591/2 log x 2/12 Dato che DE 0 = E 0(H+/H 2) - E 0(H+/H 2) = 0, si semplifica in: DE = 0 - (0. 0591/2) 2 log x/1 DE = - 0. 0591 log x Dato che x è [H+] nella soluzione incognita: DE = - 0. 0591 log [H+] e quindi DE = 0. 0591 * p. H Posso quindi misurare il p. H di una soluzione misurando la f. e. m. di una pila a concentrazione fatta da due elettrodi ad idrogeno.

Il p. H metro La cella globale è: Ag(s)|Ag. Cl(s)|Cl-(1 M), H+ (1. 0 M)|membrana di vetro|H+ (incognita)||Cl-(1. 0 M)|Ag. Cl(s)|Ag(s) Elettrodo a vetro è fatto da un bulbo di vetro sottile che contiene un elettrodo argento-argento cloruro immerso in una soluzione di HCl 1 M. Quando metto in contatto il bulbo con una soluzione a concentrazione ignota di H+, si sviluppa un potenziale a causa della differenza di concentrazione attraverso la membrana. Questa differenza di potenziale la misuro con un voltmetro rispetto ad un elettrodo di riferimento che puo’ essere un elettrodo a calomelano oppure a argento-argento cloruro. La f. e. m. DE = DE 0 + 0. 0591 p. H Nel caso di elettrodo di riferimento Ag/Ag. Cl ho DE 0 = 0 e quindi DE = 0. 0591 * p. H

Elettrolisi Pila con f. e. m. 0. 46 V alle condizioni standard: Cu + 2 Ag+ Cu 2+ + 2 Ag La pila eroga corrente fino a che si scarica. Se poi applico una differenza di potenziale maggiore di 0. 46 (per esempio usando un’altra pila che eroghi corrente con f. e. m. > 0. 46) la reazione procede nel senso opposto: Cu 2+ + 2 Ag Cu + 2 Ag+

Elettrolisi Pila galvanica Utilizzo una reazione spontanea per produrre energia elettrica => celle elettrochimiche o voltaiche Elettrolisi Utilizzo energia elettrica per fare avvenire una reazione NON spontanea => cella elettrolitica Se applico a una pila una differenza di potenziale pari alla sua f. e. m non avviene nessuna reazione, ma se applico una differenza di potenziale maggiore della sua f. e. m. avviene la reazione nel senso opposto, quindi la reazione non spontanea.

Elettrolisi di soluzioni acquose Elettrolisi di Sali fusi

Elettrolisi di Sali fusi Si usa per ottenere i metalli alcalini allo stato elementare Es. Na. Cl fuso Catodo (-) di ferro avviene la riduzione: Na+ + e. Na Anodo (+) di grafite avviene l’ossidazione: Cl 1/2 Cl 2 + e-

Elettrolisi di Sali fusi Si usa per ottenere F 2 Es. KHF 2 ·HF fuso Catodo (-) di nichel avviene la riduzione: HF + H+ + 2 e. H 2 + FK+ + e - K Anodo (+) di nichel avviene l’ossidazione: HF 2 F 2 + 2 e- + H+ Al catodo si libera l’idrogeno e non il potassio perché l’idrogeno necessita di meno lavoro elettrico
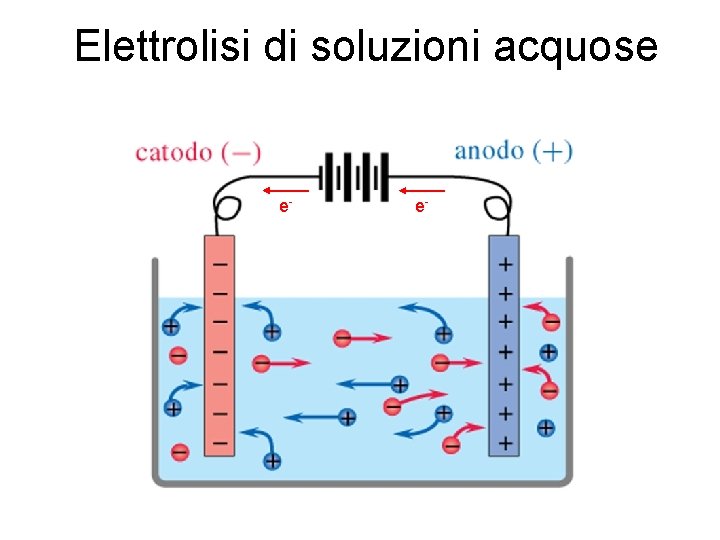
Elettrolisi di soluzioni acquose e- e-
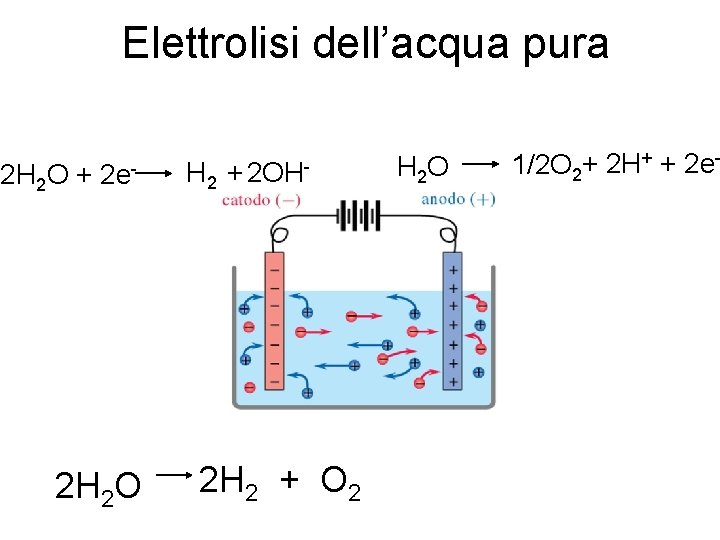
Elettrolisi dell’acqua pura 2 H 2 O + 2 e- 2 H 2 O H 2 + 2 OH- 2 H 2 + O 2 H 2 O 1/2 O 2+ 2 H+ + 2 e-

Elettrolisi dell’acqua pura 2 H 2 O 2 H 2 + O 2 E(O 2/H 2 O, p. H 7) = E(H+/H 2, p. H 7) = E 0 1 (O 2/H 2 O) – 0. 059 log =0. 82 V [H+] (H+/H 1 = -0. 41 V 2) – 0. 059 log + [H ] DE = E 0 (O 2/H 2 O) – E 0 (H+/H 2) = 1. 23 E’ il potenziale minimo necessario da applicare per la decomposizione dell’acqua. E’ indipendente dal p. H
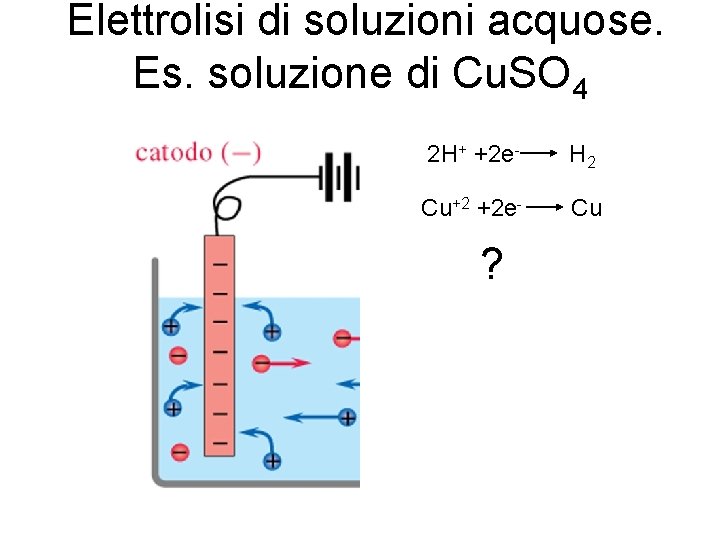
Elettrolisi di soluzioni acquose. Es. soluzione di Cu. SO 4 2 H+ +2 e- H 2 Cu+2 +2 e- Cu ?
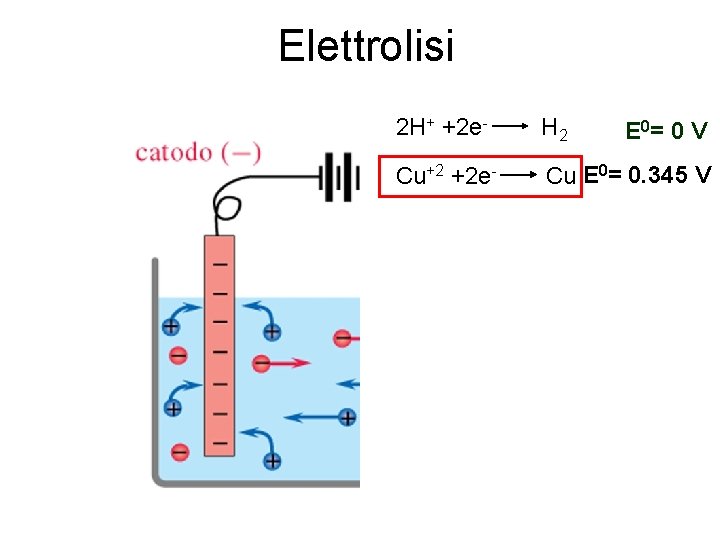
Elettrolisi 2 H+ +2 e- H 2 Cu+2 +2 e- Cu E 0= 0. 345 V E 0= 0 V
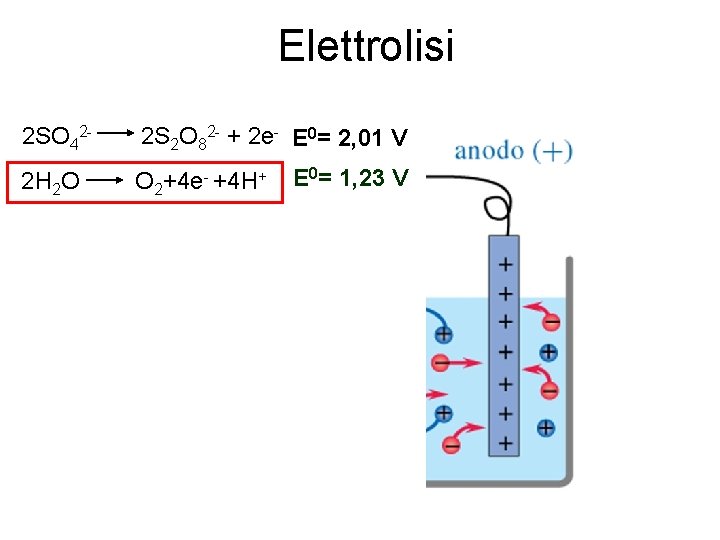
Elettrolisi 2 SO 42 - 2 S 2 O 82 - + 2 e- E 0= 2, 01 V 2 H 2 O O 2+4 e- +4 H+ E 0= 1, 23 V

Elettrolisi In generale: 1. All’anodo si ossida la specie che ha E 0 minore 2. Al catodo si riduce la specie che ha E 0 maggiore Perche’ si richiede meno lavoro elettrico

Quantità di prodotti di reazione ed quantità di elettricità Ag+ + e 2 H 2 O Ag catodo O 2+4 e- +4 H+ anodo Elettrolisi di Ag. NO 3 Per il passaggio di una carica elettrica pari a una mole di elettroni, al catodo si deposita una mole di Ag e all’anodo si sviluppa ¼ di mole di O 2 F= 96500 Coulomb = quantità di carica di 1 mole di elettroni Q = I x t Coulomb= Ampere x secondi I x t /(z x F) = moli delle specie ottenute in un processo di elettrolisi

Quantità di sostanza ed energia Quindi conoscendo I e t poso sapere quanta sostanza si sviluppa agli elettrodi. Es. Elettrolisi di Ag. NO 3 avviene per 40 minuti con una intensità di 0. 30 A (40 x 60 s) x 0. 30 A 96500 x 1 (40 x 60 s) x 0. 30 A 96500 x 4 = moli ottenute di Ag = moli ottenute di O 2
- Slides: 21