FATORES QUE AFETAM A SOLUBILIDADE DOS SAIS EFEITO

FATORES QUE AFETAM A SOLUBILIDADE DOS SAIS • EFEITO DO ÍON COMUM • EFEITO DA ADIÇÃO DE SAIS SOLÚVEIS E AUMENTO DA FORÇA IÔNICA • EFEITO DA TEMPERATURA • EFEITO DO SOLVENTE • EFEITO DO GRAU DE HIDRATAÇÃO • EFEITO DA RAZÃO ENTRE O CÁTION E NION • EFEITO DA FORMAÇÃO DE COMPLEXO NO MEIO AQUOSO • EFEITO DO p. H

• Efeito do íon comum • Ag. Cl (s) ----- Ag+ (aq) + Cl- (aq) • · íon comum: íon que também participa da constituição do precipitado (íons Ag+ e Cl-). • Ao adicionarmos um reagente que contém um íon comum com o precipitado, a solubilidade do precipitado diminui. Ex: Na. Cl 0, 01 mol. L-1. Ag. Cl (s) ---- Ag+ (aq) + Cl- (aq) início s equil. s 0, 01 + s • Qual a solubilidade do Ag. Cl em água pura? • Qual a solubilidade do Ag. Cl numa solução de Na. Cl 0, 01 mol/L?
![EQUAÇÃO DA FORÇA IÔNICA Kps Ag. Cl = a+Ag+ a-Cl. Onde a+Ag+ = [Ag+] EQUAÇÃO DA FORÇA IÔNICA Kps Ag. Cl = a+Ag+ a-Cl. Onde a+Ag+ = [Ag+]](http://slidetodoc.com/presentation_image_h/a7d67a39b9ef1fa0c6e17cb4053b3869/image-3.jpg)
EQUAÇÃO DA FORÇA IÔNICA Kps Ag. Cl = a+Ag+ a-Cl. Onde a+Ag+ = [Ag+] +Ag+ e a-Cl- = [Cl-] -Cl- EQUAÇÃO DOCOEFICIENTE DE ATIVIDADE

PRINCÍPIO DE LE CHATELIER Para uma reação endotérmica, K aumenta com aumento da temperatura, ao passo que, para uma reação exotérmica, K diminui com o aumento da temperatura. Reação endotérmica exotérmica atérmica T aumenta não varia K aumenta diminui não varia

A solubilidade de um sólido em um líquido: aumenta quando DHsol < 0 diminui quando DHsol > 0 A solubilidade aumenta com a temperatura se DHsol < 0 quando o sólido é dissolvido na água. Pontos de inflexão nas curvas de solubilidade indicam a formação de sais hidratados. A pressão não influi na solubilidade de sólidos em líquidos. R = 8, 31 J/K. mol

Equação empírica do efeito do solvente na solubilidade dos sais S 2 æ e 2 ö 3 =ç ÷ S 1 è e 1 ø
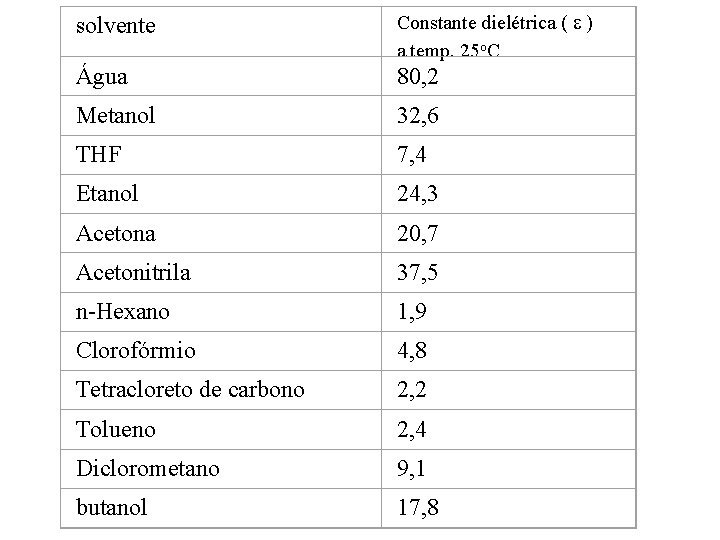
solvente Água Constante dielétrica ( ) a temp. 25 o. C 80, 2 Metanol 32, 6 THF 7, 4 Etanol 24, 3 Acetona 20, 7 Acetonitrila 37, 5 n-Hexano 1, 9 Clorofórmio 4, 8 Tetracloreto de carbono 2, 2 Tolueno 2, 4 Diclorometano 9, 1 butanol 17, 8
- Slides: 7