FARMACOVIGILANCIA Y FARMACOEPIDEMILOGIA KAREN YULIETH FIESCO SEPULVEDA ISABEL

FARMACOVIGILANCIA Y FARMACOEPIDEMILOGIA KAREN YULIETH FIESCO SEPULVEDA ISABEL DEL PILAR CARDOSO MORENO

FARMACOEPIDEMIOLOGIA

Definición • “La aplicación de los métodos epidemiológicos al estudio de los efectos, beneficiosos y adversos, y al uso de medicamentos en grupos de población. ”

Objetivo • Trata de explicar, controlar y predecir los efectos y usos del tratamiento farmacológico en un determinado tiempo, espacio y población.
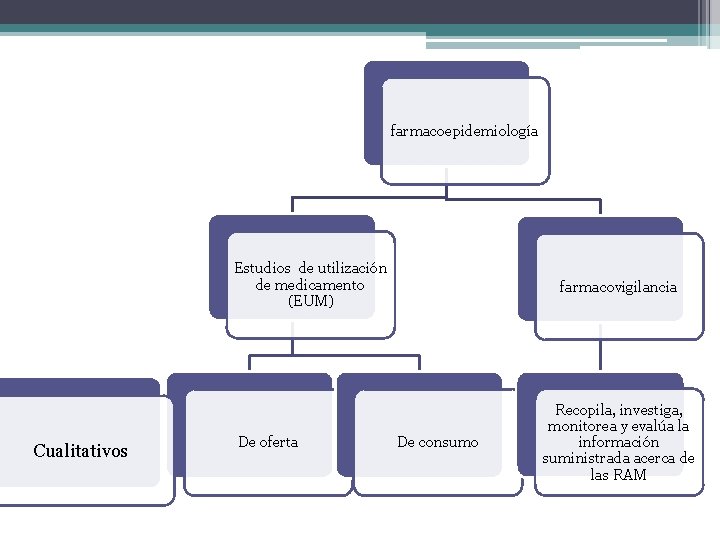
farmacoepidemiología Estudios de utilización de medicamento (EUM) Cualitativos De oferta farmacovigilancia De consumo Recopila, investiga, monitorea y evalúa la información suministrada acerca de las RAM

Estudios de la utilización de la medición • “aquellos que se ocupan de ‘la comercialización, distribución, prescripción y uso de los medicamentos en una sociedad, con acento especial sobre las consecuencias médicas, sociales y económicas resultantes. ”
PROCESO DE EVALUACIÓN 1. -La evaluación de los beneficios de los medicamentos, por ejemplo la evaluación cuantitativa y cualitativa de su eficacia. 2. - El estudio del riesgo de los medicamentos, tanto en estudios controlados como en condiciones normales 3. - La evaluación del impacto de los tratamientos en la historia natural de la enfermedad

CLASIFICACION CUALITATIVA DE LOS MEDICAMENTOS QUE SE DISPENSAN EN EL MERCADO De Valor Elevado De Valor Dudoso/Nulo • aquellos monofármacos que demostraron eficacia para el tratamiento, el diagnóstico o la prevención de enfermedades que afectan al ser humano • medicamentos que existen en el mercado pero que no han demostrado fehacientemente eficacia o utilidad terapéutica De Valor Relativo • medicamentos de Valor Elevado en combinación con otros de valor Dudoso/Nulo De Valor Inaceptable • aquellos de Valor Elevado en combinaciones que incrementan el riesgo en todos los casos
EUM • ESTUDIOS DE OFERTA üFuente de información: vademécum, guías, formularios farmacoterapéuticos. ESTUDIOS DE OFERTA Descripción cualitativa y cuantitativa de la oferta de los medicamentos Permiten comparación tiempo y espacio.
• ESTUDIOS DE CONSUMO üLas fuentes de información son las cifras de ventas del mercado obtenidas por empresas privadas, los datos suministrados por los bancos de datos de medicamentos. ESTUDIO DE CONSUMO Estudian tendencias comparadas de consumo Hay 2 tipos

• ESTUDIO DE CONSUMO v. Cuantitativos: se describen tendencias temporales de consumo de fármacos y permiten comparaciones entre países, regiones, centros institucionales, etc. Tiene 3 funciones: 1. Disponer de un indicador socio-sanitario. 2. Estimar la prevalencia de ciertas enfermedades. 3. Proporcionar datos que permitan estimar la exposición a un determinado fármaco.

v. Cualitativo: toma de base los estudios cuantitativos. Pueden ser de: § Prescripción: se analiza la relación indicación – prescripción. § Dispensación: estudia la calidad de dispensación, la información del paciente, entre otros. § Uso- administración: valora la calidad de uso de los medicamentos. § Orientados a problemas: analiza el uso de los fármacos de acuerdo con unos criterios estandar de uso correcto.

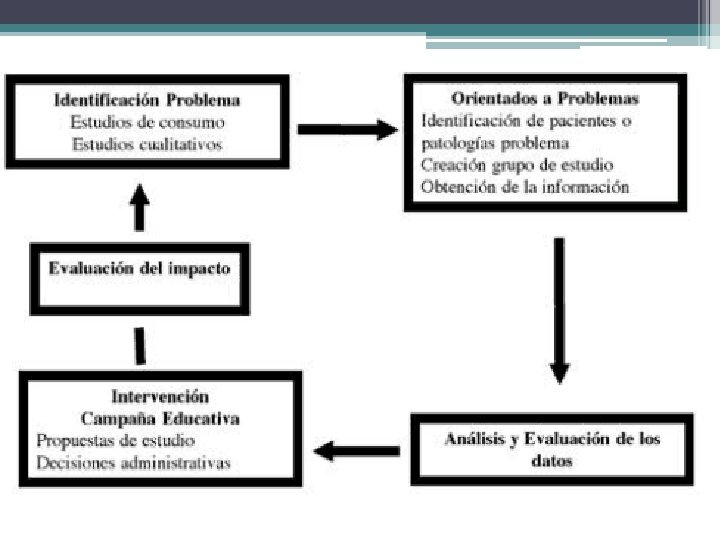
Etapas • Descripción de la utilización de medicamentos. • Análisis cualitativo de los datos obtenidos. • Identificación de áreas de intervención en función del análisis anterior. • Evaluación del impacto de las intervenciones sobre los problemas identificados.

FARMACOVIGILANCIA

Definición • La OMS define «farmacovigilancia» como la ciencia y las actividades relativas a la detección, evaluación, comprensión y prevención de los efectos adversos de los medicamentos o cualquier otro problema relacionado con ellos.

Objetivos principales • Detección temprana de las reacciones adversas e interacciones desconocidas hasta ese momento. • Detección de aumentos de la frecuencia de reacciones adversas (conocidas). • Identificación de factores de riesgo y de los posibles mecanismos subyacentes de las reacciones adversas. • Estimación de los aspectos cuantitativos de la relación beneficio/riesgo y difusión de la información necesaria para mejorar la regulación y prescripción de medicamentos.

Objetivos finales • El uso racional y seguro de los medicamentos. • La evaluación y comunicación de los riesgos y beneficios de los medicamentos a nivel institucional. • La educación y la información a los pacientes.

¿Cómo surge esta práctica? ‘ 30 EEUU Elixir de sulfanilamida Serie de Muertes ‘ 60 ALEMANIA TALIDOMINA Hipnótico y antiemético; Nauseas y vómitos dentro de los primeros meses de embarazo DIETILENGLICOL FDA TERATÓGENO POTENTE FOCOMELIA Varios países comenzaron un control mas estricto para la v Aprobación v. Comercialización v. Prescripción. v. Suministro de los medicamentos

BREVE HISTORIA DE LA FARMACOVIGILANCIA EN COLOMBIA • 1997. INVIMA • creación del Formato de Reporte de Eventos Adversos a Medicamentos (FORAM) • 2004, el programa fue reconocida como una iniciativa de carácter nacional por el centro de farmacovigilancia de la OMS. • Red Nacional de farmacovigilancia: 50 inst. • OPS y la U. Nacional de Colombia> encuentros de farmacovigilancia

Normatividad 2001 (ley 715): • vigilancia de medicamentos 2005 (decreto 2200): • programa de farmacovigilancia • proceso de farmacovigilancia 2006 (decreto 1011): • minimizar el riesgo de evento adverso • buscar seguridad de los usuarios frente a potenciales riesgos asociados a la prestación del servicio 2007 (resolucion 1403) • determina el Modelo de Gestión del Servicio Farmacéutico, se adopta el Manual de Condiciones Esenciales y Procedimientos

• REACCIÓN ADVERSA MEDICAMENTOSA • una respuesta a un fármaco que es nociva e involuntaria, y que ocurre a las dosis normalmente usadas en el hombre para profilaxis, diagnostico o terapia de alguna enfermedad, o para modificación de las funciones fisiológicas”

Evento adverso • Cualquier suceso médico desafortunado que puede presentarse durante el tratamiento con un medicamento, pero que no tiene necesariamente una relación causal con dicho tratamiento

efecto secundario • Cualquier efecto inesperado de un producto farmacéutico que ocurre a dosis normalmente usadas en el hombre y que esta relacionado con las propiedades farmacológicas de la molécula. Problema Relacionado con Medicamentos • aquellas situaciones que en el proceso de uso de medicamentos causan o pueden causar la aparición de un resultado negativo asociado a la medicación


METODOS DE LA FARMACOVIGILANCIA • Pasiva: No hay participación activa de los responsables del proceso en la búsqueda de EAM. Se nombra un líder que se encarga de recibir las sospechas de EAM que son detectadas y notificadas voluntariamente. • Activa: el líder del proceso busca activamente EAM, se fundamentan en la recolección de datos en forma sistemática y detallada
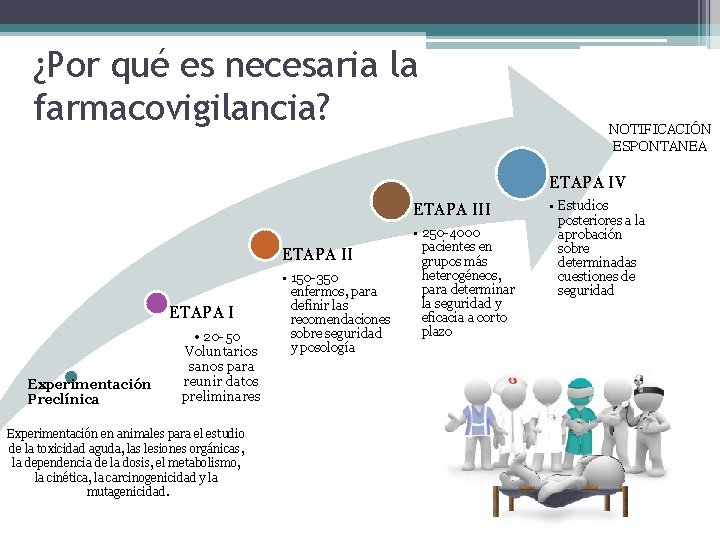
¿Por qué es necesaria la farmacovigilancia? NOTIFICACIÓN ESPONTANEA ETAPA IV ETAPA III ETAPA I Experimentación Preclínica • 20 -50 Voluntarios sanos para reunir datos preliminares Experimentación en animales para el estudio de la toxicidad aguda, las lesiones orgánicas, la dependencia de la dosis, el metabolismo, la cinética, la carcinogenicidad y la mutagenicidad. • 150 -350 enfermos, para definir las recomendaciones sobre seguridad y posología • 250 -4000 pacientes en grupos más heterogéneos, para determinar la seguridad y eficacia a corto plazo • Estudios posteriores a la aprobación sobre determinadas cuestiones de seguridad

Clasificación de las reacciones adversas por su relación con la dosis Efecto secundario indirecto RAM tipo A- (Augmented) REACCIONES ADVERSAS A MEDICAMENTOS RAM tipo B- (Bizarre) RAM Tipo C- (Chronic) RAM tipo D- (Delayed) RAM tipo E- (End of treatment): RAM tipo F- (Foreing): Efecto colateral Reaccion idiosincrásica Tipo I Inmediata Tipo I I Citotoxica Reaccion inmunológica Tipo III Complejo inmune Tipo IV Retarda

Según la gravedad de la reacción adversa LEVE: reacciones menores, no requieren hospitalización, cambio de terapéutica ni antídoto terapia. MODERADA: aquellas que provocan hospitalización o atención en servicio de urgencias. Requieren un cambio en el tratamiento farmacológico SEVERA: Amenaza la vida del paciente y requiere de la suspensión del agente terapéutico causante y de un tratamiento específico para RAM. LETAL: son las que conducen directa o indirectamente a la muerte del paciente.

• La política farmacéutica en Colombia establecida por el Ministerio de la Protección Social va encaminada a “Establecer líneas de investigación en farmacoepidemiologia y farmacoeconomia como mecanismo de promoción del uso adecuado de los medicamentos y de seguimiento a los componentes de la política” y “Diseñar y operacionalizar la red nacional de farmacovigilancia dentro del Sistema Nacional de Vigilancia en Salud Publica”.
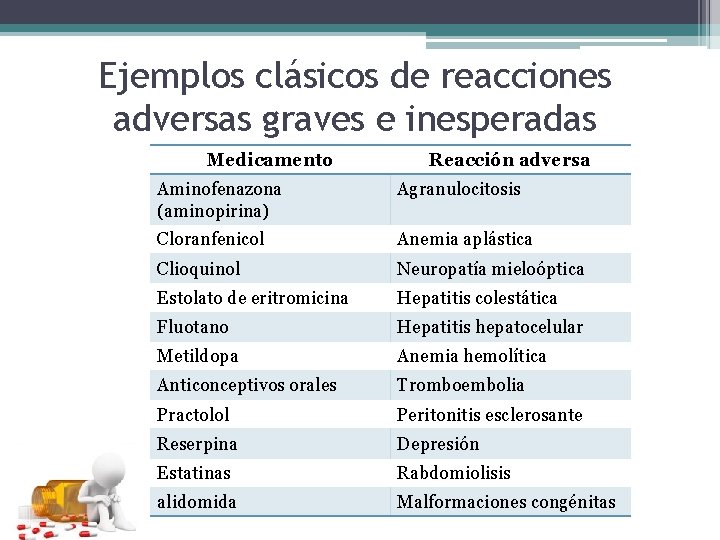
Ejemplos clásicos de reacciones adversas graves e inesperadas Medicamento Reacción adversa Aminofenazona (aminopirina) Agranulocitosis Cloranfenicol Anemia aplástica Clioquinol Neuropatía mieloóptica Estolato de eritromicina Hepatitis colestática Fluotano Hepatitis hepatocelular Metildopa Anemia hemolítica Anticonceptivos orales Tromboembolia Practolol Peritonitis esclerosante Reserpina Depresión Estatinas Rabdomiolisis alidomida Malformaciones congénitas

Entes que regulan
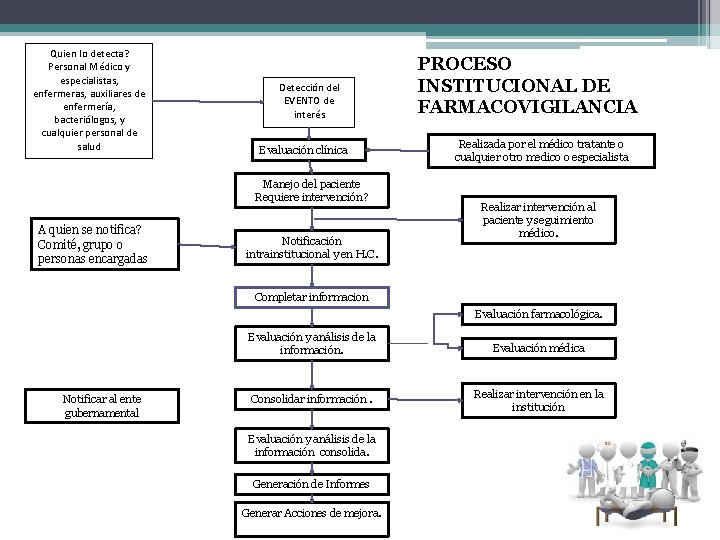
Quien lo detecta? Personal Médico y especialistas, enfermeras, auxiliares de enfermería, bacteriólogos, y cualquier personal de salud Detección del EVENTO de interés Evaluación clínica Manejo del paciente Requiere intervención? A quien se notifica? Comité, grupo o personas encargadas Notificación intrainstitucional y en H. C. PROCESO INSTITUCIONAL DE FARMACOVIGILANCIA Realizada por el médico tratante o cualquier otro medico o especialista Realizar intervención al paciente y seguimiento médico. Completar informacion Evaluación farmacológica. Notificar al ente gubernamental Evaluación y análisis de la información. Evaluación médica Consolidar información. Realizar intervención en la institución Evaluación y análisis de la información consolida. Generación de Informes Generar Acciones de mejora.

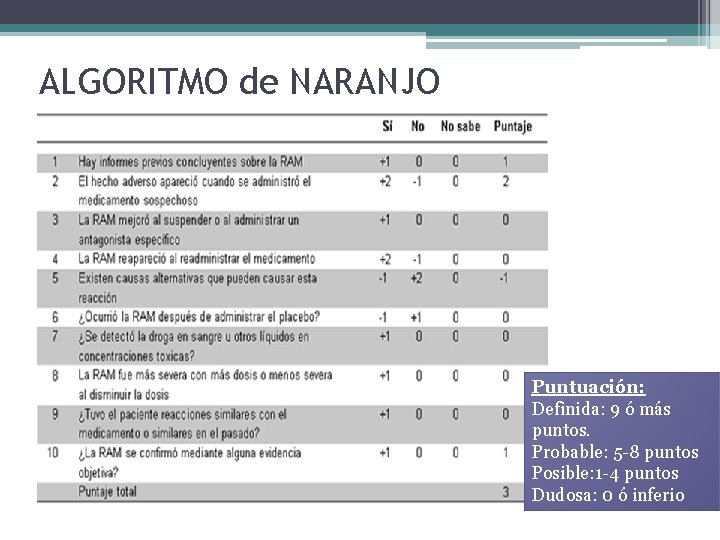
ALGORITMO de NARANJO Puntuación: Definida: 9 ó más puntos. Probable: 5 -8 puntos Posible: 1 -4 puntos Dudosa: 0 ó inferio

REFERENCIAS • La farmacovigilancia: garantía de seguridad en el uso de los medicamentos. Perspectivas políticas de la OMS sobre medicamentos • O. , Leobardo Manuel Gómez. «Farmacoepidemiología como una herramienta. » Revista Mexicana de Ciencias Farmacéuticas 38, nº 1 (2007): 42 -48. • • • Instituto Nacional de Vigilancia de Medicamentos y Alimentos. INVIMA. (8 de Noviembre de 2012). Tecnovigilancia. Programa Nacional de farmacovigilancia. Disponible en: www. invima. gov. co. Manual de Farmacovigilancia de la DSSYPSA 2012 Organización Mundial de la Salud. OMS. (Octubre de 2004). La Farmacovigilancia: garantía de seguridad en el uso de medicamentos. Perspectivas políticas de la OMS sobre medicamentos. Disponible en: http: //apps. who. int/medicinedocs/pdf/s 6166 s. pdf. • Instituto Nacional de Vigilancia de Alimentos y Medicamentos (INVIMA). Programa Nacional en Cifras. Boletin Informativo de Farmacovigilancia 2014; 3: 6. • http: //www. sefh. es/bibliotecavirtual/manualresidentefh/VU 2_98_Capitulo_2_5. pdf • Ministerio de Salud. Secretaría de Políticas, Regulación e Institutos A. N. M. A. T. (2009). Guía de Buenas Prácticas de Farmacovigilancia. Disponible en http: //www. anmat. gov. ar/farmaco/GUIA_BPFV. pdf. Revisado Enero de 2013. • Calderón Ospina, C. A. , & Urbina Bonilla, A. d. (26 de Abril de 2011). La Farmacovigilancia en los últimos 10 años: actualización de conceptos y clasificaciones. Logros y retos para el futuro en Colombia. Médicas UIS, 24, 57 -73. dsiponible en: http: //www. medicasuis. org/anteriores/volumen 24. 1/Farmacovigilancia. pdf. •

- Slides: 37