Farmacologa de Antivirales Dr Esteban Zavaleta HCB ACCP

Farmacología de Antivirales Dr. Esteban Zavaleta HCB ACCP & ASHP

Virus “Los virus son parásitos intracelulares obligados que consisten en DNA o RNA con cubierta proteica llamada a capside” • GOODMAN & GILMAN'S THE PHARMACOLOGICAL BASIS OF THERAPEUTICS 11 th Ed. (2006)

Clasificación Virus DNA • Poxvirus (viruela) • Herpesvirus (varicella, herpes zoster, oral y genital) • Adenovirus (conjuntivitis, dolor de garganta) • Hepadnavirus (hepatitis B) • Papillomavirus (verrugas) Virus RNA • • • Rubella virus (German measles) Rhabdovirus (rabia) Picornavirus (poliomielitis, meningitis, resfríos, hepatitis A) Arenavirus (meningitis, fiebre de Lassa) Flavivirus (West Nile meningoencefalitis, fiebre amarilla, hepatitis C) Ortomixovirus (influenza) Paramixovirus (sarampion, paperas) Coronavirus (resfríos, SARS) Retrovirus (HIV)
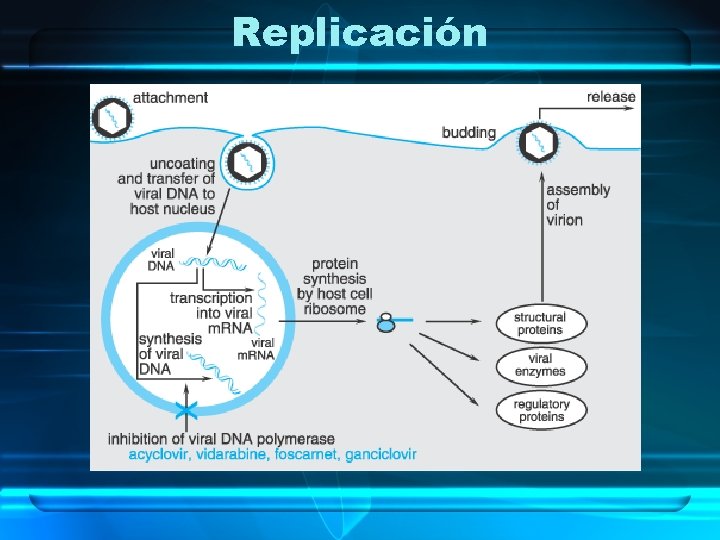
Replicación
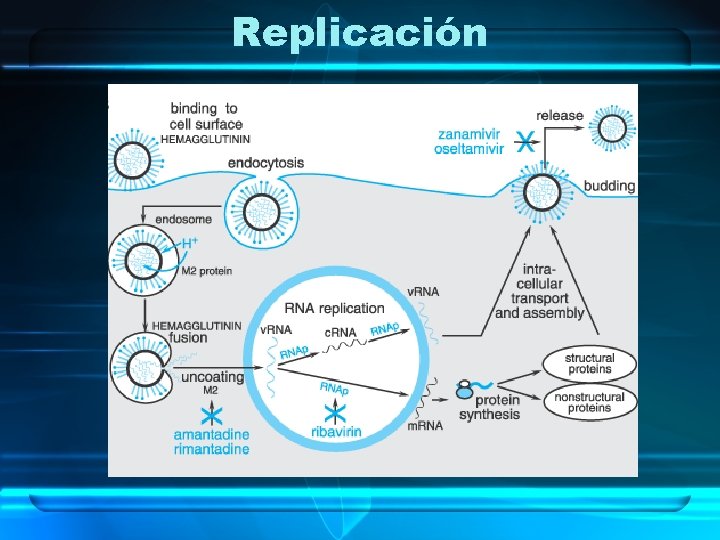
Replicación

Transmisión • Vía aérea: ej. virus de la influenza • Vía alimentos o agua: ej. Rotavirus • Vía sexual: ej. HIV • Vía vectores: ej. Virus de la fiebre amarilla

Posibles consecuencias para las células infectadas Virology: Principles and Applications John B. Carter and Venetia A. Saunders � 2007 John Wiley & Sons, Ltd

Antivirales • En el 2009, se cumplen 50 años de que la síntesis de 5 iodo-2´-deoxiuridina (IDU), el primer antiviral con licencia para uso clínico fue reportada por Prusoff (1959). • 50 años después de este reporte, existen aproximadamente 50 antivirales disponibles en el mercado, de los cuales 25 son para tratar HIV y los otros 25 para el tratamiento de HSV, CMV, HBV, HCV, o influenza. • En 1955, Frank Horsfall Jr. escribió “la mayor dificultad no ha sido encontrar sustancias que inhiban la reproducción de virus… sino descubrir sustancias que restrinjan la multiplicación de virus en el ser humano sin causar al mismo tiempo daño al paciente”

Antivirales • En 1972, Schabel y Montgomery presentaron 22 estudios clínicos favorables en la efectividad de IDU el tratamiento de queratitis herpética. • En 1960 ara-A (Arabinosiladenina), derivado arabinosil nucleósido, se sintetizó por Lee et al; el cual se consideró como un potente agente anti cáncer (Cohen, 1960; Schabel, 1968). Posteriormente se mostró que era suficientemente no tóxico para ser administrado sistémicamente. • Richard Whitley y sus colegas mostraron en 1976 que ara-A (vidarabina) en la terapia de VZV en pacientes inmunosuprimidos.

Antivirales • La selectividad de la acción anti viral del aciclovir, fue anunciada en la edición de diciembre de 1977 de “Proceedings of the US National Academy of Sciences” (Elion et al. , 1977), y su potencial antiviral fue documentado meses después en marzo de 1978 en Nature. • BVDU (descrito en 1979 en “Proc. Natl. Acad. Sci. USA) De Clerq et al. , 1979) y aciclovir fueron los primeros antivirales verdaderamente selectivos.

Antivirales Infecciones por HSV • • Aciclovir Valaciclovir Famciclovir Penciclovir (uso topico) Idoxuridina (uso topico) Trifluridina (uso topico) Vidarabina (ya no es utilizado) Infecciones por VZV • • Aciclovir Valaciclovir Famciclovir Brivudina Infecciones por CMV • • • Ganciclovir Valganciclovir Foscanet Cidofovir Fomivirsen

Antivirales Infecciones crónicas por HBV • • • Lamivudina Adefovir dipivoxil Entecabir Telvibudina Clevudina Tenofovir disoproxil fumarato (TDF) Infecciones crónicas por HCV • Ribavirina + Interferón apegilado Infecciones por el virus de la Influenza • Amantadina • Rimantadina • Zanamivir • Oseltamivir

Farmacología de agentes para infecciones por HSV y VZV
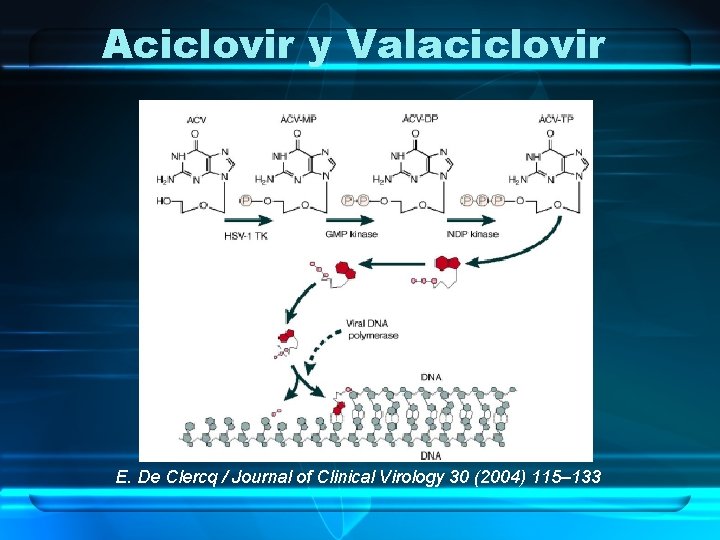
Aciclovir y Valaciclovir E. De Clercq / Journal of Clinical Virology 30 (2004) 115– 133

Aciclovir • 200: 1 TK HSV>TK mamíferos • ACV-TP 41 -100 veces más en células infectadas • Micofenolato de Mofetilo acción anti HSV al d. GTP • Mecanismos de resistencia • Biodisponibilidad oral: 10 – 30%
Aciclovir • t 1/2 eliminación plasmática 2. 5 horas, rango 1. 5 – 6 h en pacientes con FR normal • Eliminación es por FG y ST principalmente • Se distribuye ampliamente en los fluidos corporales, incluyendo fluido vesicular, humor acuoso y fluido cerebroespinal.

USOS APROBADOS • • • Tratamiento de HSV Herpes Labial Herpes Zoster Encefalitis HSV Neonatal HSV Mucocutánea en inmunocomprometidos • Varicella-Zoster EN INVESTIGACIÓN Prevención de reactivación de HSV: • En HIV Positivos • Durante períodos de neutropenia en pacientes con leucemia aguda. • En Trasplante de células progenitoras hematopoyéticas.
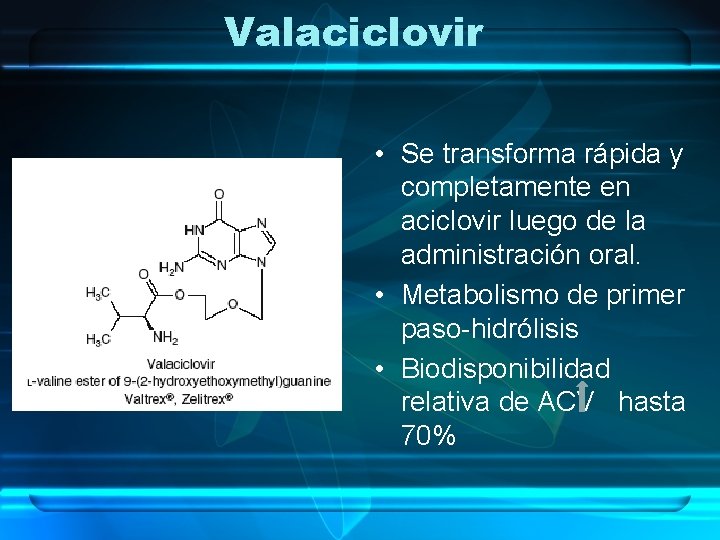
Valaciclovir • Se transforma rápida y completamente en aciclovir luego de la administración oral. • Metabolismo de primer paso-hidrólisis • Biodisponibilidad relativa de ACV hasta 70%

Usos Valaciclovir Aprobados • Tratamiento de Herpes Zoster en pacientes inmuno comprometidos • Tratamiento de Herpes Genital de primer episodio. • Tratamiento para supresión de Herpes Genital recurrente y reducción de la transmisión heterosexual de Herpes Genital en pacientes inmuno comprometidos. • Supresión de Herpes Genital en infectados con HIV. • Tratamiento de Herpes Labial.

Aciclovir y Valaciclovir Efectos adversos • • • Aciclovir, generalmente bien tolerado. – Poca frecuencia: nauseas, diarrea, rash o dolor de cabeza. Dosis de Valaciclovir, asociado confusión, alucinaciones, nefrotoxicidad. Aciclovir IV: IR y efectos en SNC; IR reversible en 5% pacientes. Neurotoxicidad en 1 a 4% pacientes. La Hemodialisis podría ser útil en casos severos. Interacciones • Zidovudina + Aciclovir: somnolencia severa y letargo • Ciclosporina + Aciclovir: riesgo de nefrotoxicidad • Aciclovir aclaramiento renal de drogas que se eliminan por secreción renal activa como Metrotexate
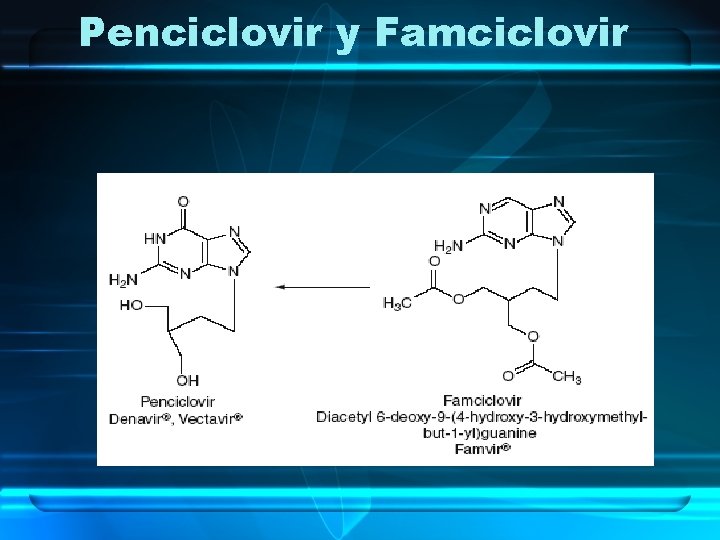
Penciclovir y Famciclovir

Penciclovir y Famciclovir • Mecanismo de acción y resistencia similar a ACV • Similar en espectro de acción y potencia que el aciclovir en HSV y VZV • Biodisponibilidad 65 a 77% tras la administración oral de Famciclovir • Se metaboliza por medio de deacetilación de la cadena lateral y oxidación del anillo de purina (intestino) • Alimentos retardan absorción • t 1/2 de eliminación plasmática aprox. 2 h • 90% de la droga es secretada sin cambios en orina • Hemodiálisis remueve eficientemente el penciclovir • EA: dolor de cabeza, diarrea y nauseas. Urticaria, rash, alucinaciones (adultos mayores)

USOS Aprobados para Penciclovir • Tratamiento tópico para el Herpes Simple Labial (ampollas febriles) Aprobados para Famciclovir • Manejo de Herpes Zoster Agudo • Tx y supresión de episodios recurrentes de Herpes Genital de inmuno comprometidos. • Tx de Herpes Simple Genital y Muco cutáneo en pacientes con HIV
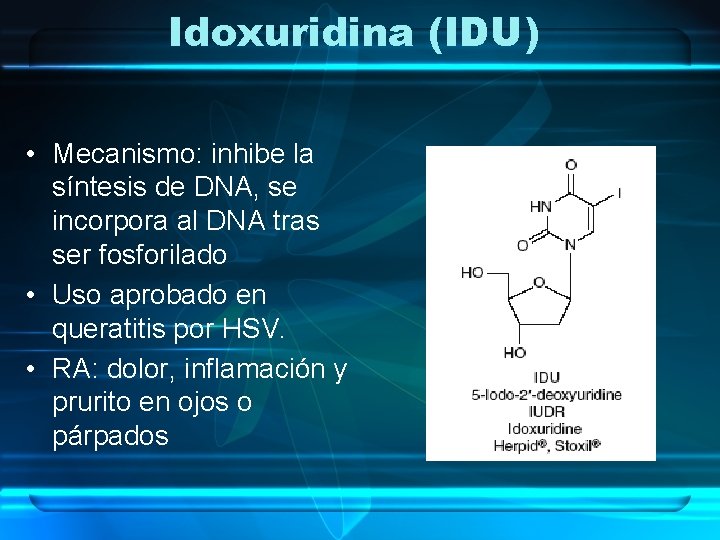
Idoxuridina (IDU) • Mecanismo: inhibe la síntesis de DNA, se incorpora al DNA tras ser fosforilado • Uso aprobado en queratitis por HSV. • RA: dolor, inflamación y prurito en ojos o párpados

USOS Aprobados • Manifestaciones cutáneas del herpes simple y del herpes zoster.
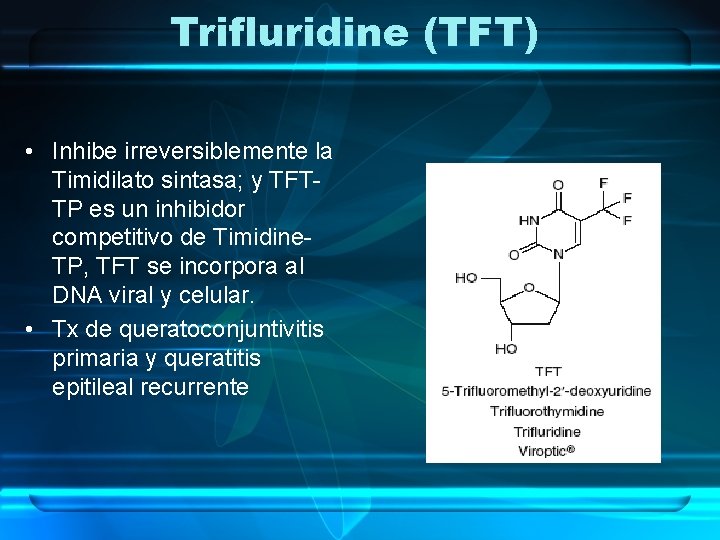
Trifluridine (TFT) • Inhibe irreversiblemente la Timidilato sintasa; y TFTTP es un inhibidor competitivo de Timidine. TP, TFT se incorpora al DNA viral y celular. • Tx de queratoconjuntivitis primaria y queratitis epitileal recurrente

USOS Aprobados • Tratamiento de queratoconjuntivitis y queratitis recurrente epitelial causada por HSV de tipo I y II
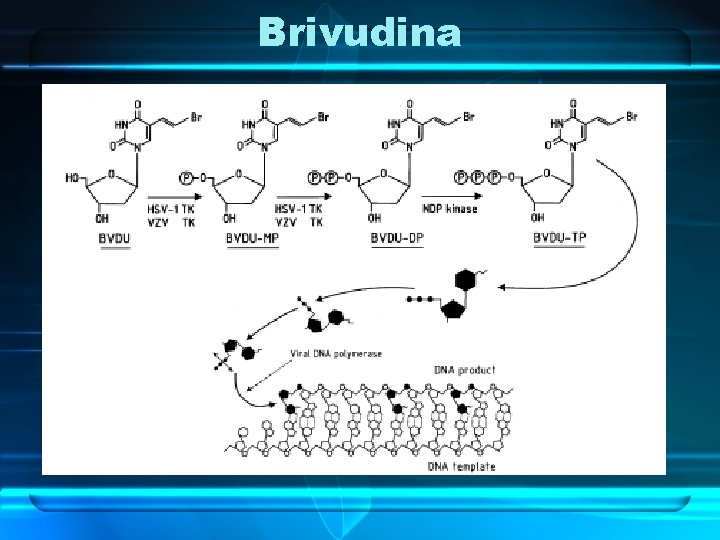
Brivudina
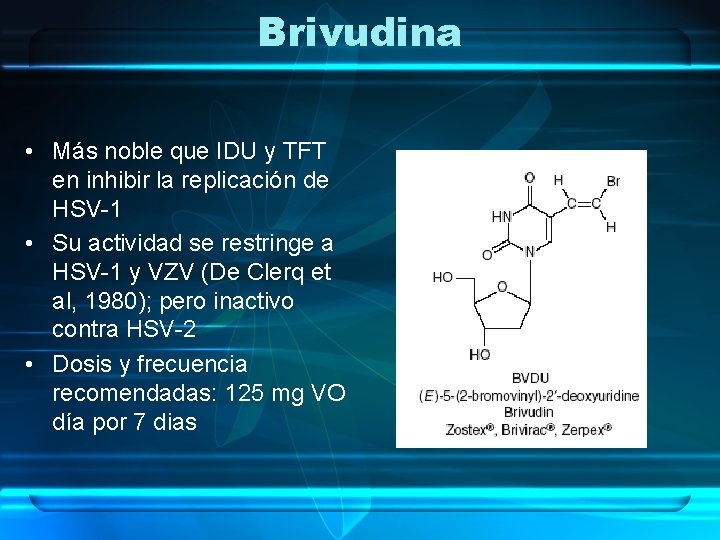
Brivudina • Más noble que IDU y TFT en inhibir la replicación de HSV-1 • Su actividad se restringe a HSV-1 y VZV (De Clerq et al, 1980); pero inactivo contra HSV-2 • Dosis y frecuencia recomendadas: 125 mg VO día por 7 dias
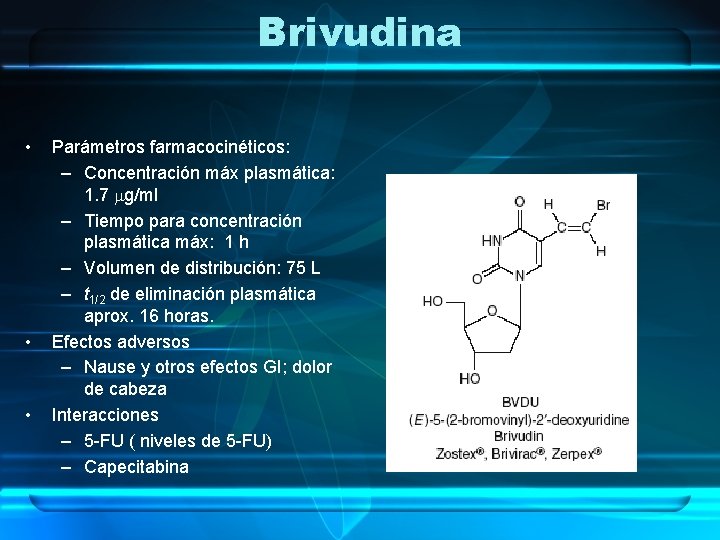
Brivudina • • • Parámetros farmacocinéticos: – Concentración máx plasmática: 1. 7 mg/ml – Tiempo para concentración plasmática máx: 1 h – Volumen de distribución: 75 L – t 1/2 de eliminación plasmática aprox. 16 horas. Efectos adversos – Nause y otros efectos GI; dolor de cabeza Interacciones – 5 -FU ( niveles de 5 -FU) – Capecitabina
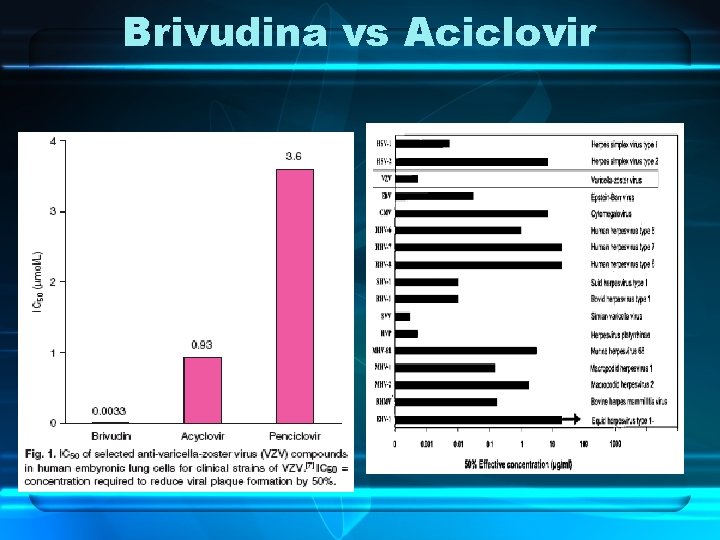
Brivudina vs Aciclovir
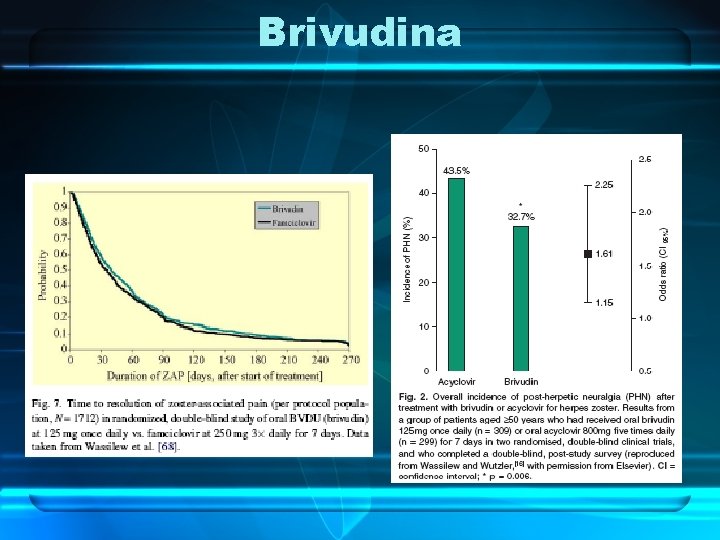
Brivudina

Farmacología de agentes para Infecciones por CMV
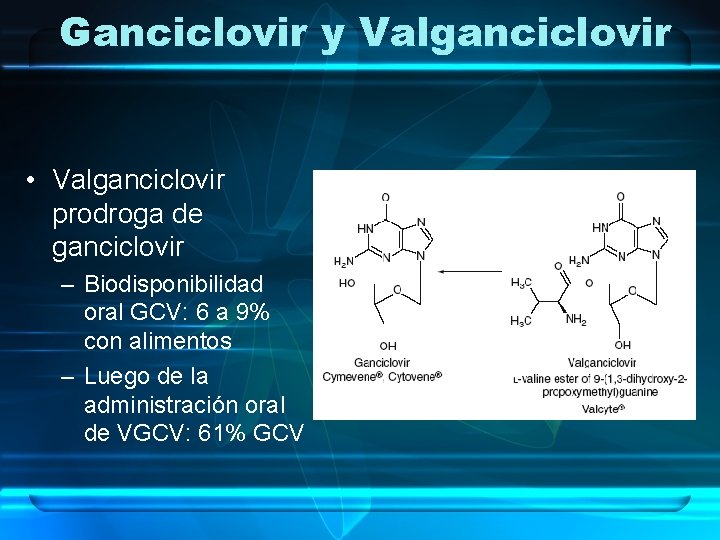
Ganciclovir y Valganciclovir • Valganciclovir prodroga de ganciclovir – Biodisponibilidad oral GCV: 6 a 9% con alimentos – Luego de la administración oral de VGCV: 61% GCV

Ganciclovir y Valganciclovir • Mecanismo de acción: GCV inhibe la síntesis de DNA – GCV-MP HSV-TK o fosfostransferasa codificada por UL 97 en la infección por CMV – GCV-DP y GCV-TP se forman por enzimas celulares – GCV-TP se incorpora al DNA – Al menos 10 veces es la Conc. de GCV-TP en células infectadas que en las no infectadas • t 1/2 de eliminación intracelular> 24 horas • 90% de GCV se elimina intacto por secreción renal por medio de FG y ST • Efectos adversos: Mielosupresión principalmente – Neutropenia: 15 a 40% pacientes – Trombocitopenia: 5 a 20% – Tx Neutropenia con G-CSF (Filgrastim) • VGCV oral – Se asocia con dolor de cabeza y molestias GI + neutropenia

USOS DEL GANCICLOVIR Aprobados Parenteral: Tx de retinitis CMV en inmuno comprometidos incluidos pacientes con SIDA. Profilaxis de infección por CMV en pacientes trasplantados. Oral: Alternativo a formulación IV para mantenimiento de tx de retinitis de CMV en pacientes inmunocomprometidos incluidos pacientes con SIDA. Implante: Tx de retinitis por CMV En Investigación En combinación con Foscarnet en pacientes con recaídas después de monoterapia con cualquiera de las dos drogas.

USOS DEL VALGANCICLOVIR Aprobados • Tratamiento del CMV • Retinitis en pacientes con SIDA • Prevención de enfermedad por CMV en pacientes de alto riesgo (trasplante de riñón, corazón, riñón/páncreas)
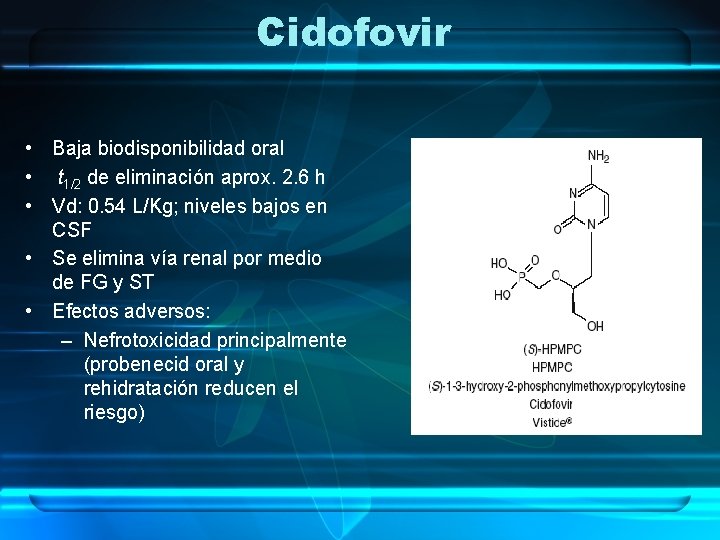
Cidofovir • Baja biodisponibilidad oral • t 1/2 de eliminación aprox. 2. 6 h • Vd: 0. 54 L/Kg; niveles bajos en CSF • Se elimina vía renal por medio de FG y ST • Efectos adversos: – Nefrotoxicidad principalmente (probenecid oral y rehidratación reducen el riesgo)
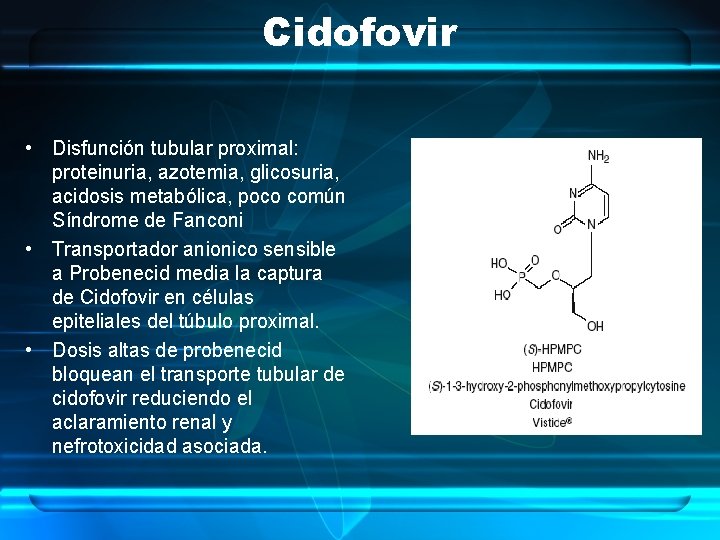
Cidofovir • Disfunción tubular proximal: proteinuria, azotemia, glicosuria, acidosis metabólica, poco común Síndrome de Fanconi • Transportador anionico sensible a Probenecid media la captura de Cidofovir en células epiteliales del túbulo proximal. • Dosis altas de probenecid bloquean el transporte tubular de cidofovir reduciendo el aclaramiento renal y nefrotoxicidad asociada.
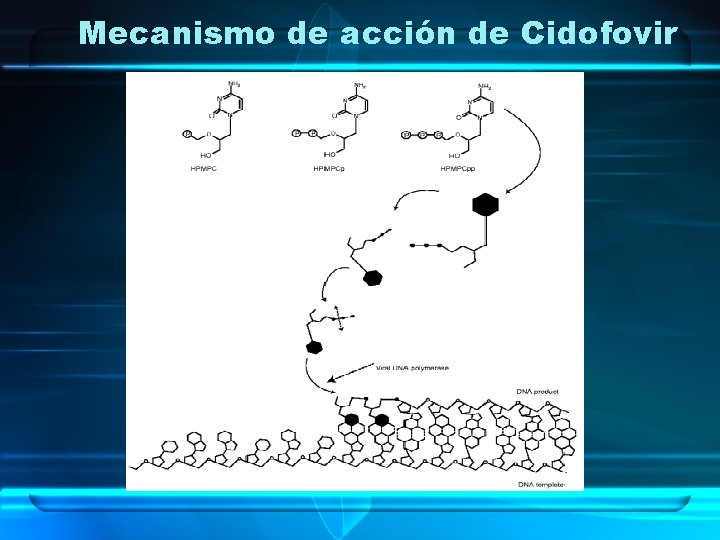
Mecanismo de acción de Cidofovir

USOS Aprobados • Tratamiento de Retinitis por CMV en pacientes con SIDA NOTA: Debe ser administrado junto con Probenecid

Foscarnet MECANISMO DE ACCIÓN Análogo de Pirofosfato que actúa como inhibidor no competitivo de muchas ADN y ARN polimerasas virales, así como con la transcriptasa reversa en HIV. No requiere activación por parte de la Timidina Kinasa. En la mayoría de los pacientes causa falla renal durante el tx.

FOSCARNET t 1/2: 3 h Excreción: Urinaria RA: >10%: - SNC: Fiebre (65%), Dolor de cabeza (26%) - GI: Náuseas (47%), Diarrea (30%), Vómito - Anemia (33%) - Renal: Función renal anormal/ disminución de aclaramiento de creatinina (27%) INTERACCIONES Aumenta el efecto/Toxicidad: Ciprofloxacina (o otras FQ’s ). Junto con ciclosporina efecto sinérgico. Evitar drogas nefrotóxicas (Anfotericina B, Aminoglucósidos), para disminuir riesgo renal con Foscarnet. Con Inhibidores de Proteasa se ha visto asociado con aumento de riesgo de falla renal

USOS Aprobados En investigación • Tx de infecciones por Herpes Virus cuando hay resistencia al Aciclovir (HSV, VZV) o resistencia al Ganciclovir (CMV). • Otras infecciones por CMV en personas con intolerancia al Ganciclovir. • Tx de retinitis por CMV en personas con SIDA • Puede darse junto con Ganciclovir en pacientes con recaídas después de monoterapia con cualquiera de las dos drogas.

FOMIVIRSEN Utilizado en el Tx de Retinitis por CMV en pacientes inmunocomprometidos incluidos los que tienen SIDA. Es un oligonucleótido con uniones de fosforotionaro (resistentes a la degradación por parte de nucleasas) y contienen la secuencia: 5'-GCG TTT GCT CTT CTT GCG-3'
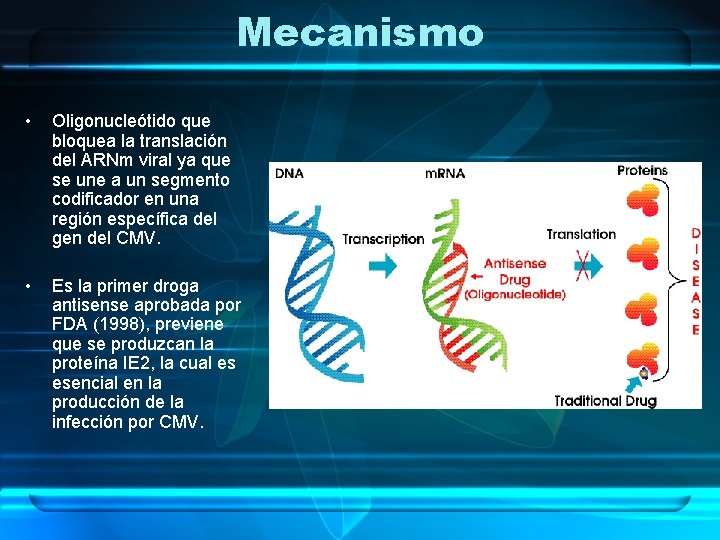
Mecanismo • Oligonucleótido que bloquea la translación del ARNm viral ya que se une a un segmento codificador en una región específica del gen del CMV. • Es la primer droga antisense aprobada por FDA (1998), previene que se produzcan la proteína IE 2, la cual es esencial en la producción de la infección por CMV.

FOMIVIRSEN RA: INTERACCIONES • Uveitis en 25% de los pacientes. • No se recomienda el uso en pacientes que han utilizado recientemente IV, Intravitreal Cidofovir debido a que aumenta el riesgo de inflamación ocular. • 5 -20% pacientes: Visión borrosa, cataratas, cambios de color en la visión, aumento de presión intraocular, fotofobia, problemas de retina.

Farmacología de agentes para infecciones por Influenza

ADAMANTANOS • Activas con virus de influenza A. • Mecanismo de acción: unión a M 2 y bloqueo de los canales iónicos. Impide el desnudamiento (no permite la disminución del p. H en el interior de la partícula viral contenida en endosoma (función controlada por M 2), que es esencial para inducir cambios conformacionales en la HA para permitir la fusión de membranas (envoltura viralmembrana del endosoma) y liberación de ribonucleoproteína al citoplasma.
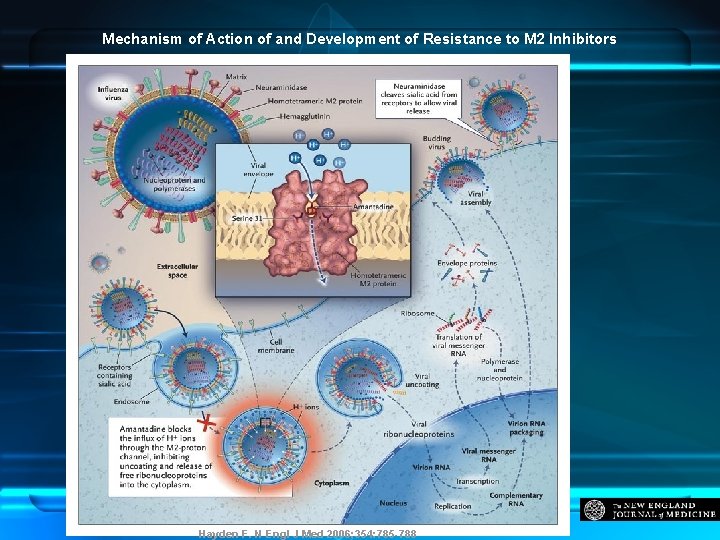
Mechanism of Action of and Development of Resistance to M 2 Inhibitors Hayden F. N Engl J Med 2006; 354: 785 -788

AMANTADINA • Buena absorción • Biodisponibilidad: 86 -90% • Unión a proteínas: Func Renal normal ~ 67%; Hemodiálisis ~ 59% • Vida media de eliminación: Func Renal normal 16 ± 6 h, Enfermedad renal de último estadío • Metabolismo: No apreciable. • Excreción: Orina (80 -90% sin cambios) por filtración glomerular y secreción tubular. • INTERACCIONES: Aumentan el efecto: a nivel de SNC los anticolinérgicos. HTC, Trimetroprim.

USOS Aprobados: • Profilaxis y Tratamiento de infección por influenza tipo A. • Tx de Parkinson – Altera dopamina, propiedades como anticolinérgico, pero más importante es el bloqueo de receptores NMDA. • Tx para síntomas extrapiramidales inducidos por drogas.

RIMANTADINA • Vida media de eliminación: 25, 4 h • Metabolismo: Hepático • Excreción: Orina (<25% sin cambios) INTERACCIONES: • Aumentan el efecto: Cimetidina • Disminuyen el efecto: Acetaminofén.

USOS Aprobados: • Profilaxis (adultos y niños mayores de un año) y tratamiento por infección viral → Influenza tipo A.

Inhibidores de Neuraminidasa • Todos los virus de la gripe presentan en su superficie dos glicoproteínas: una hemaglutinina y una neuraminidasa, que son los antígenos que definen un tipo particular de virus de la gripe. • Sin la acción de la neuraminidasa, la infección viral quedaría limitada a una sola replicación del virus, insuficiente para causar la enfermedad de la gripe. • Mecanismo: Inhibe el Virus de Influenza A y B alterando la agregación y liberación de la partícula viral.
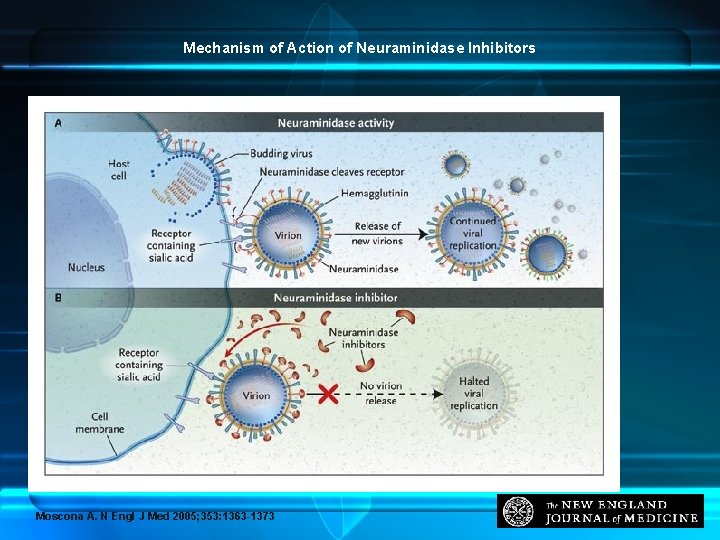
Mechanism of Action of Neuraminidase Inhibitors Moscona A. N Engl J Med 2005; 353: 1363 -1373

ZANAMIVIR • • • Absorción: Inhalación: 4 -17% Unión a Proteínas: Plama: <10% Vida media de eliminación: 2, 5 -5, 1 h Metabolismo: Ninguno Excreción: Orina y heces • Interacciones: • Disminuye el efecto terapéutico de la vacuna viva atenuada del virus de influenza

USOS Aprobados • Tx de enfermedad aguda no complicada debido a virus de la influenza A y B. • Profilaxis contra virus influenza A y B

OSETALMIVIR • Buena absorción • Biodisponibilidad: 75% como osetalmivir carboxilato. • Unión a proteínas: Osetalmivir carboxilato (3%), Osetalmivir (42%) • Vida media de eliminación: Osetalmivir (1 -3 h), Osetalmivir carboxilato (6 -10 h) • Metabolismo: Hepático (90%) • Excreción: Orina (+90%) a Osetalmivir carboxilato, heces • Interacciones: Disminuye el efecto de la vacuna del virus de influenza

USOS Aprobados • Tratamiento de enfermedad aguda no complicada debido a influenza A y B en niños mayores de un año y en adultos que han manifestado síntomas por más de dos días. • Profilaxis contra virus influenza A y B en niños mayores de un año y adultos. • Se ha convertido en el tratamiento de elección en: – Gripe aviar – Gripe por influenza A H 1 N 1

Direrectrices nacionales para prescripción y despacho de oseltamivir • El tratamiento se administrará solamente a: – Los casos sospechosos, probables o confirmar que, por su condición clínica de severidad, califican como IRAG. El tratamiento se debe iniciar en el momento y en el lugar de captación del paciente – Los casos sospechoso, probables o confirmados que pertenecen a un grupo de alto riesgo de sufrir complicaciones por influenza. • Mujeres embarazadas con o sin factores de riesgo asociados • Personas de cualquier edad que presentan algunas de las siguientes enfermedades crónicas – – – – Enfermedades pulmonares, incluida el asma Insuficiencia cardiaca congestiva clase 2 o cardiopatías congénitas Enfermedades renales, hepáticas o hematológicas con imunosupresión Pacientes con HIV o inmunosuprimidos Obesidad mórbida Enfermedades metabólicas en niños DM descompensada en cualquier edad.

Dosis de Oseltamivir • Neumonías severas (incluye embarazadas obesas) – Dosis inicial de carga: 300 mg STAT – Dosis de mantenimiento: 150 mg bid por 10 días • Neumonías en paciente obeso (IMC>30) (incluye embarazadas obesas) – Dosis inicial de carga: 300 mg STAT – Dosis de mantenimiento: 150 mg bid por 10 días • Neumonías leves y moderadas – Dosis de mantenimiento: 75 mg bid por 10 días • Neumonías en embarazadas no obesas – Dosis de mantenimiento: 75 mg bid por 10 días • Pacientes sospechosos con factores de riesgo – 75 mg bid por 5 días

Profilaxis • La profilaxis con antivirales se dará solo en casos muy calificados y previa valoración médica y epidemiológica: – Contactos cercanos de casos confirmados que pertenecen a un grupo de alto riego – Trabajadores de salud que no utilizaron el equipo adecuado y estuvieron en contacto con un caso confirmado o probable.

Farmacología de agentes para infecciones por HBV y HCB

Interferón a-PEG y Rivabirina • Interferón descubierto en 1957 por Isaacs y Lindenmann • Rivabirina descrita inicialmente por Sidwell et al. en 1976 • Actualmente la terapia estándar contra HCV se basa en la combinación de Interferón a. PEG y Rivabirina (Manns et al. 2007)

Interferones • Potentes citoquinas – Antiviral – Inmunomodulación – antiproliferación • PEG – Enlentece la absorción – Disminuye el aclaramiento – Concentraciones séricas mayores y mas prologadas • EA: – Pseudoinfluenza – Dosis limitante: mielosupresión con agranulocitosis y trombocitopenia; neurotoxicidad
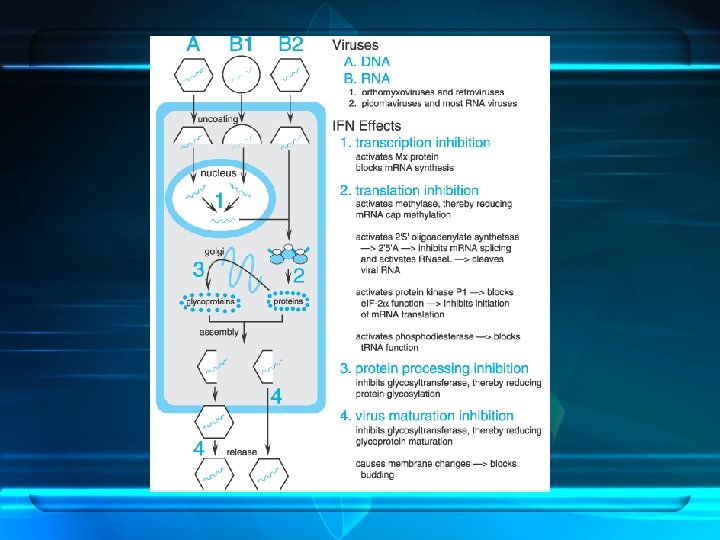

Tratamiento contra HBV • • • Lamivudina Adefovir dipivoxil Entecabir Telvibudina Clevudina Tenofovir disoproxil fumarato (TDF)
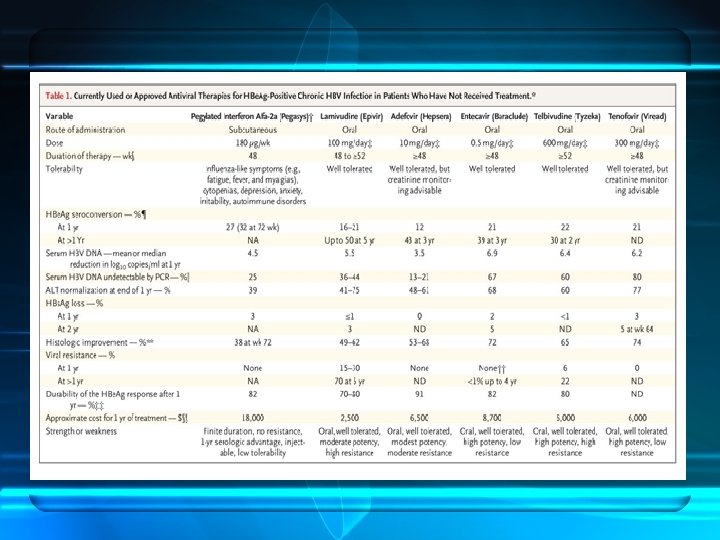

Preguntas y Comentarios Fin
- Slides: 70