FARMACI E SPORT Docente Roberto Leone EMAIL roberto

FARMACI E SPORT Docente: Roberto Leone EMAIL: roberto. leone@univr. it

Modalità d’esame Prova scritta con 31 domande a risposta multipla. Ogni risposta esatta equivale a un punto. L’esame verterà sulle specifiche tematiche svolte durante le lezioni frontali e il lavoro di gruppo (individuale). Testi di studio “Farmacologia per le lauree triennali e magistrali” Taglialatela et al. , ed. Sorbona, 2019 “ Casi farmacologici “ e loro risposte, diapositive (fornite direttamente agli studenti frequentanti)) Ricevimento Il docente prende appuntamento via email roberto. leone@univr. it Studio prof. Leone: primo piano palazzina di Farmacologia Policlinico G. B. Rossi, P. le L. A. Scuro 10, 37134 Verona

Che cosa è un farmaco? Farmaco(definizione OMS): Qualunque sostanza usata allo scopo di modificare o studiare funzioni fisiologiche o stati patologici a beneficio di chi la riceve.

Farmaco(definizione OMS): Qualunque sostanza usata allo scopo di modificare o studiare funzioni fisiologiche o stati patologici a beneficio di chi la riceve. Ø Ø Ø Ø Medicinali Prodotti erboristici (fitoterapia) Prodotti omeopatici Cosmetici Integratori alimentari Integratori per attività fisica Cellule (es. staminali)

Farmaco(definizione OMS): Qualunque sostanza usata allo scopo di modificare o studiare funzioni fisiologiche o stati patologici a beneficio di chi la riceve. Placebo: Sostanza farmacologicamente inerte che può provocare un effetto sul paziente, sintomo, malattia. L’EFFETTO DI UN FARMACO E’ LEGATO SIA ALLA SUA ATTIVITA’ SPECIFICA CHE ALL’EFFETTO PLACEBO.

Un placebo, ad esempio, può: Ø Provocare miosi, alterare la pressione sanguigna, modificare il battito cardiaco e la respirazione, influenzare le secrezioni gastrointestinali e la peristalsi, modificare la temperatura corporea, produrre eosinofilia e leucocitosi, provocare secrezione di cortisolo, modificare i livelli di creatina e lipoproteine… Ø In negativo (nocebo): causare secchezza delle fauci, nausea, cefalea, stanchezza, difficoltà di cencentrazione, sonnolenza, disturbi el sonno…
Come si distingue un farmaco da un placebo? Attività specifica? Effetto placebo?

Prima che un nuovo farmaco venga registrato, cioè prima che ne venga autorizzata la commercializzazione da parte delle autorità sanitaria, in Italia l’AIFA (Agenzia Italiana del Farmaco), in Europa l’EMA (European Medicines Agency), l’industria farmaceutica deve presentare una documentazione che attesti che il farmaco è stato sottoposto a diverse fasi di sperimentazione. Le fasi di una sperimentazione di un farmaco si possono dividere in: A- Studi pre-clinici in vitro (cellule, organi isolati) e in vivo (animali di laboratorio) B- Studi clinici (persone) suddivisi in tre fasi
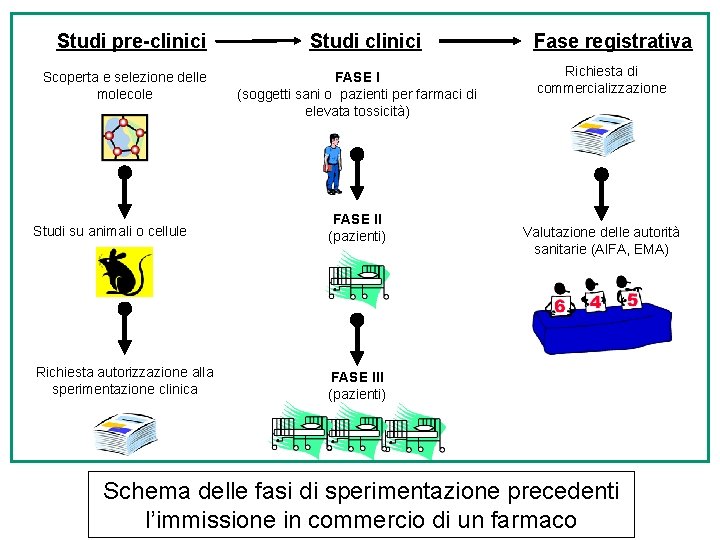
Studi pre-clinici Scoperta e selezione delle molecole Studi clinici FASE I (soggetti sani o pazienti per farmaci di elevata tossicità) Studi su animali o cellule FASE II (pazienti) Richiesta autorizzazione alla sperimentazione clinica FASE III (pazienti) Fase registrativa Richiesta di commercializzazione Valutazione delle autorità sanitarie (AIFA, EMA) Schema delle fasi di sperimentazione precedenti l’immissione in commercio di un farmaco

Sperimentazioni cliniche di fase I OBIETTIVI • Tollerabilità nell’uomo • Dati di farmacocinetica e farmacodinamica • Schema di dosaggio da impiegare nella fase II SOGGETTI • Da 20 a 80 volontari sani (o pazienti in caso di farmaci ad alta tossicità) CENTRI • Altamente specializzati autorizzati dall’AIFA DURATA • 1 -2 anni

Sperimentazioni cliniche di fase II OBIETTIVI • Definizione della efficacia e tollerabilità nei pazienti • Individuazione del rapporto dose/effetto SOGGETTI • 100 -300 pazienti, ma anche fino od oltre 1000 DURATA • 1 -2 anni METODOLOGIA • sia studi comparativi che non comparativi

Sperimentazioni cliniche di fase III OBIETTIVI • Acquisizione di dati di efficacia e tollerabilità su un ampio campione • Verifica del significato clinico delle interazioni farmacologiche prevedibili • Definizione finale del rapporto dose/effetto SOGGETTI • 1000 -3000 pazienti, ma anche fino od oltre 5000 DURATA • 3 -4 anni

Criteri fondamentali per una corretta sperimentazione clinica sui farmaci Ø Presenza di un gruppo di controllo (miglior farmaco già esistente o in sua mancanza il placebo) L’utilizzo del placebo potrebbe essere preferibile in alcune situazioni ad esempio quando si vogliono chiarire aspetti di safety, ovviamente si deve valutare attentamente l’aspetto etico di privare pazienti del trattamento farmacologico.
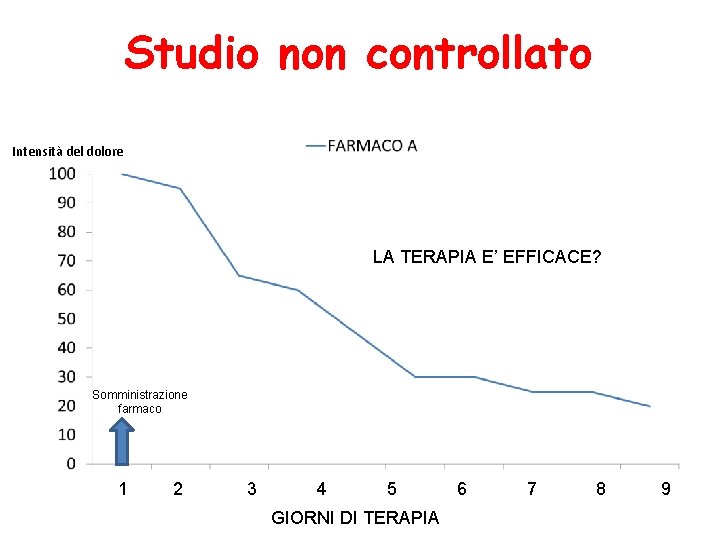
Studio non controllato Intensità del dolore LA TERAPIA E’ EFFICACE? Somministrazione farmaco 1 2 3 4 5 GIORNI DI TERAPIA 6 7 8 9
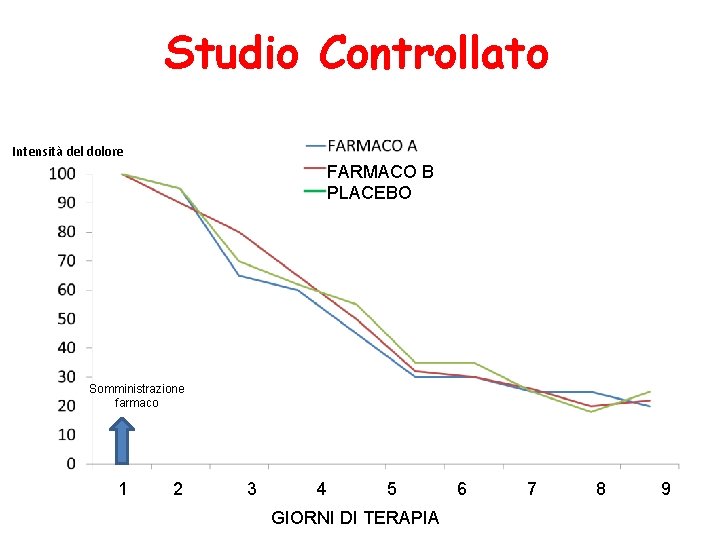
Studio Controllato Intensità del dolore FARMACO B PLACEBO Somministrazione farmaco 1 2 3 4 5 GIORNI DI TERAPIA 6 7 8 9
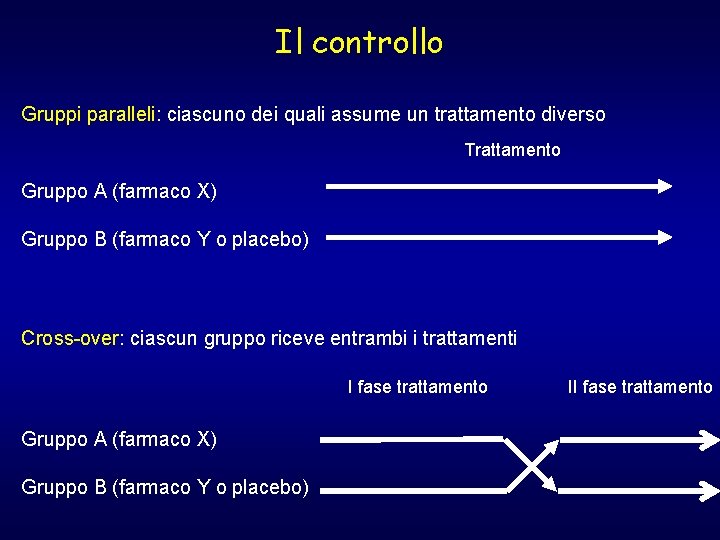
Il controllo Gruppi paralleli: ciascuno dei quali assume un trattamento diverso Trattamento Gruppo A (farmaco X) Gruppo B (farmaco Y o placebo) Cross-over: ciascun gruppo riceve entrambi i trattamenti I fase trattamento Gruppo A (farmaco X) Gruppo B (farmaco Y o placebo) II fase trattamento

Criteri fondamentali per una corretta sperimentazione clinica sui farmaci Ø Presenza di un gruppo di controllo (miglior farmaco già esistente o in sua mancanza il placebo) Ø Randomizzazione dei pazienti (assegnazione casuale): che è il metodo migliore per ottenere gruppi confrontabili (simili tra di loro)


Metodi di randomizzazione • Assegnazione sistematica (giorni pari e dispari, alternanza. . . ) • Lancio della moneta, tavole dei numeri casuali, computer, chiamata telefonica • La randomizzazione va ‘tutelata’ utilizzando tecniche opportune ad es. in sede di confezionamento
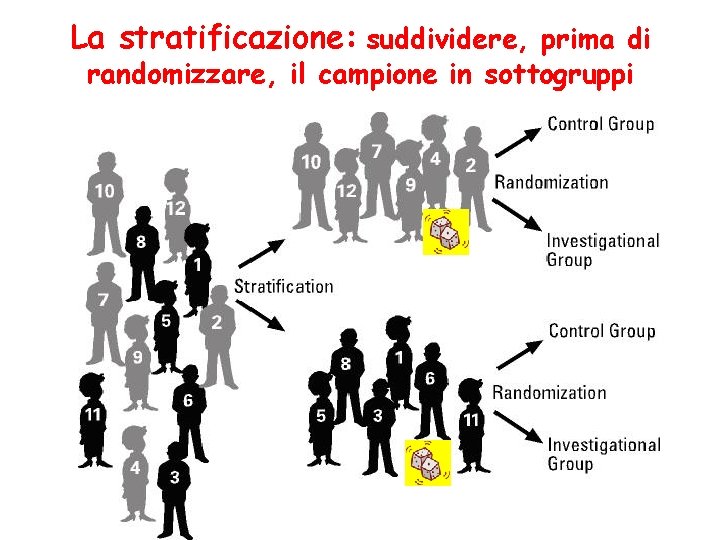
La stratificazione: suddividere, prima di randomizzare, il campione in sottogruppi

Criteri fondamentali per una corretta sperimentazione clinica sui farmaci Ø Presenza di un gruppo di controllo (miglior farmaco già esistente o in sua mancanza il placebo) Ø Randomizzazione dei pazienti (assegnazione casuale) Ø Cecità

La cecità: per vedere bene Ø Singolo cieco: solo il soggetto sotto sperimentazione non sa quale trattamento sta ricevendo Ø Doppio cieco: sia il soggetto sotto sperimentazione che gli sperimentatori non sanno quale trattamento si assume/somministra Ø Doppio simulato (double dummy): metodica utilizzata per mantenere la cecità quando si confrontano farmaci somministrati per vie o con formulazioni diverse tra di loro Ø In aperto: sperimentazione senza cecità. Accettabile quando si confrontano terapie diverse e/o complesse Ø Valutatori dovrebbero essere sempre in cieco

Criteri fondamentali per una corretta sperimentazione clinica sui farmaci Ø Presenza di un gruppo di controllo (miglior farmaco già esistente o in sua mancanza il placebo) Ø Randomizzazione dei pazienti (assegnazione casuale) Ø Cecità Ø Definizione dei criteri di inclusione ed esclusione dei pazienti Ø Rappresentatività del campione rispetto alla popolazione che assumerà il farmaco e sua adeguata dimensione

Popolazione studiata Sottogruppo della popolazione generale determinato dai criteri di inclusione/esclusione Popolazione Generale Criteri di elegibilità (incl. /escl. ) Popolazione studiata Arruolamento Campione studiato

INFERENZA STATISTICA CAMPIONE POPOLAZIONE STUDIATA La popolazione è la collettività di soggetti oggetto di studio Il campione è il gruppo di soggetti estratti dalla popolazione La casualità del campione consente di utilizzare le procedure dell’inferenza statistica trasferendo i risultati alla popolazione Il problema dei trial clinici è la definizione della popolazione (criteri di inclusione ed esclusione) e l’estrapolazione dei risultati ad una popolazione più generale rispetto a quella oggetto dello studio

Rappresentatività del campione Ø I risultati di uno studio sono estrapolabili solo ai soggetti con le stesse caratteristiche dei reclutati Ø Criteri di inclusione troppo rigidi non permettono di sapere se l’intervento in sperimentazione avrebbe gli stessi risultati nella popolazione Ø Problema donne in gravidanza, ultra anziani, bambini, spesso esclusi dalle sperimentazioni ma poi trattati quando i farmaci entrano in commercio. Problema interazioni

Criteri fondamentali per una corretta sperimentazione clinica sui farmaci Ø Definizione dei criteri di inclusione ed esclusione dei pazienti Ø Rappresentatività del campione rispetto alla popolazione che assumerà il farmaco e sua adeguata dimensione Ø Dimensione del campione Ø Superiorità o non inferiorità

Dimensione del campione ü Ricordarsi che lo studio è un esperimento che coinvolge persone ü La numerosità del campione deve essere tale da rispondere agli obiettivi dello studio (viene calcolata sull’obiettivo primario) ü Non dovrebbero mai essere arruolate più persone di quelle necessarie ü La dimensione del campione è una stima basata su calcoli statistici per garantire di raggiungere l’obiettivo clinico stabilito a priori
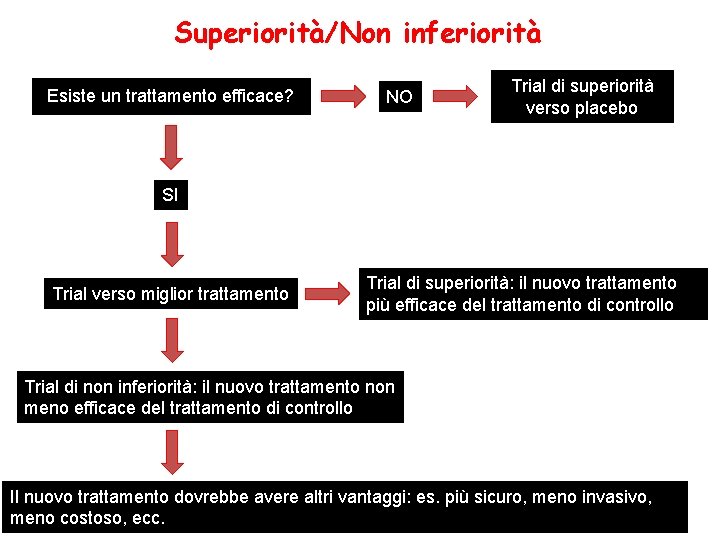
Superiorità/Non inferiorità Esiste un trattamento efficace? NO Trial di superiorità verso placebo SI Trial verso miglior trattamento Trial di superiorità: il nuovo trattamento più efficace del trattamento di controllo Trial di non inferiorità: il nuovo trattamento non meno efficace del trattamento di controllo Il nuovo trattamento dovrebbe avere altri vantaggi: es. più sicuro, meno invasivo, meno costoso, ecc.

Criteri fondamentali per una corretta sperimentazione clinica sui farmaci Ø Dimensione del campione Ø Superiorità o non inferiorità Ø Eticità della sperimentazione Ø Consenso informato dei partecipanti

Sperimentazione clinica ed etica: le origini In Italia nel 1871 il Monitore dei Tribunali si interroga, in un editoriale, sugli aspetti etici e giuridici delle sperimentazioni 1892, esperimenti di Albert Neisser su prostitute non consenzienti 29 dicembre 1900: circolare del Ministero degli affari sociali, educazione e medicina della Prussia che vieta la sperimentazione senza consenso A. Neisser (1855 -1916) Ai primi del ‘ 900 il medico russo Smidovich pubblica The confessions of a physician dove ricostruisce le pratiche cliniche in tutto il mondo e in vari settori della ricerca, mettendo in luce i notevoli problemi etici esistenti

Sperimentazione clinica ed etica: le origini La sperimentazione nei lager nazisti Dr. Joseph Mengele (1911 -? ) Alla fine del 1946 a Norimberga si apre il processo a 23 medici per avere condotto sperimenti su migliaia di prigionieri dei campi di concentramento senza loro Art. 1 «The voluntary consent of il the consenso. Risultato del processo fu anche il cosiddetto human subject isdelabsolutely essential» Codice di Norimberga 1948 con 10 norme che pur non avendo forza di legge stabilivano importanti principi etici ripresi in seguito anche nella Helsinki Declaration.

Sperimentazione clinica ed etica: le origini La sperimentazione nei lager nazisti Dr. Joseph Mengele (1911 -? ) Alla fine del 1946 a Norimberga si apre il processo a 23 medici per avere condotto sperimenti su migliaia di prigionieri dei campi di concentramento senza loro Art. 1 «The voluntary consent of il the consenso. Risultato del processo fu anche il cosiddetto human subject isdelabsolutely essential» Codice di Norimberga 1948 con 10 norme che pur non avendo forza di legge stabilivano importanti principi etici ripresi in seguito anche nella Helsinki Declaration.

Lo scandalo del Tuskegee Syphilis Study Per quarant’anni (1932 -1972), il servizio sanitario degli Stati Uniti ha condotto un esperimento su 399 agricoltori afroamericani, malati di sifilide, residenti a Tuskegee, una delle contee più povere dell'Alabama. Non fu mai detto loro di che malattia stessero soffrendo, furono solamente informati che sarebbero stati curati per “bad blood”. I ricercatori non somministrarono loro alcun trattamento anche dopo la disponibilità della penicillina. Molti morirono per la sifilide. Il governo americano pose fine all’esperimento nel 1973, dopo che la vicenda era stata riportata sul New York Times nel ‘ 72, e successivamente assicurò agli uomini di Tuskegee il trattamento efficace per curare la sifilide. Il 16 maggio 1997 il presidente Clinton porse scuse formali agli ultimi otto sopravvissuti, definendo il programma “profondamente immorale e razzista”.

Una brutta storia più recente Sperimentazione su bambini con l’antibiotico Trovan, condotta nel 1996 in Nigeria, a Kano, da una nota azienda farmaceutica senza seguire le dovute procedure. Il caso venne sollevato dal Washington Post, la ditta è stata poi condannata a pagare dei risarcimenti alle famiglie dei bambini morti a seguito della sperimentazione.

La nascita dei Comitati Etici A partire dalla fine degli anni ’ 70 Comitati Etici si costituiscono così in tutto il mondo. Le principali motivazioni che portano alla loro costituzione, in forme e modi che differiscono tra i Paesi ma con medesime finalità, sono: Ø Abusi nella sperimentazione Ø Mancanza di informazione Ø Avvento di nuove tecnologie biomediche Ø Difformità tra pratica, etica e legislazione

La nascita dei Comitati Etici In Italia i Comitati Etici vengono istituiti con il D. M. del 18 marzo 1998 e riorganizzati con il D. M. del 8 febbraio 2013
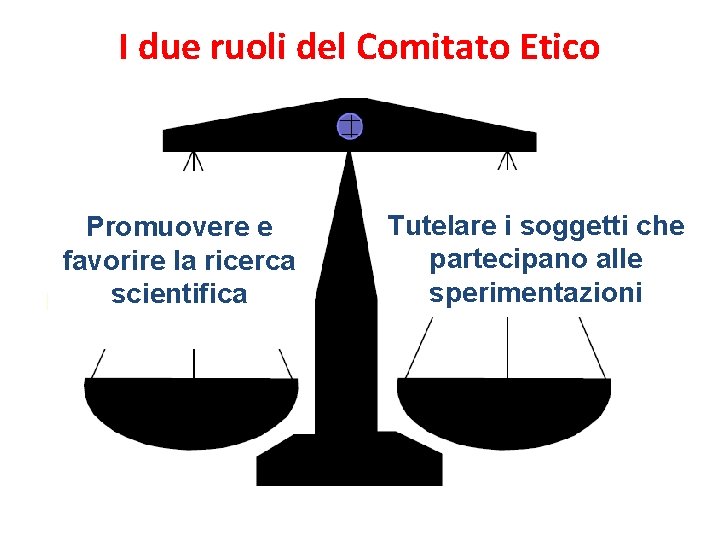
I due ruoli del Comitato Etico Promuovere e favorire la ricerca scientifica Tutelare i soggetti che partecipano alle sperimentazioni

Requisiti etici per una corretta sperimentazione clinica Validità scientifica e valore scientifico della sperimentazione è un aspetto etico Bad science = bad ethics Good science (non sempre) = good ethics La validità scientifica non comporta inevitabilmente l’eticità di una sperimentazione, è necessaria anche una eticità del metodo

ETICITÀ Non è etico effettuare una sperimentazione mal pianificata o mal eseguita Non è etico condurre una sperimentazione che non si preveda possa portare dei benefici reali alla collettività (etica collettiva) Non è etico non assicurare il miglior trattamento a ciascun paziente (etica individuale). E’ necessario che ci sia equipoise (equilibrio) tra i trattamenti a confronto. Sperimentatore e CE devono avere incertezza sui meriti delle terapie utilizzate senza preferenze per una o l’altra
Il dilemma etico

L’informativa e il consenso Ø Valutare adeguatezza e completezza delle informazioni scritte da comunicare ai soggetti da arruolare Ø Valutare le modalità di richiesta del consenso Ø Valutare che sia rispettata la riservatezza come pure la protezione dei dati Ø Adeguatezza delle modalità di informazione al MMG Ø Presenza dei consensi per analisi genetiche o per donazione campioni biologici (meglio separati) Ø Il consenso nelle situazioni di emergenza 3

Va anche considerato che esistono diversi limiti nelle sperimentazioni cliniche. Uno dei principali è la distanza tra il mondo “artificiale” della sperimentazione e quello “reale” della pratica clinica
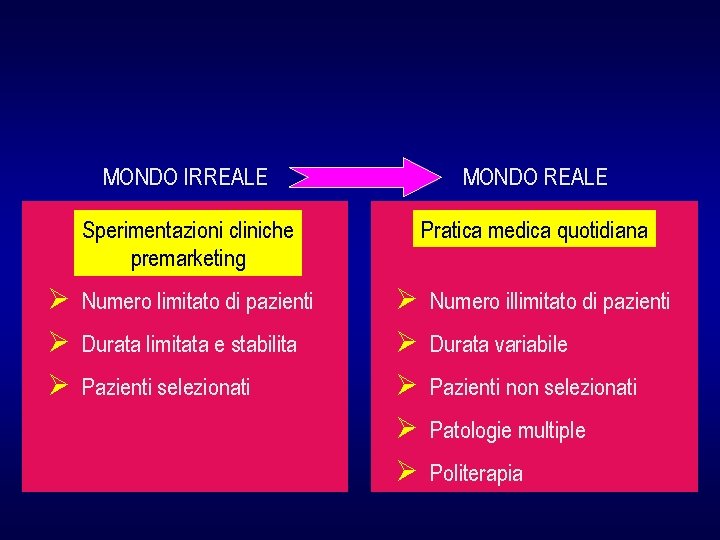
MONDO IRREALE MONDO REALE Sperimentazioni cliniche premarketing Pratica medica quotidiana Ø Numero limitato di pazienti Ø Durata limitata e stabilita Ø Pazienti selezionati Ø Ø Ø Numero illimitato di pazienti Durata variabile Pazienti non selezionati Patologie multiple Politerapia




Valore degli studi osservazionali • Gli studi osservazionali sono indispensabili per approfondire il profilo beneficio-rischio dei farmaci – soprattutto per la sicurezza – con molta più cautela per l’efficacia • Nella decisione su quale disegno utilizzare si fondono aspetti di fattibilità e la possibilità concreta di controllo del confondimento

In ogni caso, al di là dei limiti, i trial clinici controllati randomizzati condotti secondo i criteri esposti rappresentano lo strumento indispensabile per ottenere delle evidenze scientifiche Altre metodiche possono contribuire a questo risultato, ma sono meno “forti” o si basono sui trial clinici controllati randomizzati

Gli studi clinici sono oggetto delle revisioni sistematiche e delle metanalisi • A Systematic Review is a review of a clearly formulated question that uses systematic and explicit methods to identify, select and critically appraise relevant research, and to collect and analyse data from the studies that are included in the review. • Statistical methods (meta-analysis) may or may not be used to analyze and summarize the results of the included studies.

Differences between Narrative Reviews and Systematic Reviews Cook, D. J. et. al. Ann Intern Med 1997; 126: 376 -380

Levels of evidence: 1 A systematic review of RCTs; 1 B individual RCT; 2 A systematic review of cohort studies; 2 B individual cohort study, low-quality RCT; 2 C ecological studies; 3 A systematic review of case-control studies; 3 B individual case-control study; 4 case series, poor-quality studies. http: //www. cebm. net/levels_of_evidence. asp

Tutti, anche se in misura diversa, sono soggetti a bias BIAS n n n Systematic Reviews of Randomized Controlled Trials Cohort Studies and Case Control Studies Case Reports and Case Series, Non-systematic observations § Expert Opinion n

Origine dei farmaci: l’evoluzione nella farmacologia Erbe (molte) e minerali (pochi) Papiro di Ebers, 1500 a. C Le sostanze chimiche VIII secolo Alchimia XVII secolo Protochimica La sintesi chimica dei farmaci XIX secolo nasce l’industria farmaceutica Farmaci biotecnologici XX secolo: scoperta DNA Biologia molecolare Ingegneria genetica Farmacogenetica

Origine dei farmaci I farmaci possono essere NATURALI o di SINTESI I naturali possono essere di origine: • Minerale es. bicarbonato • Vegetale es. digitale • Animale es. insulina • Biologica es. penicillina I sintetici possono essere: Analoghi di sostanze naturali (es. aspirina) Molecole chimiche non presenti in natura (es. diazepam)
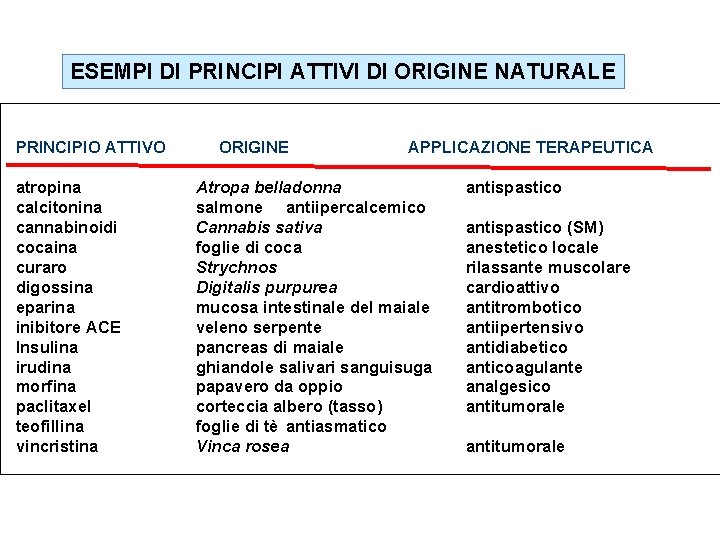
ESEMPI DI PRINCIPI ATTIVI DI ORIGINE NATURALE PRINCIPIO ATTIVO atropina calcitonina cannabinoidi cocaina curaro digossina eparina inibitore ACE Insulina irudina morfina paclitaxel teofillina vincristina ORIGINE APPLICAZIONE TERAPEUTICA Atropa belladonna salmone antiipercalcemico Cannabis sativa foglie di coca Strychnos Digitalis purpurea mucosa intestinale del maiale veleno serpente pancreas di maiale ghiandole salivari sanguisuga papavero da oppio corteccia albero (tasso) foglie di tè antiasmatico Vinca rosea antispastico (SM) anestetico locale rilassante muscolare cardioattivo antitrombotico antiipertensivo antidiabetico anticoagulante analgesico antitumorale

Farmaci biologici e biotecnologici ü I farmaci biologici sono macromolecole (es. proteine, glicoproteine o polisaccaridi) ottenuti mediante procedimenti di produzione diversi dalla sintesi chimica, estraendo il farmaco da fonti biologiche (es. culture di cellule, plasma) ü I farmaci biotecnologici sono una sottocategoria dei farmaci biologici ottenuti mediante processi di estrazione e purificazione a partire da cellule/animali che hanno subito un processo di ingegnerizzazione genetica (inserimento del gene di interesse) o modifica (fusione cellulare, anticorpi monoclonali) di varia entità
Dalla scoperta del DNA alla sua manipolazione
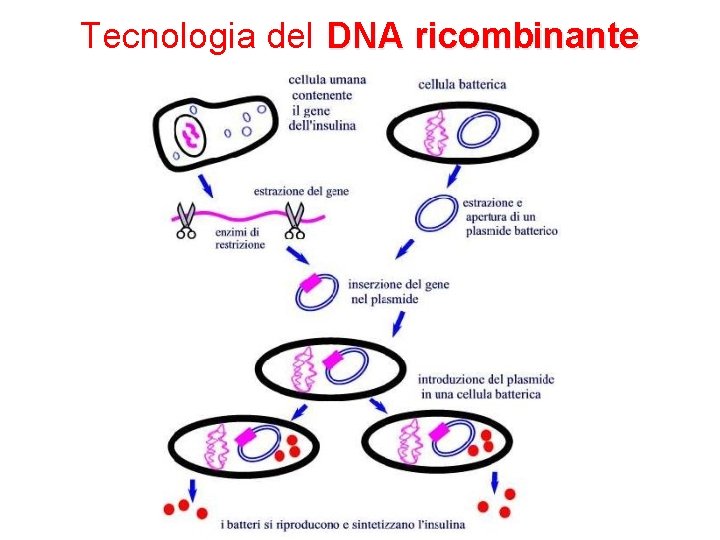
Tecnologia del DNA ricombinante
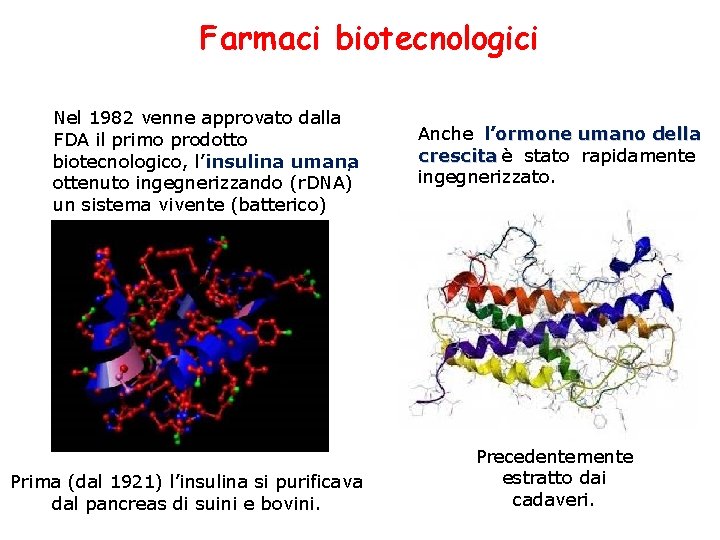
Farmaci biotecnologici Nel 1982 venne approvato dalla FDA il primo prodotto biotecnologico, l’insulina umana , ottenuto ingegnerizzando (r. DNA) un sistema vivente (batterico) Prima (dal 1921) l’insulina si purificava dal pancreas di suini e bovini. Anche l’ormone umano della crescita è stato rapidamente ingegnerizzato. Precedentemente estratto dai cadaveri.

Farmaci biotecnologici

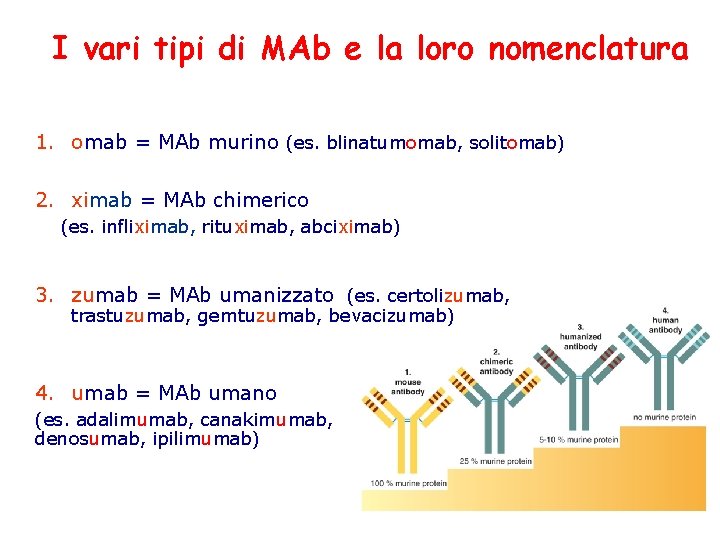
I vari tipi di MAb e la loro nomenclatura 1. omab = MAb murino (es. blinatumomab, solitomab) 2. ximab = MAb chimerico (es. infliximab, rituximab, abciximab) 3. zumab = MAb umanizzato (es. certolizumab, trastuzumab, gemtuzumab, bevacizumab) 4. umab = MAb umano (es. adalimumab, canakimumab, denosumab, ipilimumab)

Applicazione terapeutica dei farmaci biologici ü Ad oggi milioni di pazienti nel mondo hanno già beneficiato di farmaci biologici/biotecnologici approvati per la cura o prevenzione di molte malattie. I più importanti ambiti di applicazione sono: ü Oncologia ü Malattie autoimmuni ü Patologie infiammatorie (in particolare dermatologiche, gastrointestinali, reumatologiche) ü Carenze ormonali ü Deficit proteici/enzimatici ereditari ü I farmaci biotecnologici includono enzimi, ormoni, vaccini, anticorpi monoclonali, citochine, ecc.
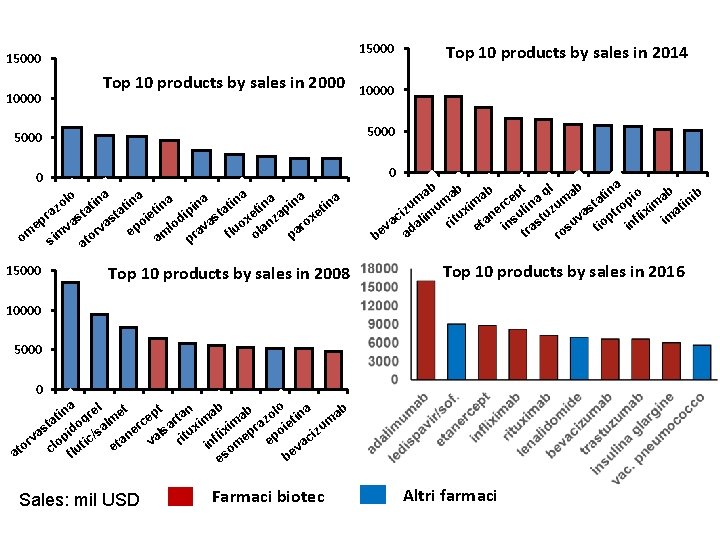
15000 Top 10 products by sales in 2000 10000 5000 0 0 Top 10 products by sales in 2008 15000 a b ept gl ab b in io b t a a um a op ima tini m m im c t n u r i u s l r z z e ci lim itux tan su stu va opt flix ima a u a r v in in tra s ti e ad ro be ab ab as Av og e No n rv as Pr c av ac ho Pr l oz a Zy c pr ex Se a ro xa t r ep ito r lip co zo lo se c a lo ina a a na na ina n i na o i n n t i t i i z t p t a a t ip t e ra st xe xe nza as vas poi o o od va ep r l v r a e flu ola pa om sim ato am pr Top 10 products by sales in 2014 ti Hu n m ir Ri a tu xa n En br e La l n He tus rc ep ti Cr n es to Sp r i Re riva m ica d Gl e ee ve c 15000 Top 10 products by sales in 2016 10000 5000 0 i Ad x va i En r br e Di l ov a Ri n tu Re xan m ica d Ne e xiu Ep m og e Av n as tin av pl Lip ito r a l et pt tan ab ab zolo tina in gre ab t e m m r a m c l i t o a im a r ie u as pid c/sa ne als itux flix epr po iz v c a r e v in om or clo luti va et e at s f b e Sales: mil USD Farmaci biotec Altri farmaci
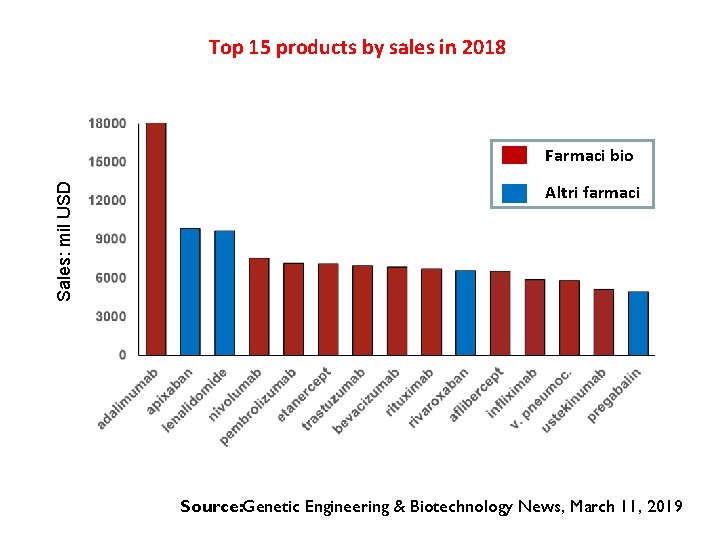
Top 15 products by sales in 2018 Sales: mil USD Farmaci bio Altri farmaci Source: Genetic Engineering & Biotechnology News, March 11, 2019

Medicinale Un medicinale è costituito dal farmaco o principio attivo e da eccipienti (sostanze solide o semisolide quali vaselina, amido, ecc. ) o veicoli (sostanze liquide, quali acqua, olio, alcool, ecc. ). In genere le industrie farmaceutiche commercializzano i farmaci dandogli un nome di fantasia. Esempio: il VALIUM (nome di fantasia) in capsule contiene DIAZEPAM (principio attivo) + amido, talco, lattosio (eccipienti) Un medicinale può essere presente sul mercato sotto forma di diverse confezioni che differiscono tra loro o per la forma farmaceutica (compresse, supposte, sciroppo, iniezioni, ecc. ) e/o per il dosaggio Esempio: il TENORMIN (atenololo, beta-bloccante) Compresse da 100 mg Fiale per somm. endovenosa 5 mg/10 ml


I medicinali possono essere MONOCOMPOSTI, cioè contenere un solo principio attivo o POLICOMPOSTI, cioè contenere più di un principio attivo. Questi ultimi sono anche detti di ASSOCIAZIONE Esempi di medicinali policomposti: BACTRIM (marchio registrato) contiene due principi attivi con attività antibatterica: sulfametossazolo + trimetoprim RIFATER (marchio registrato) contiene tre principi attivi con attività antitubercolare: isoniazide + pirazinamide + rifampicina BLOPRESID (marchio registrato) contiene due principi attivi con attività antiipertensiva: candesartan cilexetil + idroclorotiazide

Medicinale monocomposto Medicinale policomposto
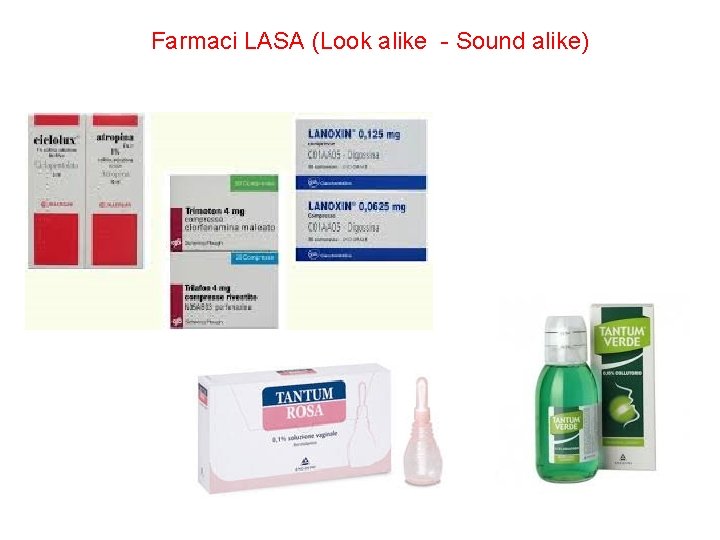
Farmaci LASA (Look alike - Sound alike) 71

Quando entra in commercio un farmaco è di proprietà di una industria farmaceutica che ne detiene il brevetto Il brevetto di un farmaco dura 15 -20 anni

Alla termine del periodo coperto dal brevetto il farmaco può essere prodotto anche da altre ditte come farmaco equivalente (o generico) con la stessa forma farmaceutica e le stessi indicazioni

Il farmaco equivalente può essere venduto sia con un nome di fantasia che con il nome del principio attivo (denominazione comune) seguito dal nome della ditta produttrice. Nella confezione esterna deve però, in ogni caso, comparire la dicitura «Medicinale Equivalente» .

Bioequivalenza Due medicinali si definiscono bioequivalenti se contengono lo stesso principio attivo e, se dopo la somministrazione della stessa dose in identiche condizioni, i loro profili di concentrazione/tempo (biodisponibilità) sono così simili da non comportare differenze significative in termini di efficacia e sicurezza. Gli studi di bioequivalenza si basano sulla biodisponibilità. Gli studi di bioequivalenza sono basati sul confronto di parametri farmacocinetici che caratterizzano la biodisponibilità: Ø concentrazione plasmatica massima (Cmax) Ø tempo necessario per raggiungerla (Tmax) Ø area sotto la curva di concentrazione plasmatica/tempo (AUC).

Anche i farmaci biologici perdono il brevetto. Possono quindi essere prodotti da altre ditte ma devono rifare parte degli studi di efficacia (la produzione è più complessa). Possono però essere venduti con un nuovo nome di specialità medicinale. I generici dei farmaci biologici si chiamano biosimilari

Definizione EMA di biosimilare “un medicinale che contiene una versione copia di un medicinale biologico già autorizzato (medicinale di riferimento) nell'Unione Europea con dimostrata somiglianza in termini di qualità, attività biologica, sicurezza ed efficacia effettuata sulla base di un esercizio di comparabilità (comparability exercise)” European Medicines Agency (EMA). Guideline on Similar Biological Medicinal Products. CHMP/437/04 Rev 1; 23 ottobre 2014.

Perchèbiosimilarie non bioequivalenti Ø La variabilità che caratterizza le varie fasi del processo di biosintesi e l’elevata complessità strutturale dei prodotti biotecnologici rendono molto difficili: La riproducibilitàdel prodotto La dimostrazione , attraverso i metodi utilizzati per i farmaci chimici, che un biosimilare sia biologicamentee funzionalmenteequivalente all’originatore Copie esatte sono impossibili Genazzani AA et al. (2007) Biodrugs 21: 351

Biosimilari approvati in Europa fino al 25/10/2019 62 Biosimilari autorizzati (5 ritirati) per 16 principi attivi

Perché usare un farmaco equivalente (generico) o biosimilare invece del farmaco «originatore» ?

Il risparmio! Chemical drugs Biological products Generics: Biosimilars: 70% less 20 -30 % less

La normativa europea e nazionale in materia di farmaco prevede che i medicinali immessi in circolazione nella Comunità Europea siano accompagnati da un’etichetta e da un foglio illustrativo contenenti informazioni, comprensibili agli utenti, per consentire l'uso appropriato e sicuro del medicinale.

Il foglietto illlustrativo üIl Foglio Illustrativo (FI) è un documento che contiene tutte le informazioni utili per un impiego sicuro e corretto di un farmaco; üLe informazioni riportate nel FI sono in linea con le informazioni riportate nel Riassunto delle Caratteristiche del Prodotto (RCP); tali informazioni rappresentano l’insieme delle caratteristiche proprie del farmaco come documentato nel dossier presentato dalle Aziende farmaceutiche alle Autorità Competenti ai fini dell’Autorizzazione all’Immissione in Commercio (AIC) di un farmaco;


Il foglietto illustrativo include informazioni su: ll nome commerciale del medicinale, la composizione (principio attivo+eccipienti), il dosaggio e la forma farmaceutica Servono a identificare univocamente il prodotto e non correre il rischio di assumere un farmaco o un dosaggio errato. Inoltre l’elenco degli eccipienti consente di evitare il rischio di reazione allergica a uno di loro. La categoria farmacoterapeutica o il tipo di attività e le indicazioni terapeutiche Indicano le diverse malattie (o i gruppi di malattie) per cui il farmaco è indicato.

Il foglietto illustrativo include informazioni su: Le controindicazioni Indicano le condizioni per le quali il farmaco non deve essere assunto. Le precauzioni d'uso Indicano in quali casi il farmaco può essere assunto ma con attenzione. Le interazioni con altri medicinali e sostanze Indicano quali medicinali o alimenti possono modificare l’effetto del medicinale. Le avvertenze speciali Informazioni sull’utilizzo in casi particolari.

Il foglietto illustrativo include informazioni su: La posologia, il modo e il tempo di somministrazione Indicano il dosaggio, la frequenza e la durata della somministrazione. Talvolta, se necessario, è espresso anche il momento appropriato in cui il medicinale può o deve essere somministrato (prima o dopo i pasti, per esempio). Sovradosaggio Vengono descritti i sintomi per riconoscere gli effetti dell’assunzione di una dose eccessiva di farmaco e le misure di primo soccorso. Effetti indesiderati Indicano i possibili effetti negativi che si possono verificare anche con il normale uso del medicinale e le misure da adottare

Il foglietto illustrativo include informazioni su: Scadenza e conservazione Informazioni sulla modalità di conservazione del farmaco (temperatura, umidità, etc). E’ opportuno controllare sempre la data di scadenza stampata sulla confezione che si riferisce al farmaco integro, correttamente conservato. Data di ultima revisione Ultima data di revisione del foglietto da parte dell’Agenzia del farmaco. Tutti i foglietti illustrativi vengono periodicamente rivalutati e aggiornati dall’autorità regolatoria I foglietti illustrativi dei farmaci sono consultabili su internet (sito dell’AIFA, EMA, o siti privati come Torrinomedica, mypersonal trainer o altri)


I numeri del mercato farmaceutico italiano Principi attivi (circa 2500) Medicinali (circa 9000) Confezione di medicinali (circa 18. 000)

I numeri del mercato farmaceutico italiano Principi attivi (circa 2500) Specialità medicinali (circa 9000) Confezione di medicinali (circa 18. 000) AIFA. L’uso dei farmaci in Italia. Rapporto Nazionale 2018
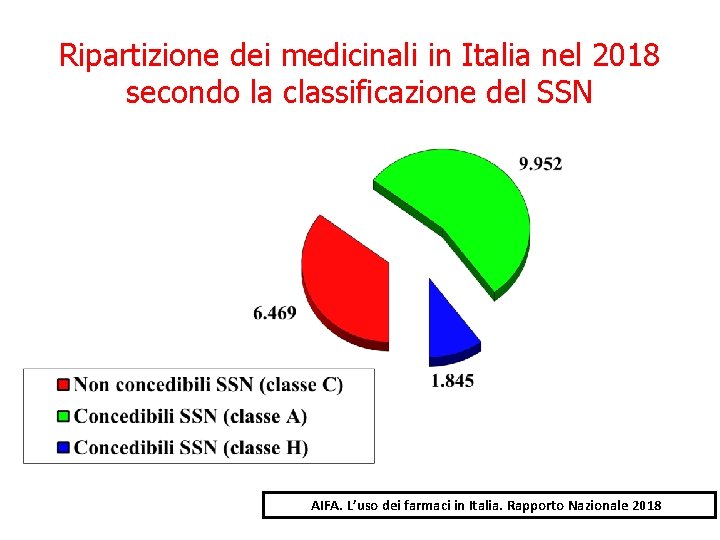
Ripartizione dei medicinali in Italia nel 2018 secondo la classificazione del SSN AIFA. L’uso dei farmaci in Italia. Rapporto Nazionale 2018


I farmaci di autoprescrizione ü I farmaci di automedicazioni riportano sulla scatola un bollino
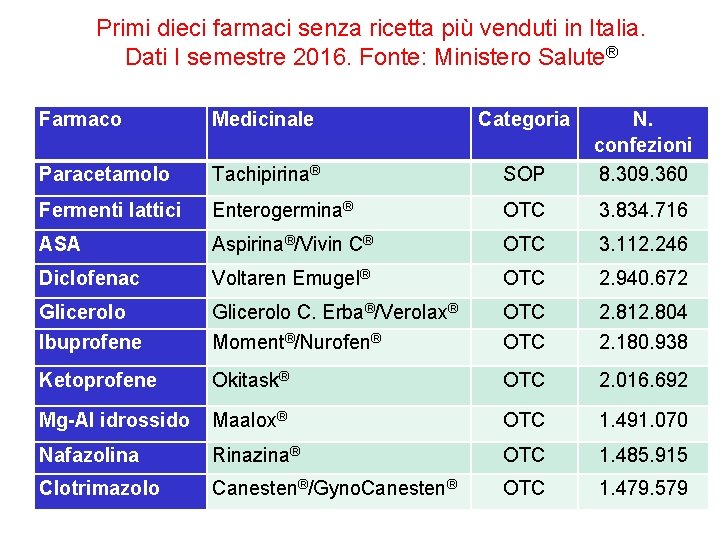
Primi dieci farmaci senza ricetta più venduti in Italia. Dati I semestre 2016. Fonte: Ministero Salute® Farmaco Medicinale Categoria Paracetamolo Tachipirina® SOP N. confezioni 8. 309. 360 Fermenti lattici Enterogermina® OTC 3. 834. 716 ASA Aspirina®/Vivin C® OTC 3. 112. 246 Diclofenac Voltaren Emugel® OTC 2. 940. 672 Glicerolo C. Erba®/Verolax® OTC 2. 812. 804 Ibuprofene Moment®/Nurofen® OTC 2. 180. 938 Ketoprofene Okitask® OTC 2. 016. 692 Mg-Al idrossido Maalox® OTC 1. 491. 070 Nafazolina Rinazina® OTC 1. 485. 915 Clotrimazolo Canesten®/Gyno. Canesten® OTC 1. 479. 579

AIFA L’uso dei Farmaci in Italia Rapporto nazionale anno 2018







Riepilogo di farmacocinetica

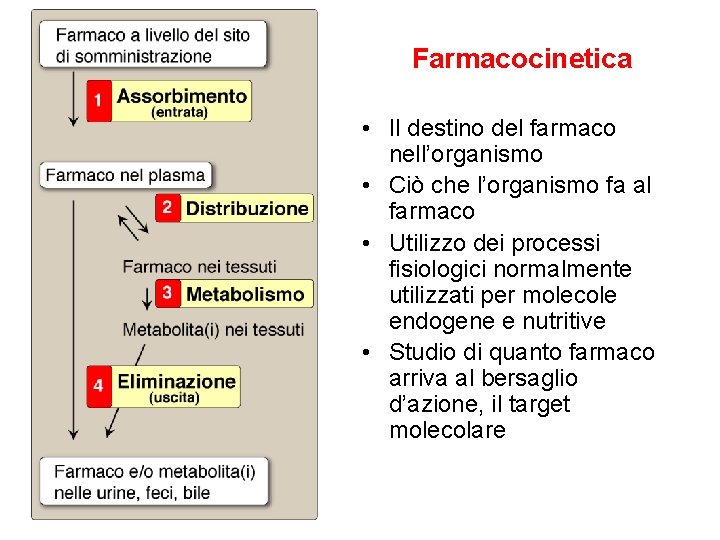
Farmacocinetica • Il destino del farmaco nell’organismo • Ciò che l’organismo fa al farmaco • Utilizzo dei processi fisiologici normalmente utilizzati per molecole endogene e nutritive • Studio di quanto farmaco arriva al bersaglio d’azione, il target molecolare
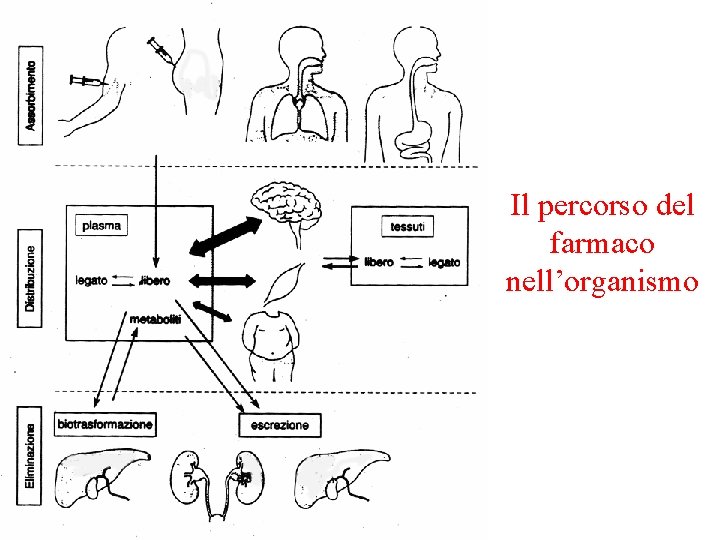
Il percorso del farmaco nell’organismo
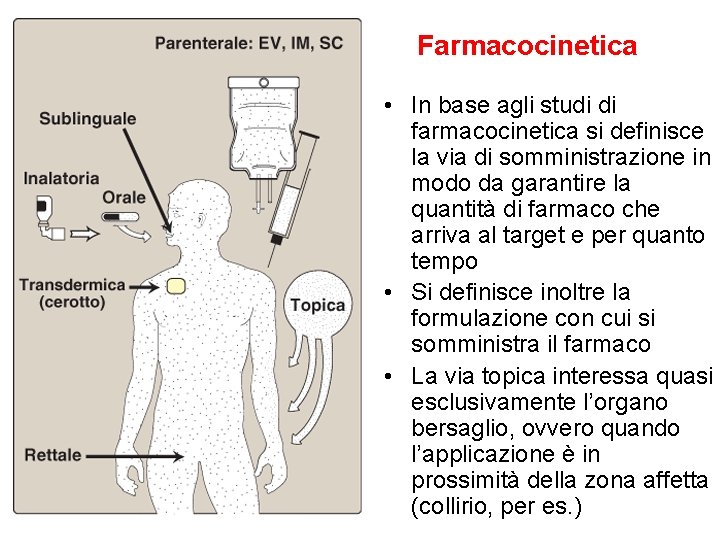
Farmacocinetica • In base agli studi di farmacocinetica si definisce la via di somministrazione in modo da garantire la quantità di farmaco che arriva al target e per quanto tempo • Si definisce inoltre la formulazione con cui si somministra il farmaco • La via topica interessa quasi esclusivamente l’organo bersaglio, ovvero quando l’applicazione è in prossimità della zona affetta (collirio, per es. )
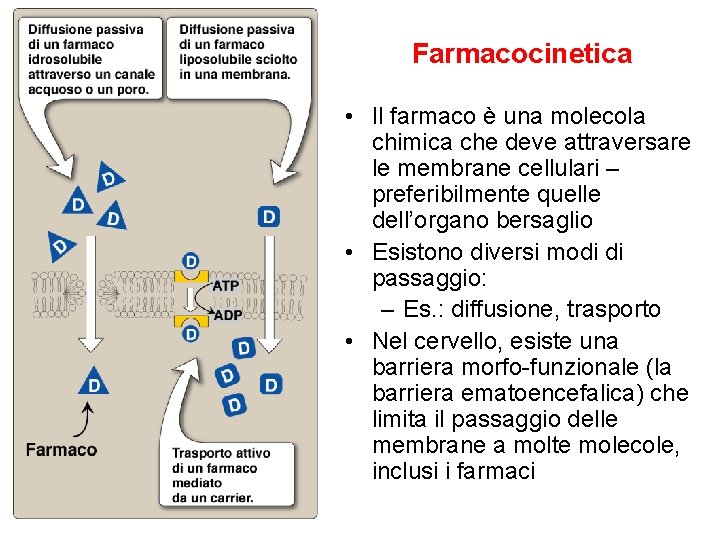
Farmacocinetica • Il farmaco è una molecola chimica che deve attraversare le membrane cellulari – preferibilmente quelle dell’organo bersaglio • Esistono diversi modi di passaggio: – Es. : diffusione, trasporto • Nel cervello, esiste una barriera morfo-funzionale (la barriera ematoencefalica) che limita il passaggio delle membrane a molte molecole, inclusi i farmaci
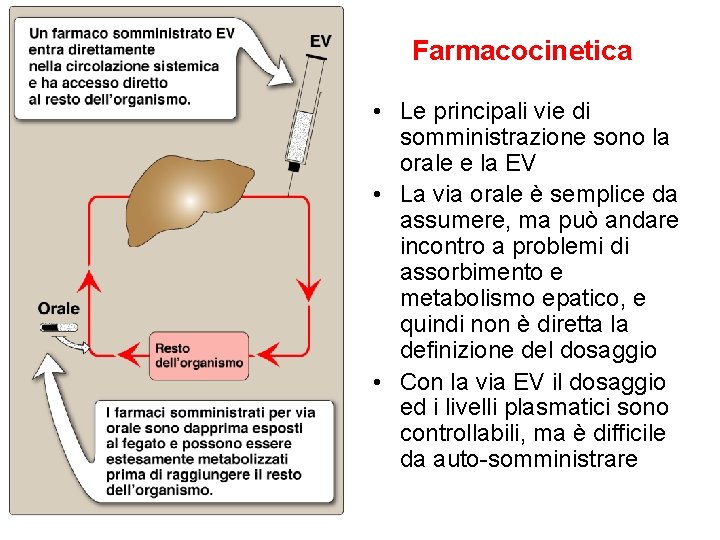
Farmacocinetica • Le principali vie di somministrazione sono la orale e la EV • La via orale è semplice da assumere, ma può andare incontro a problemi di assorbimento e metabolismo epatico, e quindi non è diretta la definizione del dosaggio • Con la via EV il dosaggio ed i livelli plasmatici sono controllabili, ma è difficile da auto-somministrare

Farmaci e cibo Ø In generale la somministrazione di un farmaco per os lontana dai pasti comporta un assorbimento più rapido e completo. Ø La somministrazione in vicinanza dei pasti può limitare i fenomeni irritativi alle mucose. Ø Alcuni farmaci possono interagire con determinati alimenti, ad esempio le tetracicline (antibatterici) si legano al calcio contenuto nel latte (o formaggi) e questo impedisce il loro assorbimento. Ø Per somministrazione prima dei pasti si intende: da 30 a 0 minuti prima del pasto Ø Per somministrazione dopo i pasti si intende: entro 30 minuti dopo il pasto Ø Per somministrazione lontano dai pasti si intende: 3 -4 ore prima o dopo il pasto

Farmacocinetica • La concentrazione plasmatica di un farmaco è sempre in equilibrio cinetico con la quantità nei tessuti • Misurare i livelli plasmatici permette di sapere quanto farmaco è disponibile • Nella EV, la relazione tra dose e livello plasmatico è diretta • Nella via orale, è al netto della quantità assorbita e metabolizzata
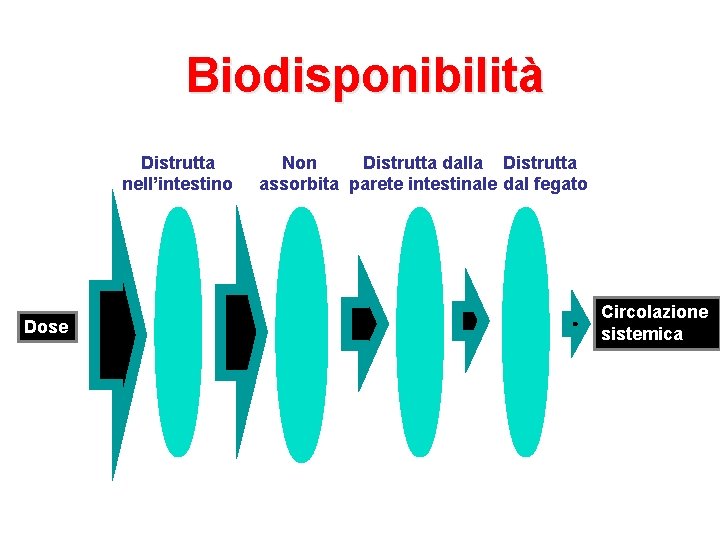
Biodisponibilità Distrutta nell’intestino Dose Non Distrutta dalla Distrutta assorbita parete intestinale dal fegato Circolazione sistemica
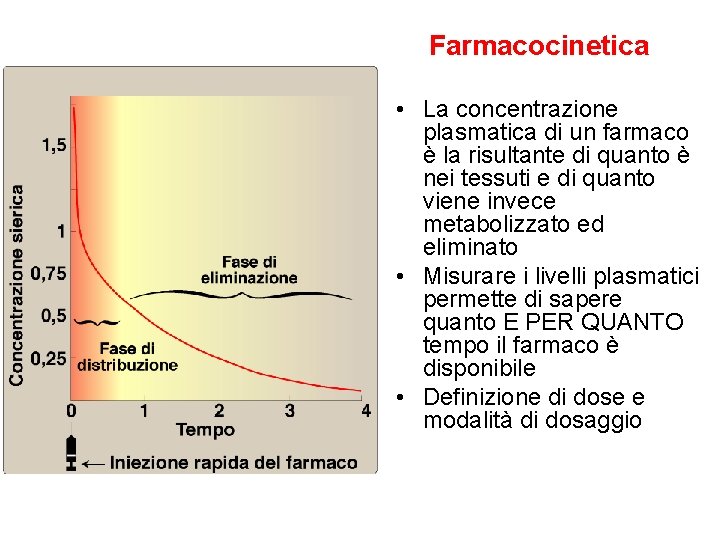
Farmacocinetica • La concentrazione plasmatica di un farmaco è la risultante di quanto è nei tessuti e di quanto viene invece metabolizzato ed eliminato • Misurare i livelli plasmatici permette di sapere quanto E PER QUANTO tempo il farmaco è disponibile • Definizione di dose e modalità di dosaggio

DISTRIBUZIONE DEI FARMACI NELL’ORGANISMO Il processo di distribuzione di un farmaco dal sangue ai diversi compartimenti dell’organismo è influenzato da diversi fattori: Ø Caratteristiche chimico-fisiche del farmaco (in particolare la sua liposolubilità) Ø Vascolarizzazione degli organi (un farmaco raggiunge più velocemente gli organi maggiormente perfusi dal sangue, quali cuore, encefalo, fegato e rene, ricevono il farmaco) Ø Percentuale di farmaco legato alle proteine plasmatiche Ø Presenza di particolari strutture anatomico/funzionali (barriera placentare, barriera emato-encefalica)

Le Barriere!
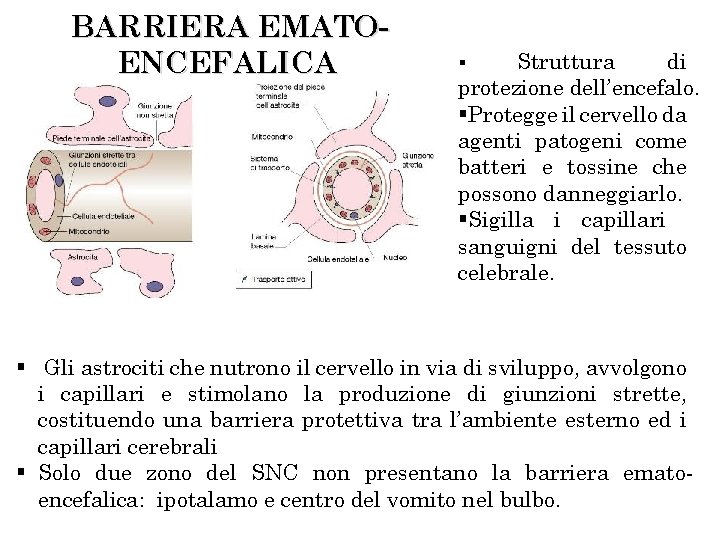
BARRIERA EMATOENCEFALICA Struttura di protezione dell’encefalo. §Protegge il cervello da agenti patogeni come batteri e tossine che possono danneggiarlo. §Sigilla i capillari sanguigni del tessuto celebrale. § § Gli astrociti che nutrono il cervello in via di sviluppo, avvolgono i capillari e stimolano la produzione di giunzioni strette, costituendo una barriera protettiva tra l’ambiente esterno ed i capillari cerebrali § Solo due zono del SNC non presentano la barriera ematoencefalica: ipotalamo e centro del vomito nel bulbo.

BARRIERA PLACENTARE Placenta: organo discoidale di origine mista (fetale/materna) per scambi e nutrizione dell’embrione e del feto. Protegge il feto da sostanze nocive presenti nel sangue materno, ma deve garantire il passaggio di numerose sostanze; processi di trasporto attivo consentono il passaggio di sostanze nutritive e vitamine dalla madre al feto. Consiste di numerosi strati di cellule, Barriera placentare interposte tra la circolazione fetale e materna, che variano con il periodo di gestazione setto placentare strato spugnoso strato limitante vasi materni villo trofoblasto amnios corion seno marginale vasi ombelicali cordone ombelicale

METABOLISMO O BIOTRASFORMAZIONE DEI FARMACI Ø Con il termine metabolismo si intendono le modificazioni chimiche un farmaco subisce nell’organismo. Ø Sede principale dei processi metabolici è il FEGATO per l’azione degli enzimi microsomiali delle cellule epatiche. Ø Altre importanti sedi di metabolizzazione sono il rene, il polmone, l’intestino (anche per azione della flora batterica), il plasma.

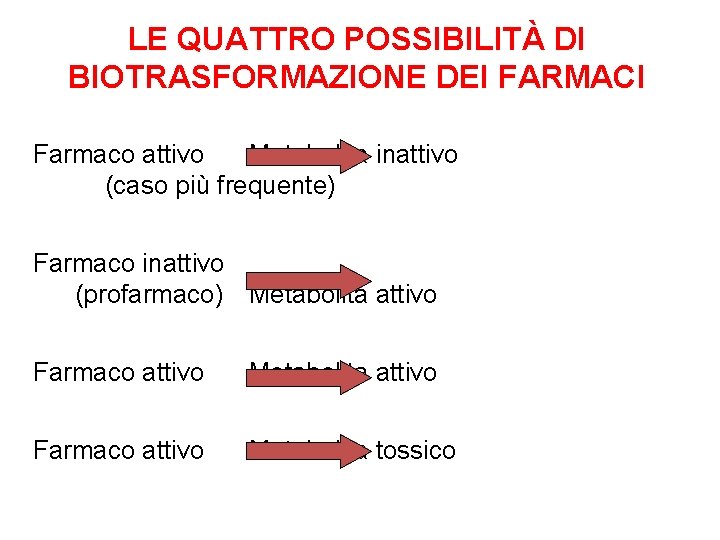
LE QUATTRO POSSIBILITÀ DI BIOTRASFORMAZIONE DEI FARMACI Farmaco attivo Metabolita inattivo (caso più frequente) Farmaco inattivo (profarmaco) Metabolita attivo Farmaco attivo Metabolita tossico


ESCREZIONE DEI FARMACI Ø La principale via di escrezione dei farmaci (e dei loro metaboliti) è il RENE Ø Altre vie di escrezione possono essere la VIA RESPIRATORIA, ad esempio per i farmaci gassosi o la VIA BILIARE (escrezione con le feci) Ø I farmaci che vengono eliminati tramite la bile possono venire in parte riassorbiti a livello intestinale: si viene cosi a creare il cosidetto CIRCOLO ENTERO-EPATICO Ø Altra via di escrezione dei farmaci è rappresentata dal LATTE MATERNO. Questo fatto deve essere tenuto in considerazione quando si prescrivono farmaci a madri che allattano, per i possibili rischi di tossicità a cui si può esporre il neonato Ø Fattori che possono modificare l’escrezione dei farmaci, con possibile ACCUMULO, sono: presenza di patologie renali (insufficienza renale), l’età del paziente (neonati e anziani), ostacolo al deflusso biliare (per farmaci eliminati per questa via).
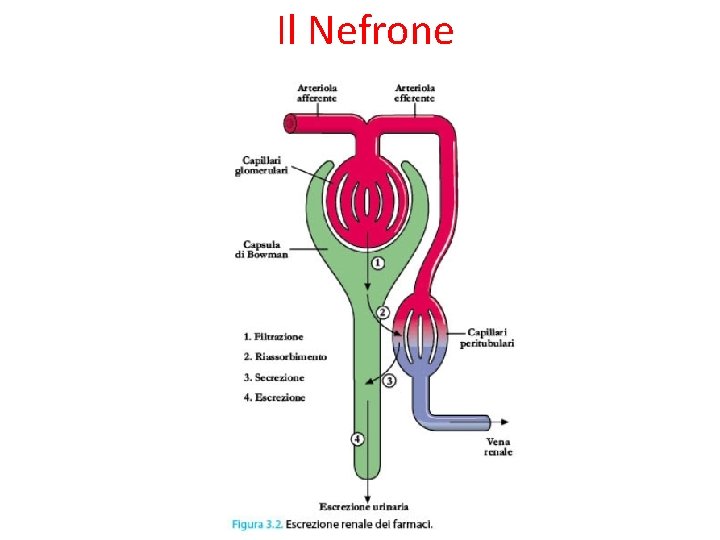
Il Nefrone
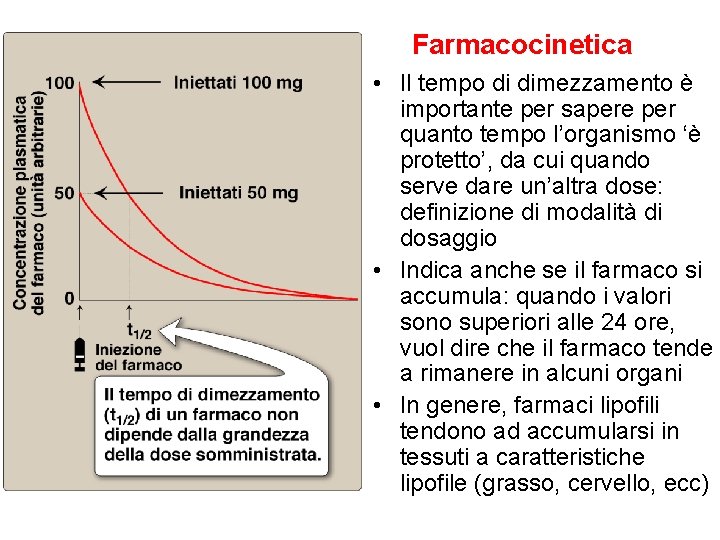
Farmacocinetica • Il tempo di dimezzamento è importante per sapere per quanto tempo l’organismo ‘è protetto’, da cui quando serve dare un’altra dose: definizione di modalità di dosaggio • Indica anche se il farmaco si accumula: quando i valori sono superiori alle 24 ore, vuol dire che il farmaco tende a rimanere in alcuni organi • In genere, farmaci lipofili tendono ad accumularsi in tessuti a caratteristiche lipofile (grasso, cervello, ecc)
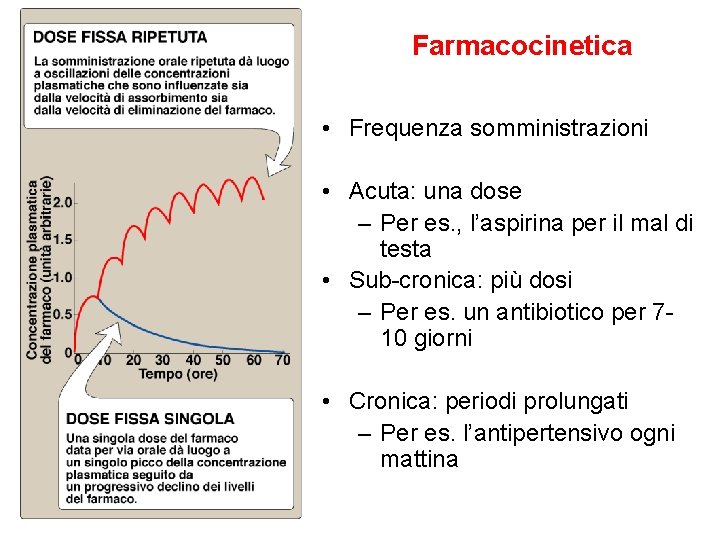
Farmacocinetica • Frequenza somministrazioni • Acuta: una dose – Per es. , l’aspirina per il mal di testa • Sub-cronica: più dosi – Per es. un antibiotico per 710 giorni • Cronica: periodi prolungati – Per es. l’antipertensivo ogni mattina
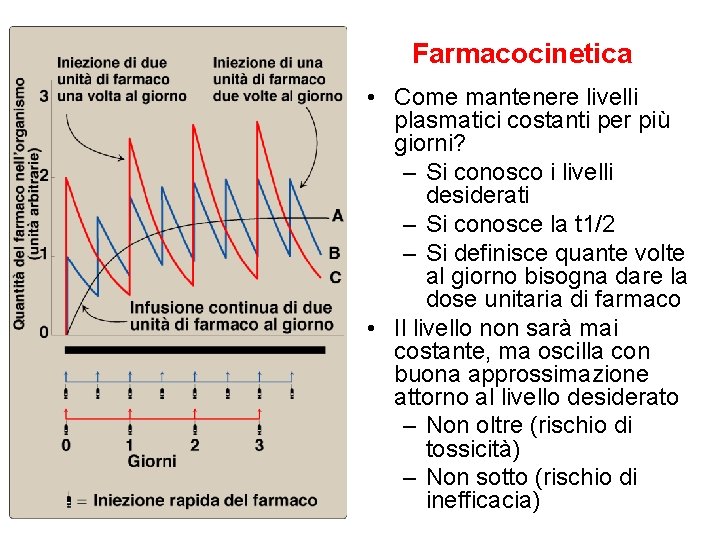
Farmacocinetica • Come mantenere livelli plasmatici costanti per più giorni? – Si conosco i livelli desiderati – Si conosce la t 1/2 – Si definisce quante volte al giorno bisogna dare la dose unitaria di farmaco • Il livello non sarà mai costante, ma oscilla con buona approssimazione attorno al livello desiderato – Non oltre (rischio di tossicità) – Non sotto (rischio di inefficacia)
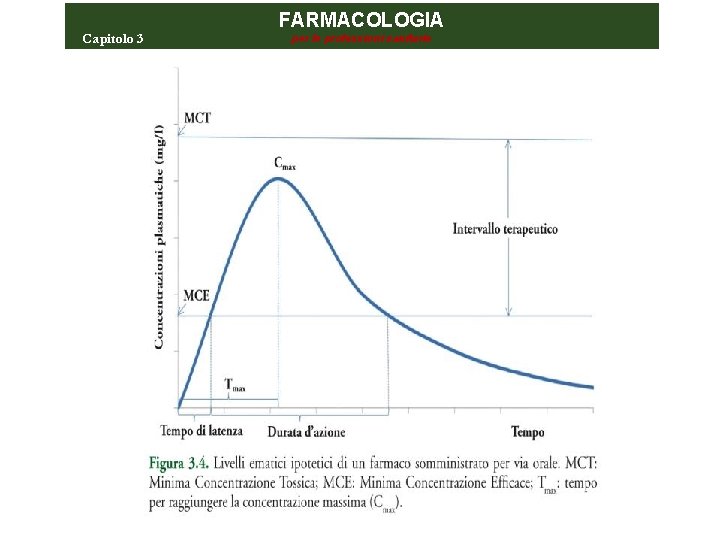
Capitolo 3 FARMACOLOGIA per le professioni sanitarie

Riepilogo di farmacodinamica


I FARMACI POSSONO ESSERE SUDDIVISI IN BASE AL TIPO DI EFFETTO/USO TERAPEUTICO ALCUNI ESEMPI SOSTITUTIVI insulina, ormoni tiroidei PREVENTIVI vaccini CURATIVI antibatterici, antitumorali SINTOMATICI FANS, benzodiazepine, antiipertensivi DIAGNOSTICI solfato di bario, tolbutamide, mezzi di contrasto

FARMACODINAMICA Le azioni di un farmaco possono essere suddivise, in base alla sede in cui si esplicano, in: AZIONE LOCALE che si esplica nella sede di applicazione del farmaco (esempi: antibatterico per le infezioni intestinali; antimicotico vaginale; creme e pomate dermatologiche; antiacidi; anestetici locali; ecc. ), non è quindi necessario che il farmaco venga assorbito (anzi l’assorbimento pone fine all’azione terapeutica del farmaco) AZIONE SISTEMICA O GENERALE che si esplica in una sede distante da quella di applicazione del farmaco è quindi necessario che il farmaco venga assorbito e passi nel circolo sanguigno

FARMACODINAMICA In linea generale si può affermare che i farmaci agiscono stimolando o bloccando funzioni presenti nell’organismo umano. I meccanismi d’azione dei farmaci si possono così ridurre schematicamente a: STIMOLAZIONE di una funzione dell’organismo (ad esempio la digitale che aumenta la forza di contrazione del miocardio) DEPRESSIONE di una funzione (ad esempio gli anestetici che deprimono le funzioni del SNC) SOSTITUZIONE o supplemento di una attività funzionale mancante o carente (es. insulina nel diabete o tiroxina nell’ipotiroidismo) ELIMINAZIONE di agenti infettivi (antibiotici, antimicotici, antivirali, antiparassitari) o di cellule tumorali (antitumorali)
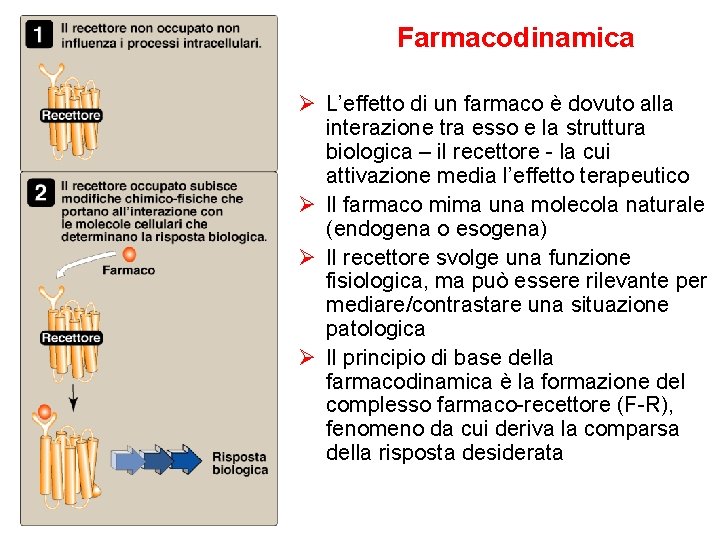
Farmacodinamica Ø L’effetto di un farmaco è dovuto alla interazione tra esso e la struttura biologica – il recettore - la cui attivazione media l’effetto terapeutico Ø Il farmaco mima una molecola naturale (endogena o esogena) Ø Il recettore svolge una funzione fisiologica, ma può essere rilevante per mediare/contrastare una situazione patologica Ø Il principio di base della farmacodinamica è la formazione del complesso farmaco-recettore (F-R), fenomeno da cui deriva la comparsa della risposta desiderata

I bersagli dei farmaci sono molteplici! BERSAGLI DEI FARMACI: Esempi 1. Recettori classici Benzodiazepine, oppioidi 2. Enzimi Aspirina, digitale 3. Canali ionici Calcio-antagonisti 4. Proteine strutturali Antidepressivi 5. Acidi nucleici Cisplatino


Alcuni (pochi) farmaci non hanno recettore/bersaglio



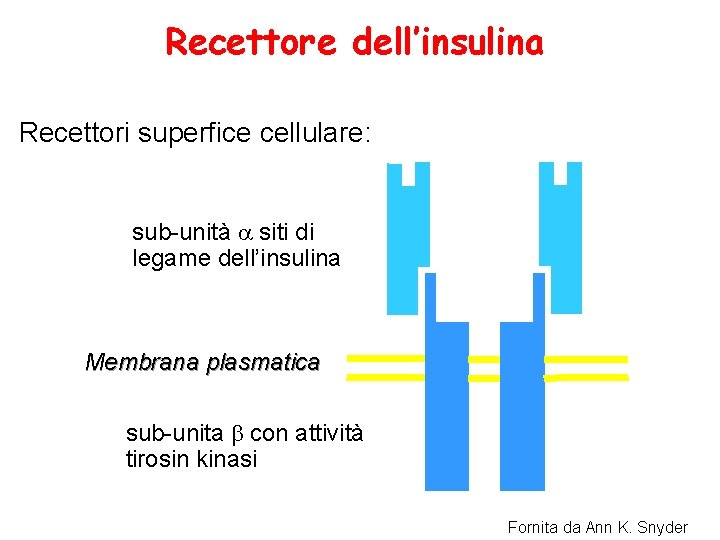
Recettore dell’insulina Recettori superfice cellulare: sub-unità a siti di legame dell’insulina Membrana plasmatica sub-unita b con attività tirosin kinasi Fornita da Ann K. Snyder
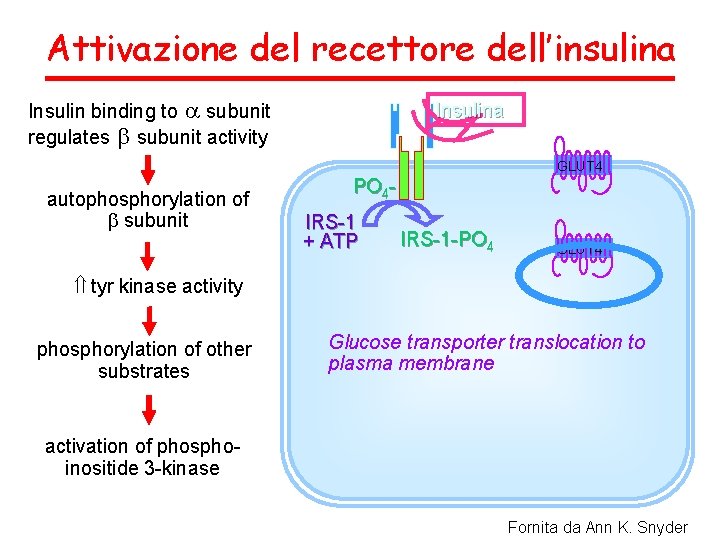
Attivazione del recettore dell’insulina Insulin binding to a subunit regulates b subunit activity Insulina GLUT 4 autophosphorylation of b subunit PO 4 IRS-1 + ATP IRS-1 -PO 4 GLUT 4 tyr kinase activity phosphorylation of other substrates Glucose transporter translocation to plasma membrane activation of phosphoinositide 3 -kinase Fornita da Ann K. Snyder
EBM 08

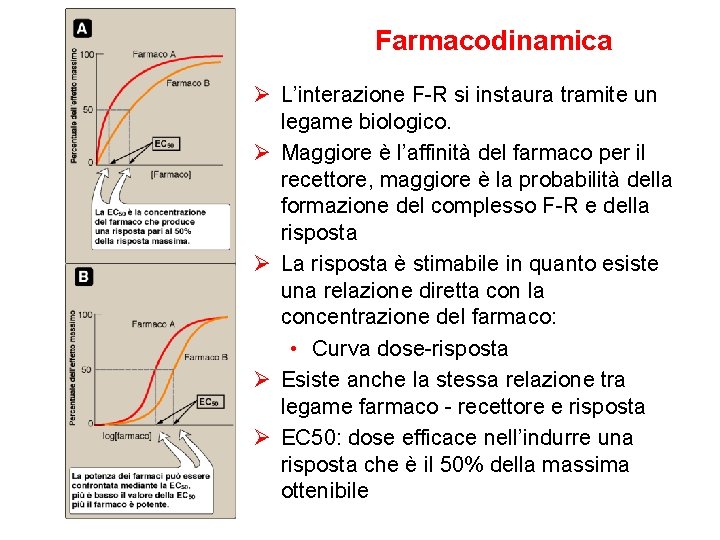
Farmacodinamica Ø L’interazione F-R si instaura tramite un legame biologico. Ø Maggiore è l’affinità del farmaco per il recettore, maggiore è la probabilità della formazione del complesso F-R e della risposta Ø La risposta è stimabile in quanto esiste una relazione diretta con la concentrazione del farmaco: • Curva dose-risposta Ø Esiste anche la stessa relazione tra legame farmaco - recettore e risposta Ø EC 50: dose efficace nell’indurre una risposta che è il 50% della massima ottenibile

FARMACODINAMICA Si definisce AGONISTA un farmaco che legandosi ad un recettore provoca una risposta biologica. Esempi di farmaci agonisti: morfina (analgesico oppioide), benzodiazepine (sedativi-ipnotici), adrenalina (anti-anafilassi, stimolante cardiaco), salmeterolo (antiasmatico), nafazolina (decongestionante nasale), dopamina (analettico centrale, utilizzato negli stati di shock), desmopressina (ormone ipofisario), ecc ANTAGONISTA è un farmaco che legandosi ad un recettore NON provoca una risposta biologica, può tuttavia avere un effetto impedendo il legame a quel recettore, di una sostanza endogena. Esempi di farmaci antagonisti: atropina (midiatrico), metoprololo (antiipertensivo, antiaritmico), naloxone (per il sovradosaggio da oppioidi), domperidone (procinetico), metoclopramide (procinetico), losartan (antiipertensivo), ecc.
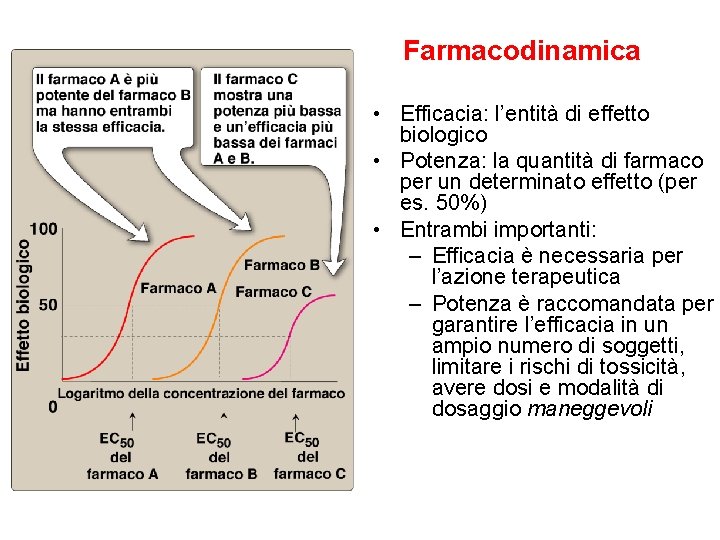
Farmacodinamica • Efficacia: l’entità di effetto biologico • Potenza: la quantità di farmaco per un determinato effetto (per es. 50%) • Entrambi importanti: – Efficacia è necessaria per l’azione terapeutica – Potenza è raccomandata per garantire l’efficacia in un ampio numero di soggetti, limitare i rischi di tossicità, avere dosi e modalità di dosaggio maneggevoli
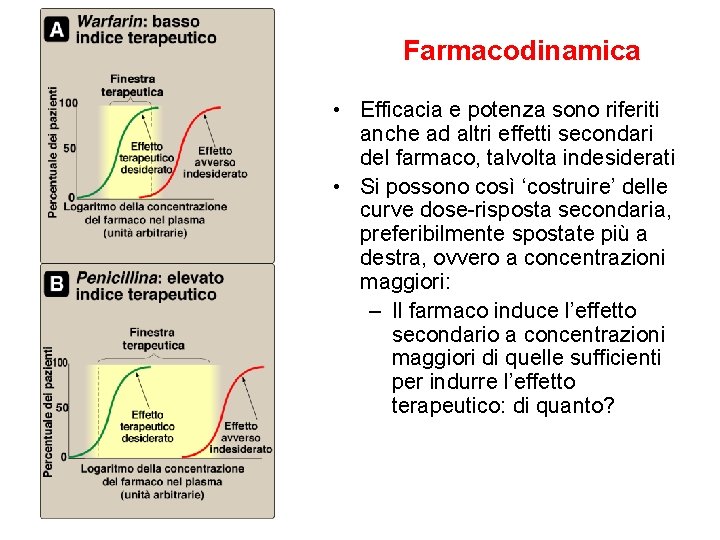
Farmacodinamica • Efficacia e potenza sono riferiti anche ad altri effetti secondari del farmaco, talvolta indesiderati • Si possono così ‘costruire’ delle curve dose-risposta secondaria, preferibilmente spostate più a destra, ovvero a concentrazioni maggiori: – Il farmaco induce l’effetto secondario a concentrazioni maggiori di quelle sufficienti per indurre l’effetto terapeutico: di quanto?
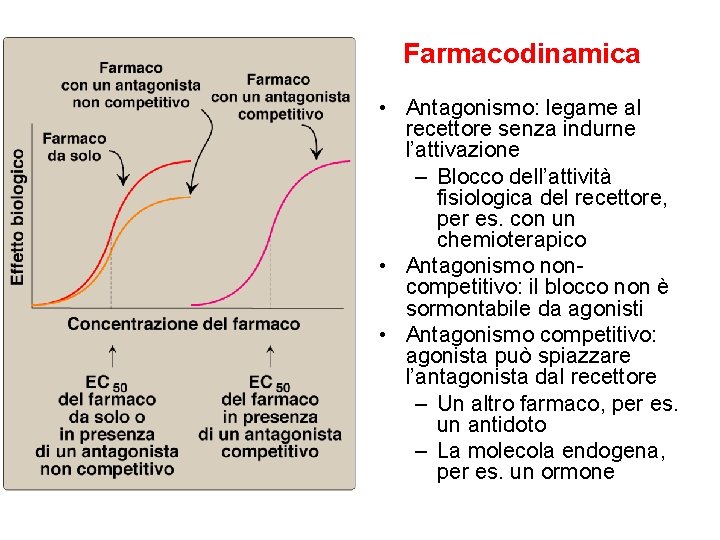
Farmacodinamica • Antagonismo: legame al recettore senza indurne l’attivazione – Blocco dell’attività fisiologica del recettore, per es. con un chemioterapico • Antagonismo noncompetitivo: il blocco non è sormontabile da agonisti • Antagonismo competitivo: agonista può spiazzare l’antagonista dal recettore – Un altro farmaco, per es. un antidoto – La molecola endogena, per es. un ormone

Adattamento Modulazione della risposte recettoriali v Controllo a livello della produzione e della degradazione del mediatore v La capacità di trasdurre il segnale è controllata v DESENSITIZZAZIONE v UP - REGULATION riduzione della capacità di un recettore di trasdurre il segnale, anche se legato all’agonista v DOWN - REGULATION

Usare farmaci con meccanismo d’azione diverso per ottenere uno stesso effetto. Esempio: gli antipertensivi Fattori implicati nella regolazione della pressione arteriosa
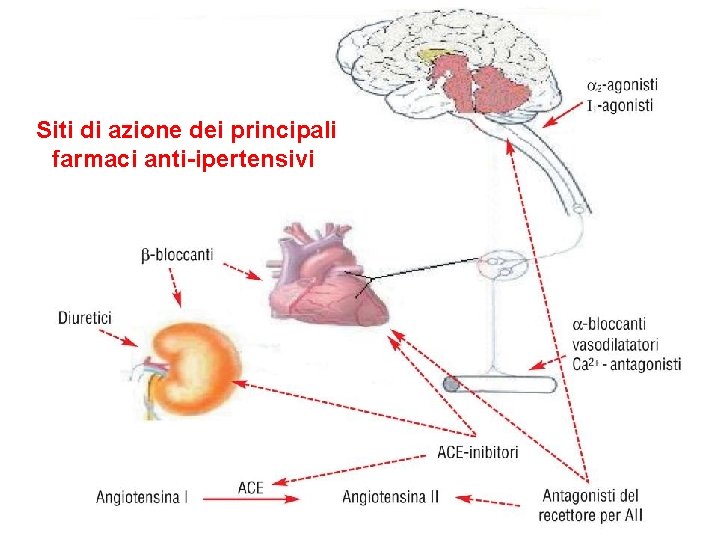
Siti di azione dei principali farmaci anti-ipertensivi

Reazioni avverse da farmaci

INDICE TERAPEUTICO Ø L’indice terapeutico di un farmaco è rappresentato dal numero derivante dal rapporto tra la dose tossica e la dose terapeutica. Ø Ad esempio per un farmaco che ha una dose tossica di 10 grammi ed una dose terapeutica di 2 grammi: Ø Risulta evidente che quanto più l’indice terapeutico di un farmaco è basso (vicino all’unità) tanto più ristretto è il margine di sicurezza nel dosaggio del farmaco.

INDICE TERAPEUTICO Ø L’indice terapeutico non rappresenta la valutazione di un farmaco dal punto di vista dell’efficacia e/o della tollerabilità ma ci indica soltanto la vicinanza o meno della dose tossica rispetto a quella terapeutica. Ø Farmaci con un basso indice terapeutico (ad esempio antiepilettici, teofillina, aminoglicosidi, antitumorali, warfarin) devono essere monitorati. Il monitoraggio si può effettuare direttamente, cioè prelevando dei campioni di sangue e determinando la quantità di farmaco presente, o indirettamente attraverso dei parametri di laboratorio, ad esempio per il warfarin o altri anticoagulanti misurando il tempo di coagulazione del sangue. In base ai risultati ottenuti si aggiusta la dose da somministrare.

RAPPORTO RISCHIO/BENEFICIO Ø La valutazione clinica di un farmaco è un processo complesso non esprimibile con un semplice rapporto tra dose tossica e dose terapeutica (indice terapeutico). Si tratta, infatti, di esprimere un giudizio valutando da una parte i benefici che si ottengono e dall’altra i rischi che si corrono utilizzando il farmaco (rapporto beneficio/rischio). Ø Per stabilire un corretto rapporto beneficio/rischio per un farmaco è necessario conoscere i benefici che si ottengono (quindi conoscere i dati sulla sua efficacia clinica) e i rischi derivanti dal suo uso (quindi conoscere i suoi effetti avversi). Ø Bisogna tenere presente che il rapporto beneficio/rischio di un farmaco può essere diverso a seconda del paziente e/o della patologia da trattare. Quindi in certe situazioni un farmaco, che ha in generale un rapporto beneficio/rischio favorevole (cioè i benefici superano i rischi), potrebbe avere un rapporto sfavorevole (i rischi superano i benefici).

Conoscere per una migliore definizione del rapporto benefici/rischi Efficacia clinica Reazioni avverse

REAZIONI AVVERSE DA FARMACI REAZIONE AVVERSA DA FARMACI DEFINIZIONE DELL’EMA (Direttiva 2010/84/EU del Parlamento e del Consiglio Europeo) Una risposta ad un medicinale che provoca danno e che sia non intenzionale. L’abbreviazione di Reazione Avversa da Farmaci maggiormente utilizzata è ADR dall’inglese Adverse Drug Reaction Tutti i farmaci possono provocare delle reazioni avverse. Naturalmente esistono delle differenze tra i diversi principi attivi in termini di gravità delle reazioni, di apparati colpiti, di frequenza delle reazioni.

Directive 2010/84/EU La definizione dell’EMA include non solo le reazioni averse che avvengono quando il medicinale è utilizzato correttamente, alle dosi normali e secondo l’uso autorizzato (Scheda Tecnica), m anche quelle che derivano da errori medici, da sovradosaggi accidentali, da usi fuori indicazione (off-label), da misuso, da abuso o da esposizione occupazionale

Chiarimenti AIFA in merito ad alcuni termini Uso off-label: si riferisce a impieghi del medicinale usato intenzionalmente per finalità mediche non in accordo con le indicazioni di impiego autorizzate Misuso: si riferisce a situazioni in cui il medicinale è usato intenzionalmente ed in modo inappropriato non in accordo con le indicazioni di impiego autorizzate Abuso: si riferisce ad un intenzionale uso eccessivo del medicinale, sporadico o persistente, accompagnato da effetti dannosi fisici o psicologici Esposizione occupazionale: si riferisce all'esposizione ad un medicina come risultato di un impiego professionale o non professionale.

REAZIONE AVVERSA DA FARMACI DEFINIZIONE DI GRAVITÀ Qualsiasi reazione che provoca la morte di un individuo, ne mette in pericolo la vita, ne richiede o prolunga l'ospedalizzazione, provoca disabilità o incapacità persistente o significativa, comporta una anomalia congenita o un difetto alla nascita.

Quanto sono frequenti le reazioni avverse da farmaci?

INCIDENZA DELLE REAZIONI AVVERSE DA FARMACI: TERMINOLOGIA Scala suggerita dal CIOMS (Council for International Organizations of Medical Sciences) N. ADR/n. esposti Molto frequente > 1/10 Frequente > 1/100 Non frequente < 1/100 Rara < 1/1000 Molto rara < 1/10000

Frequenza delle reazioni avverse ü Circa il 10% dei pazienti trattati con farmaci ha una reazione avversa Ann Pharmacother. 2007 41(9): 1411 -26 ü Il 3 -6% dei ricoveri in ospedale è dovuto ad una reazione avversa Arch Intern Med. 2008 22; 168(17): 1890 -6 ü Il 6 -10% dei pazienti ricoverati in ospedale ha una reazione avversa PLo. S ONE. 2009; 4(2): e 4439

Reazioni avverse da farmaci (ADR): dimensione del problema: la mortalità Ø Lazarou e coll. (JAMA 1998) hanno stimato che negli USA, nel 1994, si sono avuti 106. 000 morti (95% CI: 76. 000 -137. 000) provocati da ADR. Questo dato classificherebbe le ADR come la quarta causa di morte negli USA Ø Pirmohamed e coll. (BMJ 2004) hanno stimato in 5. 700 (95% CI: 3. 800 -7. 600) le morti annuali da ADR in UK a livello territoriale e in più di 10. 000 le morti complessive annuali da ADR (territorio + ospedale)
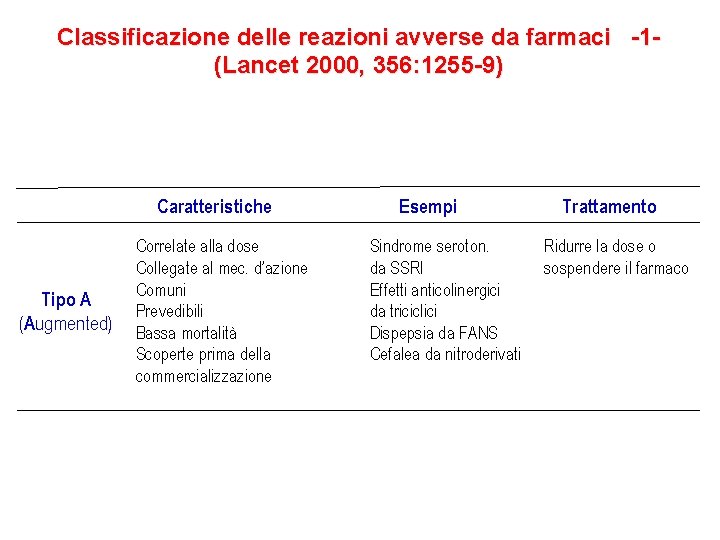
Classificazione delle reazioni avverse da farmaci -1(Lancet 2000, 356: 1255 -9) Caratteristiche Tipo A (Augmented) Correlate alla dose Collegate al mec. d’azione Comuni Prevedibili Bassa mortalità Scoperte prima della commercializzazione Esempi Sindrome seroton. da SSRI Effetti anticolinergici da triciclici Dispepsia da FANS Cefalea da nitroderivati Trattamento Ridurre la dose o sospendere il farmaco

EFFETTI COLLATERALI Effetti che accompagnano l’azione terapeutica del farmaco e che si verificano in organi o distretti diversi da quelli desiderati. Sono dovuti essenzialmente alla sua distribuzione in tutto l’organismo e si manifestano alle dosi terapeutiche Ø Cefalea da nitrati Ø Nausea da digitale Ø Ipokaliemia da diuretici

EFFETTI TOSSICI Sono espressione della tossicità del farmaco e si possono verificare anche a dosi terapeutiche in particolari pazienti, o in determinate condizioni cliniche Ø Alcalosi respiratoria da aspirina Ø Danno epatico da paracetamolo Ø Aritmie da digitale
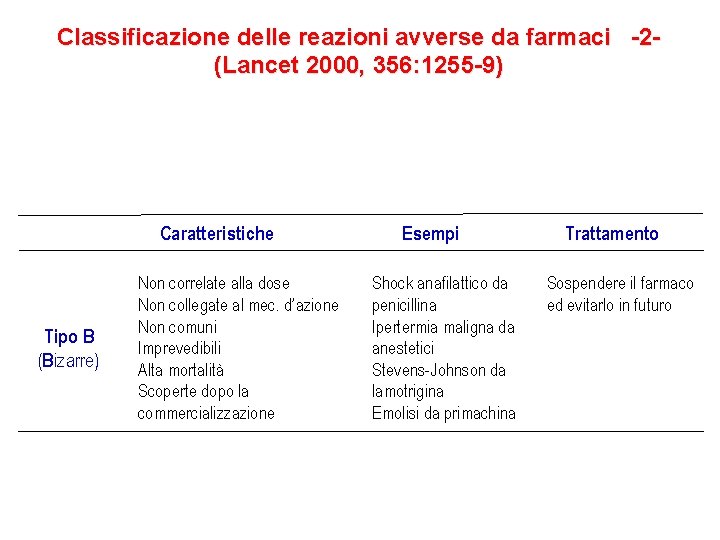
Classificazione delle reazioni avverse da farmaci -2(Lancet 2000, 356: 1255 -9) Caratteristiche Tipo B (Bizarre) Non correlate alla dose Non collegate al mec. d’azione Non comuni Imprevedibili Alta mortalità Scoperte dopo la commercializzazione Esempi Shock anafilattico da penicillina Ipertermia maligna da anestetici Stevens-Johnson da lamotrigina Emolisi da primachina Trattamento Sospendere il farmaco ed evitarlo in futuro

Reazioni immuno-mediate Il meccanismo dell’allergia dipende dall’interazione fra un antigene esterno e anticorpi prodotti dall’organismo o linfociti sensibilizzati. I farmaci possono indurre reazioni allergiche nei seguenti modi: 1. Il farmaco può essere una proteina potenzialmente immunogenica 2. Può diventare un antigene completo in seguito al legame con proteine endogene 3. Può causare o potenziare una reazione fra un antigene self modificato e un anticorpo 4. Può causare la sintesi di autoanticorpi


Esempi di reazioni avverse da farmaci su base immunologica Cute • Orticaria • Rash maculopapulare • Eritema nodoso • Eczema • Eruzione lichenoide • Vasculite • Sindrome di Stevens-Johnson • Necrolisi epidermica tossica Sangue • Trombocitopenia • Agranulocitosi • Anemia emolitica • Anemia aplastica Fegato • Epatite colestatica • Epatite epatocellulare Rene • Nefrite interstiziale • Glomerulonefrite Polmone • Polmonite (eosinofila, alveolare, interstiziale) Sistemiche • Anafilassi • Vasculiti • Malattia da siero • LES

Esempi di farmaci che provocano reazioni allergiche Anafilassi • Aspirina • Cefalosporine • Diclofenac • Penicilline • Streptochinasi • Cotrimossazolo • Suxametonio • Tiopentale • Tubocurarina Discrasie ematiche • Captopril • Clorpromazina • Penicilline • Sulfasalazina • Cotrimossazolo • Ac. Valproico • Ticlopidina Reazioni epatiche • Carbamazepina • FANS • Alotano • Fenitoina • ACE-inibitori • Amiodarone Reazioni cutanee • Carbamazepina • Penicilline • Lamotrigina • Fenitoina • Fenobarbitale • Fluorochinoloni

Reazioni avverse su base genetica Legate a variazioni su base genetica che possono alterare la farmacocinetica (iper-reattività) o la risposta tissutale (idiosincrasia) ai farmaci. IPER-REATTIVITA’ Polimorfismi genetici a livello del sistema citocromo P-450 o di altri enzimi farmacometabolizzanti (es. apnea da succinilcolina, neuropatie da isoniazide) IDIOSINCRASIA Carenza di G 6 PD (anemia emolitica da agenti ossidanti) Carenza di metaemoglobina reduttasi (metaemoglobinemia da clorochina) Carenza di glutatione (epatotossicità da paracetamolo)

La base della farmacogenomica: le differenze nel codice genetico delle persone • Mutazione: variazione nel DNA che si verifica in meno del 1% della popolazione – Spesso associata a patologie rare • es. Fibrosi cistica, malattia di Huntington • Polimorfismo: variazione nel DNA che si verifica in più del 1% della popolazione
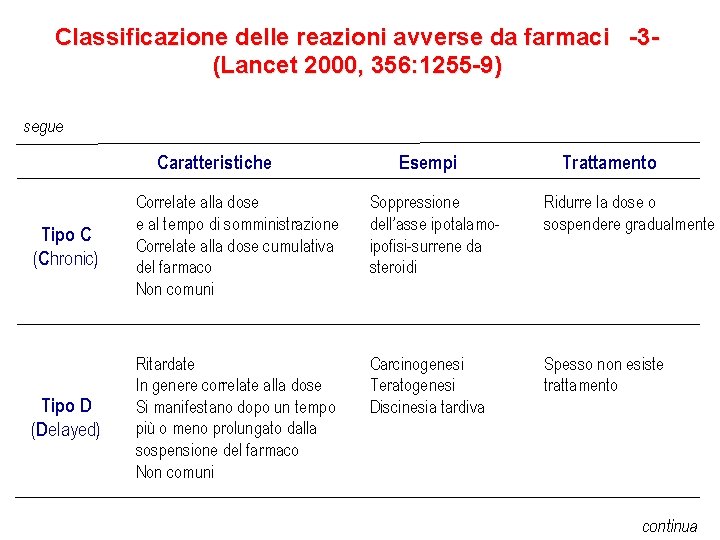
Classificazione delle reazioni avverse da farmaci -3(Lancet 2000, 356: 1255 -9) segue Caratteristiche Esempi Trattamento Tipo C (Chronic) Correlate alla dose e al tempo di somministrazione Correlate alla dose cumulativa del farmaco Non comuni Soppressione dell’asse ipotalamoipofisi-surrene da steroidi Ridurre la dose o sospendere gradualmente Tipo D (Delayed) Ritardate In genere correlate alla dose Si manifestano dopo un tempo più o meno prolungato dalla sospensione del farmaco Non comuni Carcinogenesi Teratogenesi Discinesia tardiva Spesso non esiste trattamento continua

Malformazioni alla nascita causate da farmaci L’incidenza delle malformazioni congenite viene stimata intorno al 3 -4% Il 5% di queste sarebbero causate da sostanze chimiche Quelle da farmaci sarebbero poco meno del 1% Ogni anno in Italia potrebbero esserci 100 -200 casi di malformazioni da farmaci ?


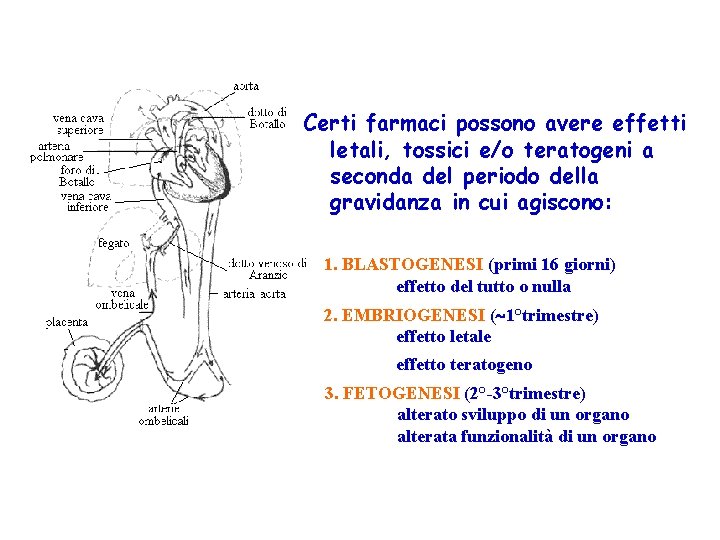
Certi farmaci possono avere effetti letali, tossici e/o teratogeni a seconda del periodo della gravidanza in cui agiscono: 1. BLASTOGENESI (primi 16 giorni) effetto del tutto o nulla 2. EMBRIOGENESI ( 1°trimestre) effetto letale effetto teratogeno 3. FETOGENESI (2°-3°trimestre) alterato sviluppo di un organo alterata funzionalità di un organo
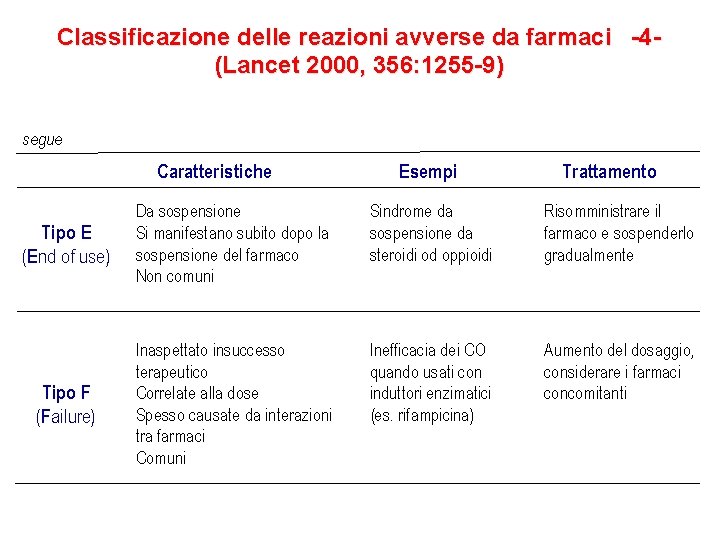
Classificazione delle reazioni avverse da farmaci -4(Lancet 2000, 356: 1255 -9) segue Caratteristiche Esempi Trattamento Tipo E (End of use) Da sospensione Si manifestano subito dopo la sospensione del farmaco Non comuni Sindrome da sospensione da steroidi od oppioidi Risomministrare il farmaco e sospenderlo gradualmente Tipo F (Failure) Inaspettato insuccesso terapeutico Correlate alla dose Spesso causate da interazioni tra farmaci Comuni Inefficacia dei CO quando usati con induttori enzimatici (es. rifampicina) Aumento del dosaggio, considerare i farmaci concomitanti

FARMACODIPENDENZA Ø La dipendenza da una sostanza (che viene da questo punto di vista definita come droga) si caratterizza come un desiderio compulsivo e irrefrenabile di assunzione della stessa (dipendenza psichica). Ø La dipendenza fisica si manifesta attraverso la sindrome d’astinenza che compare quando non si assume più la droga. La sindrome d’astinenza si verifica dopo un certo periodo di tempo dall’ultima assunzione (variabile a seconda del tipo di droga) ed caratterizzata da una serie di eventi spiacevoli, anche gravi, tipici di ciascuna droga.

FARMACODIPENDENZA Ø La dipendenza fisica si instaura dopo un tempo variabile, anche in questo caso, a seconda del tipo di droga (ad esempio è più rapida con l’eroina) e della dose. Ø La dipendenza fisica è sempre accompagnata dal fenomeno della tolleranza, cioè dalla necessità di aumentare la dose della droga per ottenere l’effetto desiderato. Ø Esempi di farmacodipendenza: oppioidi, benzodiazepine, amfetamine, alcool, cannabinoidi, cocaina, purganti

RILEVANTI FATTORI PER LA COMPARSA DI ADR -1 - Relativi al farmaco Ø Caratteristiche chimico-fisiche e farmacocinetiche Ø Ø Dose Frequenza e via di somministrazione Durata della terapia Formulazione farmaceutica

RILEVANTI FATTORI PER LA COMPARSA DI ADR -2 - Relativi al paziente Ø Ø Ø Ø Età Sesso Gravidanza Gravità della patologia Patologie concomitanti-intercorrenti Allergie Predisposizioni genetiche

RILEVANTI FATTORI PER LA COMPARSA DI ADR -3 - Estrinseci addizionali Ø Ø Ø Ø Interazioni tra farmaci Autosomministrazione Interazioni con cibo/bevande Consumo di alcool Farmaci scaduti Conservazione del farmaco Inquinanti ambientali

Si possono evitare le ADR?

Percentuale ADR prevenibili dalla letteratura % Leendertse et al. Arch Intern Med 2008 47 Davies et al. PLo. S ONE 2009 50 Franceschi et al Drug Safety 2008 77 Gurwitz et al. JAMA 2003 43 Pirmohamed M et al. BMJ 2004 72 Corral Baena S et al. Farm Hosp 2004 57 Temple ME et al. Drug Saf 2004 21

Se sono evitabili vuol dire che c’è stato un errore Un errore nella farmacoterapia (medication error) è un insuccesso nel processo terapeutico che provoca, o che potenzialmente può provocare, un danno al paziente “insuccesso” significa che il processo è finito al di sotto dello standard ottenibile

Gli errori possono avvenire a qualsiasi livello del processo terapeutico che coinvolge i farmaci Fabbricazione, confezionamento, conservazione Prescrizione (sia nella scelta della terapia che nell’atto della scrittura) Trascrizione/interpretazione Dispensazione/preparazione Somministrazione Monitoraggio/raccomandazioni

Prescrivere efficacemente 1 • Considerare trattamenti non farmacologici • Modificare dieta • No fumo, ridurre alcool • Esercizio fisico • Supporto sociale

Prescrivere efficacemente 2 • • Trattare le patologie in ordine di priorità Attenzione alle insufficenze d’organo Partire con basse dosi, incrementare con cautela Usare pochi farmaci Monitorare la compliance e la risposta Rivedere periodicamente la terapia COINVOLGERE IL PAZIENTE

Compliance • Circa 1/3 dei pazienti non aderisce alla terapia • Scarsa motivazione • Scarsa comprensione • Problemi pratici • Non-compliance consapevole • Migliorare la compliance con • Trattamenti semplici; istruzioni scritte • Aiutare la memoria • Coinvolgere altri soggetti
- Slides: 192