Farmaci a Bersaglio Molecolare Indicazioni ed Appropriatezza duso

Farmaci a Bersaglio Molecolare Indicazioni ed Appropriatezza d’uso in Oncologia ERNESTO DURINI U. O. di ONCOLOGIA

Farmaci “target based” , “Mirati” o “Intelligenti “ Mentre la chemioterapia agisce in modo indiscriminato sulle cellule in rapida replicazione , i farmaci “ target” agiscono su un bersaglio(recettore) particolare presente in eccesso sulle cellule tumorali che ne favorisce il rapido sviluppo
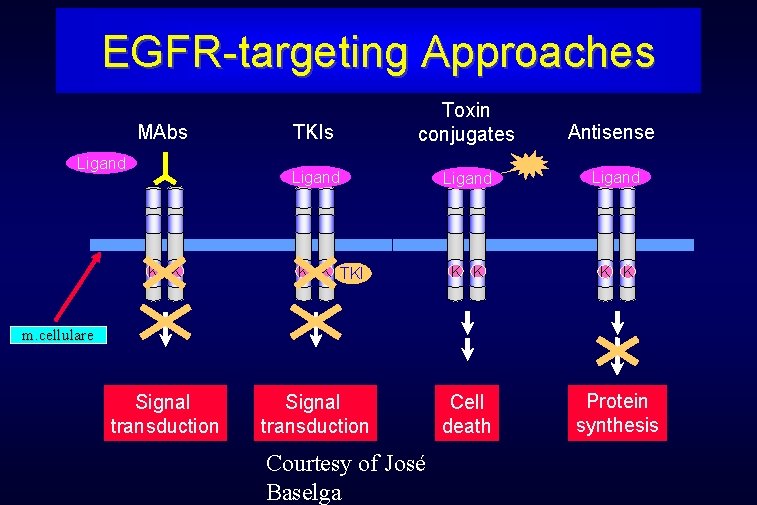
EGFR-targeting Approaches MAbs Ligand K K TKIs Toxin conjugates Antisense Ligand K K Cell death Protein synthesis K K TKI m. cellulare Signal transduction Courtesy of José Baselga

Farmaci biologici approvati in Italia e loro indicazioni in Oncologia Farmaco 1) Trastuzumab (Herceptin®) 2) Cetuximab (Erbitux®) 3) Bevacizumab (Avastin ®) 4) Ipilimumab (Yervoy) 5) Erlotinib (Tarceva ®) 6) Lapatinib ( Tyverb) 7) Sunitinib (Sutent) 8) Sorafenib (Nexavar) 9) Gefitinib (Iressa) 10) Temsirolimus (Torisel ) 11) Everolimus (Afinitor) Indicazione Ca mammella Her 2+ (3+ o FISH+) Ca colorettale, ca testa collo Ca colorettale –renale –mammella-NSCLC Melanoma Maligno NSCLC Ca mammella HER 2+ (2° linea ) Ca renale cellule chiare – HCC- Ca renale NSCLC Ca renale (non cellule chiare ) Ca renale ( 2° linea ) Bollettino Ufficiale Regione Puglia n. ° 45 del 29/03/2011 - Prontuario Terapeutico Ospedaliero Regionale (PTOR)- Monitoraggio AIFA

Anticorpi monoclonali Gli anticorpi monoclonali sono dotati di un frammento che si lega agli antigeni presenti nelle cellule tumorali (cosiddetto Fab = fragment antigen binding) e inibiscono in tal modo i processi essenziali allo sviluppo ed alla moltiplicazione di dette cellule. Inoltre possono potenziare l'immunità naturale attivando le cellule natural killer o la cascata del complemento, oppure possono funzionare come veicoli venendo legati a radioisotopi o sostanze tossiche per le cellule neoplastiche. La somministrazione avviene per via venosa perchè, se introdotti per os, verrebbero degradati a livello gastrointestinale; a differenza degli inibitori delle piccole molecole, non vengono metabolizzati dal fegato per cui sono in genere privi di interazioni importanti con altri farmaci Anticorpi monoclonali
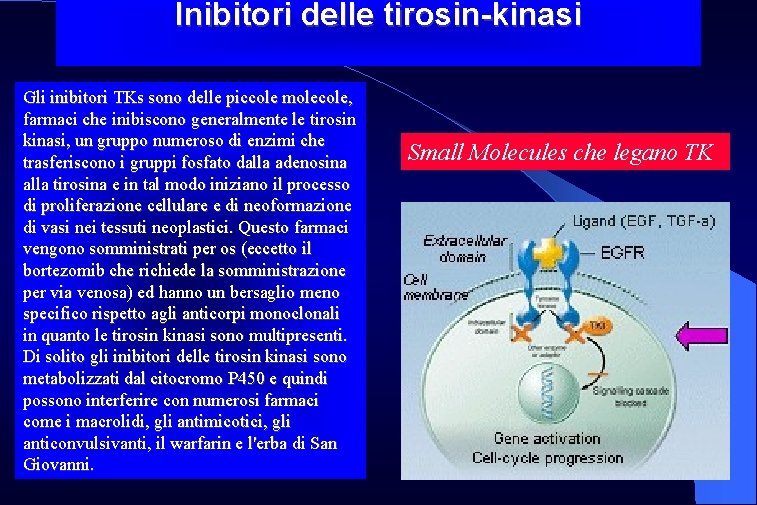
Inibitori delle tirosin-kinasi Gli inibitori TKs sono delle piccole molecole, farmaci che inibiscono generalmente le tirosin kinasi, un gruppo numeroso di enzimi che trasferiscono i gruppi fosfato dalla adenosina alla tirosina e in tal modo iniziano il processo di proliferazione cellulare e di neoformazione di vasi nei tessuti neoplastici. Questo farmaci vengono somministrati per os (eccetto il bortezomib che richiede la somministrazione per via venosa) ed hanno un bersaglio meno specifico rispetto agli anticorpi monoclonali in quanto le tirosin kinasi sono multipresenti. Di solito gli inibitori delle tirosin kinasi sono metabolizzati dal citocromo P 450 e quindi possono interferire con numerosi farmaci come i macrolidi, gli antimicotici, gli anticonvulsivanti, il warfarin e l'erba di San Giovanni. Small Molecules che legano TK

Confronto Mo. Ab- TKI Macromolecole: -degradate nel tratto GI Small Molecules: -assorbite dal tratto GI -No somministrazione orale -somministrazione orale Ma… -somministrazione settimanale -somministrazione giornaliera Extracellulare: -complesso Ab-recettore Intracellulare: -intervengono a diversi livelli di -risposta immunitaria cross reattività delle varie TK

Applicazioni delle analisi dei profili di espressione genica con microarray in Oncologia L’avvento dei microarray ha aperto nuove frontiere nella ricerca oncologica conseguenze rilevanti nella diagnosi, prognosi e terapia di molte neoplasie solide (Pusztai L. , 2006). Il ricorso a nuove molecole “targeted” come anticorpi monoclonali, inibitori delle Tirosin. Kinasi , Inibitori Multitarget, Inibitori antiangiogenetici rappresentano una reale possibilità nell’armamentario terapeutico; altri come Inibitori delle Parp e m. TOR hanno già in parte trovato applicazione nella pratica clinica corrente.
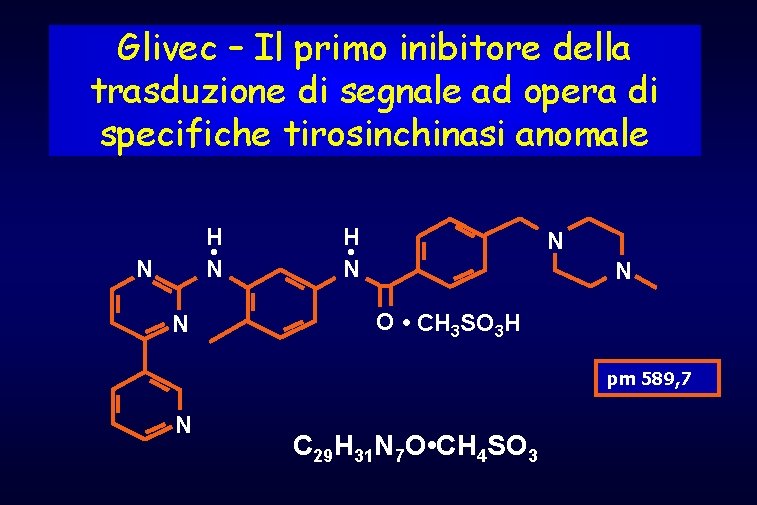
Glivec – Il primo inibitore della trasduzione di segnale ad opera di specifiche tirosinchinasi anomale H • N N N O • CH 3 SO 3 H pm 589, 7 N C 29 H 31 N 7 O • CH 4 SO 3
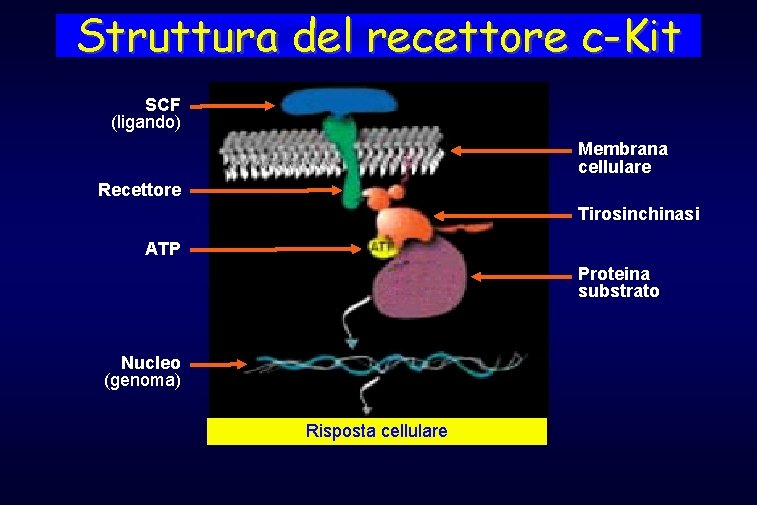
Struttura del recettore c-Kit SCF (ligando) Membrana cellulare Recettore Tirosinchinasi ATP Proteina substrato Nucleo (genoma) Risposta cellulare
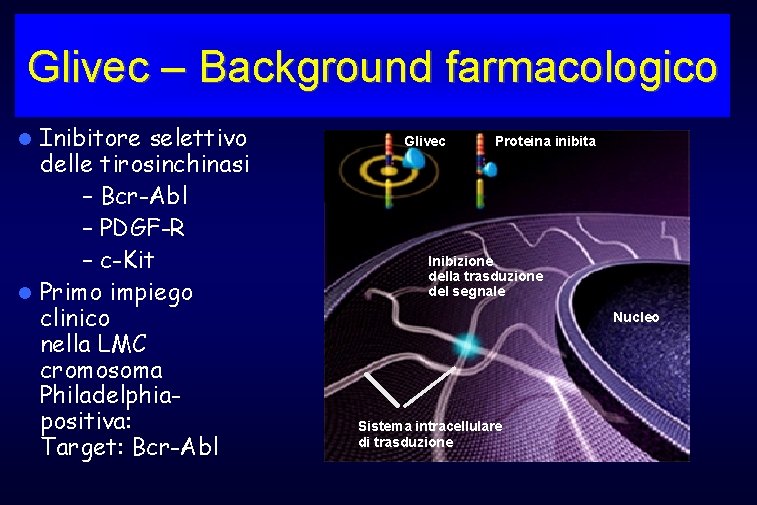
Glivec – Background farmacologico Inibitore selettivo delle tirosinchinasi – Bcr-Abl – PDGF-R – c-Kit Primo impiego clinico nella LMC cromosoma Philadelphiapositiva: Target: Bcr-Abl Glivec Proteina inibita Inibizione della trasduzione del segnale Nucleo Sistema intracellulare di trasduzione

Glivec – Il caso 0 Il Glivec venne approvato nel 2001 negli USA dalla FDA (Food and Drug Administration), con una procedura di registrazione accelerata, che si concluse in poche settimane. L’iter registrativo accelerato, che rappresentò un record di velocità nel panorama delle terapie oncologiche, fu accettato perché il Glivec venne riconosciuto come farmaco salvavita, capostipite di una nuova era.

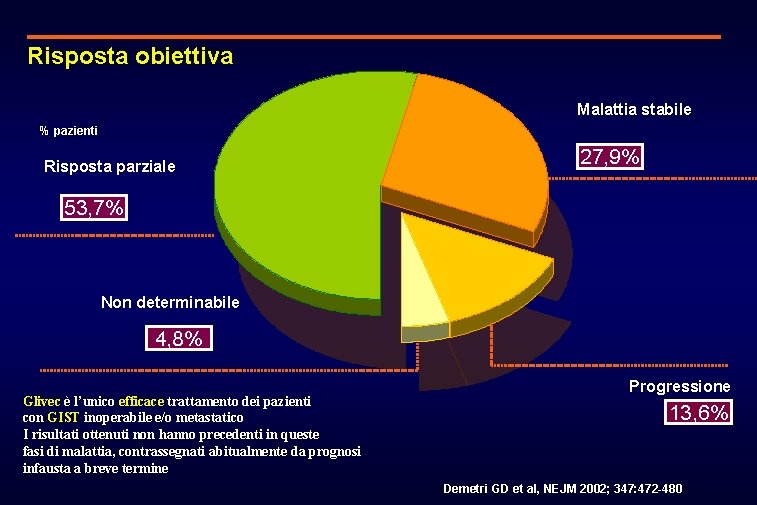
Risposta obiettiva Malattia stabile % pazienti Risposta parziale 27, 9% 53, 7% Non determinabile 4, 8% Glivec è l’unico efficace trattamento dei pazienti con GIST inoperabile e/o metastatico I risultati ottenuti non hanno precedenti in queste fasi di malattia, contrassegnati abitualmente da prognosi infausta a breve termine Progressione 13, 6% Demetri GD et al, NEJM 2002; 347: 472 -480
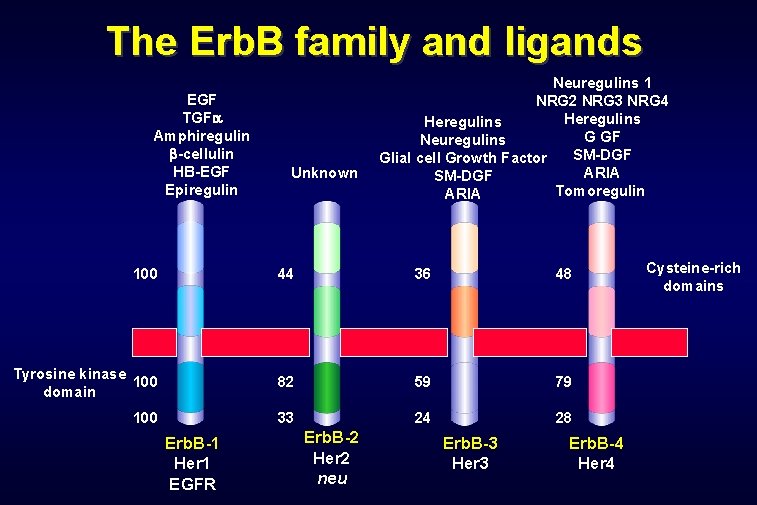
The Erb. B family and ligands EGF TGF Amphiregulin -cellulin HB-EGF Epiregulin Unknown Neuregulins 1 NRG 2 NRG 3 NRG 4 Heregulins G GF Neuregulins SM-DGF Glial cell Growth Factor ARIA SM-DGF Tomoregulin ARIA 100 44 36 48 Tyrosine kinase 100 domain 82 59 79 100 33 24 28 Erb. B-1 Her 1 EGFR Erb. B-2 Her 2 neu Erb. B-3 Her 3 Erb. B-4 Her 4 Cysteine-rich domains
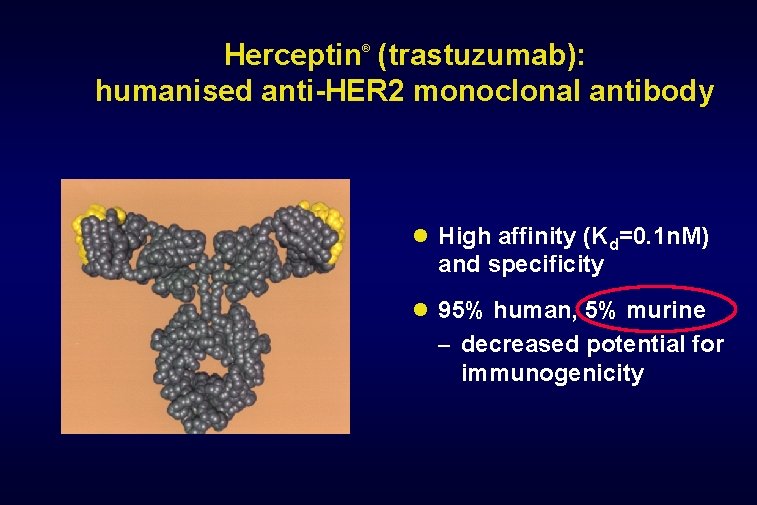
Herceptin (trastuzumab): humanised anti-HER 2 monoclonal antibody ® High affinity (Kd=0. 1 n. M) and specificity 95% human, 5% murine – decreased potential for immunogenicity
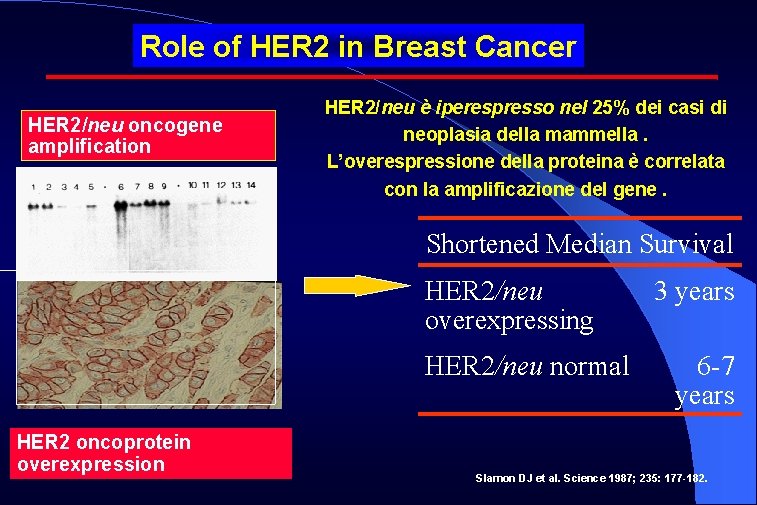
Role of HER 2 in Breast Cancer HER 2/neu oncogene amplification HER 2/neu è iperespresso nel 25% dei casi di neoplasia della mammella. L’overespressione della proteina è correlata con la amplificazione del gene. Shortened Median Survival HER 2/neu overexpressing HER 2/neu normal HER 2 oncoprotein overexpression 3 years 6 -7 years Slamon DJ et al. Science 1987; 235: 177 -182.

Trastuzumab: Studi di combinazione Disegno e Arruolamento • Ca. Mammario Met. • Positività HER 2 2+/3+ • N 0 prec. CT per MBC • Malattia misurabile • KPS > 60% Pazienti eleggibili (n = 469) Nessuna prec. Antraciclina Trastuzumab + AC AC (n = 143) (n = 138) Slamon D et al. NEJM 2001 Prec. Antraciclina Trastuzumab + Paclitaxel (n = 92) Paclitaxel (n = 96)
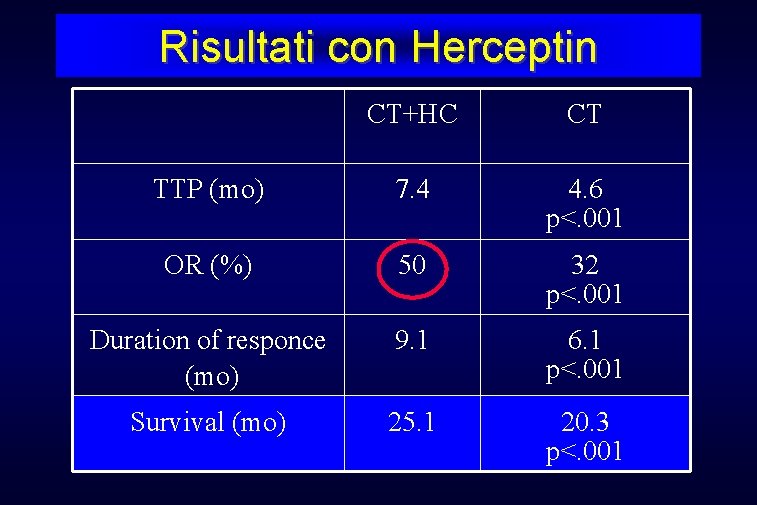
Risultati con Herceptin CT+HC CT TTP (mo) 7. 4 4. 6 p<. 001 OR (%) 50 32 p<. 001 Duration of responce (mo) 9. 1 6. 1 p<. 001 Survival (mo) 25. 1 20. 3 p<. 001

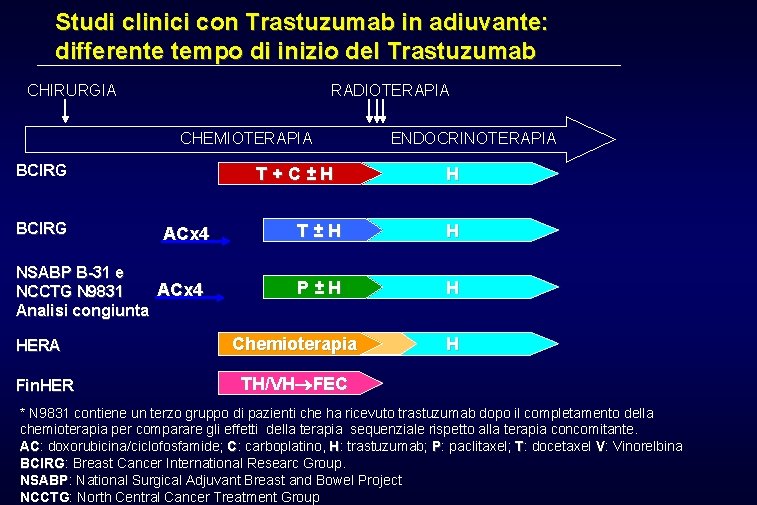
Studi clinici con Trastuzumab in adiuvante: differente tempo di inizio del Trastuzumab CHIRURGIA RADIOTERAPIA CHEMIOTERAPIA BCIRG T+C±H ACx 4 NSABP B-31 e ACx 4 NCCTG N 9831 Analisi congiunta HERA Fin. HER ENDOCRINOTERAPIA H T±H H P±H H Chemioterapia H TH/VH FEC * N 9831 contiene un terzo gruppo di pazienti che ha ricevuto trastuzumab dopo il completamento della chemioterapia per comparare gli effetti della terapia sequenziale rispetto alla terapia concomitante. AC: AC doxorubicina/ciclofosfamide; C: carboplatino, H: trastuzumab; P: paclitaxel; T: docetaxel V: Vinorelbina BCIRG: BCIRG Breast Cancer International Researc Group. NSABP: NSABP National Surgical Adjuvant Breast and Bowel Project NCCTG: NCCTG North Central Cancer Treatment Group
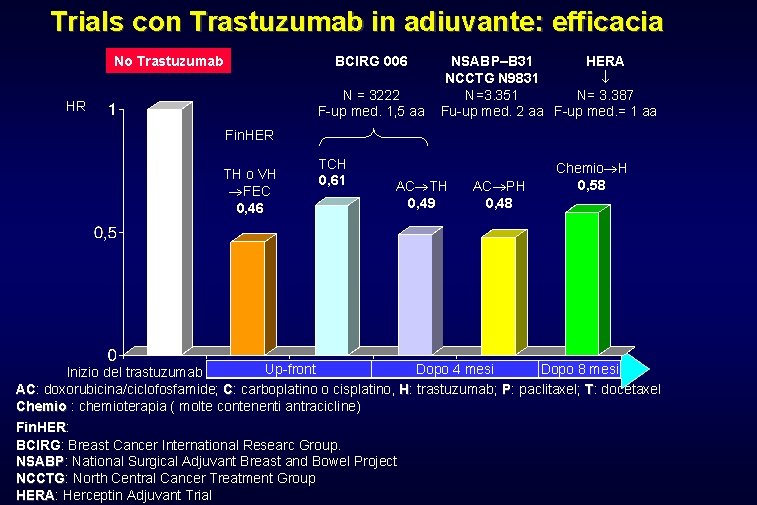
Trials con Trastuzumab in adiuvante: efficacia No Trastuzumab BCIRG 006 N = 3222 F-up med. 1, 5 aa HR NSABP–B 31 HERA NCCTG N 9831 N=3. 351 N= 3. 387 Fu-up med. 2 aa F-up med. = 1 aa Fin. HER TH o VH FEC 0, 46 TCH 0, 61 AC TH 0, 49 AC PH 0, 48 Chemio H 0, 58 Up-front Dopo 4 mesi Dopo 8 mesi Inizio del trastuzumab AC: AC doxorubicina/ciclofosfamide; C: carboplatino o cisplatino, H: trastuzumab; P: paclitaxel; T: docetaxel Chemio : chemioterapia ( molte contenenti antracicline) Fin. HER: Fin. HER BCIRG: BCIRG Breast Cancer International Researc Group. NSABP: NSABP National Surgical Adjuvant Breast and Bowel Project NCCTG: NCCTG North Central Cancer Treatment Group HERA: HERA Herceptin Adjuvant Trial
Indicazioni sottoposte a monitoraggio: n. 100/2006 Trattamento in fase iniziale: trattamento di pazienti con carcinoma mammario in fase iniziale HER-2 - positivo dopo chirurgia, chemioterapia (neoadiuvante o adiuvante) e radioterapia (se applicabile), «Herceptin» deve essere utilizzato soltanto in pazienti affette da tumore con iperespressione di HER 2 o con amplificazione del gene HER 2 come determinato mediante un test accurato e convalidato. n. 467/2010 Herceptin in associazione a capecitabina o 5 -fluorouracile e cisplatino e' indicato nel trattamento di pazienti con adenocarcinoma metastatico dello stomaco o della giunzione gastroesofagea HER 2 positivo, che non siano stati precedentemente sottoposti a trattamento antitumorale per la malattia metastatica.
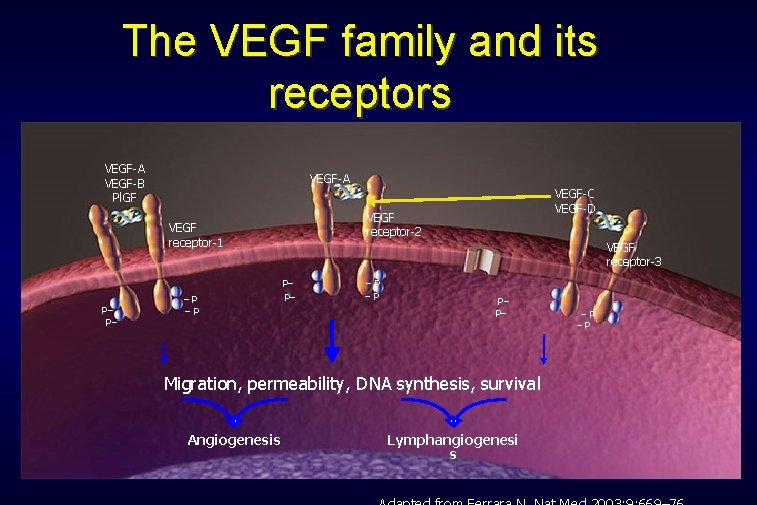
The VEGF family and its receptors VEGF-A VEGF-B Pl. GF VEGF-A VEGF receptor-2 VEGF receptor-1 P– P– –P –P VEGF-C VEGF-D VEGF receptor-3 P– P– –P –P P– P– Migration, permeability, DNA synthesis, survival Angiogenesis Lymphangiogenesi s –P –P
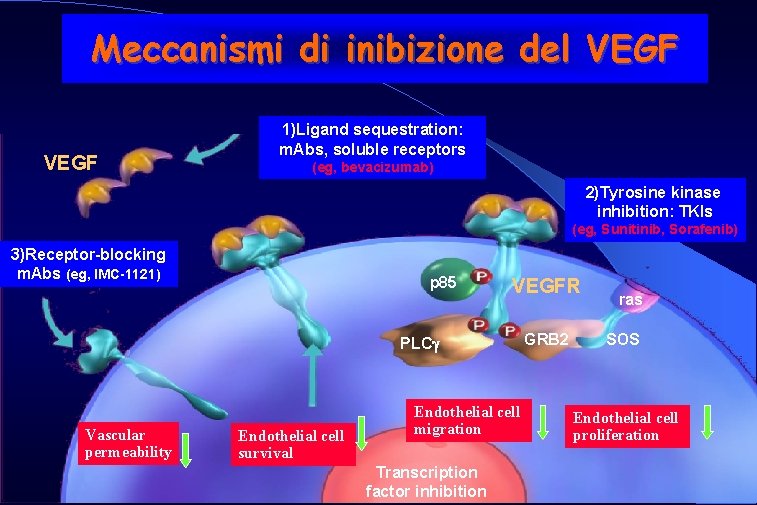
Meccanismi di inibizione del VEGF 1)Ligand sequestration: m. Abs, soluble receptors (eg, bevacizumab) 2)Tyrosine kinase inhibition: TKIs (eg, Sunitinib, Sorafenib) 3)Receptor-blocking m. Abs (eg, IMC-1121) p 85 VEGFR PLC Vascular permeability Endothelial cell survival Endothelial cell migration Transcription factor inhibition GRB 2 ras SOS Endothelial cell proliferation
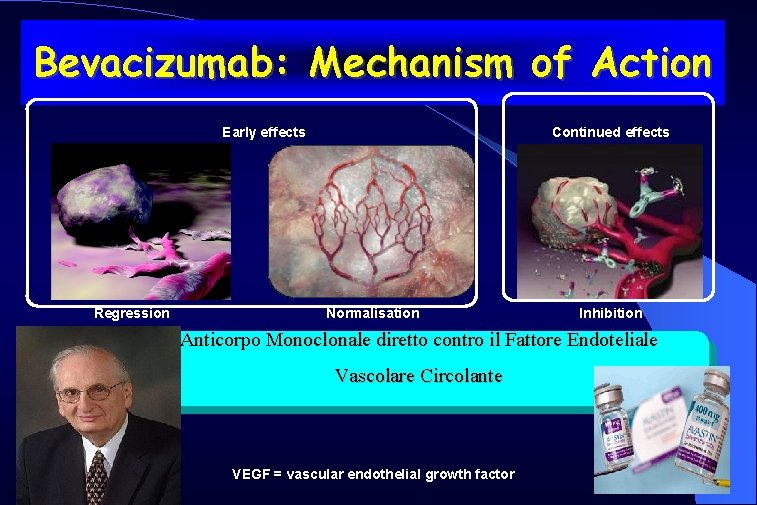
Bevacizumab: Mechanism of Action Early effects Regression Continued effects Normalisation Inhibition Anticorpo Monoclonale diretto contro il Fattore Endoteliale Vascolare Circolante VEGF = vascular endothelial growth factor
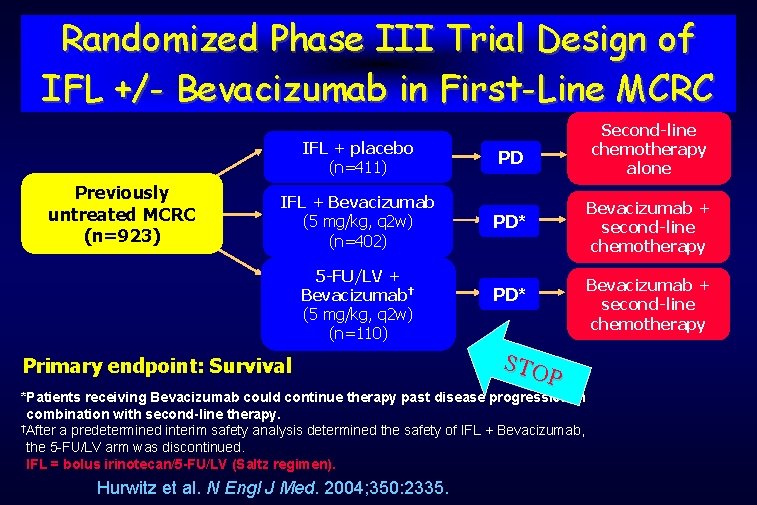
Randomized Phase III Trial Design of IFL +/- Bevacizumab in First-Line MCRC Previously untreated MCRC (n=923) IFL + placebo (n=411) PD IFL + Bevacizumab (5 mg/kg, q 2 w) (n=402) PD* 5 -FU/LV + Bevacizumab† (5 mg/kg, q 2 w) (n=110) Primary endpoint: Survival PD* ST O P *Patients receiving Bevacizumab could continue therapy past disease progression in combination with second-line therapy. †After a predetermined interim safety analysis determined the safety of IFL + Bevacizumab, the 5 -FU/LV arm was discontinued. IFL = bolus irinotecan/5 -FU/LV (Saltz regimen). Hurwitz et al. N Engl J Med. 2004; 350: 2335. Second-line chemotherapy alone Bevacizumab + second-line chemotherapy
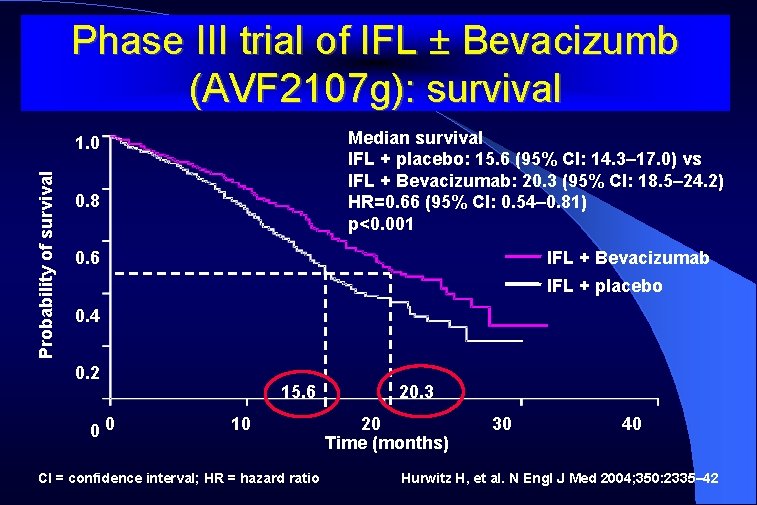
Phase III trial of IFL ± Bevacizumb (AVF 2107 g): survival Median survival IFL + placebo: 15. 6 (95% CI: 14. 3– 17. 0) vs IFL + Bevacizumab: 20. 3 (95% CI: 18. 5– 24. 2) HR=0. 66 (95% CI: 0. 54– 0. 81) p<0. 001 Probability of survival 1. 0 0. 8 IFL + Bevacizumab 0. 6 IFL + placebo 0. 4 0. 2 00 15. 6 10 CI = confidence interval; HR = hazard ratio 20. 3 20 Time (months) 30 40 Hurwitz H, et al. N Engl J Med 2004; 350: 2335– 42

Bevacizumab nel ca del colo-retto
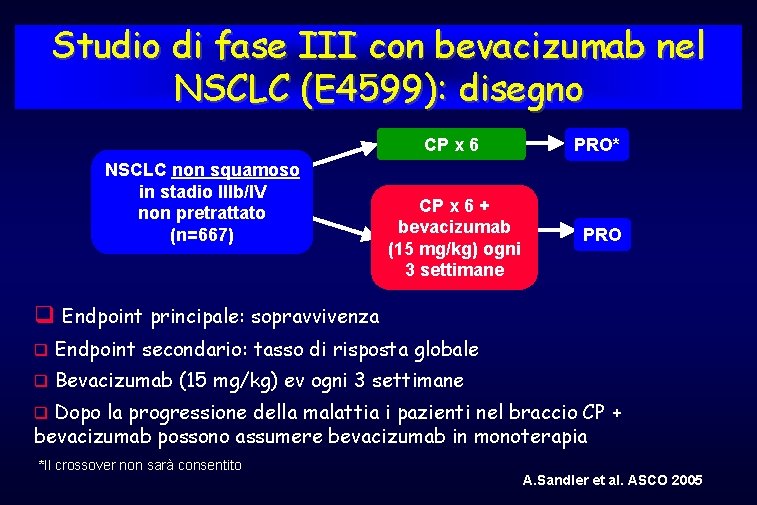
Studio di fase III con bevacizumab nel NSCLC (E 4599): disegno NSCLC non squamoso in stadio IIIb/IV non pretrattato (n=667) CP x 6 PRO* CP x 6 + bevacizumab (15 mg/kg) ogni 3 settimane PRO Endpoint principale: sopravvivenza Endpoint secondario: tasso di risposta globale Bevacizumab (15 mg/kg) ev ogni 3 settimane Dopo la progressione della malattia i pazienti nel braccio CP + bevacizumab possono assumere bevacizumab in monoterapia *Il crossover non sarà consentito A. Sandler et al. ASCO 2005
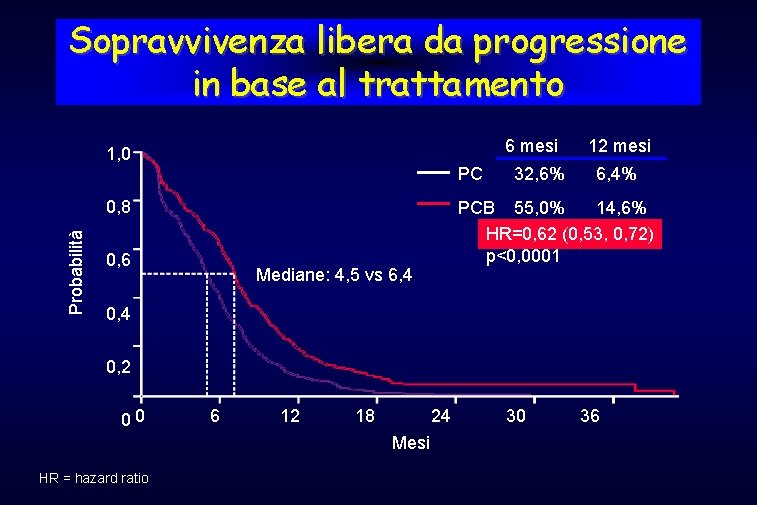
Sopravvivenza libera da progressione in base al trattamento 6 mesi 1, 0 PC Probabilità 0, 8 0, 6 32, 6% 12 mesi 6, 4% PCB 55, 0% 14, 6% HR=0, 62 (0, 53, 0, 72) p<0, 0001 Mediane: 4, 5 vs 6, 4 0, 2 00 6 12 18 24 Mesi HR = hazard ratio 30 36

Trial AVOREN Bevacizumab + IFN vs IFN Patients with metastatic clear cell RCC, status post nephrectomy Interferon alfa-2 a 9 MU 3 times weekly for up to 52 weeks + Placebo every 2 weeks until disease progression (N = 638) Interferon alfa-2 a 9 MU 3 times weekly for up to 52 weeks + Bevacizumab 10 mg/kg every 2 weeks until disease progression Primary endpoint – OS (improvement from 13 -17 months) Escudier B. et al. ASCO 2008
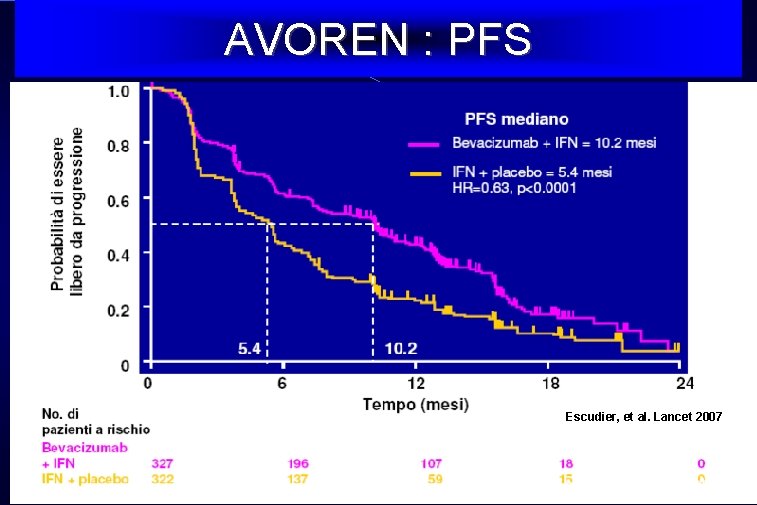
AVOREN : PFS Escudier, et al. Lancet 2007

Studio di fase III con bevacizumab in prima linea nel MBC (E 2100) MBC non pretrattato (n=685) Paclitaxel PRO* Paclitaxel + bevacizumab 10 mg/kg ogni 2 settimane PRO Lo studio è rivolto a una popolazione meno pesantemente pretrattata rispetto allo studio AVF 2119 Tra gli endpoint, il tempo alla progressione, il tasso di risposta globale e la sopravvivenza Miller KD. Clin Breast Cancer 2003; 3: 421– 2 *Il crossover non sarà consentito
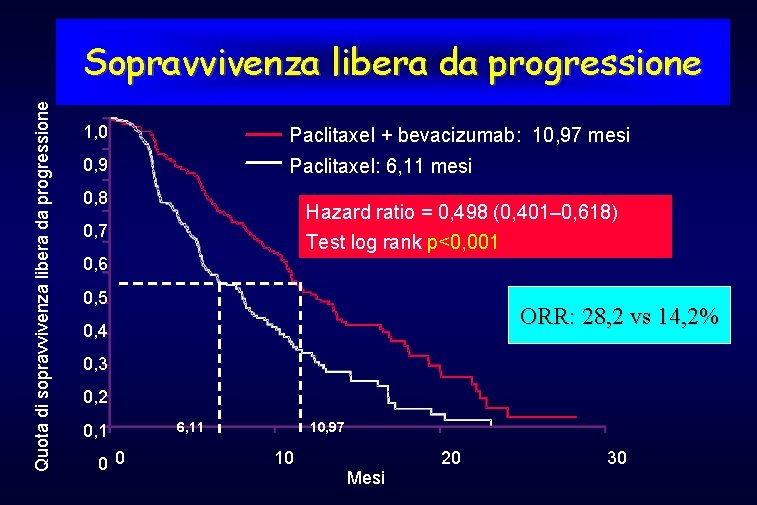
Quota di sopravvivenza libera da progressione Sopravvivenza libera da progressione 1, 0 Paclitaxel + bevacizumab: 10, 97 mesi 0, 9 Paclitaxel: 6, 11 mesi 0, 8 Hazard ratio = 0, 498 (0, 401– 0, 618) 0, 7 Test log rank p<0, 001 0, 6 0, 5 ORR: 28, 2 vs 14, 2% 0, 4 0, 3 0, 2 0, 1 00 6, 11 10, 97 10 Mesi 20 30

Avastin (Bevacizumab ) (Det. 63/2005) Avastin in combinazione con 5 -fluorouracile/acido folico endovena o 5 fluorouracile/acido folinico/irinotecan endovena e' indicato per il trattamento di prima linea dei pazienti con carcinoma del colon e del retto metastatico. (Det. 210/2008) Avastin (bevacizumab) in combinazione con chemioterapia a base di fluoropirimidine e' indicato per il trattamento di pazienti con carcinoma metastatico del colon e del retto Avastin, in aggiunta a chemioterapia a base di platino, è indicato per il trattamento in prima linea di pazienti con carcinoma polmonare non a piccole cellule, non resecabile, avanzato, metastatico o in ricaduta, con istologia a predominanza non squamocellulare Avastin in combinazione con paclitaxel è indicato per il trattamento in prima linea di pazienti con carcinoma mammario metastatico. Avastin in combinazione con interferone alfa-2 a è indicato per il trattamento in prima linea di pazienti con carcinoma renale avanzato e/o metastatico.

FDA Decides Against Bevacizumab for Breast Cancer, Europe Differs December 16, 2010 The US Food and Drug Administration (FDA) Ha annunciato il primo passo della procedura per la rimozione dell’indicazione del Bevacizumab +Paclitaxel nel MBC sulla base dei risultati della OS negli Studi E 2100; AVADO, RIBBON-1 European Medicines Agency (EMA) : in contrasto con la decisione Americana ; in Europa rimane l’appovazionone dell’uso di Bevacizumab in combinazione con Paclitaxel nel MBC
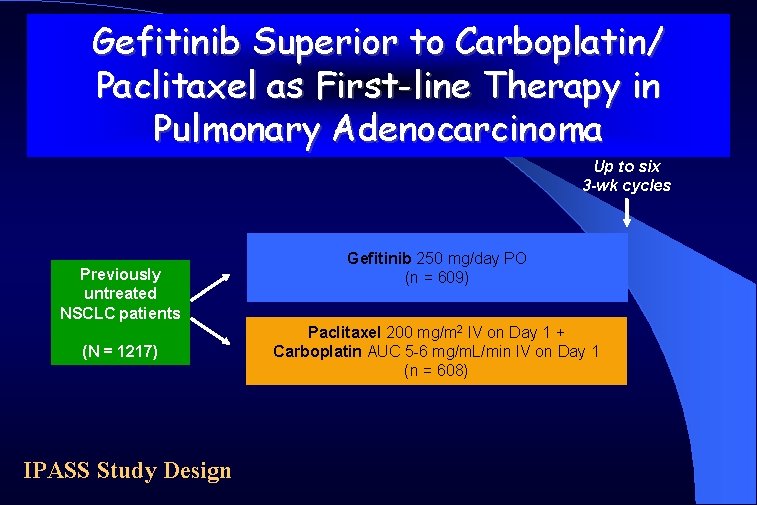
Gefitinib Superior to Carboplatin/ Paclitaxel as First-line Therapy in Pulmonary Adenocarcinoma Up to six 3 -wk cycles Previously untreated NSCLC patients (N = 1217) IPASS Study Design Gefitinib 250 mg/day PO (n = 609) Paclitaxel 200 mg/m 2 IV on Day 1 + Carboplatin AUC 5 -6 mg/m. L/min IV on Day 1 (n = 608)
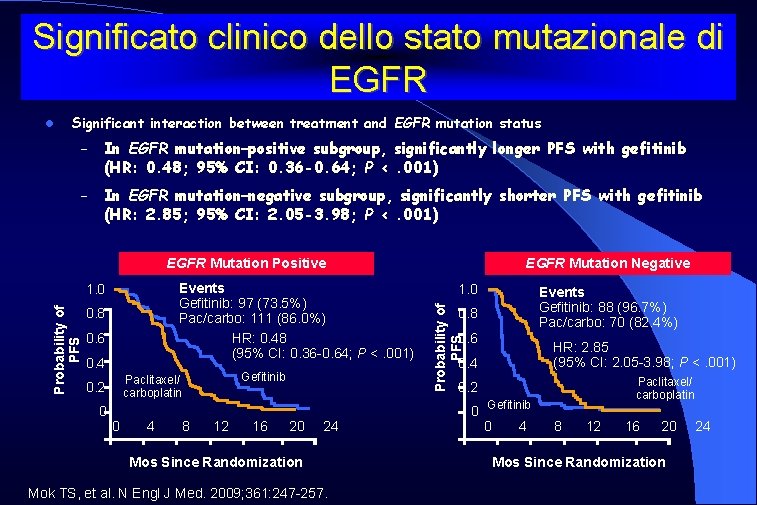
Significato clinico dello stato mutazionale di EGFR Significant interaction between treatment and EGFR mutation status – In EGFR mutation–positive subgroup, significantly longer PFS with gefitinib (HR: 0. 48; 95% CI: 0. 36 -0. 64; P <. 001) – In EGFR mutation–negative subgroup, significantly shorter PFS with gefitinib (HR: 2. 85; 95% CI: 2. 05 -3. 98; P <. 001) EGFR Mutation Positive Probability of PFS 0. 8 0. 6 0. 4 0 Gefitinib Paclitaxel/ carboplatin 0. 2 0 4 8 12 16 1. 0 Events Gefitinib: 88 (96. 7%) Pac/carbo: 70 (82. 4%) Probability of PFS Events Gefitinib: 97 (73. 5%) Pac/carbo: 111 (86. 0%) HR: 0. 48 (95% CI: 0. 36 -0. 64; P <. 001) 1. 0 EGFR Mutation Negative 0. 8 0. 6 HR: 2. 85 (95% CI: 2. 05 -3. 98; P <. 001) 0. 4 Paclitaxel/ carboplatin 0. 2 20 24 Mos Since Randomization Mok TS, et al. N Engl J Med. 2009; 361: 247 -257. 0 Gefitinib 0 4 8 12 16 20 Mos Since Randomization 24

Louis de Leon. Mistico spagnolo del’ 500
- Slides: 40