FAESO FACULDADE ESTCIO DE S DE OURINHOS BACHARELADOS

FAESO – FACULDADE ESTÁCIO DE SÁ DE OURINHOS BACHARELADOS EM ENGENHARIA CIVIL, ENGENHARIA DE PRODUÇÃO E ENGENHARIA DE CONTROLE E AUTOMAÇÃO INDUSTRIAL Aula 11 Primeira Lei Termodinâmica Mecanismos de Transferência de Calor Física Teórica Experimental II Prof. Dr. Alysson Cristiano Beneti OURINHOS-SP 2017
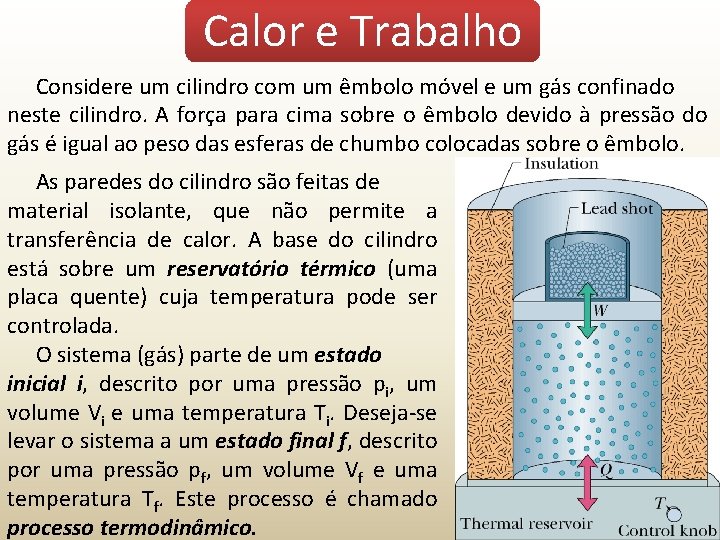
Calor e Trabalho Considere um cilindro com um êmbolo móvel e um gás confinado neste cilindro. A força para cima sobre o êmbolo devido à pressão do gás é igual ao peso das esferas de chumbo colocadas sobre o êmbolo. As paredes do cilindro são feitas de material isolante, que não permite a transferência de calor. A base do cilindro está sobre um reservatório térmico (uma placa quente) cuja temperatura pode ser controlada. O sistema (gás) parte de um estado inicial i, descrito por uma pressão pi, um volume Vi e uma temperatura Ti. Deseja-se levar o sistema a um estado final f, descrito por uma pressão pf, um volume Vf e uma temperatura Tf. Este processo é chamado processo termodinâmico.
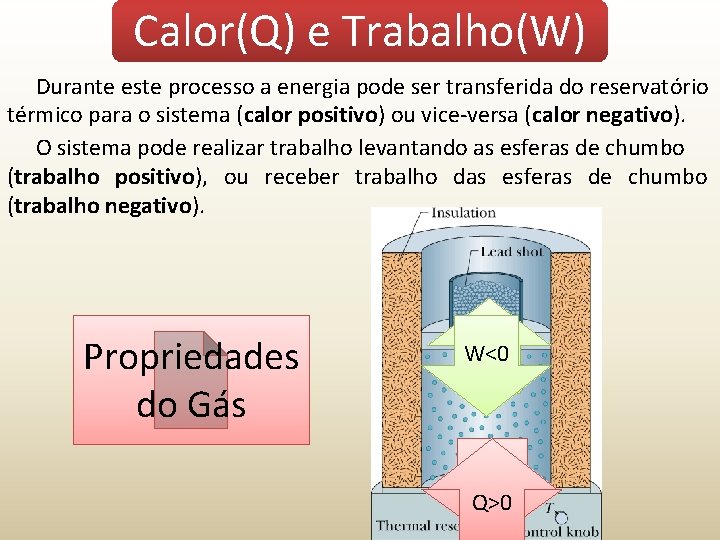
Calor(Q) e Trabalho(W) Durante este processo a energia pode ser transferida do reservatório térmico para o sistema (calor positivo) ou vice-versa (calor negativo). O sistema pode realizar trabalho levantando as esferas de chumbo (trabalho positivo), ou receber trabalho das esferas de chumbo (trabalho negativo). Propriedades do Gás W<0 W>0 Q<0 Q>0

Calor(Q) e Trabalho(W) Suponha que algumas esferas de chumbo são removidas do êmbolo, permitindo que o gás empurre o êmbolo e as esferas restantes para cima com uma força F, que produz um deslocamento infinitesimal d. S. Como o deslocamento é pequeno, podemos supor que F é constante durante o deslocamento. Nesse caso, o módulo de F é igual a p. A, onde p é a pressão e A é a área do êmbolo. O trabalho infinitesimal d. W realizado pelo gás durante o deslocamento é dado por:

Calor(Q) e Trabalho(W) Na prática existem muitas formas de levar o gás do estado i para o estado f. a) A área sombreada representa o trabalho W realizado por um sistema ao passar do estado inicial i para um estado inicial f. O trabalho é positivo porque o volume do sistema aumenta; b) W continua a ser positivo, mas agora é maior; c) W continua a ser positivo, mas agora é menor; d) W pode ser ainda menor (trajetória icdf) ou ainda maior (trajetória ighf); e) Neste caso, o sistema vai do estado f para o estado i quando o gás é comprimido por uma força externa e seu volume diminui, o trabalho realizado pelo sistema é negativo; f) O trabalho líquido Wliq realizado pelo sistema durante um ciclo completo é representado pela área sombreada.

Primeira Lei da Termodinâmica Experimentos mostram algo surpreendente! A grandeza Q W é a mesma para todos os processos termodinâmicos. Ela depende apenas dos estados inicial e final e não depende da maneira como o sistema passou de um estado para outro. Esta diferença Q W representa uma propriedade intrínseca do sistema, que é a energia interna ( Eint). Assim: A energia interna (Eint) de um sistema tende a aumentar, se acrescemos energia Para uma variação infinitesimal: na forma de calor (Q) , e a diminuir, se removemos energia na forma de trabalho realizado pelo sistema.

Alguns Casos Especiais da Primeira Lei da Termodinâmica 1) Processo adiabático: não ocorre troca de calor entre o sistema (gás) e o ambiente. 2) Processo a volume constante: o sistema não realiza trabalho. 3) Processos cíclicos: Após certas trocas de calor e de trabalho, o sistema volta ao estado inicial. 3) Expansões livres: São processos adiabáticos nos quais nenhum trabalho é realizado.

Alguns Casos Especiais da Primeira Lei da Termodinâmica Resumindo:

Exemplos 1) (Halliday, p. 199) Suponha que 1 Kg de água a 100 C é convertido em vapor a 100 C à pressão atmosférica padrão (1 atm=1, 01. 105 Pa) no arranjo da figura abaixo. O volume da água varia de um valor inicial de 1. 10 -3 m 3 do líquido para 1, 671 m 3 do vapor. (Dado: Lv=2256 KJ/Kg) a) Qual é o trabalho realizado pelo sistema durante esse processo? b) Qual é a energia transferida em forma de calor durante o processo? c) Qual é a variação da energia interna do sistema durante o processo?

Problemas Propostos 1) (Halliday, p. 209) Um gás em uma câmara fechada passa pelo ciclo mostrado no diagrama p-v da figura. Calcule a energia líquida adicionada ao sistema em forma de calor durante um ciclo completo. 2) (Halliday, p. 209) Um trabalho de 200 J é realizado sobre um sistema, e uma quantidade de calor de 70 cal é removida do sistema. Qual é o valor (incluindo o sinal) (a) de W, (b) de Q e (c) de Eint? (Obs: 4, 18 J=1 cal)
- Slides: 10