Facultad de Farmacia I Ciclo lectivo 2002 Epidemiologa















- Slides: 22

Facultad de Farmacia I Ciclo lectivo 2002 Epidemiología y Salud Pública (FA – 5021) Profesora: Carmen Marín

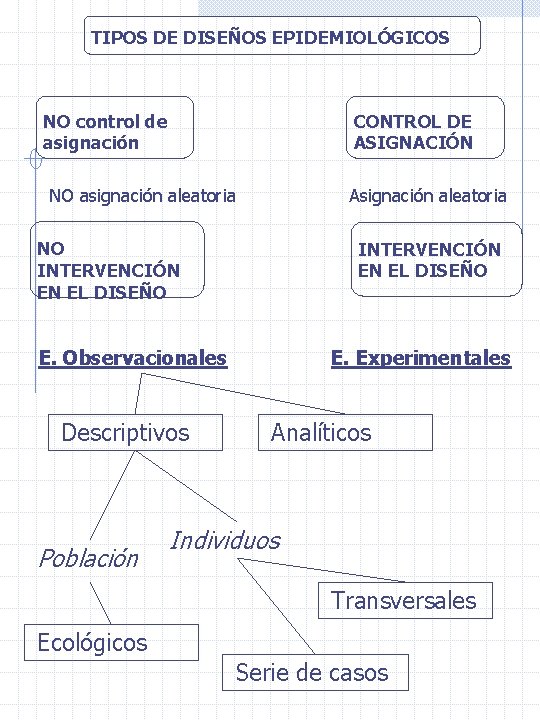
TIPOS DE DISEÑOS EPIDEMIOLÓGICOS NO control de asignación CONTROL DE ASIGNACIÓN NO asignación aleatoria Asignación aleatoria NO INTERVENCIÓN EN EL DISEÑO E. Observacionales Descriptivos Población E. Experimentales Analíticos Individuos Transversales Ecológicos Serie de casos

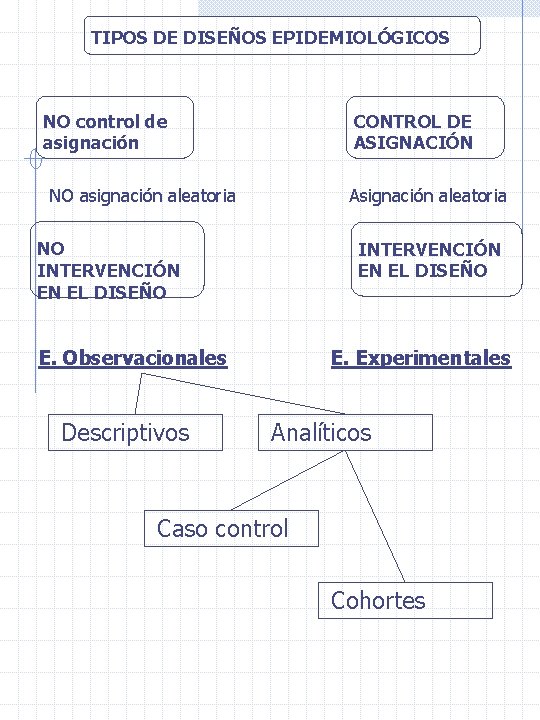
TIPOS DE DISEÑOS EPIDEMIOLÓGICOS NO control de asignación CONTROL DE ASIGNACIÓN NO asignación aleatoria Asignación aleatoria NO INTERVENCIÓN EN EL DISEÑO E. Observacionales Descriptivos E. Experimentales Analíticos Caso control Cohortes

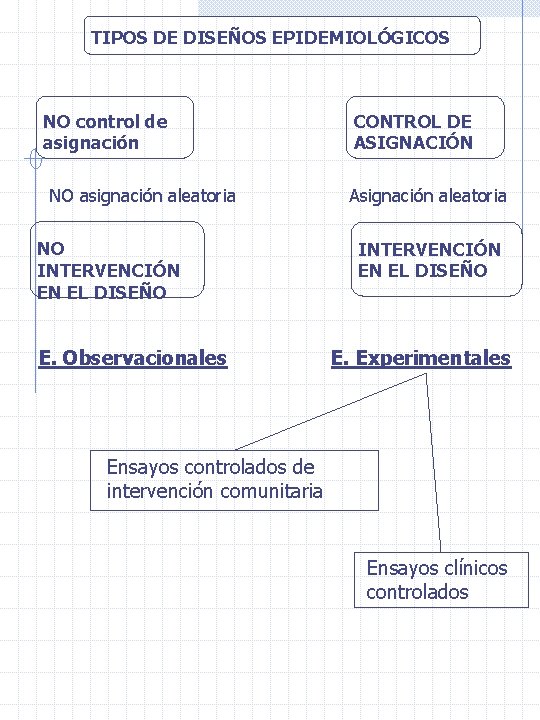
TIPOS DE DISEÑOS EPIDEMIOLÓGICOS NO control de asignación NO asignación aleatoria NO INTERVENCIÓN EN EL DISEÑO E. Observacionales CONTROL DE ASIGNACIÓN Asignación aleatoria INTERVENCIÓN EN EL DISEÑO E. Experimentales Ensayos controlados de intervención comunitaria Ensayos clínicos controlados

La figura que esquematiza el tipo de diseños epidemiológicos fue elaborada por Perea-Milla, 1996. Tomado de Joaquín Díaz Atienza: Unidad de trastornos alimentarios. Hospital Provincial Almería

Estudios experimentales Objetivo: Evaluar la eficacia de diferentes terapias, de actividades preventivas o para la evaluación de actividades de planificación y programación sanitarias. En los estudios experimentales es el investigador el que decide la exposición. Las decisiones sobre el diseño facilitan la interpretación de las asociaciones como causales.

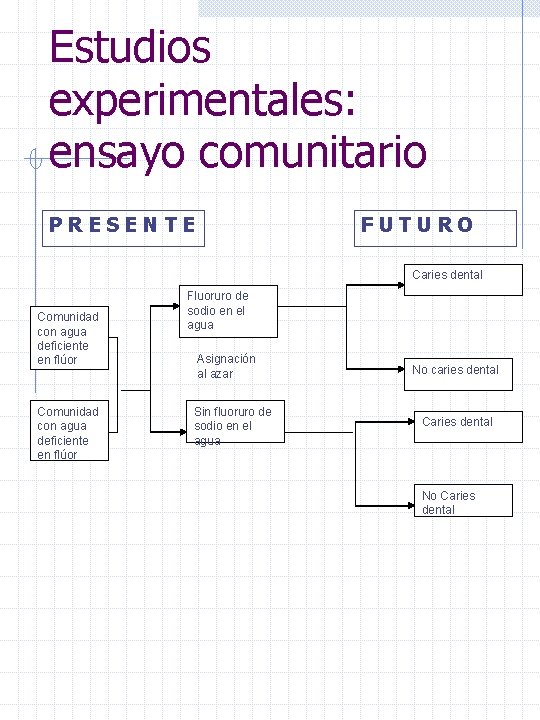
Estudios experimentales: ensayo comunitario PRESENTE FUTURO Caries dental Comunidad con agua deficiente en flúor Fluoruro de sodio en el agua Asignación al azar Sin fluoruro de sodio en el agua No caries dental Caries dental No Caries dental

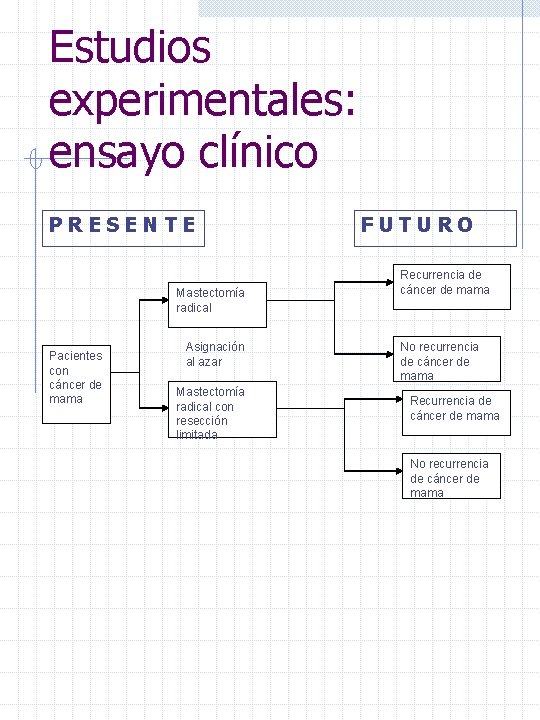
Estudios experimentales: ensayo clínico PRESENTE Mastectomía radical Pacientes con cáncer de mama Asignación al azar Mastectomía radical con resección limitada FUTURO Recurrencia de cáncer de mama No recurrencia de cáncer de mama

Ensayos clínicos Son los estudios experimentales más frecuentes. Los sujetos son pacientes y se evalúa uno o más tratamientos para una enfermedad o proceso. La validez de estudio radica fundamentalmente en que el proceso aleatorio haga los grupos comparables en las variables más relevantes en relación al problema a estudiar.

Ensayos clínicos

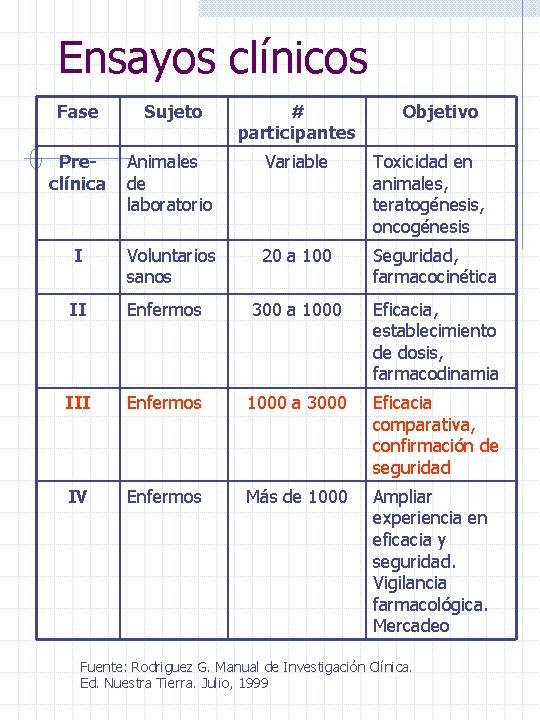
Ensayos clínicos Fase Sujeto # participantes Objetivo Preclínica Animales de laboratorio Variable Toxicidad en animales, teratogénesis, oncogénesis I Voluntarios sanos 20 a 100 Seguridad, farmacocinética II Enfermos 300 a 1000 Eficacia, establecimiento de dosis, farmacodinamia III Enfermos 1000 a 3000 Eficacia comparativa, confirmación de seguridad IV Enfermos Más de 1000 Ampliar experiencia en eficacia y seguridad. Vigilancia farmacológica. Mercadeo Fuente: Rodriguez G. Manual de Investigación Clínica. Ed. Nuestra Tierra. Julio, 1999

Ensayo clínico El diseño del estudio contempla: a. La ética y justificación del ensayo. b. La población susceptible de ser estudiada. c. La selección de los pacientes con su consentimiento a participar. d. El proceso de aleatorización. e. La descripción minuciosa de la intervención. f. El seguimiento de las pérdidas y los no cumplidores. g. La medición de la variable final. h. La comparación de los resultados en los grupos de intervención y control.

Ensayos clínicos El diseño debe incluir: Descripción del tipo de ensayo a realizar (doble ciego, controlado con placebo, cruzado o paralelo). Tipo de control (placebo u otros). Descripción detallada del proceso de aleatorización (procedimiento y consideraciones prácticas).

Ensayos clínicos Selección de los sujetos Criterios de inclusión y exclusión. Criterios de diagnóstico. Número de sujetos previstos y justificación del tamaño muestral. Variables a estudiar en cada sujeto, con su escala de medida y calendario de recolección. Criterios de retiro y análisis previsto de los retiros y los abandonos. Tratamiento de las pérdidas prerandomización. Duración aproximada del reclutamiento en función del número de pacientes previstos.

Ensayos clínicos Asignación de los sujetos, tipo de estrategias “ciegas” Simple Sujeto Observa dor Analista de datos + Doble Triple + + + (+) no conoce qué tratamiento está recibiendo el paciente ( ) conoce qué tratamiento está recibiendo el paciente

Ensayos clínicos Descripción del tratamiento Descripción de dosis, intervalo, vía y forma de administración, duración del tratamiento. Criterios de modificación de pautas a lo largo del ensayo. Tratamientos concomitantes permitidos y prohibidos. Normas especiales del manejo de fármacos en estudio. Para tratamientos no permitidos, considerar el período de tiempo mínimo desde su suspensión para la inclusión del sujeto. Medidas para valorar el cumplimiento terapéutico.

Ensayos clínicos Desarrollo del ensayo y evaluación de la respuesta Enfermedad, trastorno a estudio. Variable principal de valoración. Número y tiempo de las visitas durante el mismo, especificar las pruebas o exploraciones que se realizarán para valorar la respuesta. Descripción de los métodos (radiológicos, de laboratorio) utilizados para valorar la respuesta y control de calidad de los mismos.

Ensayos clínicos Acontecimientos adversos Información mínima (descripción, gravedad, duración, secuencia temporal, método de detección, tratamiento administrado en su caso; causas alternativas). Indicar criterios de imputabilidad que se van a utilizar. Indicar los procedimientos para la notificación inmediata de los acontecimientos adversos graves o inesperados. Incluir un modelo de hoja de notificación de acontecimientos adversos a las autoridades sanitarias.

Ensayos clínicos Aspectos éticos. Aceptación de las normas nacionales e internacionales al respecto (Declaración de Helsinki). Información a los pacientes y tipo de consentimiento a solicitar. Especificación del acceso a los datos, para garantizar la confidencialidad. Presupuesto del ensayo clínico (compensación para los pacientes del ensayo, investigadores) se comunican al comité ético correspondiente. Garantía de la existencia de una póliza de seguro o indemnización suscrita y característica de la misma.

Ensayos clínicos Consideraciones prácticas Especificar las responsabilidades de todos los participantes en el ensayo clínico. Especificar las condiciones de archivo de datos, su manejo, procesamiento y correcciones. Identificación de las muestras de investigación clínica y responsables de su suministro, etiquetado y conservación. Condiciones de publicación.

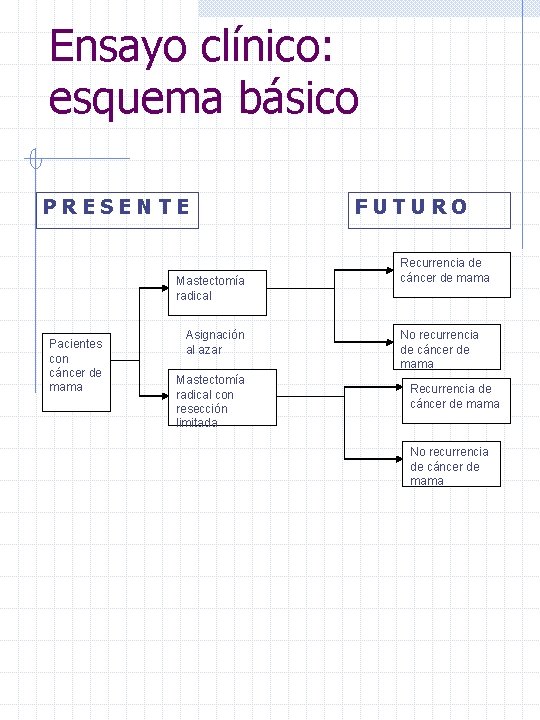
Ensayo clínico: esquema básico PRESENTE Mastectomía radical Pacientes con cáncer de mama Asignación al azar Mastectomía radical con resección limitada FUTURO Recurrencia de cáncer de mama No recurrencia de cáncer de mama

Ensayo clínico Ejemplo: la tasa de recuperación de tuberculosis según tratamiento: Tipo de Resultado Total tratamien Baciloscopía to Positivo Negativo Corto a b a + b Largo c d c + d Total a + c b + d a + b + c + d Tasa de recuperación por tratamiento corto: b / (a + b) = g % Tasa de recuperación por tratamiento largo: d / (c + d) = h % Si g % > h % entonces preferimos tratamiento corto.