Facult de Mdecince Ibn El Jazar A U

Faculté de Médecince Ibn El. Jazar A. U: 2010 -2011 Département de Biochimie BIOENERGETIQUE Thermodynamique chimique Oxydoréduction Chaîne respiratoire mitochondriale Dr. GHRAIRI Taoufik 1
La bioénergétique, c’est quoi? Les êtres vivants utilisent d’énergies pour exécuter des travaux aliments Catabolisme ATP R° nécessitant de l’énergie Ø La bioénergétique s’intéresse aux lois qui régissent la production, les échanges d’énergie à l’intérieur de la cellule et les réaction chimiques qui sont impliquées Ø Ces transferts d’énergies obéissent aux lois de la thermodynamique 2

3

Bref Historique! La thermodynamique est une science qui naît à la fin du XVIIème siècle. Denis Papin (1647 -1714) physicien français, qui a imaginé l’ancêtre des machines à vapeur. von helmholtz (1847) 1 er principe R. Clausius (1865) 2ème principe J. Gibbs (1839 -1903) enthalpie libre (G) 4

I. INTRODUCTION GENERALE La thermodynamique : Repose sur le concept de Système (ouvert, fermé ou isolé) & Deux lois. A pour objet l’étude des échanges d’énergie qui accompagnent les changements d’états d’un système. Energie interne (U) : énergie thermique totale Elle se préoccupe que de l’état initial et final du système. 5

1 ière Loi : C’est le principe de la conservation de l’énergie L’énergie de l’univers est constante. Elle peut être transformée, transportée ; elle ne peut être ni détruite, ni créée. U=Q+W U: énergie interne, exprimé en J Q: chaleur échangée w: travail effectué lors du changement (Chimique, électrique…) 6
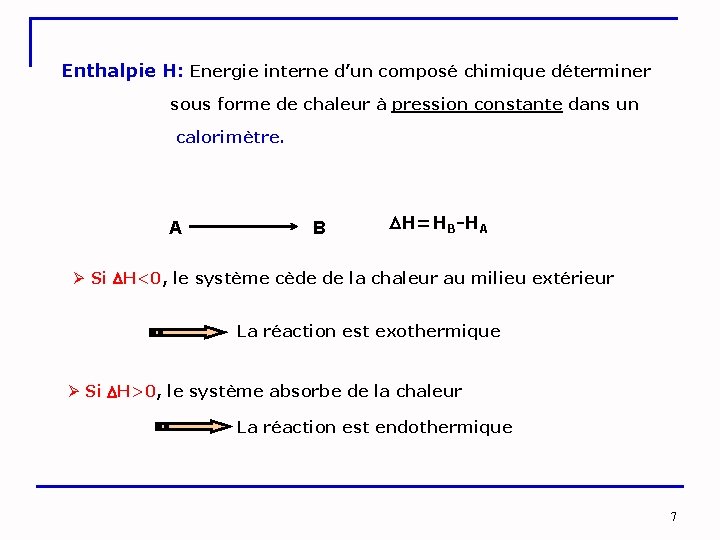
Enthalpie H: Energie interne d’un composé chimique déterminer sous forme de chaleur à pression constante dans un calorimètre. A B H=HB-HA Ø Si H<0, le système cède de la chaleur au milieu extérieur La réaction est exothermique Ø Si H>0, le système absorbe de la chaleur La réaction est endothermique 7

q Enthalpie standard de formation 6 C +12 H+ 6 O C 6 H 1206 glucose : Hf°=-1274 k. J. mol-1 q Enthalpiede liaison 2 H + O H 2 O H=-927 k. Jmol-1 q Loi de Hess L’enthalpie globale d’une réaction est la somme des enthalpies des réactions individuelles qui la composent. 8

2ème Loi : L’entropie du système et de son environnement augmente au cours d’une réaction spontané : S>0 Définition de l’entropie: - L’entropie «S» est considérée comme un reflet du désordre d’un système. - Toute réaction chimique tendant à diminuer l’ordre dans une molécule est favorisée au plan énergétique 9

II. Notions d’énergie totale et d’énergie libre II. 1. Définition Tout composé biochimique possède une énergie interne A pression constante, cette énergie est appelée enthalpie H. La fraction utilisable de cette énergie est appelé énergie libre (G) G=H-T. S (exprimée en calorie. mol-1 ou en joule. mol-1). 10

en Biochimie en s’intéresse au G A B On : G=GB- GA Donc G= H-T S Si G<0 ( GB< GA), réaction exergonique et spontanée Si G>0 ( GB> GA), réaction endergonique et non spontanée Si G=0, la réaction est en équilibre 11
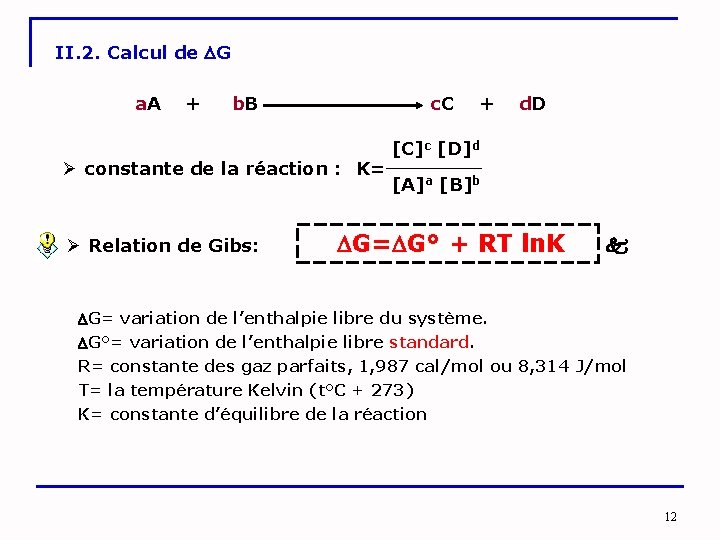
II. 2. Calcul de G a. A + b. B c. C + d. D Ø constante de la réaction : K= Ø Relation de Gibs: [C]c [D]d [A]a [B]b G= G° + RT ln. K G= variation de l’enthalpie libre du système. G°= variation de l’enthalpie libre standard. R= constante des gaz parfaits, 1, 987 cal/mol ou 8, 314 J/mol T= la température Kelvin (t°C + 273) K= constante d’équilibre de la réaction 12

II. 3. Conditions standard et calcul de G° Les conditions standard chimique : q La concentration de chaque réactant est égale à 1 M ou 1 mol/l q La température T est égale à 298°K q La concentration des protons est égale à 1 M soit un p. H=0 Dans ces conditions K=1 et ln. K=0 G= G° + RT. ln. K G= G° =0 A l’équilibre G=0 G= G° + RT. ln. K =0 G° = -RT. ln. Ke 13

II. 4. Conditions biologiques et calcul de G’ et G°’ En biologie, les réactions se déroulent à p. H 7. La variation d’enthalpie libre est notée G’ G’= G°’ + RT ln. K Les conditions standard biologiques sont: q Concentration des réactants dissous =1 M q Température : 25 °C ou 298 °K q Concentration des protons =10 -7 ou p. H 7 G°’ dans les conditions standard : G°’=-RT ln. Ke 14

Expemple: La phospohoglucoisomérase catalyse la réaction suivante : Glucose-6 -Phosphate Fructose-6 -Phosphate Ke=2 G°= -RT ln. Ke = -8, 314 x 298 xln 2=-1, 7 k. J/mol 15

II. 5. Nature additives de la variation de G Dans une cellule aucune réaction n’est isolée. Elle est impliquée dans une séquence de réaction A B C D Pour chaque étape on peut écrire : A B G’AB B C G’BC C D G’CD La réaction globale est : A D G’AD= G’AB+ G’BC+ G’CD 16
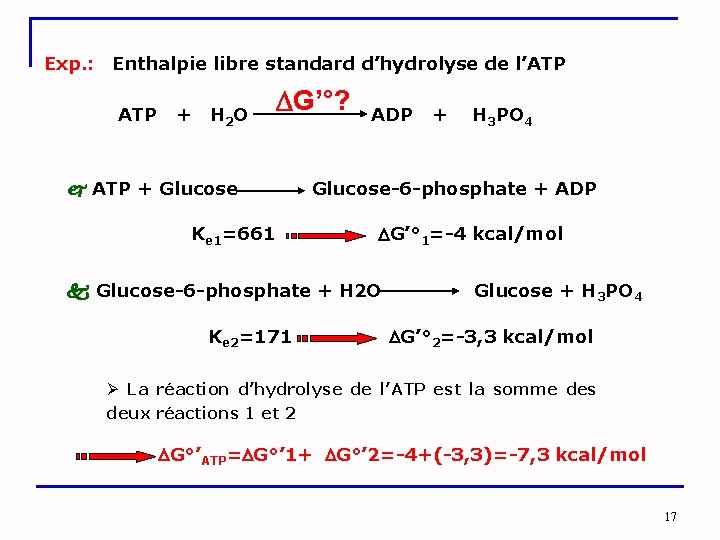
Exp. : Enthalpie libre standard d’hydrolyse de l’ATP G’°? ATP + H 2 O ADP + H 3 PO 4 ATP + Glucose-6 -phosphate + ADP Ke 1=661 G’° 1=-4 kcal/mol Glucose-6 -phosphate + H 2 O Glucose + H 3 PO 4 Ke 2=171 G’° 2=-3, 3 kcal/mol Ø La réaction d’hydrolyse de l’ATP est la somme des deux réactions 1 et 2 G°’ATP= G°’ 1+ G°’ 2=-4+(-3, 3)=-7, 3 kcal/mol 17

II. 6. Enthalpie libre standard d’hydrolyse des liaisons phosphates riches en énergie II. 6. 1. Les phosphodérivés riches en énergie Le métabolisme cellulaire permet la formation ce liaison phosphate riche en énergie. L’hydrolyse de ces liaisons libère de l’énergie qui peut être utilisée R-O PO 3 + H 20 ROH + H 3 PO 4 G°’ <0 E 18
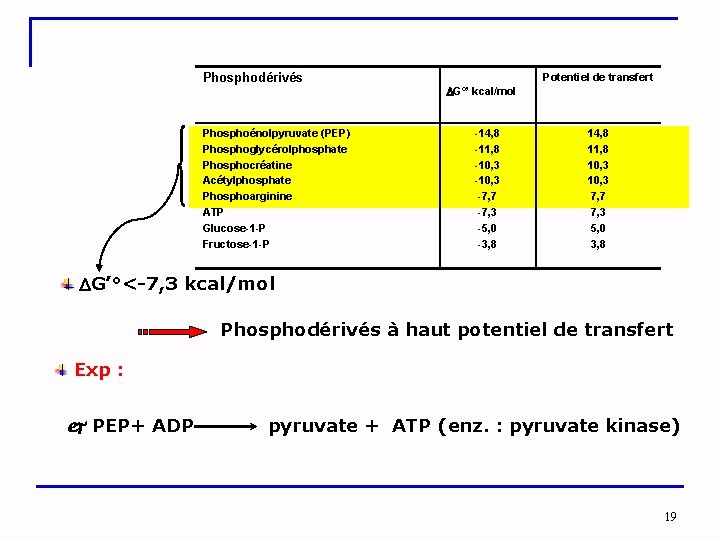
Phosphodérivés Phosphoénolpyruvate (PEP) Phosphoglycérolphosphate Phosphocréatine Acétylphosphate Phosphoarginine ATP Glucose-1 -P Fructose-1 -P Potentiel de transfert G°’ kcal/mol -14, 8 -11, 8 -10, 3 -7, 7 -7, 3 -5, 0 -3, 8 14, 8 11, 8 10, 3 7, 7 7, 3 5, 0 3, 8 G’°<-7, 3 kcal/mol Phosphodérivés à haut potentiel de transfert Exp : PEP+ ADP pyruvate + ATP (enz. : pyruvate kinase) 19
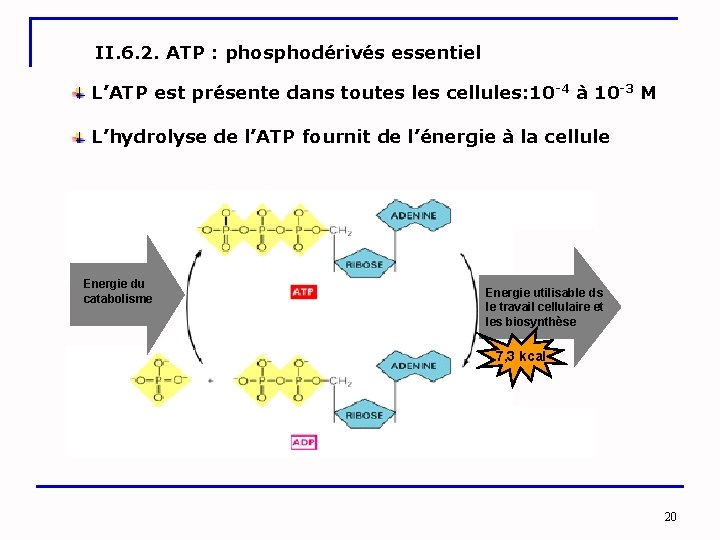
II. 6. 2. ATP : phosphodérivés essentiel L’ATP est présente dans toutes les cellules: 10 -4 à 10 -3 M L’hydrolyse de l’ATP fournit de l’énergie à la cellule Energie du catabolisme Energie utilisable ds le travail cellulaire et les biosynthèse 7, 3 kcal 20

Rôle de l’ATP • Donneur d’énergie Energie mécanique Energie osmotique Energie chimique Energie électrique Energie calorique • Donneur de phosphate (phosphorylation) • Donneur de pyrophosphate (activation de B 1) • Donneur d’AMP (activation des AG ou AA) • Donneur d’adénosine (synthèse de coenzyme B 12) 21
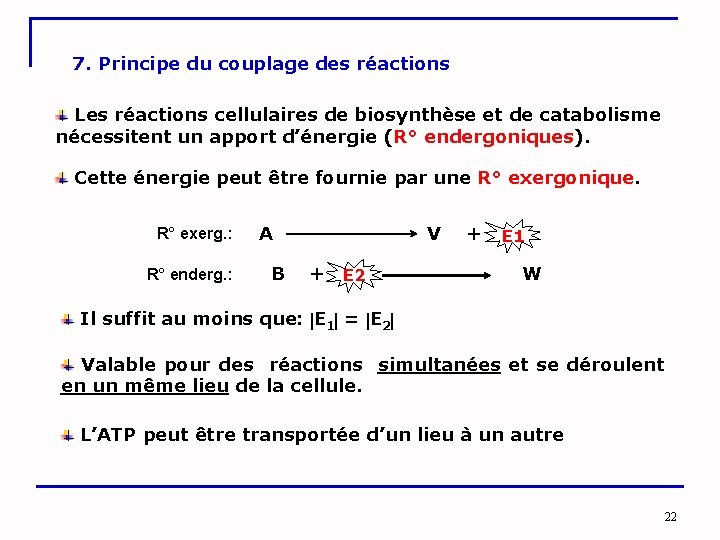
7. Principe du couplage des réactions Les réactions cellulaires de biosynthèse et de catabolisme nécessitent un apport d’énergie (R° endergoniques). Cette énergie peut être fournie par une R° exergonique. R° exerg. : R° enderg. : A V + E 1 B + W E 2 Il suffit au moins que: E 1 = E 2 Valable pour des réactions simultanées et se déroulent en un même lieu de la cellule. L’ATP peut être transportée d’un lieu à un autre 22

Exemple de couplage : PEP + H 2 O Pyruvate + Pi G’°=-50 k. J. mol-1 ADP + Pi H 2 O + ATP G’°=+30 k. J. mol-1 PEP + ADP Pyruvate + ATP pyruvate kinase G’°=-15 k. J. mol-1 ATP + H 2 O ADP + Pi G’°=-30 k. J. mol-1 Glucose + Pi Glucose-P + ADP G’°=+15 k. J. mol-1 Glucose + ATP Glucose-P + ADP hexokinase G’°=-15 k. J. mol-1 23
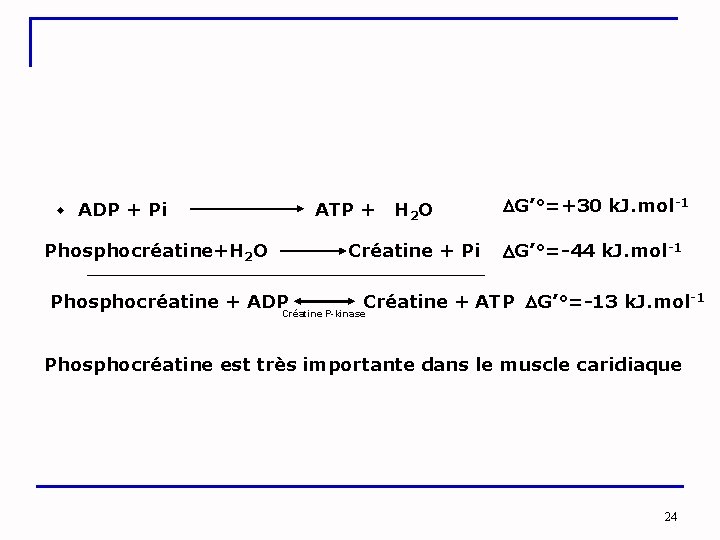
ADP + Pi ATP + H 2 O G’°=+30 k. J. mol-1 Phosphocréatine+H 2 O Créatine + Pi G’°=-44 k. J. mol-1 Phosphocréatine + ADP Créatine + ATP G’°=-13 k. J. mol-1 Créatine P-kinase Phosphocréatine est très importante dans le muscle caridiaque 24

Les différent types de couplages cellulaires couplage chimio-chimique (couplage d'une réaction exergonique à une réaction endergonique). coulage chimio-osmotique (couplage d'une exergonique à un transport de matière défavorisé). réaction couplage osmo-chimique (couplage d'un transport spontané de matière à une réaction endergonique). 25

RESUMÉ Les transferts d’énergie dans les systèmes biologiques obéissent aux loi générales de la thermodynamique - L’énergie n’est pas gratuite (1 er principe), - Les transformations spontanées induisent un gaspillage d’énergie vers des formes moins «nobles» , notamment un échange sous forme de chaleur (2ème principe). Il est bon d’insister sur la différence entre G et G°! - G° est une constante pour une réaction chimique. - la valeur de G dépend des concentrations respectives des réactants et c’est le signe de G qui dans des conditions déterminées indique le sens de la réaction 26

27

I. REACTION D’OXYDO-REDUCTION I. 1. Définition • Oxydation: perte d’électrons ox 1 red 1 Zn Zn 2+ + 2é • Réduction : gain d’électrons Cu 2+ + ox 2 2é Cu red 2 Les réactions d’oxydo-réduction font intervenir des transferts d’électrons d’un composé à un autre. Bilan Zn + Cu 2+ Zn 2+ + Cu (Zn 2+/Zn) et (Cu 2+/Cu) sont des couples redox (ou des demipiles) 28
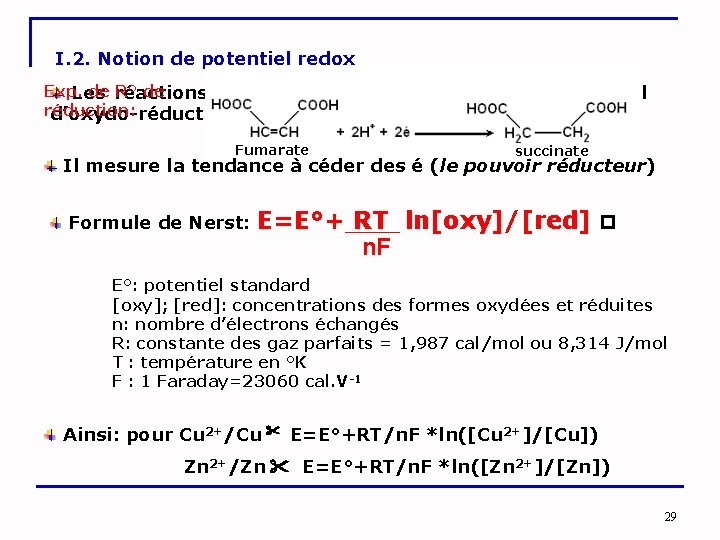
I. 2. Notion de potentiel redox Exp. de R° de Les réactions rédox sont caractérisées par un potentiel réduction: d’oxydo-réduction (E). Fumarate succinate Il mesure la tendance à céder des é (le pouvoir réducteur) Formule de Nerst: E=E°+ RT ln[oxy]/[red] n. F E°: potentiel standard [oxy]; [red]: concentrations des formes oxydées et réduites n: nombre d’électrons échangés R: constante des gaz parfaits = 1, 987 cal/mol ou 8, 314 J/mol T : température en °K F : 1 Faraday=23060 cal. V-1 Ainsi: pour Cu 2+/Cu E=E°+RT/n. F *ln([Cu 2+]/[Cu]) Zn 2+/Zn E=E°+RT/n. F *ln([Zn 2+]/[Zn]) 29

Le potentiel d’oxydo-réduction est mesuré par rapport à un couple de référence: l’électrode à hydrogène. H+ + é ½H 2 E°=0 par définition Ainsi : Cu 2+ + 2é Cu E°= +0, 35 Zn 2+ + 2é Zn E°= -0, 75 E°<0 la substance a une affinité faible pour les électrons E°>0 la substance a une affinité élevée pour les électrons oxydant réducteur D’où pour le système E°=E°Cu- E°Zn=0, 35+0, 75=1, 1 v Si E°>0: réactions d’oxydo-red. possible spontanément Si E°<0: réactions d’oxydo-red. non possible nécessitent de l’énergie 30
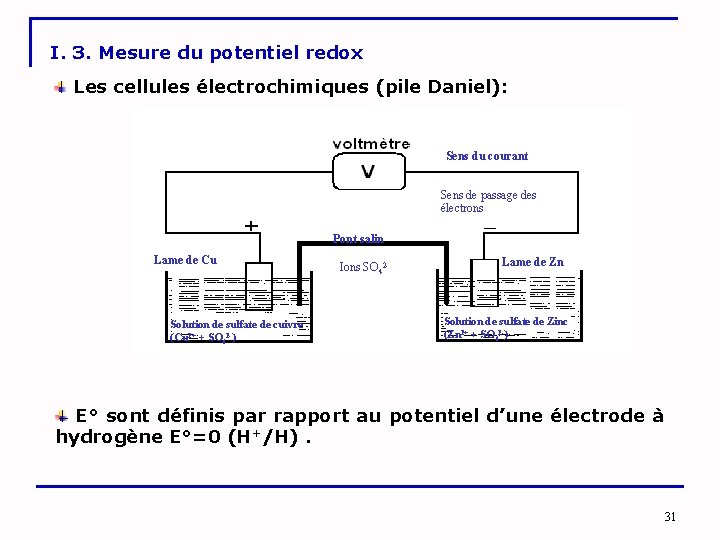
I. 3. Mesure du potentiel redox Les cellules électrochimiques (pile Daniel): Sens du courant Sens de passage des électrons Pont salin Lame de Cu Solution de sulfate de cuivre (Cu 2+ + SO 42 -) Ions SO 42 - Lame de Zn Solution de sulfate de Zinc (Zn 2+ + SO 42 -) E° sont définis par rapport au potentiel d’une électrode à hydrogène E°=0 (H+/H). 31

I. 4. Conditions standard : calcul de E° d’un couple dépend de la concentration des formes réduite et oxydée, de la température et du p. H Pour cette raison on défini les conditions standard suivante: § Température: 25 °C ou 298 °K § Concentration de chacun des réactant dissous = à 1 M § Concentration des protons égale à 1 M (p. H 0) Dans ces conditions ln[oxy]/[red]=0 Formule en déduit que E=E° 32

I. 5. Conditions standard biologiques : calcul de E’ et E°’ Ds les tissus biologiques le p. H est 7. Le potentiel est défini à p. H 7. Il est noté E’. Les conditions biologiques standard sont: § Température: 25 °C ou 298 °K § Concentration de chacun des réactant dissous = à 1 M § Concentration des protons égale à 10 -7 M (p. H 7) Avec le même raisonnement on définit le potentiel redox standard noté E°’. 33

I. 6. Variation d’énergie libre dans les réactions redox On sait que : - Seules R° rédox dont E>0 sont spontanées - Seules R° dont G<0 sont spontanées Ainsi ds une R° d’oxydo-réduction spontanée, E>0 et G<0 La relation ente les deux paramètre est: G=-n. F E n: nombre d’électrons échangés entre le réducteur et l’oxydant F: Constante de Faraday E= variation du potentiel en volt =différence entre le potentiel de l’accepteur et le potentiel du donneur d’électrons Ds les condition standard chimiques: G°=-n. F E° à p. H 0 biologiques: G°’=-n. F E°’ à p. H 7 34
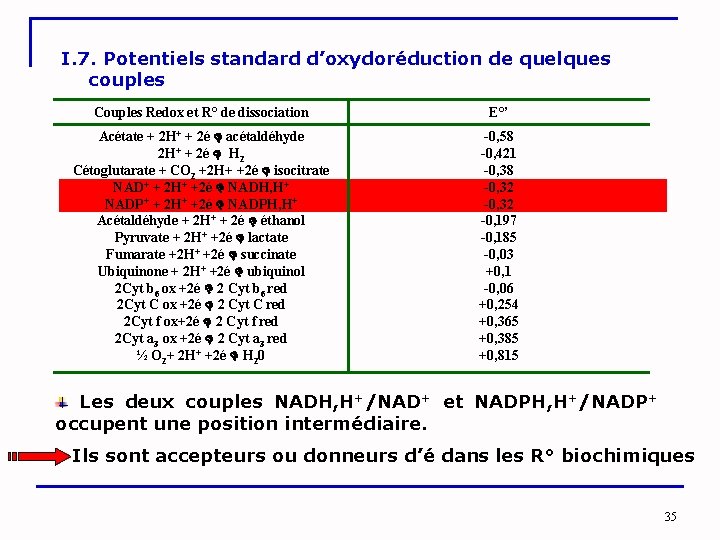
I. 7. Potentiels standard d’oxydoréduction de quelques couples Couples Redox et R° de dissociation E°’ Acétate + 2 H+ + 2é acétaldéhyde 2 H+ + 2é H 2 Cétoglutarate + CO 2 +2 H+ +2é isocitrate NAD+ + 2 H+ +2é NADH, H+ NADP+ + 2 H+ +2é NADPH, H+ Acétaldéhyde + 2 H+ + 2é éthanol Pyruvate + 2 H+ +2é lactate Fumarate +2 H+ +2é succinate Ubiquinone + 2 H+ +2é ubiquinol 2 Cyt b 6 ox +2é 2 Cyt b 6 red 2 Cyt C ox +2é 2 Cyt C red 2 Cyt f ox+2é 2 Cyt f red 2 Cyt a 3 ox +2é 2 Cyt a 3 red ½ O 2+ 2 H+ +2é H 20 -0, 58 -0, 421 -0, 38 -0, 32 -0, 197 -0, 185 -0, 03 +0, 1 -0, 06 +0, 254 +0, 365 +0, 385 +0, 815 Les deux couples NADH, H+/NAD+ et NADPH, H+/NADP+ occupent une position intermédiaire. Ils sont accepteurs ou donneurs d’é dans les R° biochimiques 35
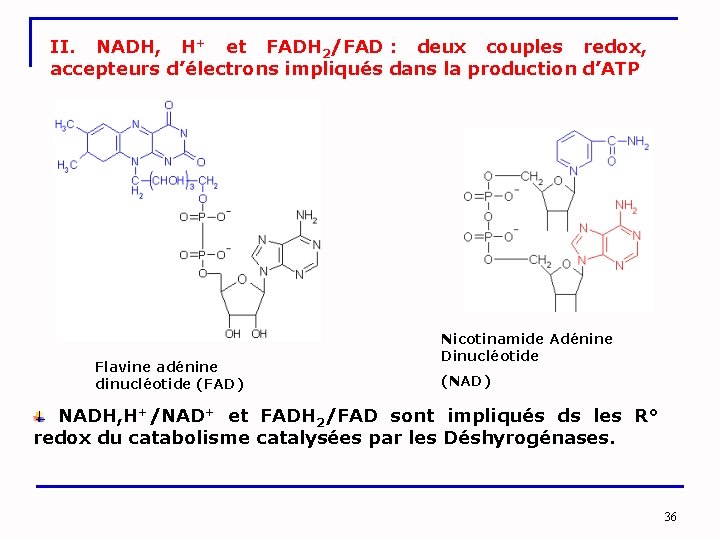
II. NADH, H+ et FADH 2/FAD : deux couples redox, accepteurs d’électrons impliqués dans la production d’ATP Flavine adénine dinucléotide (FAD) Nicotinamide Adénine Dinucléotide (NAD) NADH, H+/NAD+ et FADH 2/FAD sont impliqués ds les R° redox du catabolisme catalysées par les Déshyrogénases. 36
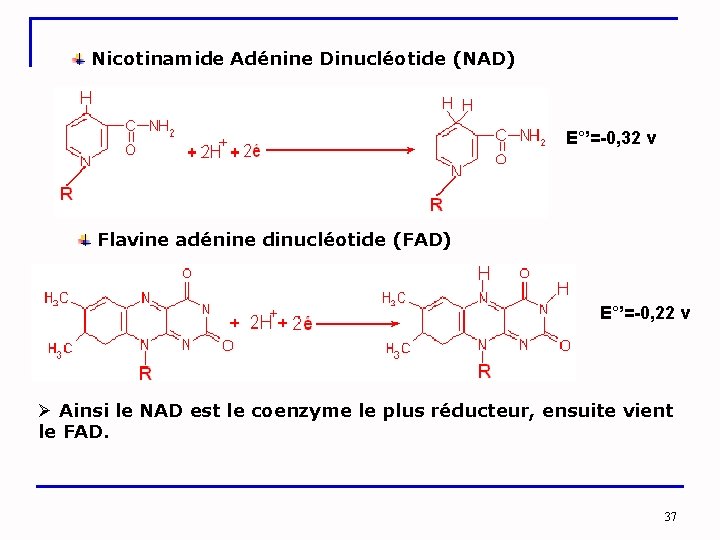
Nicotinamide Adénine Dinucléotide (NAD) E°’=-0, 32 v Flavine adénine dinucléotide (FAD) E°’=-0, 22 v Ø Ainsi le NAD est le coenzyme le plus réducteur, ensuite vient le FAD. 37
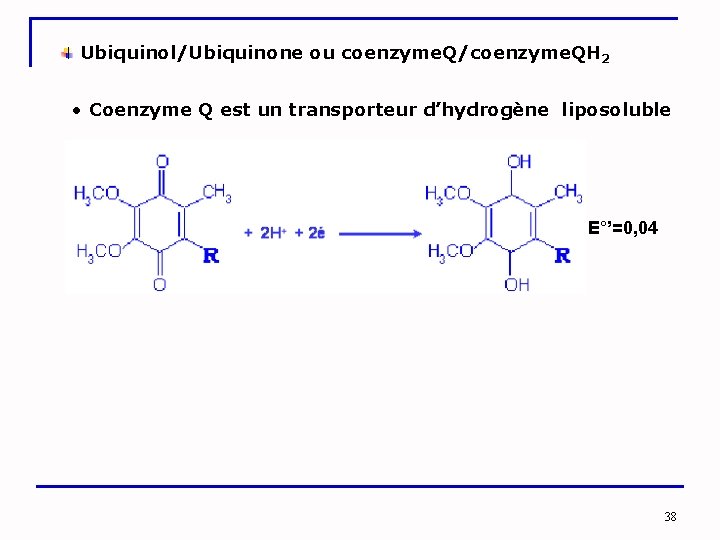
Ubiquinol/Ubiquinone ou coenzyme. Q/coenzyme. QH 2 • Coenzyme Q est un transporteur d’hydrogène liposoluble E°’=0, 04 38
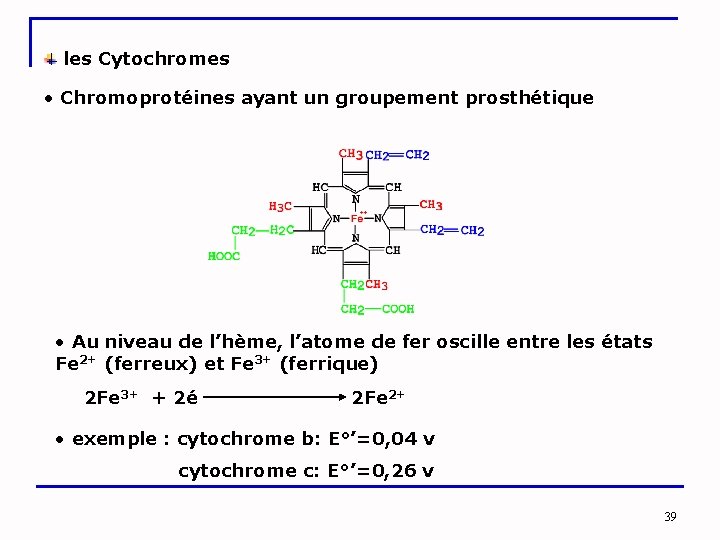
les Cytochromes • Chromoprotéines ayant un groupement prosthétique • Au niveau de l’hème, l’atome de fer oscille entre les états Fe 2+ (ferreux) et Fe 3+ (ferrique) 2 Fe 3+ + 2é 2 Fe 2+ • exemple : cytochrome b: E°’=0, 04 v cytochrome c: E°’=0, 26 v 39
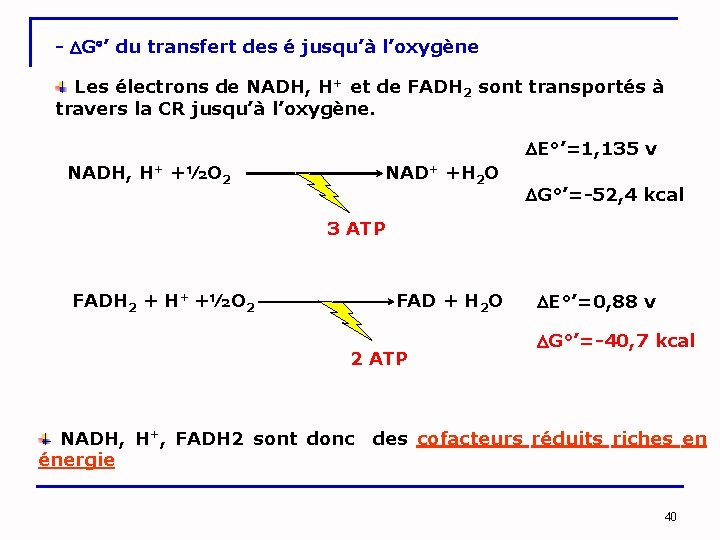
- G ’ du transfert des é jusqu’à l’oxygène Les électrons de NADH, H+ et de FADH 2 sont transportés à travers la CR jusqu’à l’oxygène. E°’=1, 135 v NADH, H+ +½O 2 NAD+ +H 2 O G°’=-52, 4 kcal 3 ATP FADH 2 + H+ +½O 2 FAD + H 2 O 2 ATP E°’=0, 88 v G°’=-40, 7 kcal NADH, H+, FADH 2 sont donc des cofacteurs réduits riches en énergie 40

RESUMÉ R° d’oxydoréduction Réaction mettant en jeu l’échange des électrons entre deux couples Redox Oxydation : perte d’électrons : H 2 2 H+ + 2é Réduction : gain d’électrons : ½O 2 + 2é O 2 Total : H 2 + ½O 2 H 2 O Potentiel biologique E°<0 la substance a une affinité faible pour les é E°>0 la substance a une affinité élevée pour les é standard E°’ Différence de potentiel Travail de d’électrons transport Relation entre G° et E° E E=E(accepteur)-E(donneur) Equation de Nerst E=E°+RT*log([ox]/[red])/n. F E°: potentiel standard n: nombre d’électrons échangés R: constante des gaz parfaits=8, 314 J/mol T : température en °K F : constante de Faraday=96500 coulombs G°=- E°. n. F 41

Faculté de Médecince Ibn El. Jazar A. U: 2008 -2009 Département de Biochimie BIOENERGETIQUE Chaîne respiratoire Dr. GHRAIRI Taoufik 42
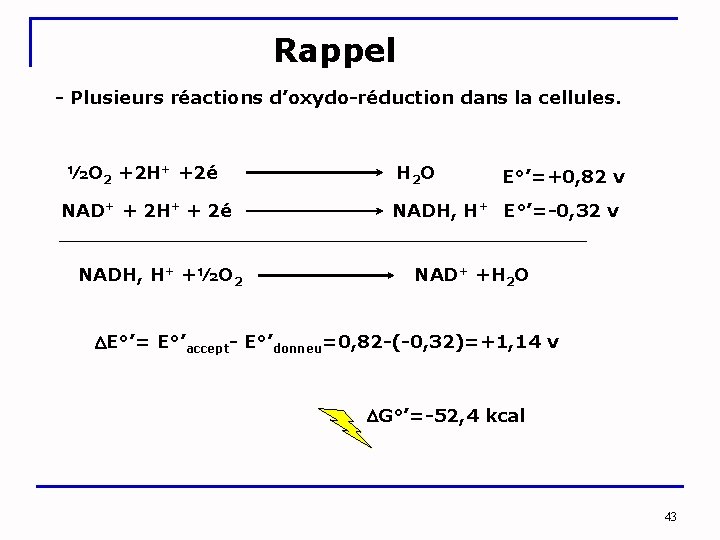
Rappel - Plusieurs réactions d’oxydo-réduction dans la cellules. ½O 2 +2 H+ +2é H 2 O E°’=+0, 82 v NAD+ + 2 H+ + 2é NADH, H+ E°’=-0, 32 v NADH, H+ +½O 2 NAD+ +H 2 O E°’= E°’accept- E°’donneu=0, 82 -(-0, 32)=+1, 14 v G°’=-52, 4 kcal 43
- NADH, H+ et FADH 2 sont accepteurs d’électrons impliqués dans la production d’ATP Flavine adénine dinucléotide (FAD) Nicotinamide Adénine Dinucléotide (NAD) - L’ATP est phosphodérivés essentiel mais…! - L’hydrolyse de ces liaisons libère de l’énergie utilisable 44

45

1. INTRODUCTION L’ATP est la seule source universelle d’ATP pour la cellule 3 modalités de formation d’ATP dans la cellule: 1. Phosphorylation photosynthétique 2. Phosphorylation au niveau du substrat PEP + ADP pyruvate + ATP 3. Phosphorylation Oxydative Glucose 6 CO 2+2 ATP+2 GTP +10 NADH, H+ + 2 FADH 2 Ré-oxydation dans la mitochondrie Transfert d’é jusqu’à l’Oxygène 46
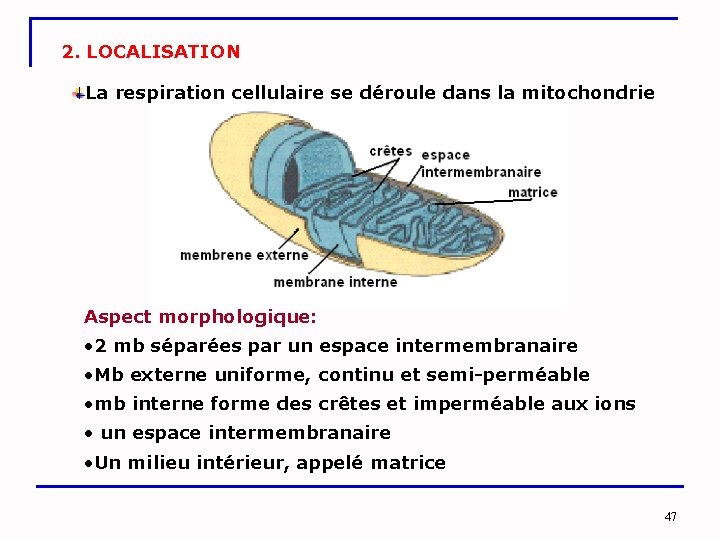
2. LOCALISATION La respiration cellulaire se déroule dans la mitochondrie Aspect morphologique: • 2 mb séparées par un espace intermembranaire • Mb externe uniforme, continu et semi-perméable • mb interne forme des crêtes et imperméable aux ions • un espace intermembranaire • Un milieu intérieur, appelé matrice 47
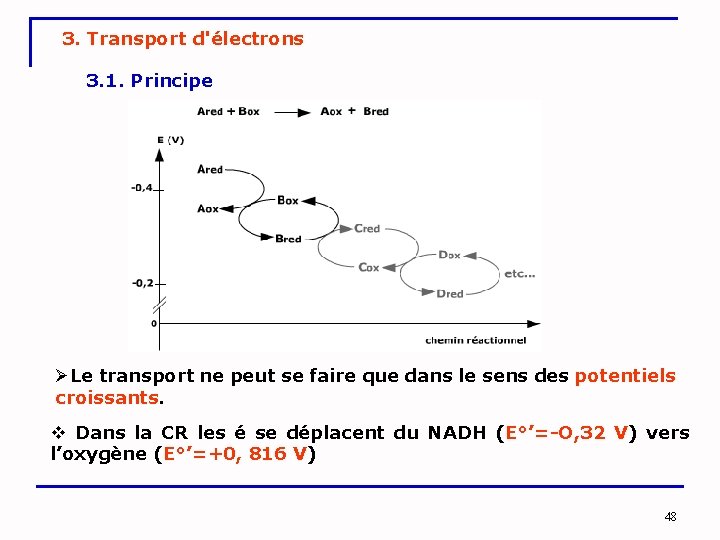
3. Transport d'électrons 3. 1. Principe ØLe transport ne peut se faire que dans le sens des potentiels croissants. Dans la CR les é se déplacent du NADH (E°’=-O, 32 V) vers l’oxygène (E°’=+0, 816 V) 48
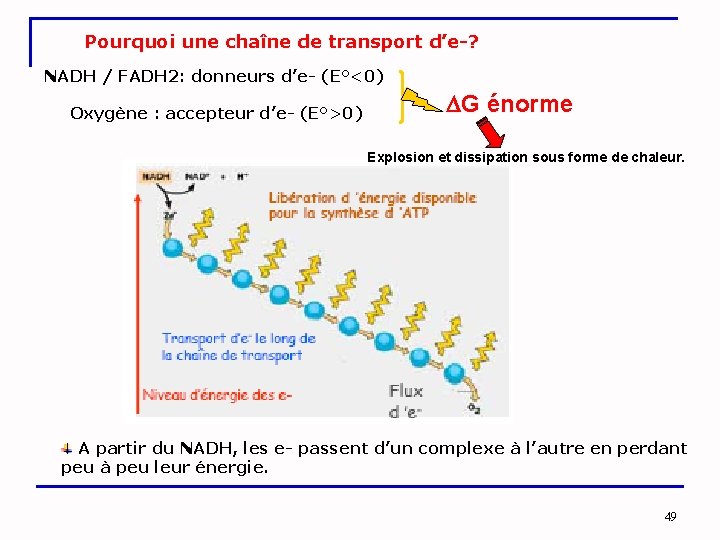
Pourquoi une chaîne de transport d’e-? NADH / FADH 2: donneurs d’e- (E°<0) Oxygène : accepteur d’e- (E°>0) G énorme Explosion et dissipation sous forme de chaleur. A partir du NADH, les e- passent d’un complexe à l’autre en perdant peu à peu leur énergie. 49

3. 2. Chaine de transport des électrons Ø Elle sert à fractionner l’énergie des électrons qui vont passer du NADH, H+ à l’O 2 via des transporteurs. Ø Les transporteurs sont : • • Flavines Complexes Fe-S Quinones Hèmes ØIls se trouvent liés à des protéines, à l’exception des quinones (On les considères comme des groupes prosthétiques d’enzymes) 50
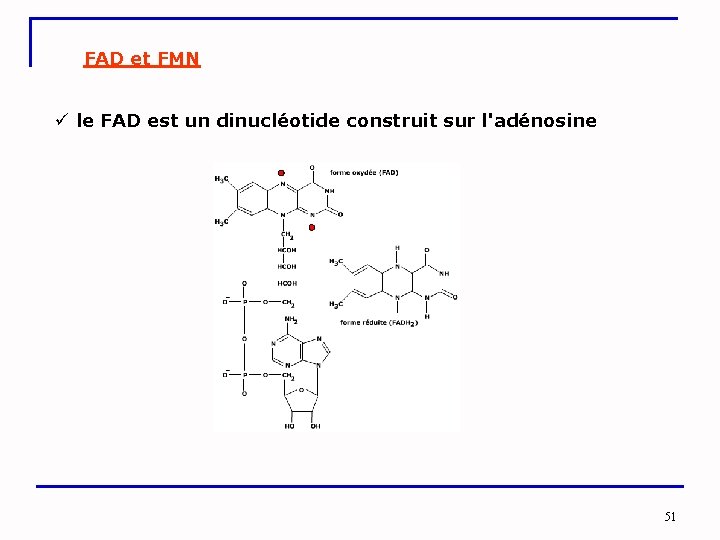
FAD et FMN ü le FAD est un dinucléotide construit sur l'adénosine 51
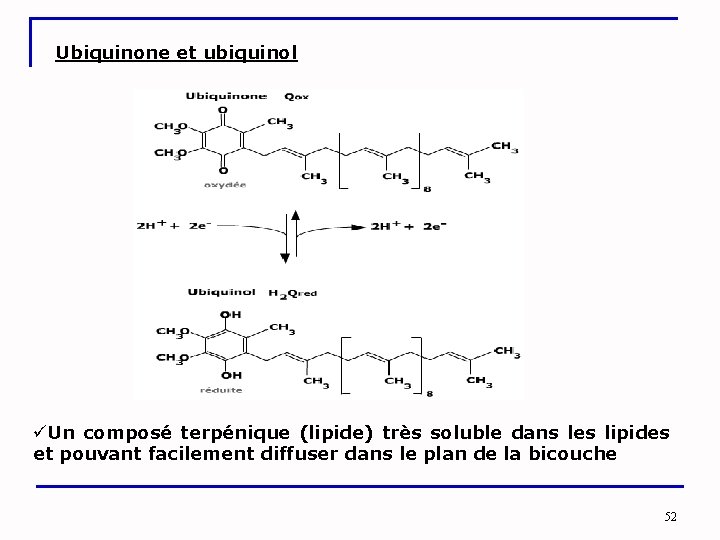
Ubiquinone et ubiquinol üUn composé terpénique (lipide) très soluble dans les lipides et pouvant facilement diffuser dans le plan de la bicouche 52
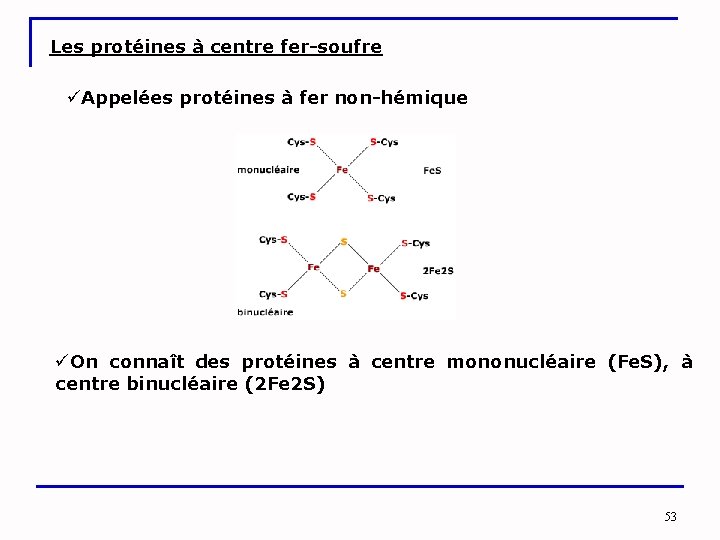
Les protéines à centre fer-soufre üAppelées protéines à fer non-hémique üOn connaît des protéines à centre mononucléaire (Fe. S), à centre binucléaire (2 Fe 2 S) 53
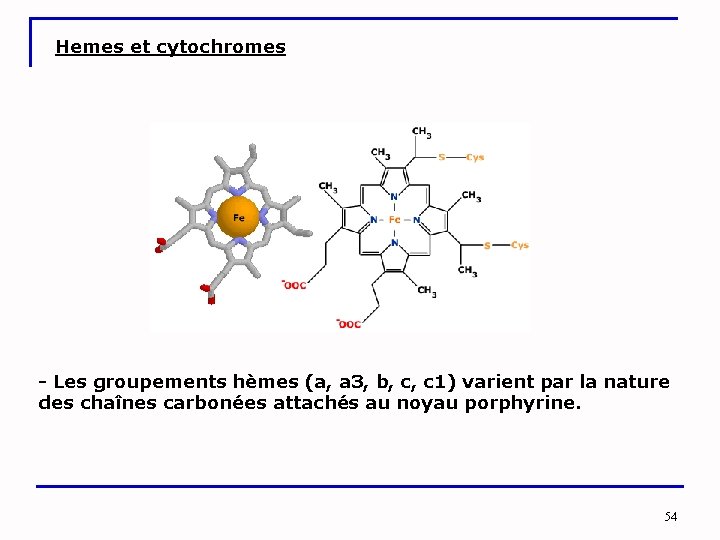
Hemes et cytochromes - Les groupements hèmes (a, a 3, b, c, c 1) varient par la nature des chaînes carbonées attachés au noyau porphyrine. 54

Partie III- Chaîne respiratoire et Phosphorylation oxydative 1. Introduction-Définition 2. Localisation 3. Transport d'électrons 4. Séquence du transport d’électrons dans la membrane mitochondriale 4. 1. Complexe I-NADH, H+-Co. Q réductase 4. 2. Complexe II-Succinate-Co. QH 2 réductase 4. 3. Complexe III-Co. QH 2 - Cythochrome réductase 4. 4. Complexe IV-Cytochrome réductase 4. 5. Organisation du transport des électrons dans la CR 5. Création de gradient de densité de protons et synthèse de l’ATP 5. 1. Gradient de densité de protons 5. 1. Mécanisme de formation de l’ATP 6. Inhibiteurs du complexe ATP synthétase 6. 1. Oigomycine 6. 2. Les découplants 7. Déficiences héritées liées à la phosphorylation oxydative 55

4. Séquence du transport d’électrons dans la membrane mitochondriale 4 complexes multienzymatiques de transporteurs d’é: Complexe I: NADH, H+-Co. Q Réductase Complexe II: Succinate-Co. Q Réductase Complexe III: Co. QH 2 -Cytochrome c Réductase Complexe IV: Cytochrome c Oxydase Un 5ème complexe, ATP synthase responsable de la phosphorylation de l’ADP en ATP L’ATP translocase permet le transport de l’ATP synthétisé vers l’e. IM en échange d’un ADP (antiport ATP-ADP ) 56
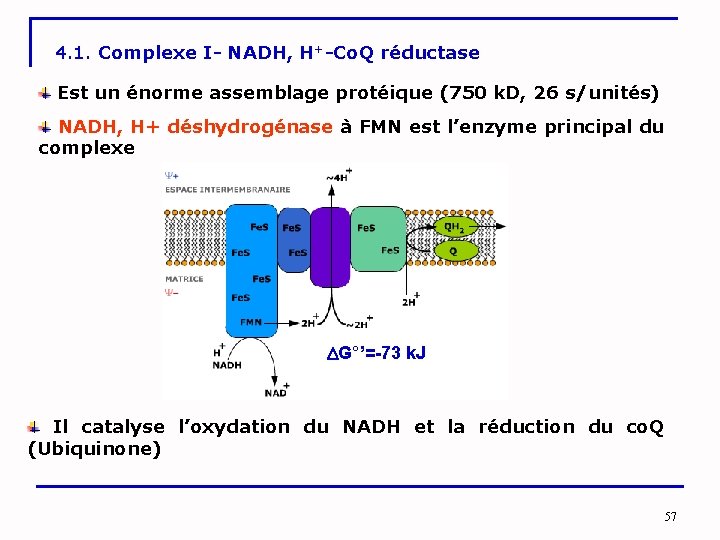
4. 1. Complexe I- NADH, H+-Co. Q réductase Est un énorme assemblage protéique (750 k. D, 26 s/unités) NADH, H+ déshydrogénase à FMN est l’enzyme principal du complexe G°’=-73 k. J Il catalyse l’oxydation du NADH et la réduction du co. Q (Ubiquinone) 57
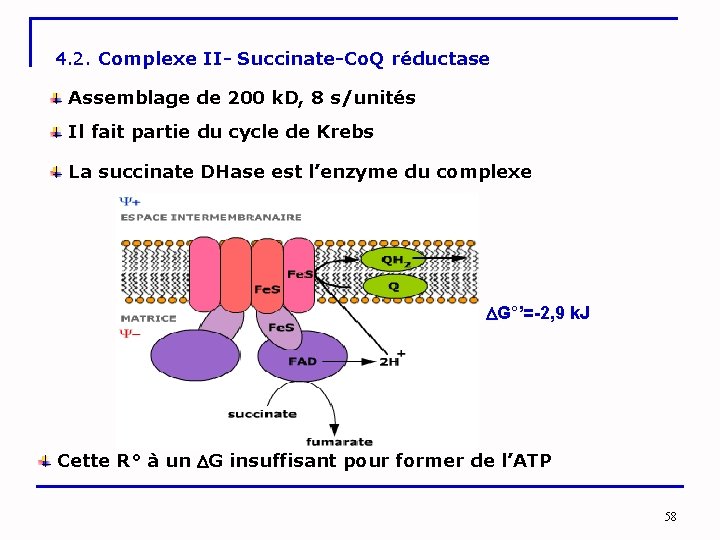
4. 2. Complexe II- Succinate-Co. Q réductase Assemblage de 200 k. D, 8 s/unités Il fait partie du cycle de Krebs La succinate DHase est l’enzyme du complexe G°’=-2, 9 k. J Cette R° à un G insuffisant pour former de l’ATP 58
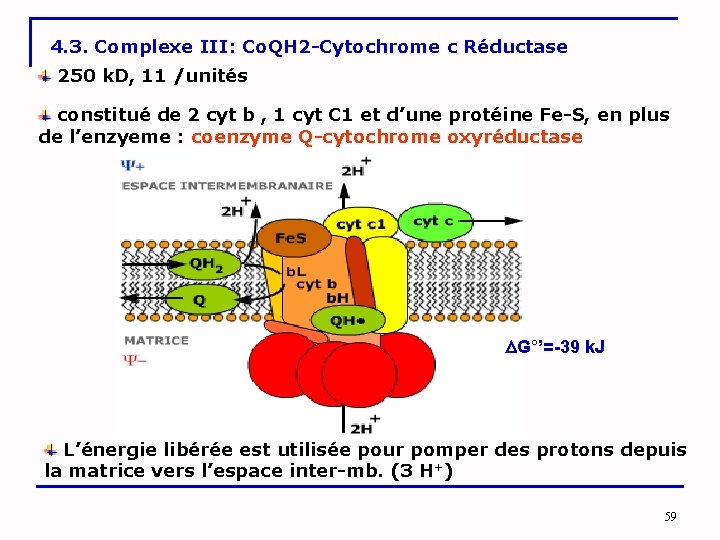
4. 3. Complexe III: Co. QH 2 -Cytochrome c Réductase 250 k. D, 11 /unités constitué de 2 cyt b , 1 cyt C 1 et d’une protéine Fe-S, en plus de l’enzyeme : coenzyme Q-cytochrome oxyréductase G°’=-39 k. J L’énergie libérée est utilisée pour pomper des protons depuis la matrice vers l’espace inter-mb. (3 H+) 59
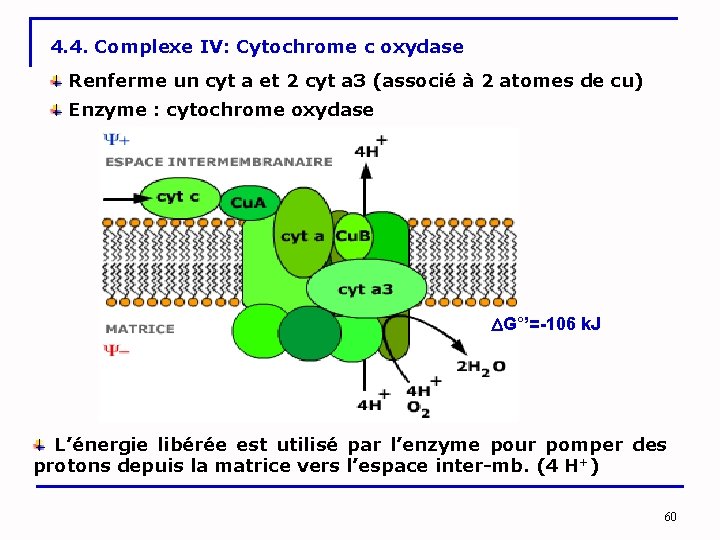
4. 4. Complexe IV: Cytochrome c oxydase Renferme un cyt a et 2 cyt a 3 (associé à 2 atomes de cu) Enzyme : cytochrome oxydase G°’=-106 k. J L’énergie libérée est utilisé par l’enzyme pour pomper des protons depuis la matrice vers l’espace inter-mb. (4 H+) 60
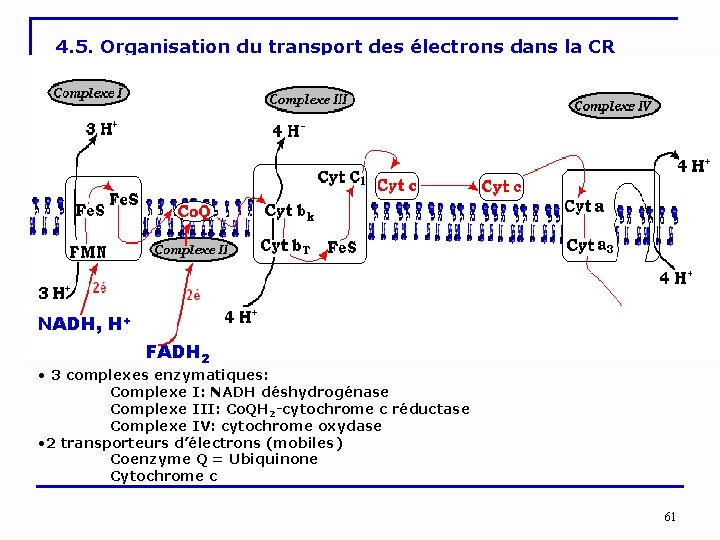
4. 5. Organisation du transport des électrons dans la CR NADH, H+ FADH 2 • 3 complexes enzymatiques: Complexe I: NADH déshydrogénase Complexe III: Co. QH 2 -cytochrome c réductase Complexe IV: cytochrome oxydase • 2 transporteurs d’électrons (mobiles) Coenzyme Q = Ubiquinone Cytochrome c 61
La circulation d’électrons entraîne une variation de potentiel E°’ ainsi qu’ une variation d’énergie libre G°’ NADH, H+ + ½ 0 2 NAD+ + H FADH 2 + ½ 02 FAD + H 2 O 2 O E°’=1, 135 V et G°’=-52, 4 kcal E°’=0, 88 V et G°’=-40, 7 kcal 1 molécule de NADH oxydée 3 molécules d’ 1 molécule de FADH 2 oxydée 2 molécules d’ ATP 62
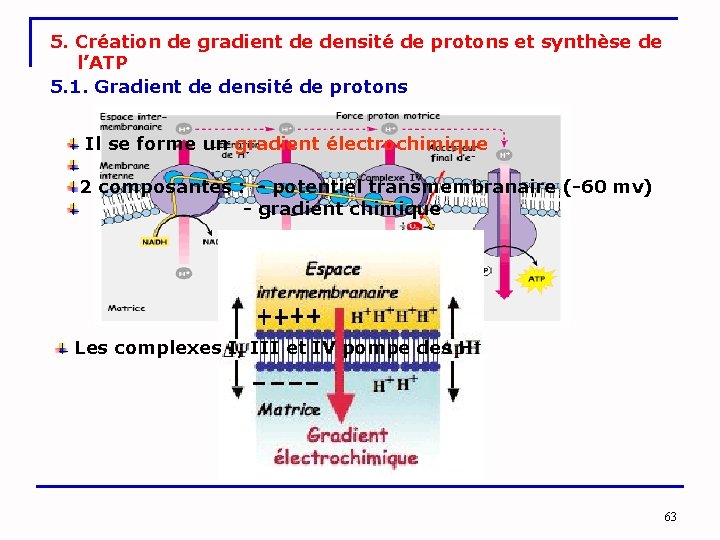
5. Création de gradient de densité de protons et synthèse de l’ATP 5. 1. Gradient de densité de protons Il se forme un gradient électrochimique 2 composantes : - potentiel transmembranaire (-60 mv) - gradient chimique Les complexes I, III et IV pompe des H+ 63
5. 2. Mécanisme de formation de l’ATP (Théorie de Mitchell) La Théorie de Mitchell: Il s’agit du couplage entre la phosphorylation et l’oxydation par l’intermédire d’un gradient de protons - Le flux d’électrons est un processus exergonique NADH, H+ +½O 2 NAD+ +H 2 O G°’=-52, 4 kcal - La phosphorylation est un processus enderognique ADP + Pi H 2 O + ATP G’°=+7, 3 kcal 64
![Lorsque la CR fonctionne le gradient de protons se forme [H+]eim> [H+]mat (X 25 Lorsque la CR fonctionne le gradient de protons se forme [H+]eim> [H+]mat (X 25](http://slidetodoc.com/presentation_image/5496fe7048e6f8faaca3798de69d5edc/image-65.jpg)
Lorsque la CR fonctionne le gradient de protons se forme [H+]eim> [H+]mat (X 25 fois) p. H 6, 2 p. H 7, 6 Les H+ situés dans l’espace intermembranaire traverser la membrane interne au niveau du « tunnel à H+ » de l ’ATPase. 65
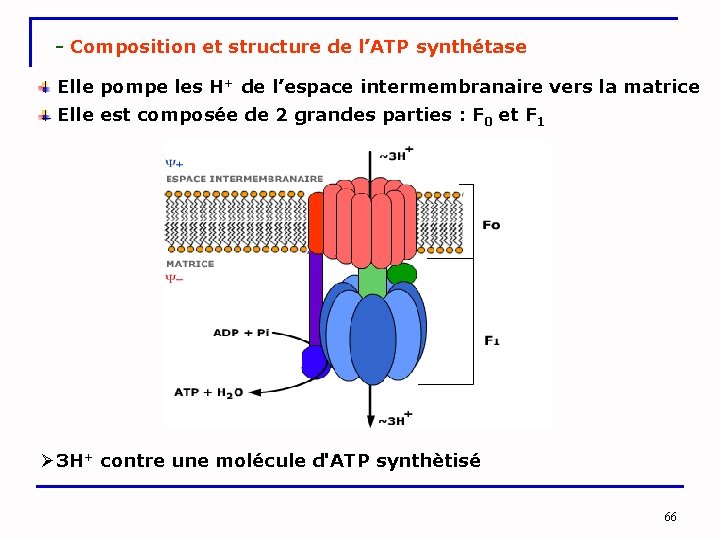
- Composition et structure de l’ATP synthétase Elle pompe les H+ de l’espace intermembranaire vers la matrice Elle est composée de 2 grandes parties : F 0 et F 1 Ø 3 H+ contre une molécule d'ATP synthètisé 66
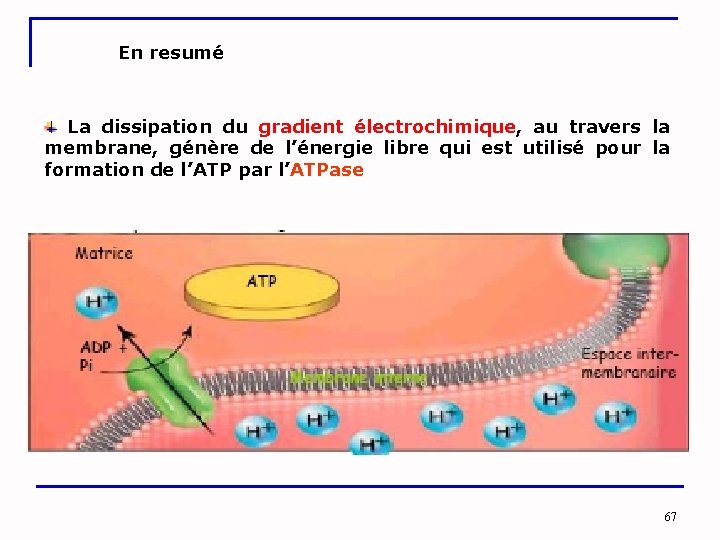
En resumé La dissipation du gradient électrochimique, au travers la membrane, génère de l’énergie libre qui est utilisé pour la formation de l’ATP par l’ATPase 67

- Contrôle de la phosphorylation oxydative La teneur en ADP assure le contrôle de la Posporylation oxydative Au repos: [ATP]>[ADP] Lors d’un effort: [ATP] (-50%) et [ADP] (10 à 100 X) [ADP]cyt [ADP]mit (Gradient H+) Pompage de H+ Activat° de l’ATPase Phosphorylat° de l’ADP R° redox couplées à ce pompage Accélération de l’oxydation des substrats et consommation O 2 68
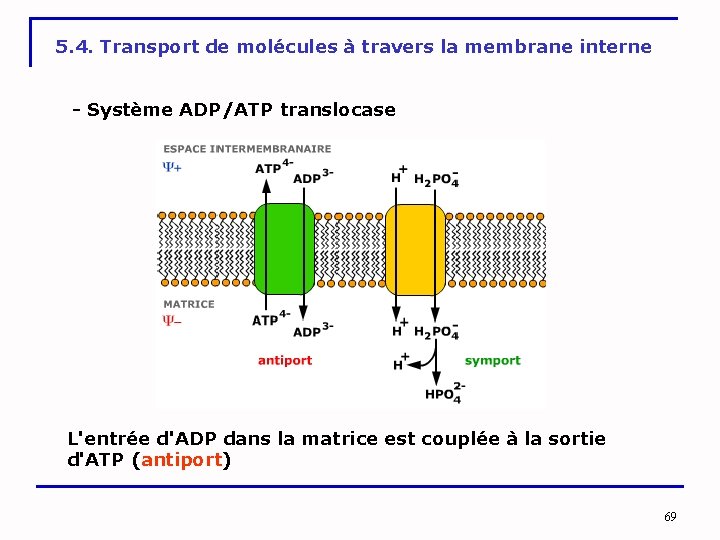
5. 4. Transport de molécules à travers la membrane interne - Système ADP/ATP translocase L'entrée d'ADP dans la matrice est couplée à la sortie d'ATP (antiport) 69

6. Inhibiteurs de la phosphorylation oxydative Les inhibiteurs du transport d’électrons • Exemples: Antymicine A, Cyanure, Amytal Il n’y a pas de création de force protonmotrice, donc pas d’ATP Les inhibiteurs de la phosphorylation oxydative • Exemples: Oligomycine L’inhibition se fait au niveau de F 0, Les découplants Dissipent le gradient de protons sans perturber le transport d’é. • Exemples: 2, 4 dinitophénol (DNP), Hormones thyroïdiennes, arséniate (Ar. O 32 -), AG non estérifiés 70
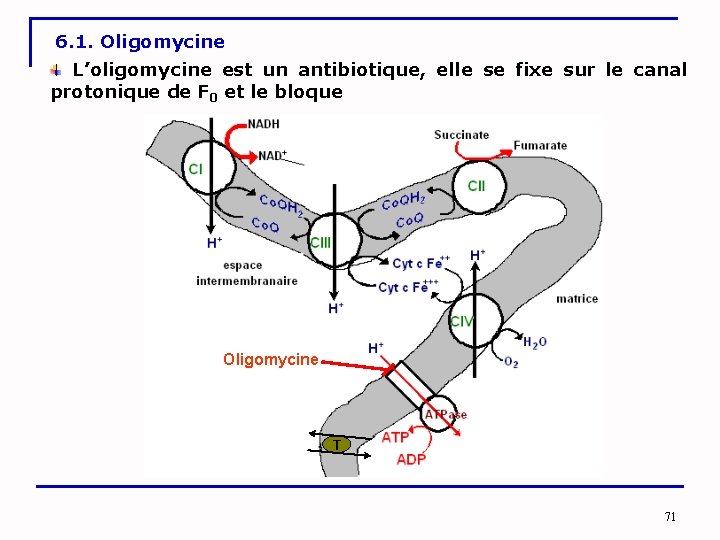
6. 1. Oligomycine L’oligomycine est un antibiotique, elle se fixe sur le canal protonique de F 0 et le bloque Oligomycine T 71
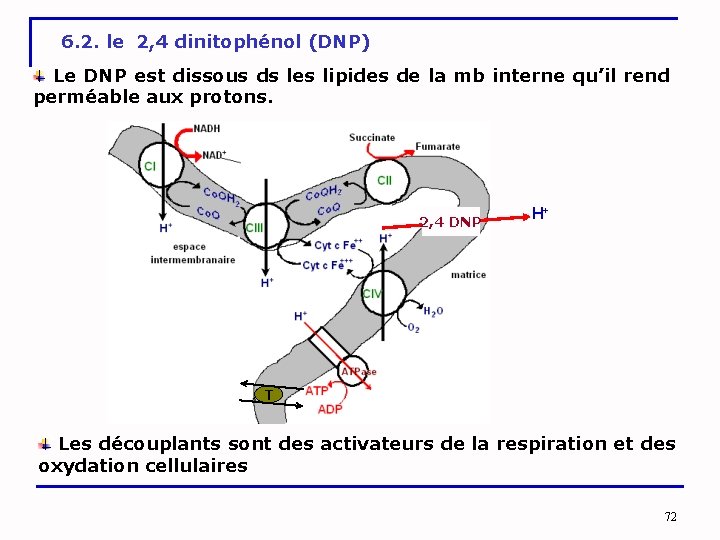
6. 2. le 2, 4 dinitophénol (DNP) Le DNP est dissous ds les lipides de la mb interne qu’il rend perméable aux protons. 2, 4 DNP H+ T Les découplants sont des activateurs de la respiration et des oxydation cellulaires 72
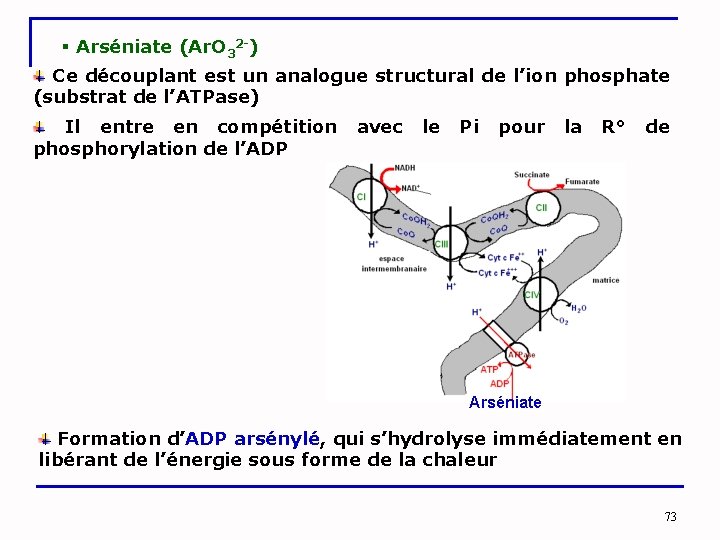
§ Arséniate (Ar. O 32 -) Ce découplant est un analogue structural de l’ion phosphate (substrat de l’ATPase) Il entre en compétition avec le Pi pour la R° de phosphorylation de l’ADP Arséniate Formation d’ADP arsénylé, qui s’hydrolyse immédiatement en libérant de l’énergie sous forme de la chaleur 73

Resumé des inhiniteurs de la CR • Complexe I: Roténone, Barbituriques • Complexe II: Malonate • Complexe III: Antymicine A, Myxothiazol • Complexe IV: Cyanure, Oxyde de carbone, azide de sodium • Complexe F 0 -F 1: Oligomycine • ATP translocase : Atractylate 74

7. Déficiences héritées liées à la phosphorylation oxydative Les cellules contiennent 100 à +1000 de mitochondries La mitochondrie contient environ 100 protéines. 13 protéines, engagées ds la CRM sont synthétisées ds la mitochondrie à partir de l’ADNmit L’ADN mitochondrial • Dans la matrice • Circulaire • Deux brins • Taille: 16, 5 kilobases chez l’homme 78, 5 kilobases chez la levure • Pas d’introns chez l’homme • Hérédité maternelle 75

7. Déficiences héritées liées à la phosphorylation oxydative Les défaut observées ds la POx sont dus aux mutations de l’ADNmit. Ces pathologies sont généralement à hérédité maternelle Ces défauts affectent essentiellement les tissus grands consommateurs d’ATP Expemple: • Syndrome de Kearns-Sayre: mutations ponctuelles touchant les gènes codant pour l’ATPase (atteinte des muscles) • Neuropathie optique de Leber (perte bilatéral de la vision central par manque de production d’ATP): mutation du gène codant pour la NADH déshydrogénase 76

Merci 77

78
![- Contrôle de la phosphorylation oxydative : régulation par l’ADP Au repos: [ATP]>[ADP] ds - Contrôle de la phosphorylation oxydative : régulation par l’ADP Au repos: [ATP]>[ADP] ds](http://slidetodoc.com/presentation_image/5496fe7048e6f8faaca3798de69d5edc/image-79.jpg)
- Contrôle de la phosphorylation oxydative : régulation par l’ADP Au repos: [ATP]>[ADP] ds cytoplasme et mitochondrie Lors d’un effort: [ATP] diminue (-50%) et [ADP] augmente considérablement (10 à 100 X) l’augmentation de la [ADP]cyt active les Protéines de transport de l’ADP L’ADP entre ds la matrice de la mitochondrie L’aug. [ADP]mit active l’ATPase qui phosphoryle aussitôt cet ADP Diminution du gradient de protons autour de la mb. interne Facilitation du pompage de H+ par les comp. I, III et IV Facilitation des R° redox couplées à ce pompage Accélération de l’oxydation des substrats(NADH et Succinate) et de la consommation de l’oxygène 79
- Slides: 79