Expriences daudits BPF de fabricants gnriques en Afrique


Expériences d'audits BPF de fabricants génériques en Afrique : Quels enjeux pour l’Afrique ?
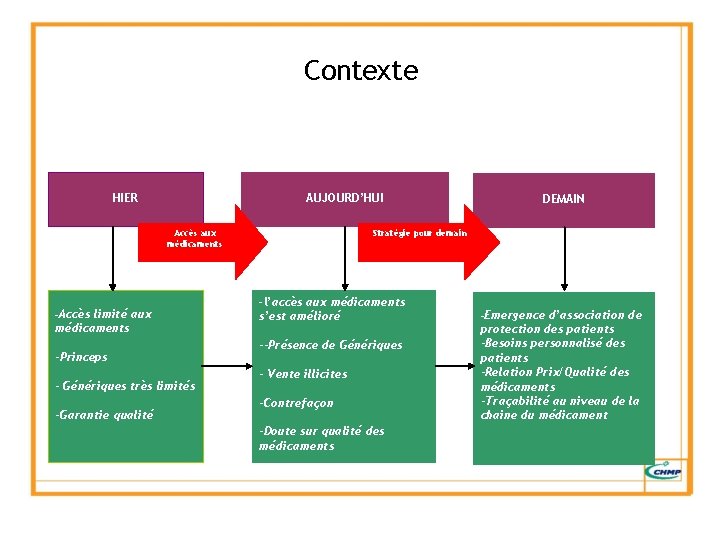
Contexte HIER AUJOURD’HUI Accès aux médicaments -Accès limité aux médicaments -Princeps - Génériques très limités -Garantie qualité DEMAIN Stratégie pour demain -l’accès aux médicaments s’est amélioré --Présence de Génériques - Vente illicites -Contrefaçon -Doute sur qualité des médicaments -Emergence d’association de protection des patients -Besoins personnalisé des patients -Relation Prix/Qualité des médicaments -Traçabilité au niveau de la chaine du médicament

Périmètre des audits • • Cinq(5) pays: Afrique francophone et anglophone Année des audits : 2009 Sept(7) fabricants Formes pharmaceutiques fabriqués: *Comprimés-Gélules *Pommades-Suspension buvable *Suspension injectable*Poudre pour injection Médicaments génériques avec des classes thérapeutiques multiples

Les contraintes Techniques et Réglementaires • Enregistrement dans le pays / GMP par DPM • Accords commerciaux • Lutte contre les contrefaçons • Logique Qualité pour les autorités pays • Logique commerciale pour le fabricant • Logique santé publique : Fabricant et autorités

Constat global Absence de transfert industriel Choix des méthodes analytique non maitrisé Equivalence pharmaceutique : absence tests de dissolution comparés Fournisseurs de matières premières : absence de mise à jour de la documentation (CEP-DMF) et suivi des plans d’action suite aux audits Absence de maitrise des activités clés: Pharmacovigilance -Contrefaçon de médicaments : Revue annuel Produit -Gestion des produits retournés - Gestion des Risques -Corrective action -Préventive action « CAPA » Conséquences De nombreux sites de fabrication ne produisent pas conformément aux principes des BPF. Contamination et contamination croisée non maîtrisées Locaux et équipements vétustes Documents insuffisants Validations absentes ou incomplètes
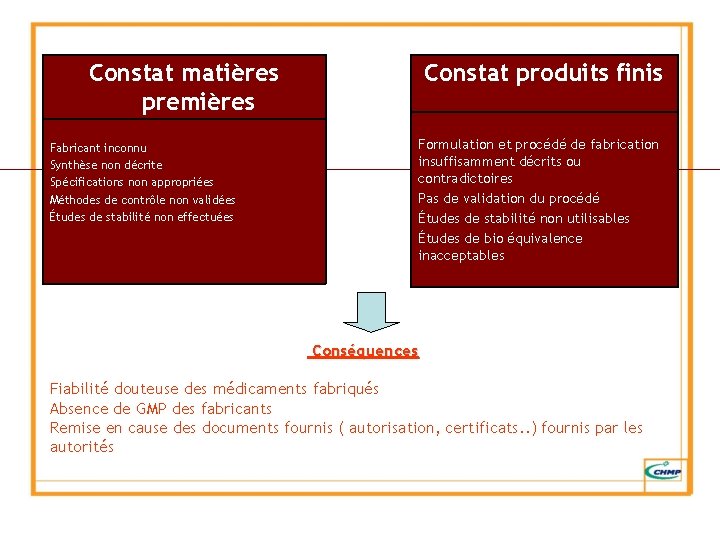
Constat matières premières Fabricant inconnu Synthèse non décrite Spécifications non appropriées Méthodes de contrôle non validées Études de stabilité non effectuées Constat produits finis Formulation et procédé de fabrication insuffisamment décrits ou contradictoires Pas de validation du procédé Études de stabilité non utilisables Études de bio équivalence inacceptables Conséquences Fiabilité douteuse des médicaments fabriqués Absence de GMP des fabricants Remise en cause des documents fournis ( autorisation, certificats. . ) fournis par les autorités
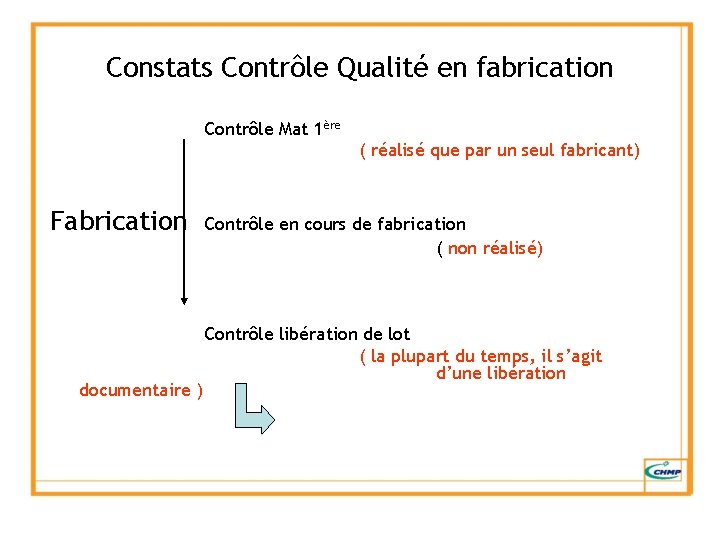
Constats Contrôle Qualité en fabrication Contrôle Mat 1ère ( réalisé que par un seul fabricant) Fabrication documentaire ) Contrôle en cours de fabrication ( non réalisé) Contrôle libération de lot ( la plupart du temps, il s’agit d’une libération
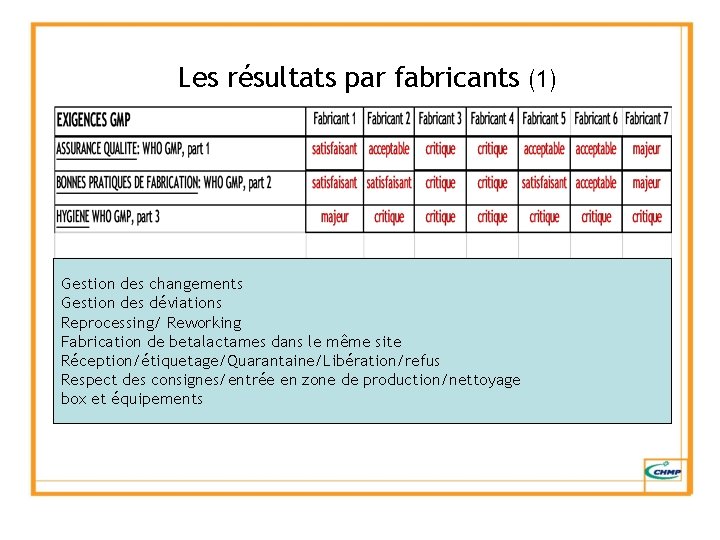
Les résultats par fabricants (1) Gestion des changements Gestion des déviations Reprocessing/ Reworking Fabrication de betalactames dans le même site Réception/étiquetage/Quarantaine/Libération/refus Respect des consignes/entrée en zone de production/nettoyage box et équipements
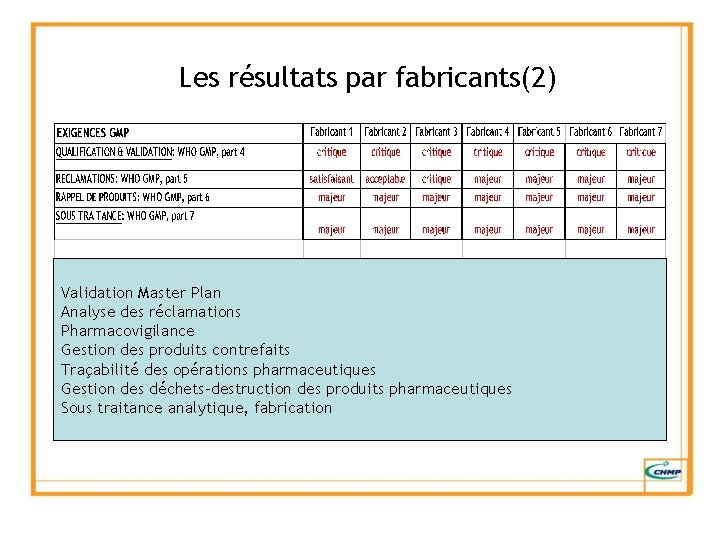
Les résultats par fabricants(2) Validation Master Plan Analyse des réclamations Pharmacovigilance Gestion des produits contrefaits Traçabilité des opérations pharmaceutiques Gestion des déchets-destruction des produits pharmaceutiques Sous traitance analytique, fabrication
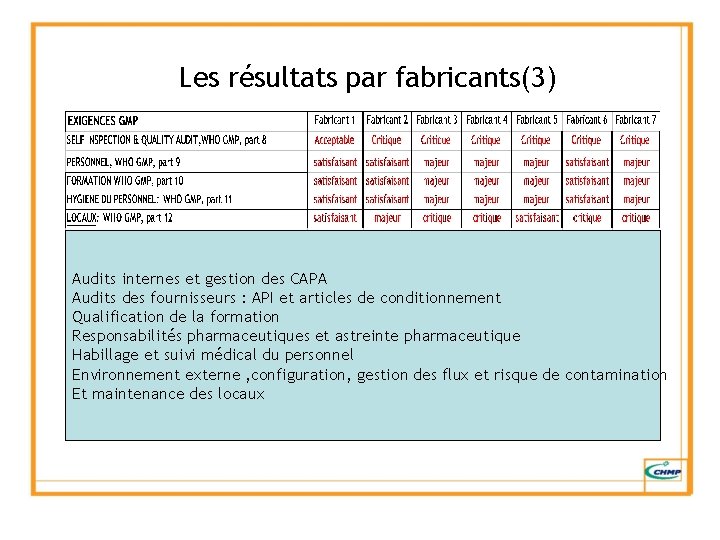
Les résultats par fabricants(3) Audits internes et gestion des CAPA Audits des fournisseurs : API et articles de conditionnement Qualification de la formation Responsabilités pharmaceutiques et astreinte pharmaceutique Habillage et suivi médical du personnel Environnement externe , configuration, gestion des flux et risque de contamination Et maintenance des locaux
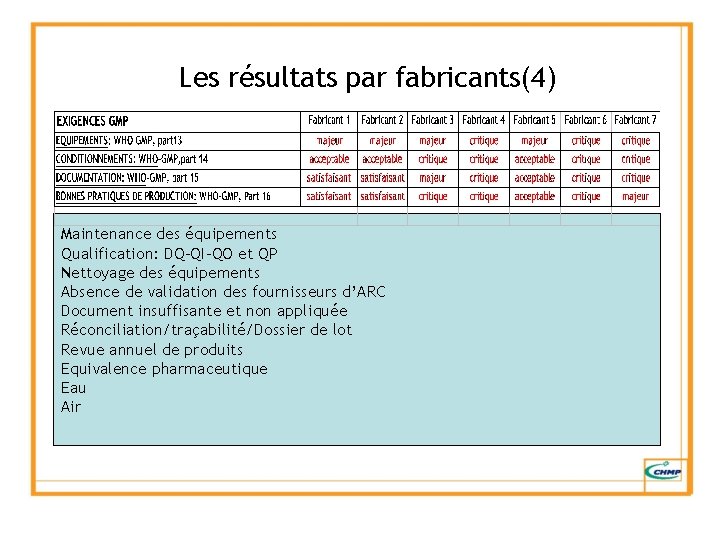
Les résultats par fabricants(4) Maintenance des équipements Qualification: DQ-QI-QO et QP Nettoyage des équipements Absence de validation des fournisseurs d’ARC Document insuffisante et non appliquée Réconciliation/traçabilité/Dossier de lot Revue annuel de produits Equivalence pharmaceutique Eau Air

Les résultats par fabricants(5) Organisation Traçabilité des échantillons : API et FP Substances de référence Etudes de stabilité Libération de lots Transfert de méthode Gestion des résultats non conforme : OOS procédure

Le minimum nécessaire SOP de PQ des matières premières Prélèvement (box séparé – système de pression) Pesée (évite contamination croisée) Schéma de pression et enregistrement en zone de fabrication Validation master plan Etiquetage des produits (API / Ingrédients / produits intermédiaires / Produits finis) Etiquetage des pièces Etiquetage des équipements Validation des procédés de fabrication Validation du nettoyage Eau purifié (validation et management)

Quelques résultats analytiques • Névirapine : 4 fabricants différents 2 non conformités • Artésunate + amodiaquine : 15 produits analysés dont 6 PQ OMS 7 non conformités

Friabilité comprimés Névirapine

Friabilité comprimés Névirapine Test de friabilité selon Ph Européenne 6ème Ed : Sur 10 comprimés 9 comprimés cassés Comprimés cassés dans une boîte de 60 comprimés Comprimés après le test de friabilité

Dissolution comprimés Névirapine Dissolution USP 31 • Spécifications: % dissous supérieur ou égal à 80 % • Résultats : min 66 % max 74%
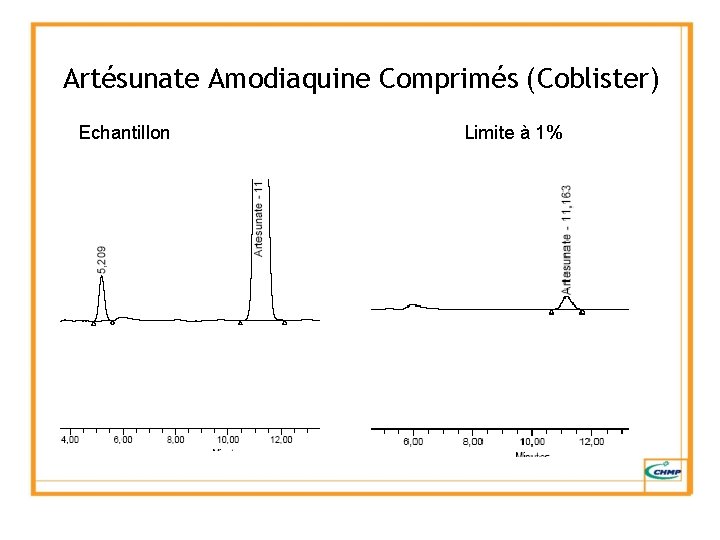
Artésunate Amodiaquine Comprimés (Coblister) Echantillon Limite à 1%
Quelle stratégie pour demain ? PRIX + QUALITE + PROTECTION DU PATIENT + Lutte contre vente illicite et contrefaçon de médicaments Traçabilité = STRATEGIE : Mariage raisonné entre le PRIX et la QUALITE
Perspectives • Renforcer l’appui au DPM – – • Evaluation des dossiers d’enregistrement Conseil ; Expertise ; Formation Collaboration active Renforcer l’appui au LNCQ – – – • Conseil ; Expertise ; Proposition de formations adaptées ( DIU CQMEG) Contre expertise dossiers critiques Solutions Pays sans LNCQ – – Suivi, accompagnement Collaboration avec un LNCQ Pays voisin

- Slides: 22