Expresin de ADN recombinante I 2016 Lic Daro

Expresión de ADN recombinante I 2016 – Lic. Darío Paladini

Para qué Análisis de la función en la célula huésped, estudios de localización, etc. : no se requiere purificación. Estudios de la proteína in vitro, cristalografía, espectroscopía, producción de anticuerpos, etc. : producción a baja y mediana escala. Producción de la proteína a gran escala: por ejemplo para comercialización.

Pasos a optimizar Elección de la secuencia a clonar Elección del vector apropiado y del huésped apropiado Cómo optimizar la expresión de la proteína de interés Método correcto de extracción y clarificación Esquema de purificación Correcto almacenamiento de la proteína purificada

Sistemas de expresión Bacterias: Escherichia coli. Muchos vectores y cepas comerciales. Simple, barato y veloz. Eucariotas Levaduras: Saccharomyces cerevisiae, Pichia pastoris, Kluyveromyces lactis. Células de insecto: Sf 9, Sf 21 (tejido de ovario de la pupa de Spodoptera frugiperda) mediante baculovirus. Modificaciones post-traduccionales más complejas, mejor plegado. Células de mamíferos: mediante plásmidos, adenovirus, retrovirus, etc. Cultivo con muchos requerimientos. Animales y plantas transgénicos

Elección del sistema Tamaño: las proteínas citosólicas pequeñas (<100 aas. ) y péptidos se expresan mejor en E. coli y como proteínas de fusión. Las >100 aas. Son problemáticas en cualquier sistema. En E. coli suelen ser inestables y formar cuerpos de inclusión insolubles. Cantidad: Si se necesita mucha cantidad conviene explorar varias combinaciones vector/huésped/esquema de inducción/esquema de purificación. Actividad: No es necesaria (ej. producción anticuerpos), entonces sirven los cuerpos de inclusión o los tags para purificación por afinidad. Actividad necesaria, es importante mantenerla o re-establecerla; la facilidad de la purificación se vuelve secundaria. Estudios estructurales: Es mejor expresarla como proteína soluble (minimizar el mal plegamiento y la desnaturalización in vitro).


Expresión en E. coli o Promotor: lac: p. UC, p. TZ, p. SK, p. Bluescript, p. GEM, etc. Represor lac, inducible por IPTG: isopropil-ß-Dtiogalactósido (muy costoso). Vectores diseñados para selección de colonias azules/blancas por interrupción del gen de la ß-galactosidasa. No tan fuerte pero en plásmidos de alto nº de copias los niveles de expresión son respetables.
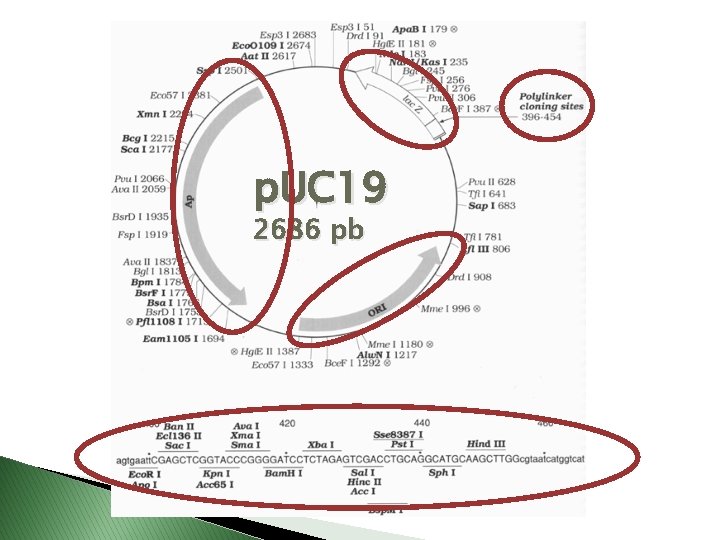
p. UC 19 2686 pb
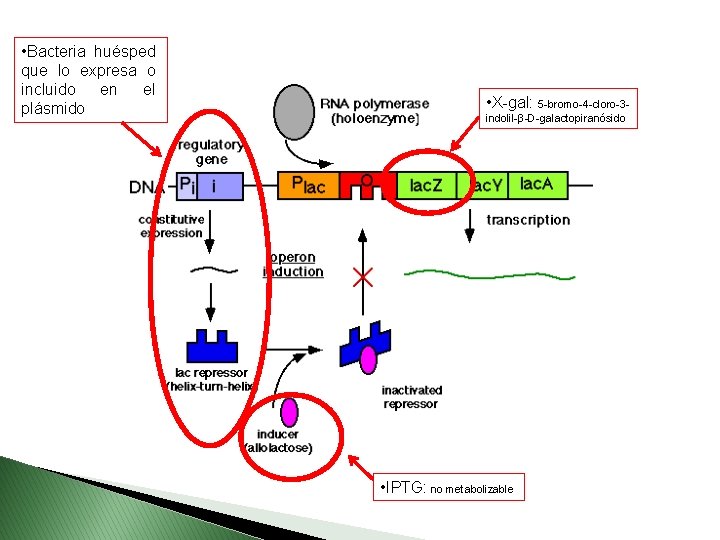
• Bacteria huésped que lo expresa o incluido en el plásmido • X-gal: 5 -bromo-4 -cloro-3 indolil-β-D-galactopiranósido • IPTG: no metabolizable

Expresión en E. coli o Promotor: tac y trc: p. Trc. His-TOPO®, p. GEX Fuerte. Fusiones entre promotores trp (región -35) y lac (región -10), éstos son regulados por el represor lac. Son 3 veces más fuertes que trp y 10 veces más fuertes que lac
- Slides: 10