Explorations fonctionnelles Fe NO MBW DLCO Plamen Bokov

Explorations fonctionnelles Fe. NO, MBW, DLCO Plamen Bokov, MCU-PH Service d’Explorations Fonctionnelles, Hôpital Robert Debré, Paris Cours DIU de Pneumopédiatrie, 12/01, Hôpital Trousseau

Nitric oxide and asthma: the relationships Clinical expression Allergen exposure Mild symptoms Asthma attack Atopy Ig. E NO Airflow limitation Physiopathology Eosinophilic inflammation Remodeling Airway Hyper-responsiveness

Nitric oxide and asthma: the relationships Atopy Ig. E NO Physiopathology Eosinophilic inflammation Remodeling Airway Hyper-responsiveness
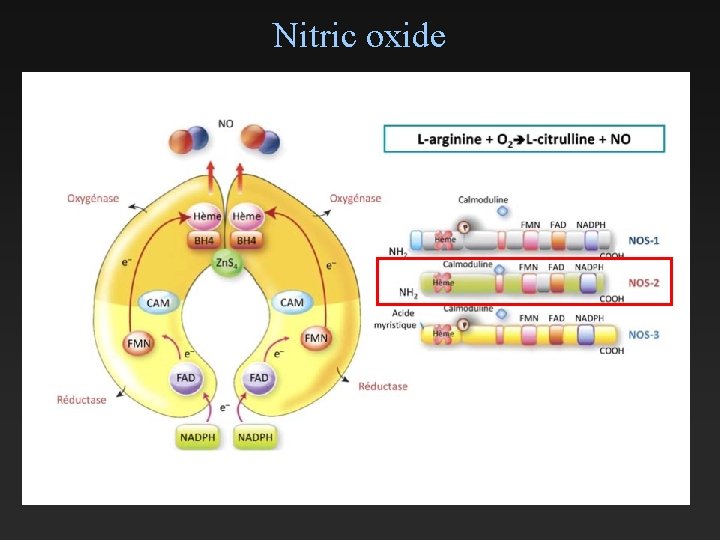
Nitric oxide
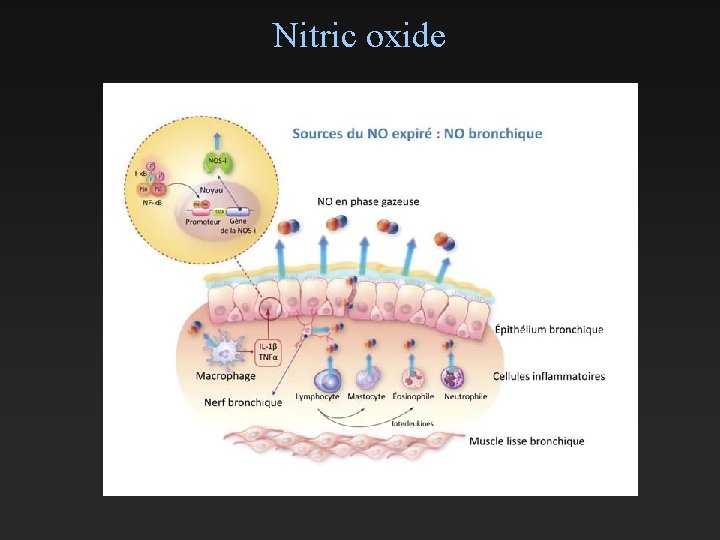
Nitric oxide
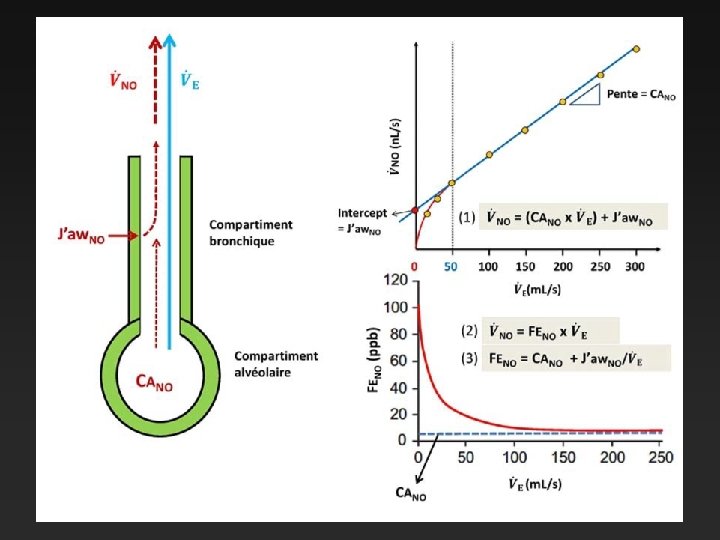
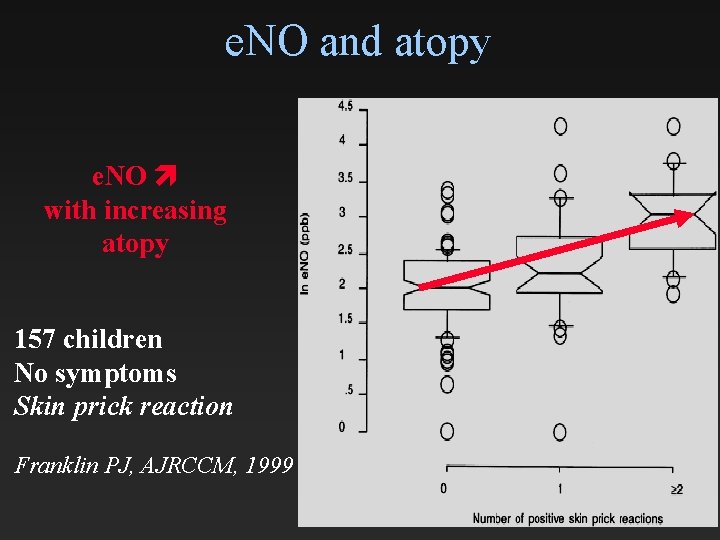
e. NO and atopy e. NO with increasing atopy 157 children No symptoms Skin prick reaction Franklin PJ, AJRCCM, 1999
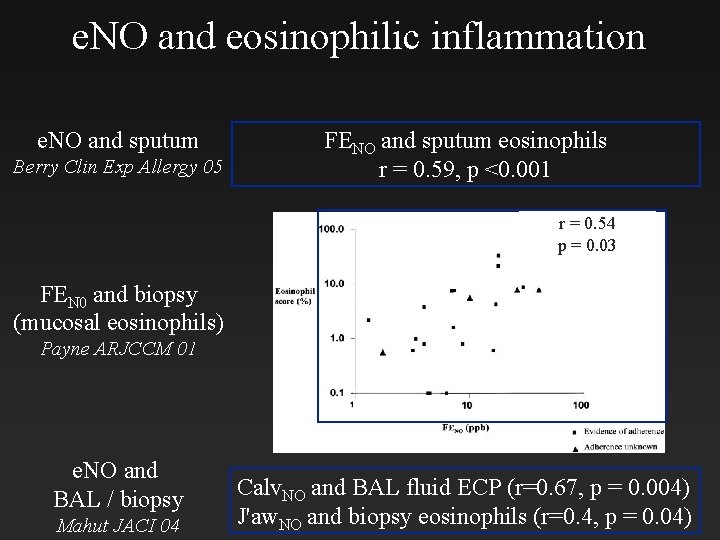
e. NO and eosinophilic inflammation e. NO and sputum Berry Clin Exp Allergy 05 FENO and sputum eosinophils r = 0. 59, p <0. 001 r = 0. 54 p = 0. 03 FEN 0 and biopsy (mucosal eosinophils) Payne ARJCCM 01 e. NO and BAL / biopsy Mahut JACI 04 Calv. NO and BAL fluid ECP (r=0. 67, p = 0. 004) J'aw. NO and biopsy eosinophils (r=0. 4, p = 0. 04)
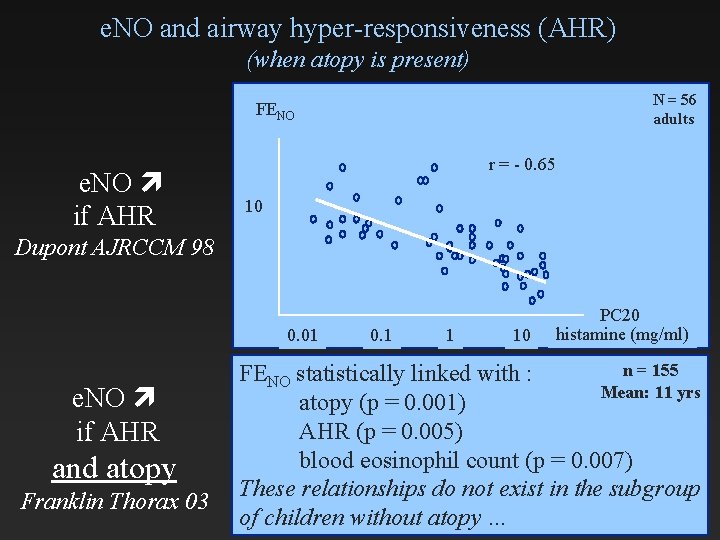
e. NO and airway hyper-responsiveness (AHR) (when atopy is present) N = 56 adults FENO e. NO if AHR r = - 0. 65 10 Dupont AJRCCM 98 0. 01 e. NO if AHR and atopy Franklin Thorax 03 0. 1 1 10 PC 20 histamine (mg/ml) n = 155 FENO statistically linked with : Mean: 11 yrs atopy (p = 0. 001) AHR (p = 0. 005) blood eosinophil count (p = 0. 007) These relationships do not exist in the subgroup of children without atopy …

Nitric oxide and asthma: the relationships Clinical expression Allergen exposure Mild symptoms Asthma attack NO Airflow limitation
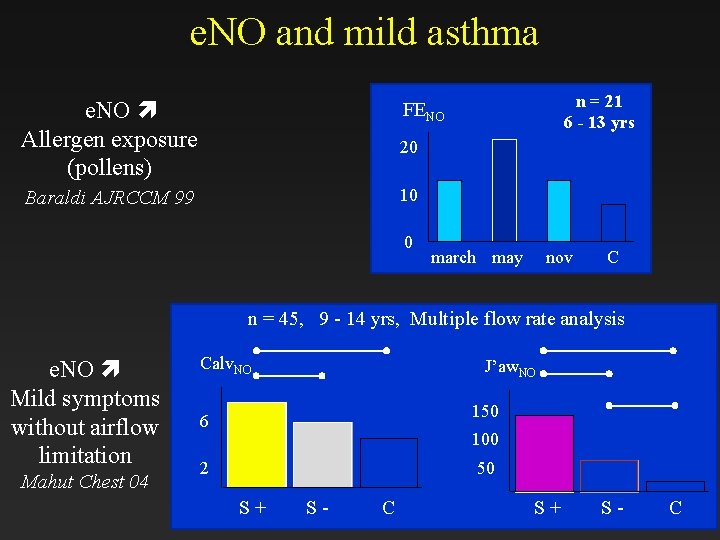
e. NO and mild asthma e. NO Allergen exposure (pollens) 20 Baraldi AJRCCM 99 10 n = 21 6 - 13 yrs FENO 0 march may nov C n = 45, 9 - 14 yrs, Multiple flow rate analysis e. NO Mild symptoms without airflow limitation Mahut Chest 04 Calv. NO J’aw. NO 150 6 100 2 50 S+ S- C
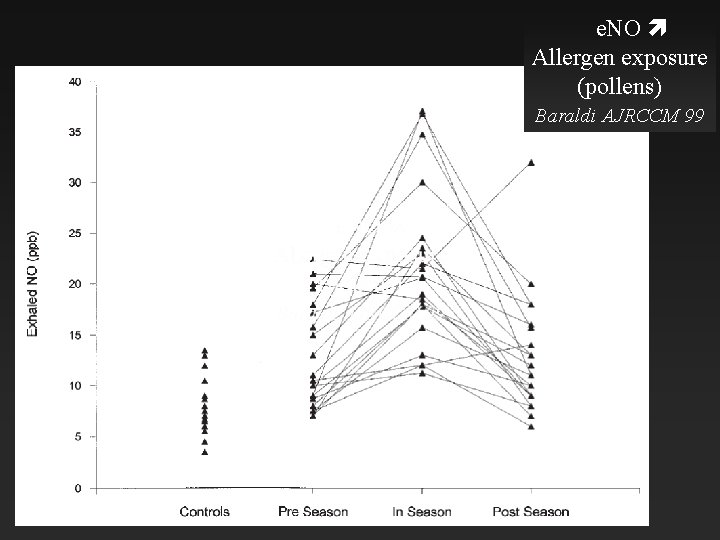
e. NO Allergen exposure (pollens) Baraldi AJRCCM 99
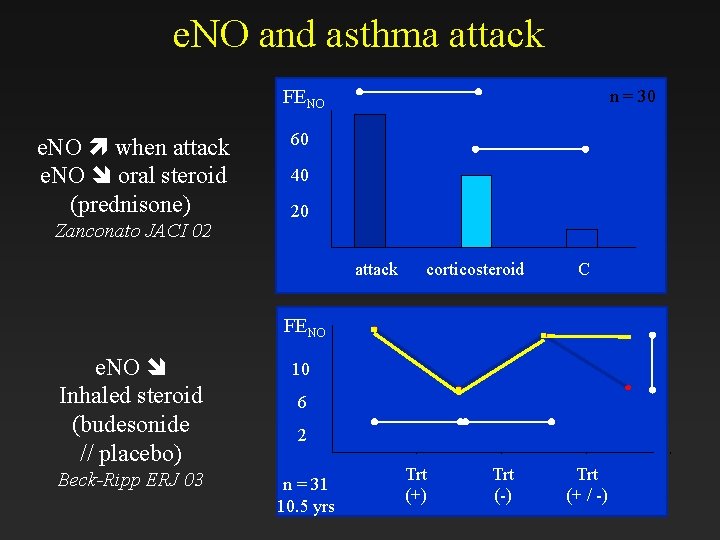
e. NO and asthma attack FENO e. NO when attack e. NO oral steroid (prednisone) Zanconato JACI 02 n = 30 60 40 20 attack corticosteroid C FENO e. NO Inhaled steroid (budesonide // placebo) Beck-Ripp ERJ 03 10 6 2 n = 31 10. 5 yrs Trt (+) Trt (-) Trt (+ / -)

NO expiré: intérêt au cours de l’asthme 1. Diagnostic de l’asthme 2. Evaluation de l’asthme sévérité contrôle
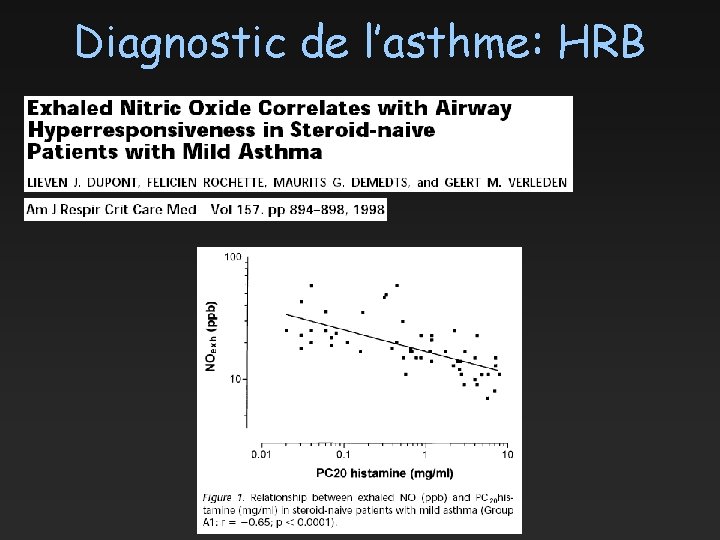
Diagnostic de l’asthme: HRB
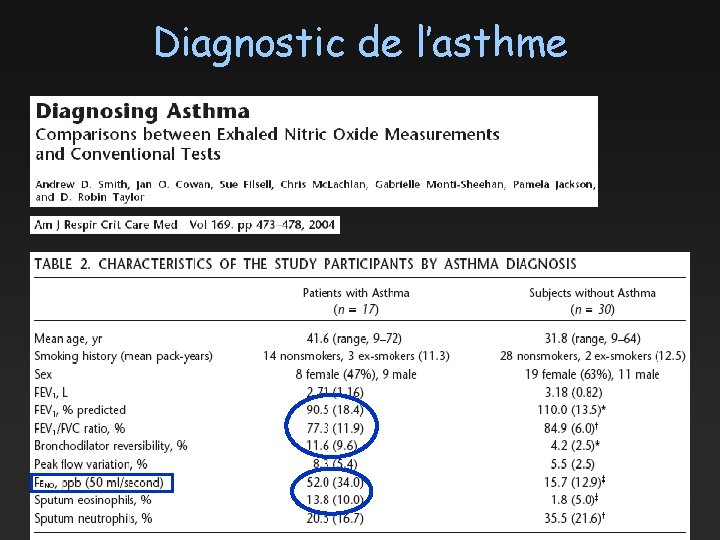
Diagnostic de l’asthme
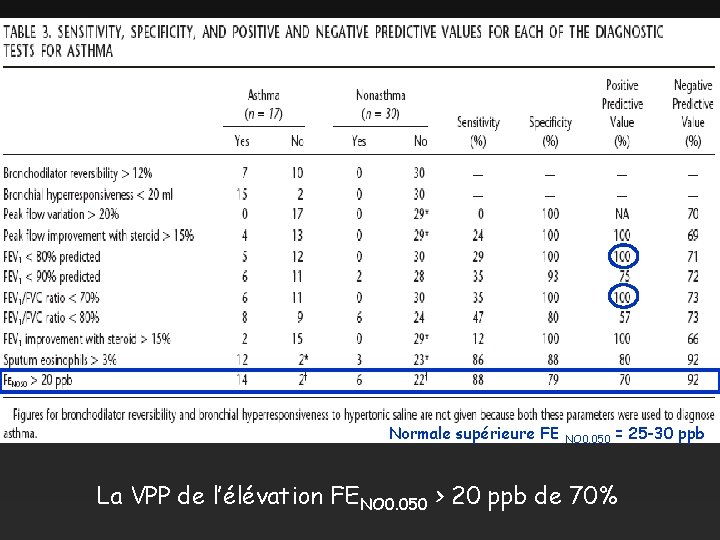
Normale supérieure FE NO 0. 050 = 25 -30 ppb La VPP de l’élévation FENO 0. 050 > 20 ppb de 70%

Diagnostic de l’asthme 52 patients Symptômes respiratoires chroniques Étiologie indéterminée (suspicion d’asthme) Essai de corticothérapie inhalée (fluticasone) FENO 0. 050

27/52 patients sont classés « asthme » Normale supérieure FE NO 0. 050 = 25 -30 ppb Meilleure valeur seuil : FENO 0. 050 = 47 ppb

Diagnostic de l’asthme ou de l’atopie … 150 enfants 80 atopiques 70 non atopiques FE NO 0. 035
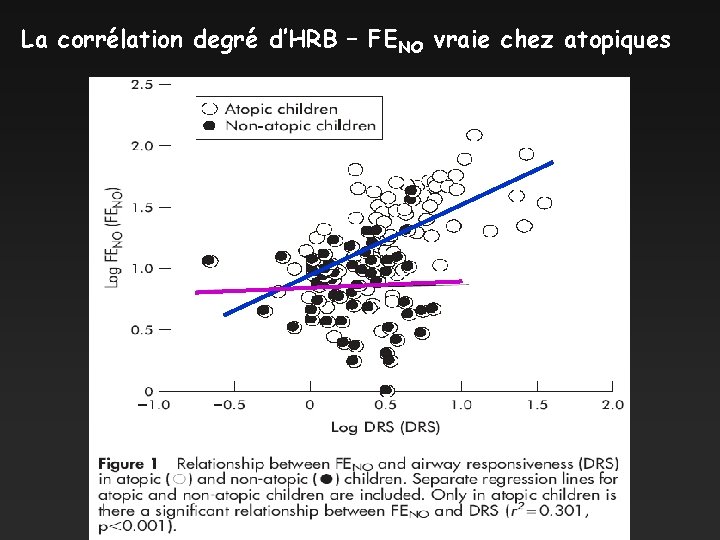
La corrélation degré d’HRB – FENO vraie chez atopiques

Réel intérêt diagnostique de FENO L’augmentation de NO expiré: • traduit le terrain atopique avant tout • relation degré HRB et FENO vraie chez l’atopique • équivalence FENO et test métacholine (atopique)

Marqueur de contrôle ou de sévérité ? 100 asthmatiques Étude transversale FENO 0. 03
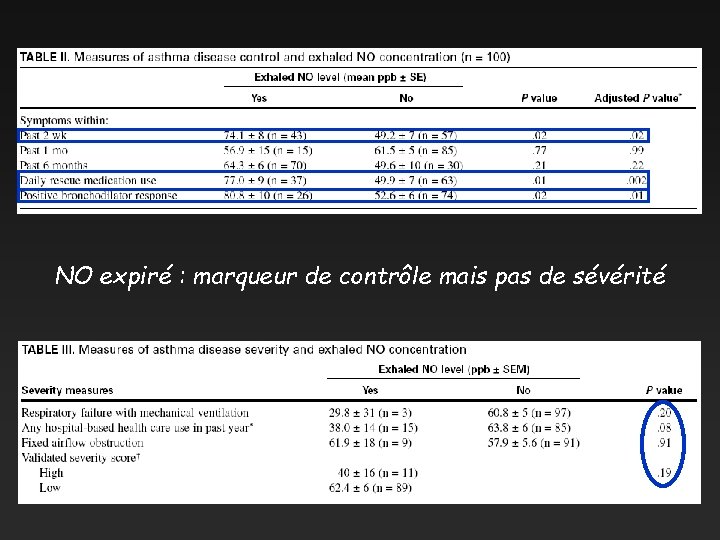
NO expiré : marqueur de contrôle mais pas de sévérité

Marqueur de contrôle Le NO expiré est augmenté chez l’asthmatique atopique Le NO expiré diminue lors de la corticothérapie 1. Dépistage du non contrôle 2. Prédiction du risque d’exacerbation 3. Aide au sevrage de la corticothérapie

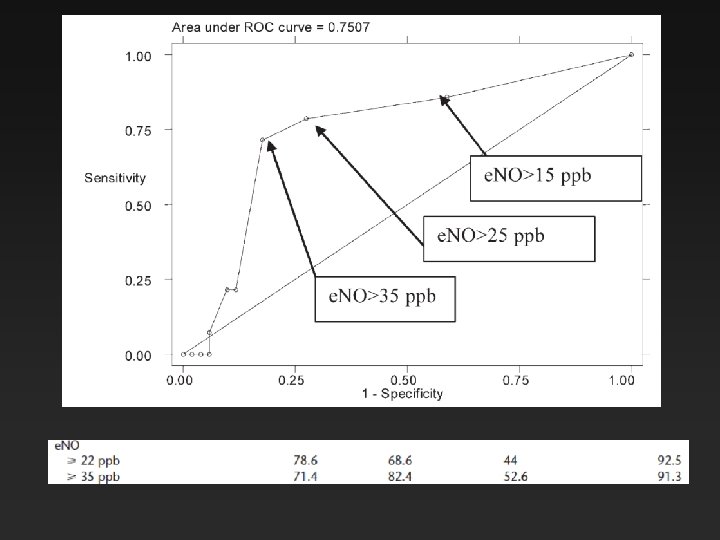
15 patients, âges 18 -70 ans Asthme stable: beclo 800 µg/j Réduction à budesonide 200 µg/j Suivi/semaine pendant 8 semaines Exacerbation minime: 8/15 FENO 0. 100
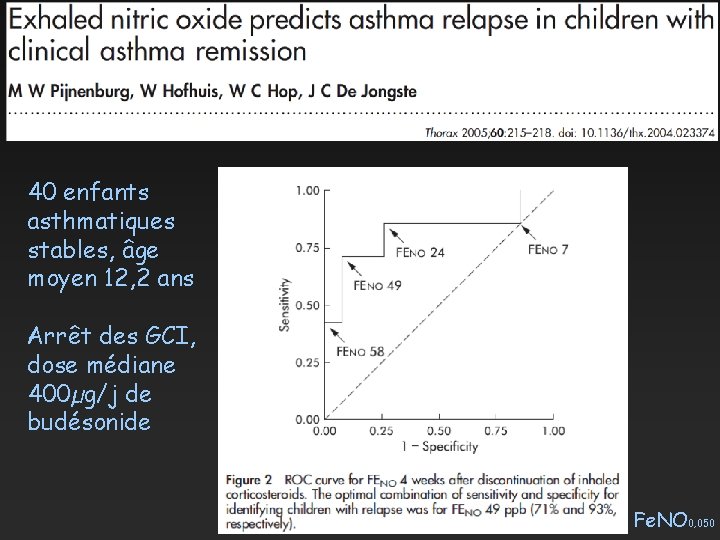
40 enfants asthmatiques stables, âge moyen 12, 2 ans Arrêt des GCI, dose médiane 400µg/j de budésonide Fe. NO 0, 050

97 patients asthmatiques Fluticasone 750 µg/j Diminution sur FENO 0. 250 > 15 ppb (35 ppb pour FENO 0. 050) ou clinique (GINA)
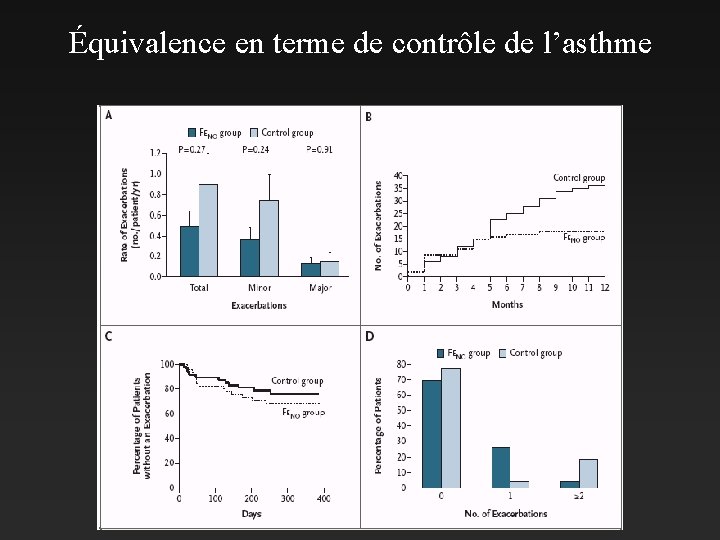
Équivalence en terme de contrôle de l’asthme
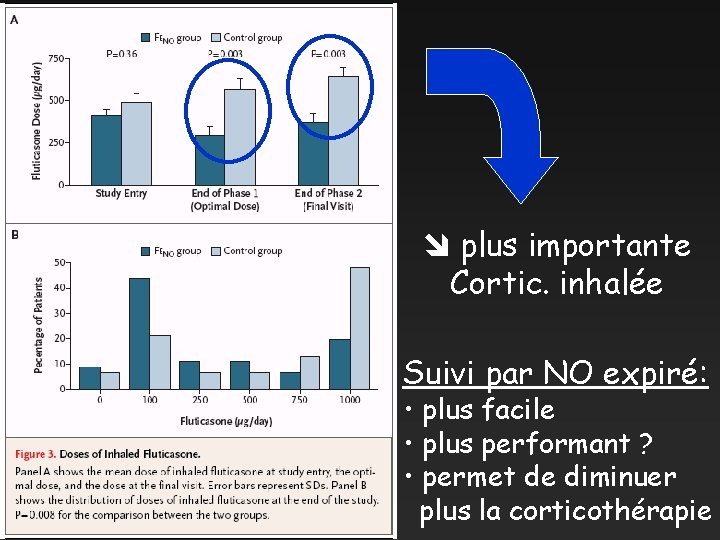
plus importante Cortic. inhalée Suivi par NO expiré: • plus facile • plus performant ? • permet de diminuer plus la corticothérapie

Conclusions La mesure de NO dans le gaz expiré: • est liée étroitement à l’éosinophilie bronchique • évalue le degré d’HRB chez l’atopique • dépiste la perte de contrôle de l’asthme • permet de guider la décroissance des corticoïdes Utilité certaine pour le suivi des asthmatiques ?

Dweik R. ATS recommandations, AJRCCM 2011

Dweik R. ATS recommandations, AJRCCM 2011
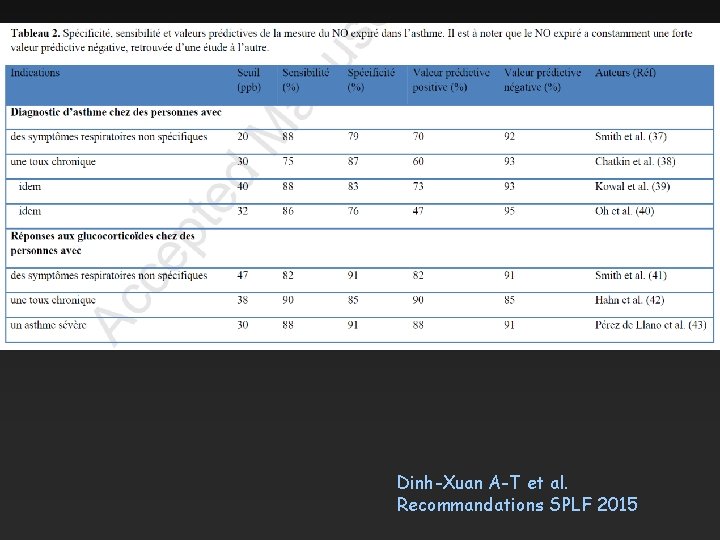
Dinh-Xuan A-T et al. Recommandations SPLF 2015

Dinh-Xuan A-T et al. Recommandations SPLF 2015

Conclusions FENO (ppb) Asthma attack Mild symptoms Allergen exposure Atopy without symptoms Healthy condition Asthmatic patient (with atopy) under corticosteroid
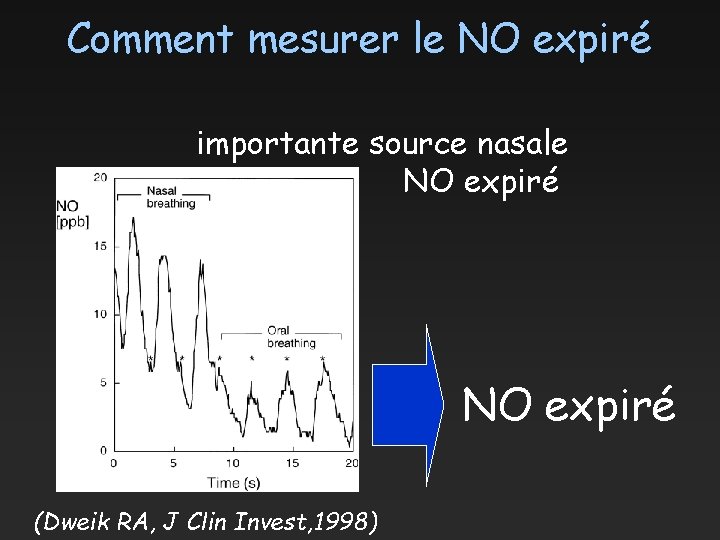
Comment mesurer le NO expiré importante source nasale NO expiré (Dweik RA, J Clin Invest, 1998)
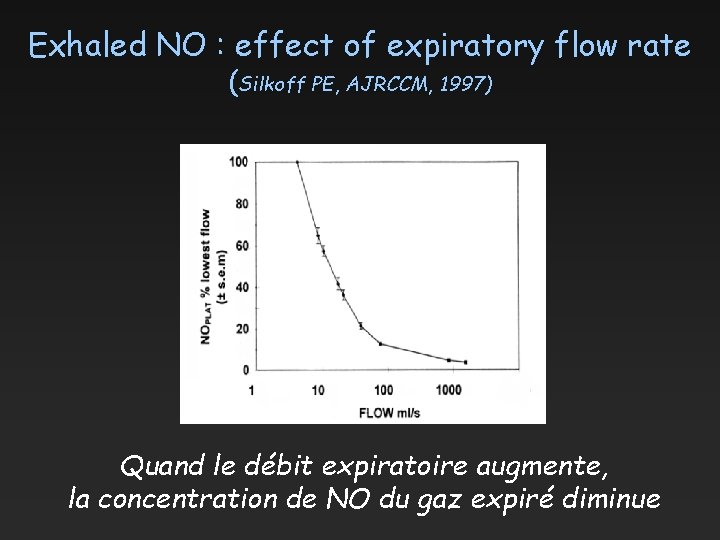
Exhaled NO : effect of expiratory flow rate (Silkoff PE, AJRCCM, 1997) Quand le débit expiratoire augmente, la concentration de NO du gaz expiré diminue
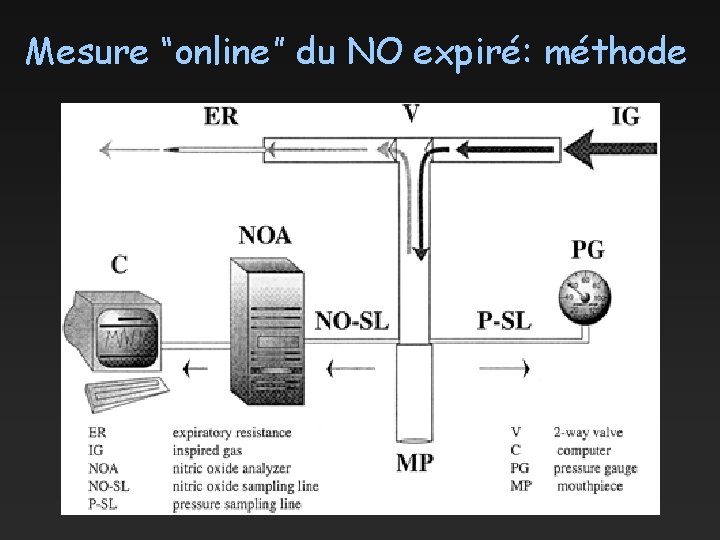
Mesure “online” du NO expiré: méthode Figure 1 ATS
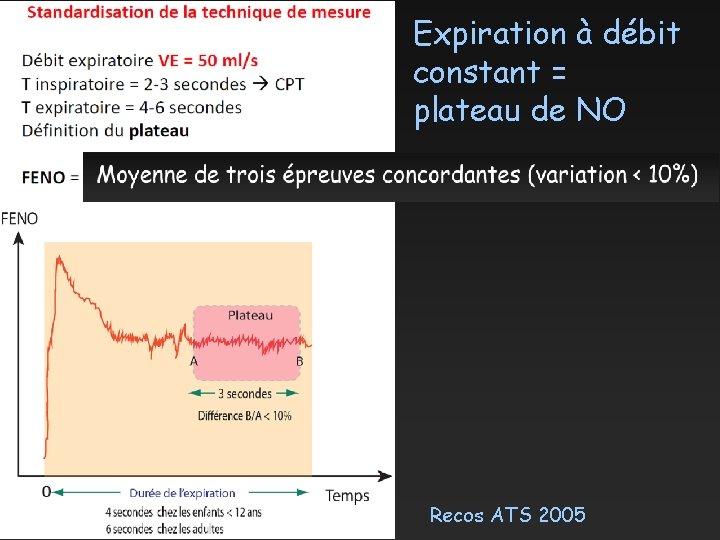
Expiration à débit constant = plateau de NO Recos ATS 2005
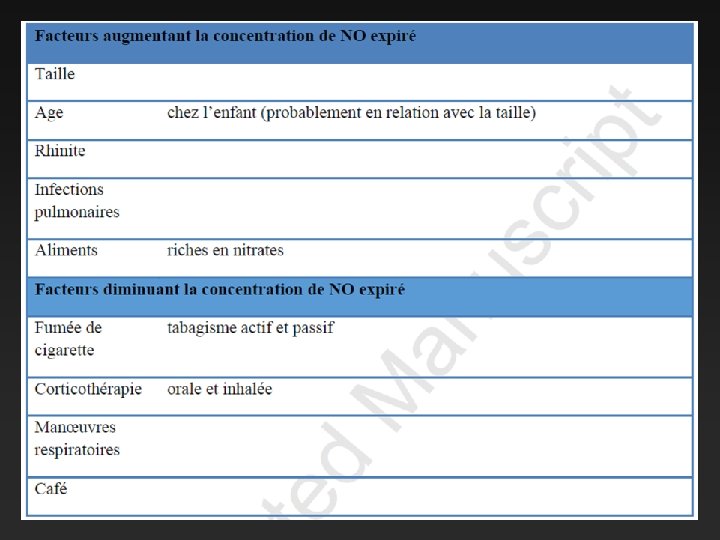
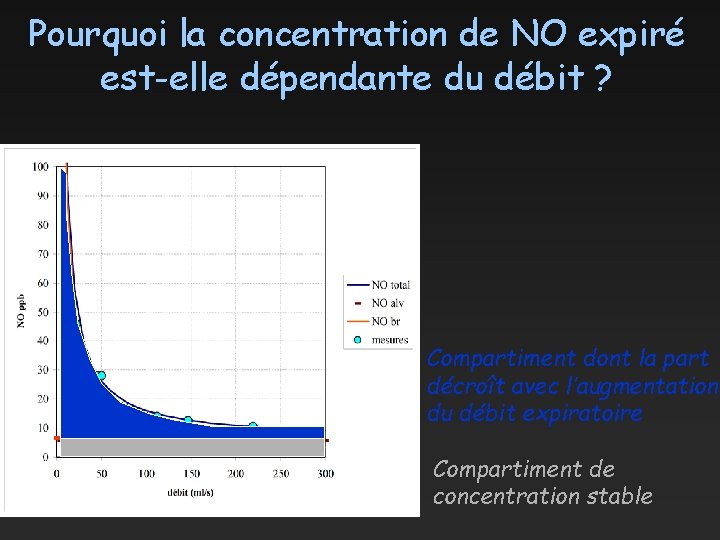
Pourquoi la concentration de NO expiré est-elle dépendante du débit ? Compartiment dont la part décroît avec l’augmentation du débit expiratoire Compartiment de concentration stable
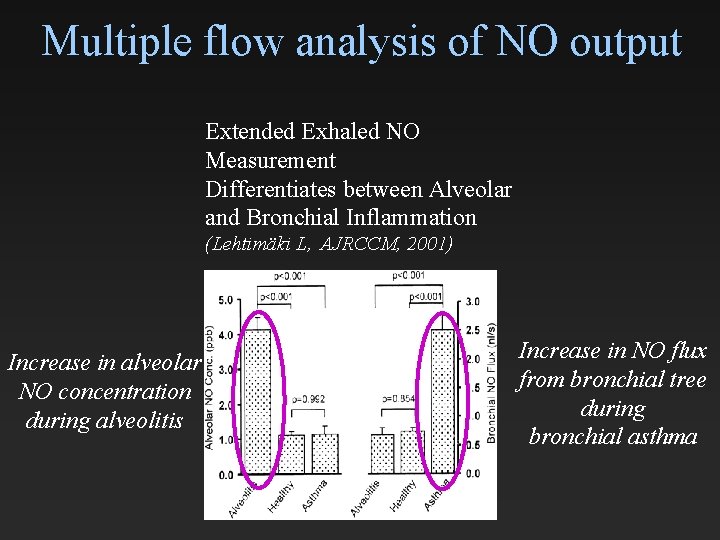
Multiple flow analysis of NO output Extended Exhaled NO Measurement Differentiates between Alveolar and Bronchial Inflammation (Lehtimäki L, AJRCCM, 2001) Increase in alveolar NO concentration during alveolitis Increase in NO flux from bronchial tree during bronchial asthma

Multiple Breath Washout • Technique permettant l’évaluation des inhomogénéités de ventilation • Intérêt dans des pathologies débutant par des atteintes distales - Mucoviscidose - Bronchiolite oblitérante post -greffe de CSH - Asthme?
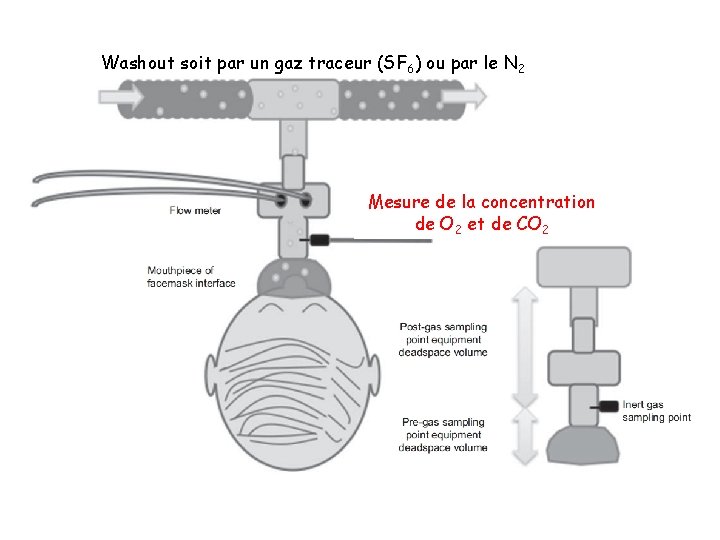
Washout soit par un gaz traceur (SF 6) ou par le N 2 Mesure de la concentration de O 2 et de CO 2
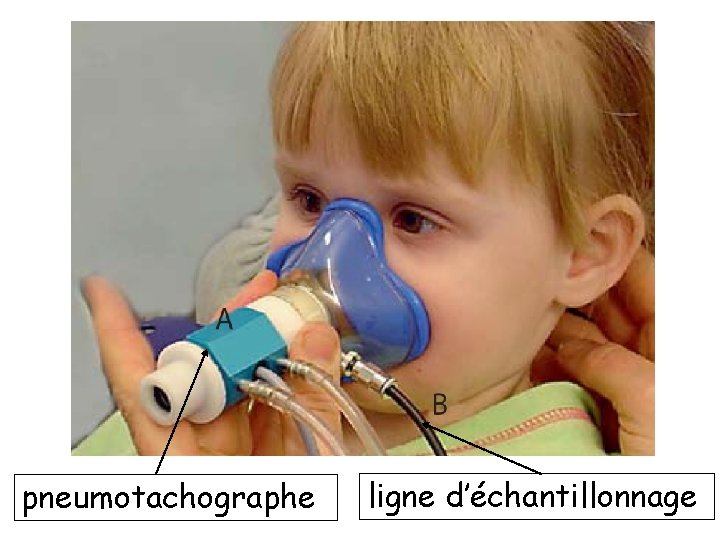
pneumotachographe ligne d’échantillonnage
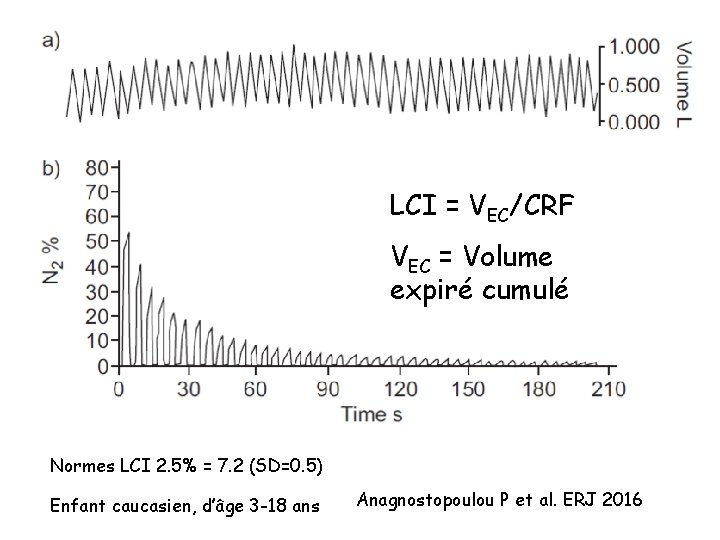
LCI = VEC/CRF VEC = Volume expiré cumulé Normes LCI 2. 5% = 7. 2 (SD=0. 5) Enfant caucasien, d’âge 3 -18 ans Anagnostopoulou P et al. ERJ 2016
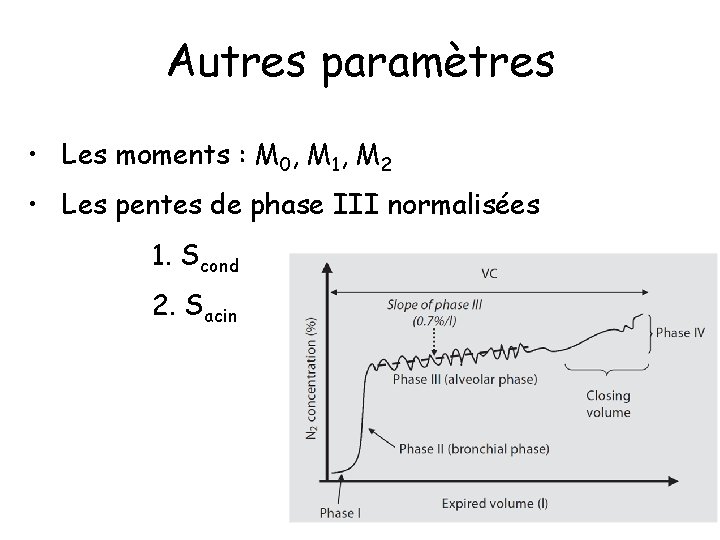
Autres paramètres • Les moments : M 0, M 1, M 2 • Les pentes de phase III normalisées 1. Scond 2. Sacin
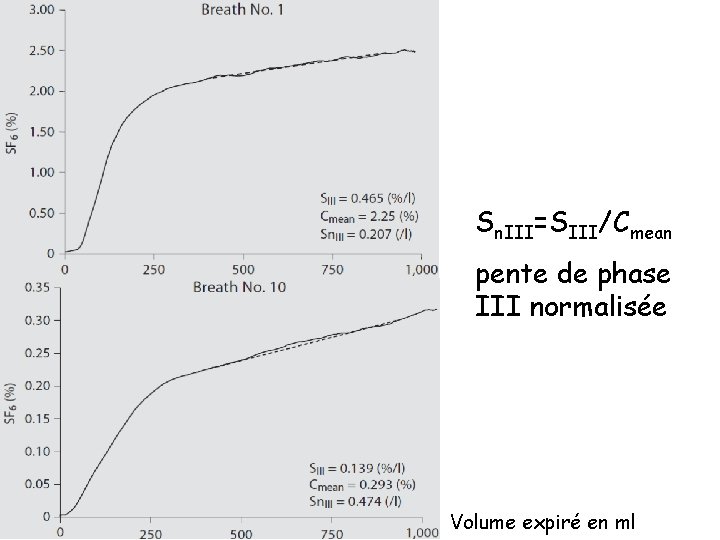
Sn. III=SIII/Cmean pente de phase III normalisée Volume expiré en ml
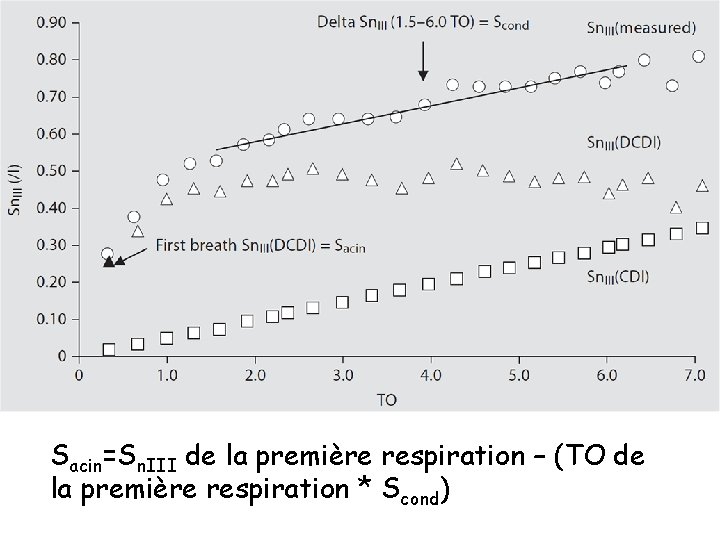
Sacin=Sn. III de la première respiration – (TO de la première respiration * Scond)
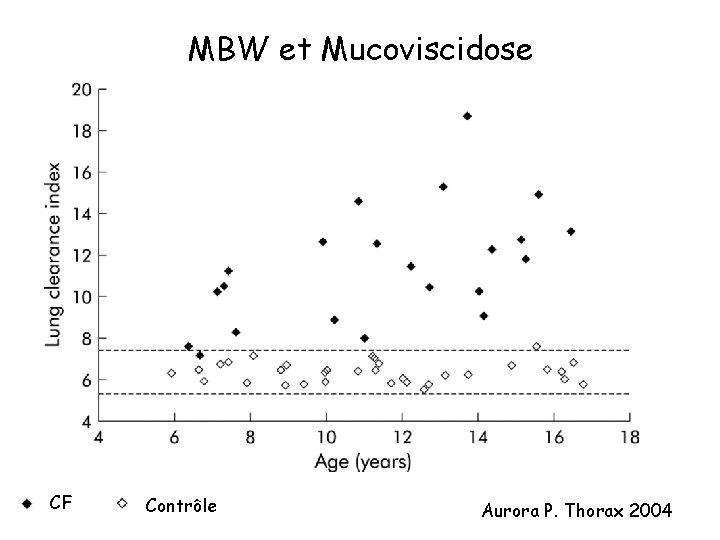
MBW et Mucoviscidose CF Contrôle Aurora P. Thorax 2004
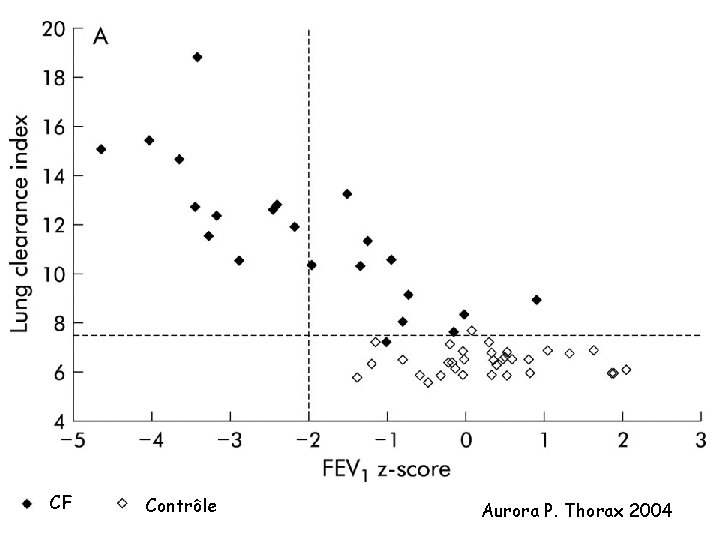
CF Contrôle Aurora P. Thorax 2004
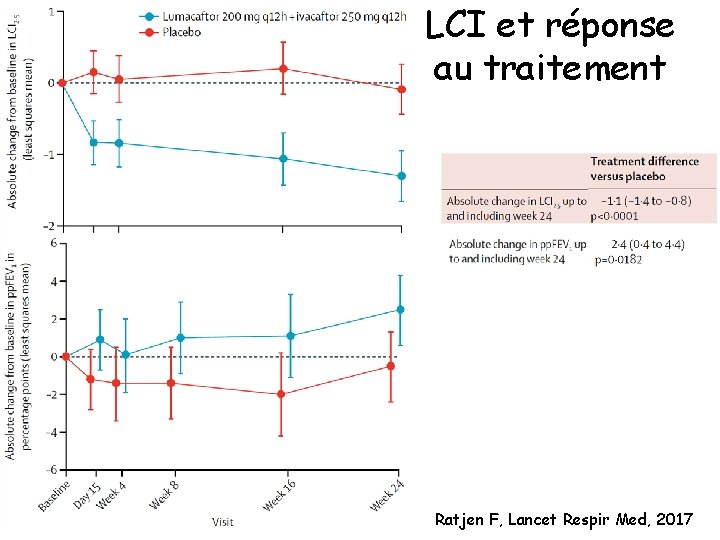
LCI et réponse au traitement Ratjen F, Lancet Respir Med, 2017
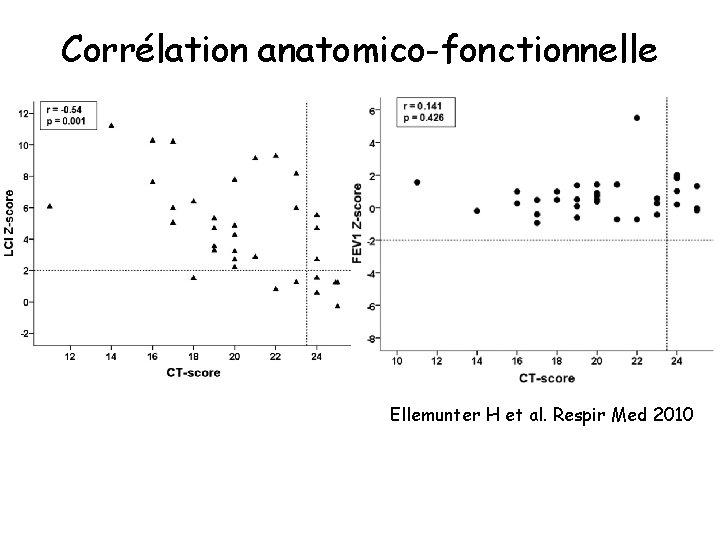
Corrélation anatomico-fonctionnelle Ellemunter H et al. Respir Med 2010
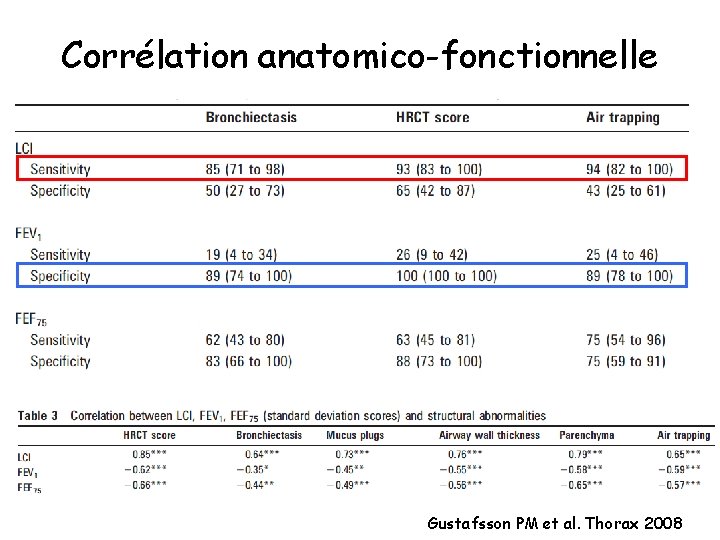
Corrélation anatomico-fonctionnelle Gustafsson PM et al. Thorax 2008
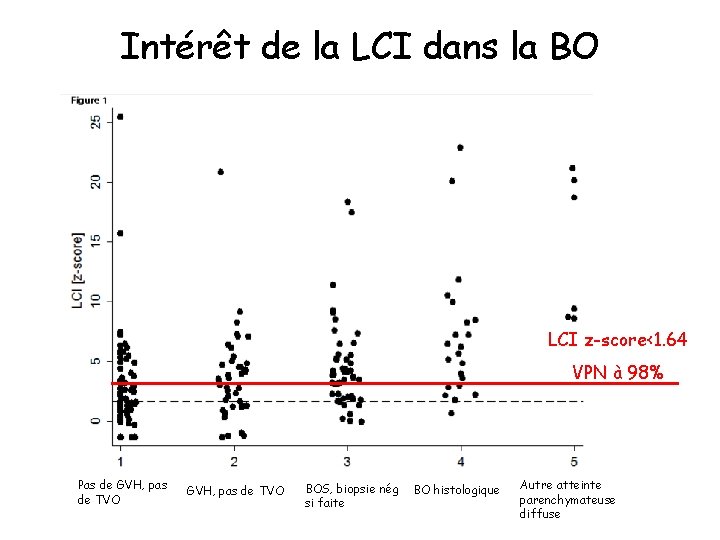
Intérêt de la LCI dans la BO LCI z-score<1. 64 VPN à 98% Pas de GVH, pas de TVO BOS, biopsie nég si faite BO histologique Autre atteinte parenchymateuse diffuse
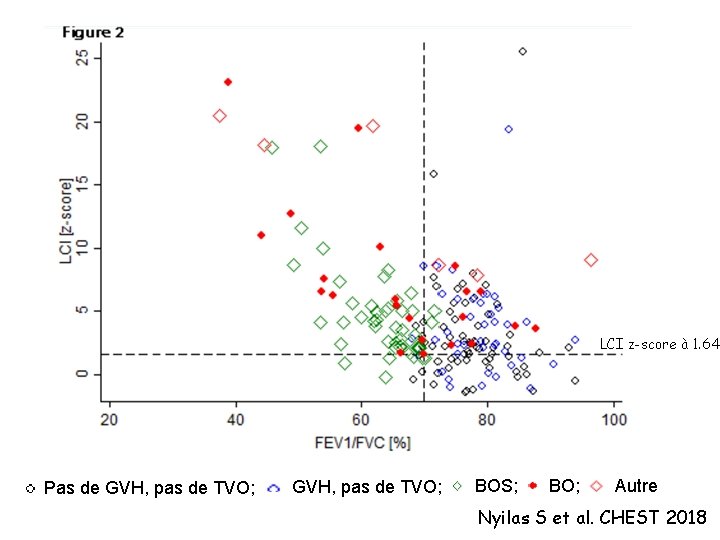
LCI z-score à 1. 64 Pas de GVH, pas de TVO; BOS; BO; Autre Nyilas S et al. CHEST 2018
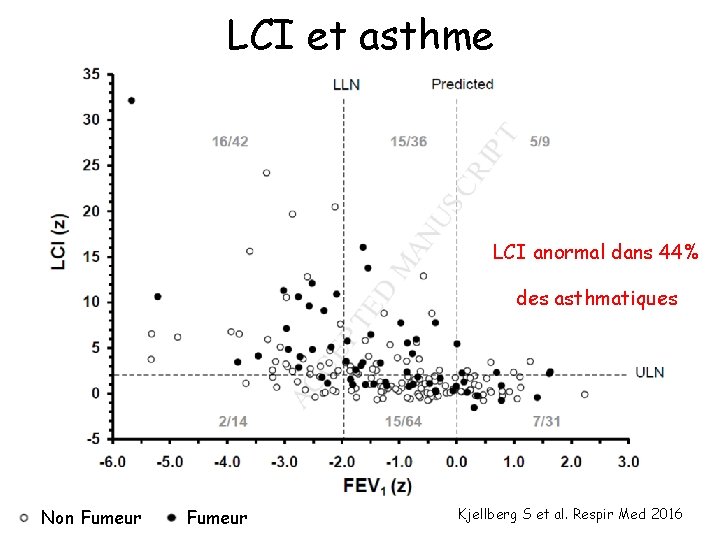
LCI et asthme LCI anormal dans 44% des asthmatiques Non Fumeur Kjellberg S et al. Respir Med 2016
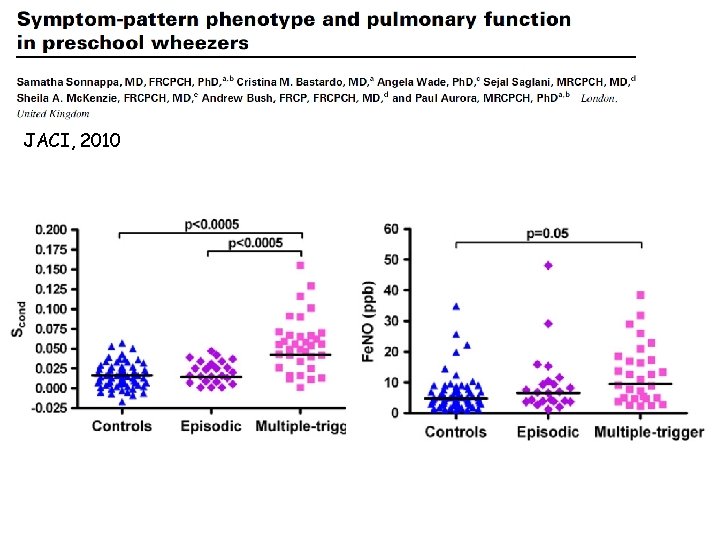
JACI, 2010
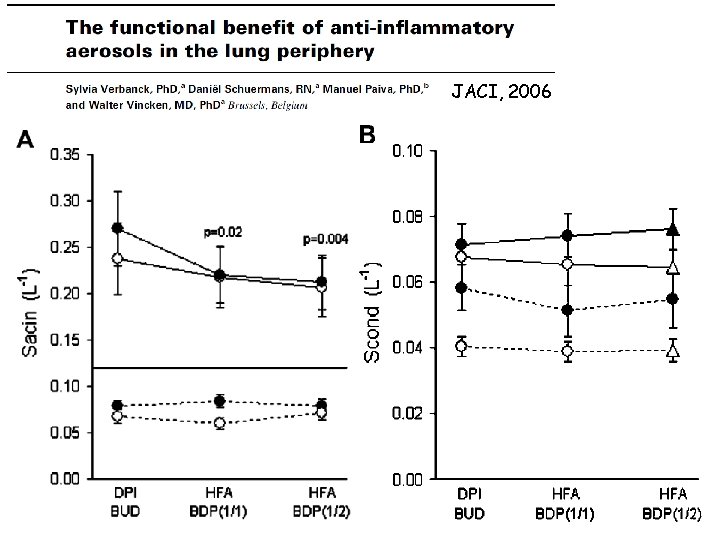
JACI, 2006

Compte-rendu type Critères de bonne exécution: • Respiration stable et Vt acceptable +++ • Première respiration du WO comprise entre 0, 5 et 1, 5 fois le Vt moyen • Absence de larges respirations (>2 Vt) pendant le WO • Absence de fuites • Ne tousse pas, ne parle pas • Dernière respiration du WO entre 0, 5 et 1, 5 fois le Vt Trois tests acceptables Critère de reproductibilité: • Typiquement on chera Max-Min/Moyenne LCI et CRF <10%

Transfert alvéolo-capillaire Comment les gaz traversent les parois alvéolaires
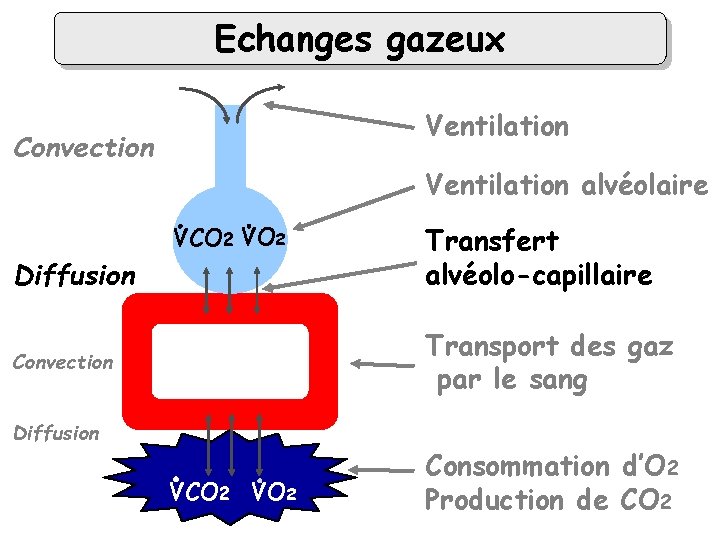
Echanges gazeux Ventilation Convection Ventilation alvéolaire VCO 2 VO 2 alvéole Diffusion Transfert alvéolo-capillaire Transport des gaz par le sang Convection Diffusion VCO 2 VO 2 Consommation d’O 2 Production de CO 2
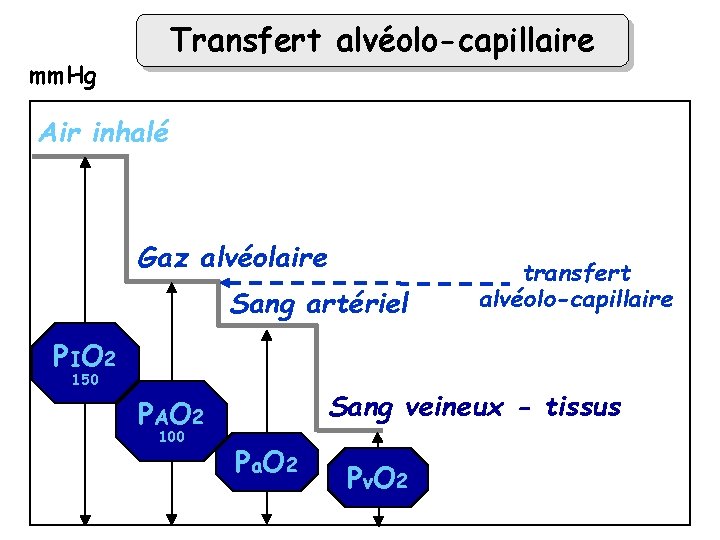
Transfert alvéolo-capillaire mm. Hg Air inhalé Gaz alvéolaire Sang artériel transfert alvéolo-capillaire P IO 2 150 Sang veineux - tissus P AO 2 100 P a O 2 P v. O 2
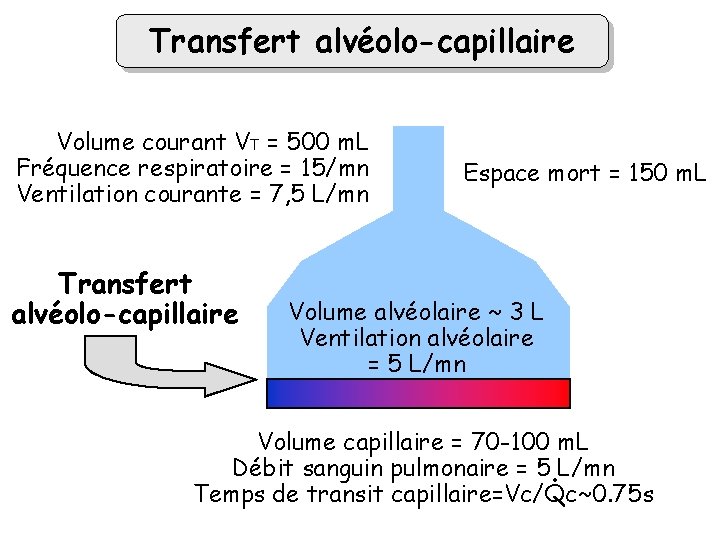
Transfert alvéolo-capillaire Volume courant VT = 500 m. L Fréquence respiratoire = 15/mn Ventilation courante = 7, 5 L/mn Transfert alvéolo-capillaire Espace mort = 150 m. L Volume alvéolaire ~ 3 L Ventilation alvéolaire = 5 L/mn Volume capillaire = 70 -100 m. L Débit sanguin pulmonaire = 5. L/mn Temps de transit capillaire=Vc/Qc~0. 75 s
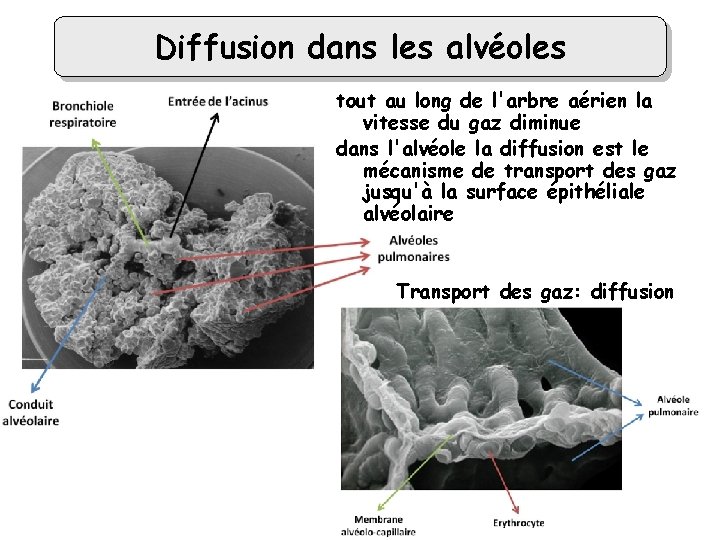
Diffusion dans les alvéoles tout au long de l'arbre aérien la vitesse du gaz diminue dans l'alvéole la diffusion est le mécanisme de transport des gaz jusqu'à la surface épithéliale alvéolaire Transport des gaz: diffusion
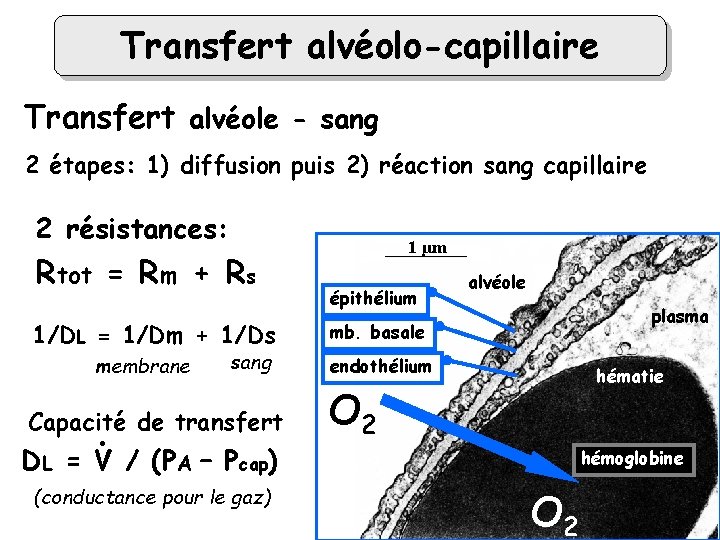
Transfert alvéolo-capillaire Transfert alvéole - sang 2 étapes: 1) diffusion puis 2) réaction sang capillaire 2 résistances: Rtot = Rm + Rs 1/DL = 1/Dm + 1/Ds membrane sang . Capacité de transfert DL = V / (PA – Pcap) (conductance pour le gaz) 1 µm épithélium alvéole plasma mb. basale endothélium hématie O 2 hémoglobine O 2

Capacité de transfert de la membrane Diffusion: loi de Fick surface : A (50 -100 m 2) alvéole P 1 P 2 plasma débit de diffusion . épaisseur : e (0, 5 µm) gaz: solubilité (a), D V = ax. D x A/e Dm x (P 1 – P 2) : capacité de transfert (conductance) membranaire

Capacité de transfert du sang : cinétique (f°Hb) hématie hémoglobine Vc : volume capillaire Ds = . Vc Capacité transfert du sang Modélisation du transfert du dioxygène . VO 2 = DLO 2 x (PAO 2 – Pcap. O 2)

Indications d’explorations du transfert A-C Modification de la DLCO : • modification du volume sanguin capillaire • modification de la surface échange S : volume alvéolaire • modification de l’épaisseur de la barrière alvéolo-capillaire Chez Bilan Suivi Bilan l’enfant : étiologique/fonctionnel de pathologie interstitielle de toxicité pulmonaire post chimio/radiothérapie étiologique/fonctionnel vascularite

Indications d’explorations du transfert A-C
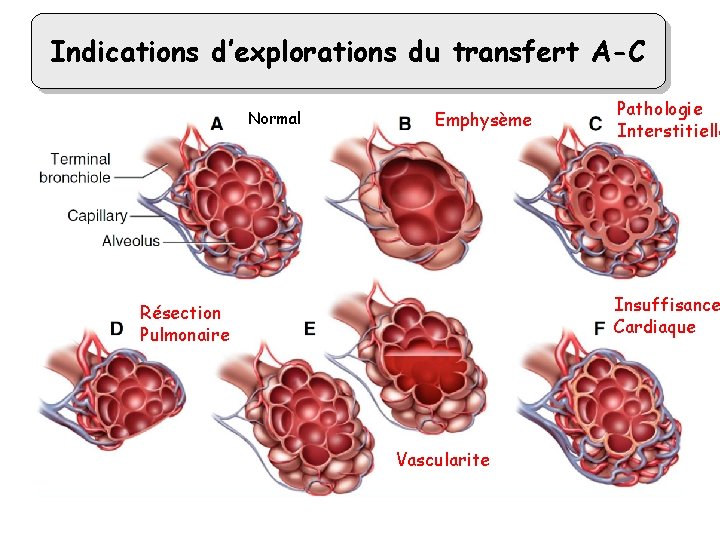
Indications d’explorations du transfert A-C Normal Emphysème Pathologie Interstitielle Insuffisance Cardiaque Résection Pulmonaire Vascularite
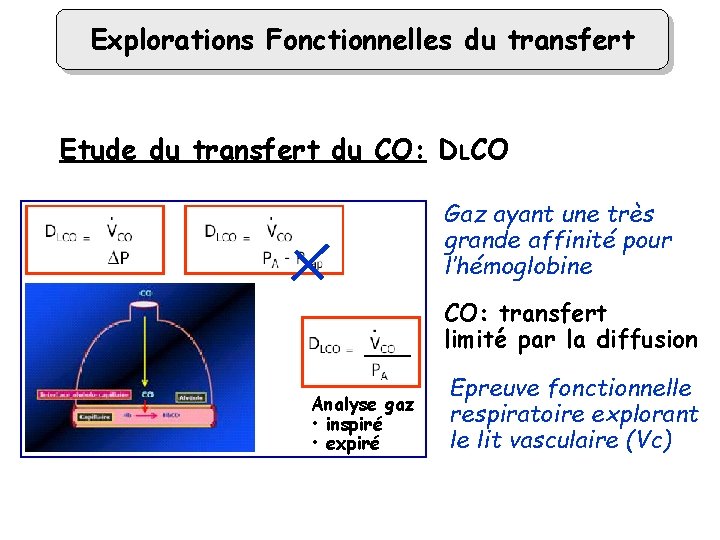
Explorations Fonctionnelles du transfert Etude du transfert du CO: DLCO Gaz ayant une très grande affinité pour l’hémoglobine CO: transfert limité par la diffusion Analyse gaz • inspiré • expiré Epreuve fonctionnelle respiratoire explorant le lit vasculaire (Vc)
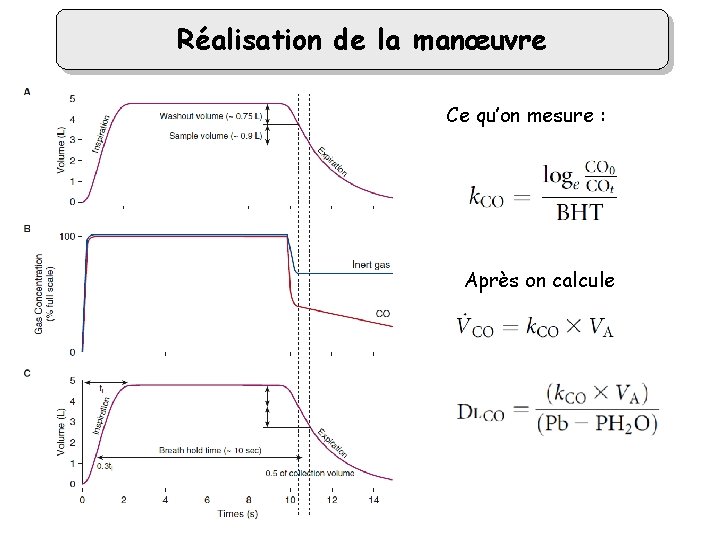
Réalisation de la manœuvre Ce qu’on mesure : Après on calcule
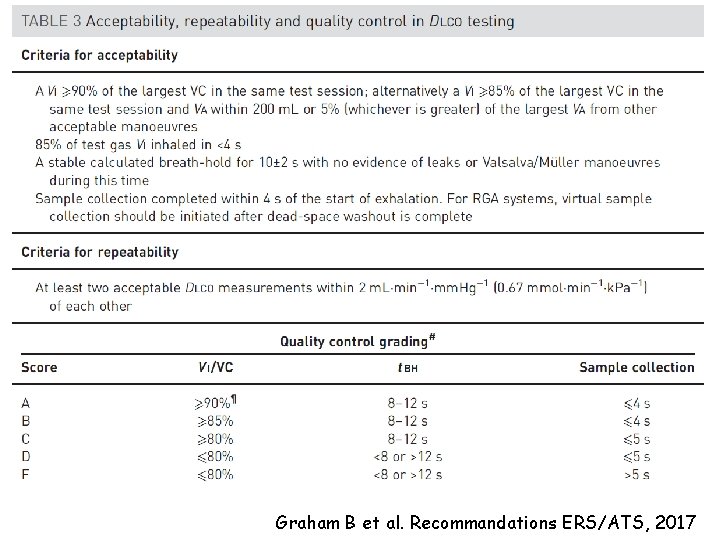
Graham B et al. Recommandations ERS/ATS, 2017
- Slides: 76