Experimento 1 Densidad Densidad masa de substancia por

Experimento #1: Densidad • Densidad = masa de substancia por unidad de volumen que ocupa. Las unidades más comunes son: gramos/m. L o g/cm 3. • La densidad se puede usar como un factor de conversión y para identificar una substancia. Si se conoce su masa se puede calcular su volumen y viceversa. • Ej. Digamos que se tiene una substancia cuya densidad es 0. 982 g/m. L. A) Calcule la masa de 25 ml de la substancia. B) Calcule el volumen de 5. 65 g de la substancia. A) B) • Propiedad Intensiva vs Extensiva: • Intensiva = masa, volumen, distancia, tiempo, etc. , dependen de la cantidad o magnitud. • Extensiva = densidad, velocidad o cualquier valor que sea una razón de propiedades intensivas.
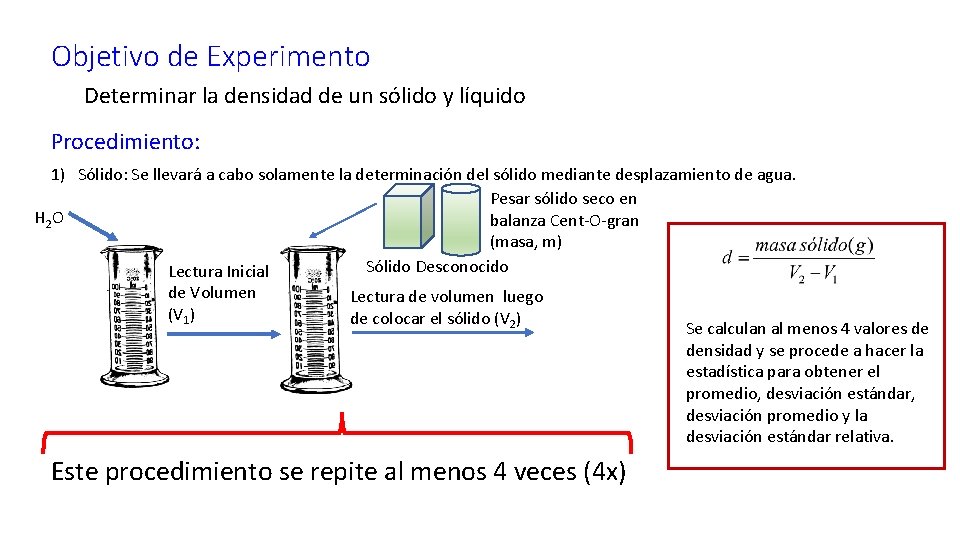
Objetivo de Experimento Determinar la densidad de un sólido y líquido Procedimiento: 1) Sólido: Se llevará a cabo solamente la determinación del sólido mediante desplazamiento de agua. Pesar sólido seco en H 2 O balanza Cent-O-gran (masa, m) Sólido Desconocido Lectura Inicial de Volumen Lectura de volumen luego (V 1) de colocar el sólido (V 2) Se calculan al menos 4 valores de densidad y se procede a hacer la estadística para obtener el promedio, desviación estándar, desviación promedio y la desviación estándar relativa. Este procedimiento se repite al menos 4 veces (4 x)
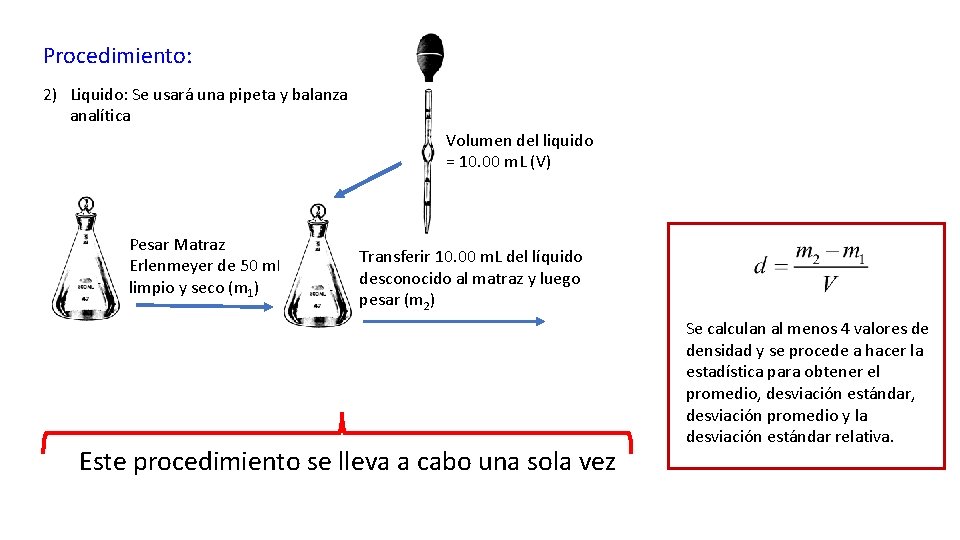
Procedimiento: 2) Liquido: Se usará una pipeta y balanza analítica Volumen del liquido = 10. 00 m. L (V) Pesar Matraz Erlenmeyer de 50 m. L limpio y seco (m 1) Transferir 10. 00 m. L del líquido desconocido al matraz y luego pesar (m 2) Este procedimiento se lleva a cabo una sola vez Se calculan al menos 4 valores de densidad y se procede a hacer la estadística para obtener el promedio, desviación estándar, desviación promedio y la desviación estándar relativa.
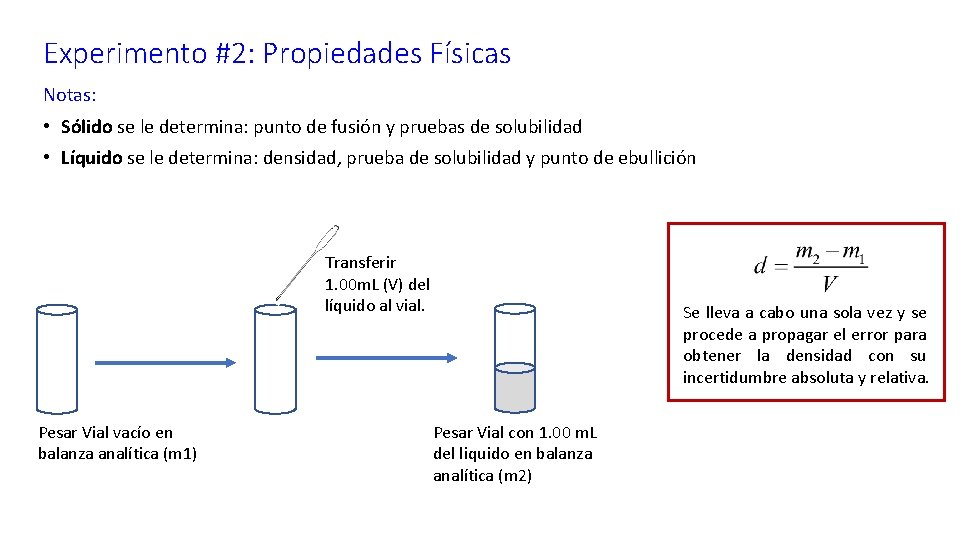
Experimento #2: Propiedades Físicas Notas: • Sólido se le determina: punto de fusión y pruebas de solubilidad • Líquido se le determina: densidad, prueba de solubilidad y punto de ebullición Transferir 1. 00 m. L (V) del líquido al vial. Pesar Vial vacío en balanza analítica (m 1) Se lleva a cabo una sola vez y se procede a propagar el error para obtener la densidad con su incertidumbre absoluta y relativa. Pesar Vial con 1. 00 m. L del liquido en balanza analítica (m 2)
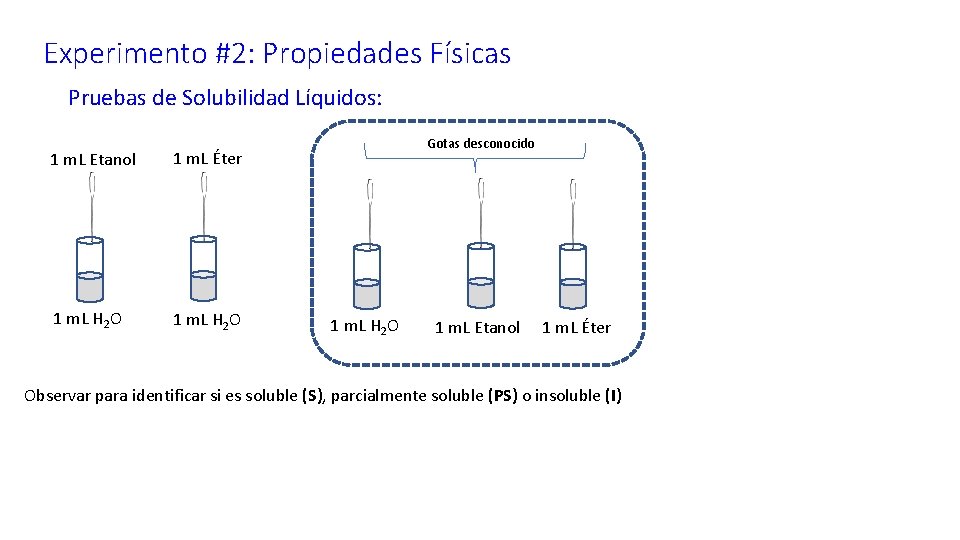
Experimento #2: Propiedades Físicas Pruebas de Solubilidad Líquidos: 1 m. L Etanol 1 m. L Éter 1 m. L H 2 O Gotas desconocido 1 m. L H 2 O 1 m. L Etanol 1 m. L Éter Observar para identificar si es soluble (S), parcialmente soluble (PS) o insoluble (I)
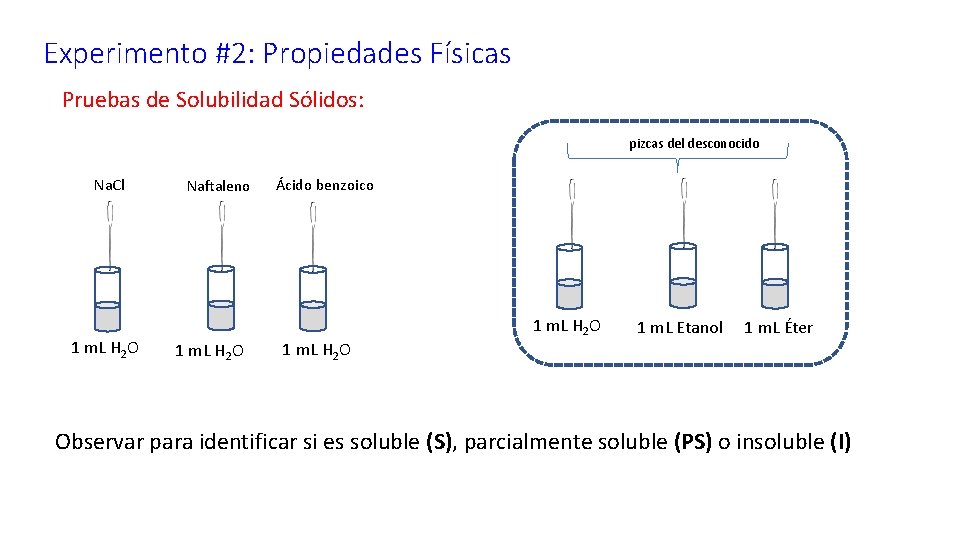
Experimento #2: Propiedades Físicas Pruebas de Solubilidad Sólidos: pizcas del desconocido Na. Cl 1 m. L H 2 O Naftaleno 1 m. L H 2 O Ácido benzoico 1 m. L H 2 O 1 m. L Etanol 1 m. L Éter Observar para identificar si es soluble (S), parcialmente soluble (PS) o insoluble (I)
Experimento #2: Propiedades Físicas Determinación Punto Ebullición (líquido): Se presentará esquema del equipo en el laboratorio Determinación Punto Fusión (sólido):
- Slides: 7