Experimentln metody bioenergetiky 4 ronk biochemie Spektroskopick metody

Experimentální metody bioenergetiky 4. ročník biochemie
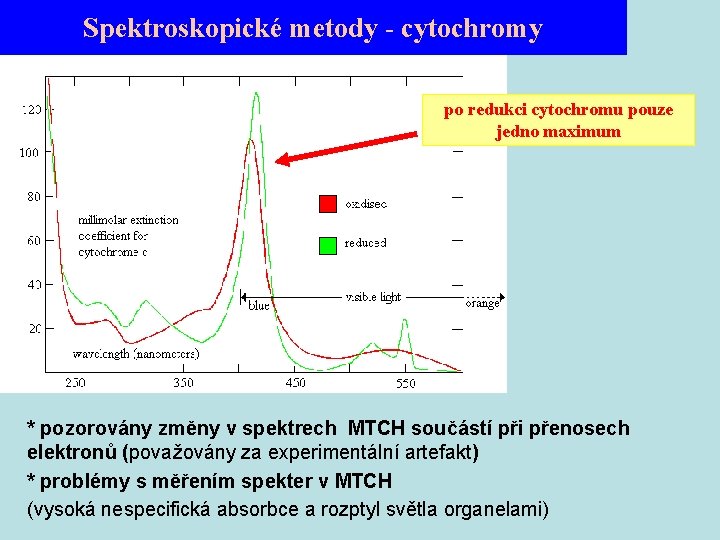
Spektroskopické metody - cytochromy po redukci cytochromu pouze jedno maximum * pozorovány změny v spektrech MTCH součástí při přenosech elektronů (považovány za experimentální artefakt) * problémy s měřením spekter v MTCH (vysoká nespecifická absorbce a rozptyl světla organelami)
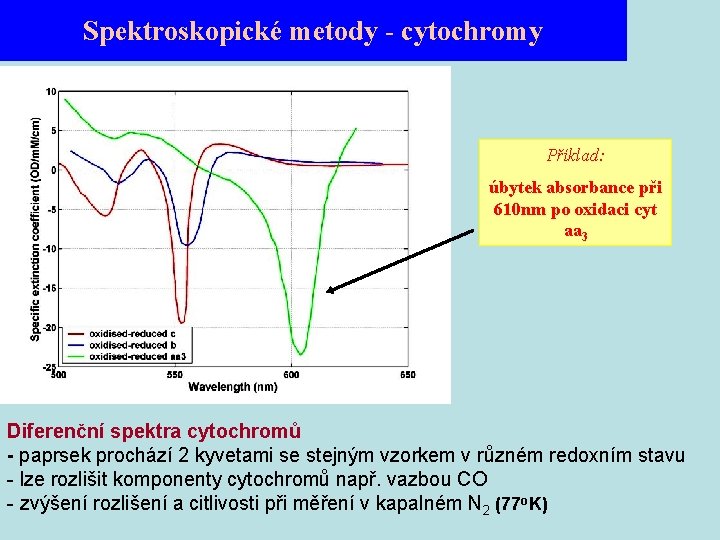
Spektroskopické metody - cytochromy Příklad: úbytek absorbance při 610 nm po oxidaci cyt aa 3 Diferenční spektra cytochromů - paprsek prochází 2 kyvetami se stejným vzorkem v různém redoxním stavu - lze rozlišit komponenty cytochromů např. vazbou CO - zvýšení rozlišení a citlivosti při měření v kapalném N 2 (77 o. K)
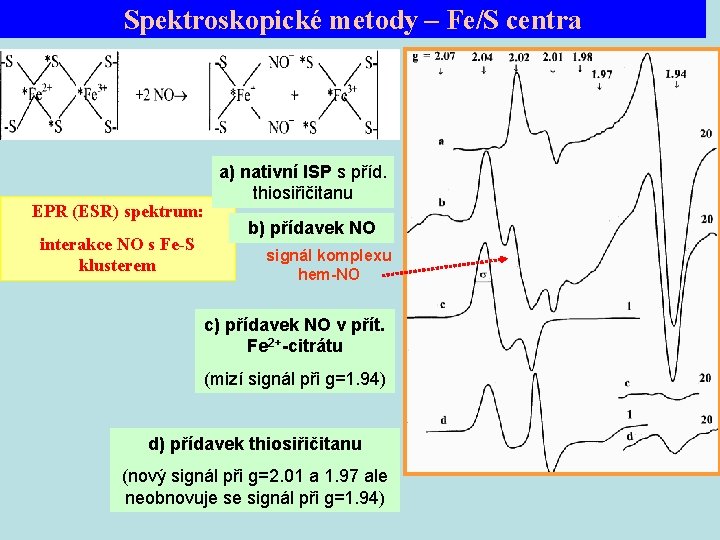
Spektroskopické metody – Fe/S centra EPR (ESR) spektrum: interakce NO s Fe-S klusterem a) nativní ISP s příd. thiosiřičitanu b) přídavek NO signál komplexu hem-NO c) přídavek NO v přít. Fe 2+-citrátu (mizí signál při g=1. 94) d) přídavek thiosiřičitanu (nový signál při g=2. 01 a 1. 97 ale neobnovuje se signál při g=1. 94)
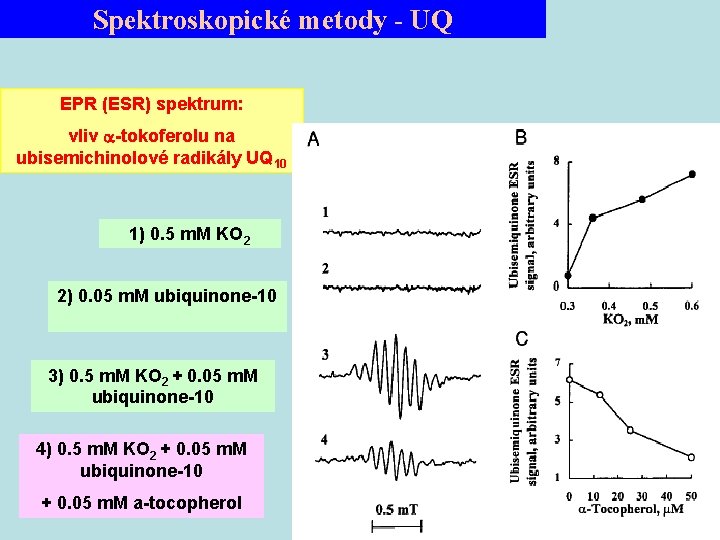
Spektroskopické metody - UQ EPR (ESR) spektrum: vliv -tokoferolu na ubisemichinolové radikály UQ 10 1) 0. 5 m. M KO 2 2) 0. 05 m. M ubiquinone-10 3) 0. 5 m. M KO 2 + 0. 05 m. M ubiquinone-10 4) 0. 5 m. M KO 2 + 0. 05 m. M ubiquinone-10 + 0. 05 m. M a-tocopherol
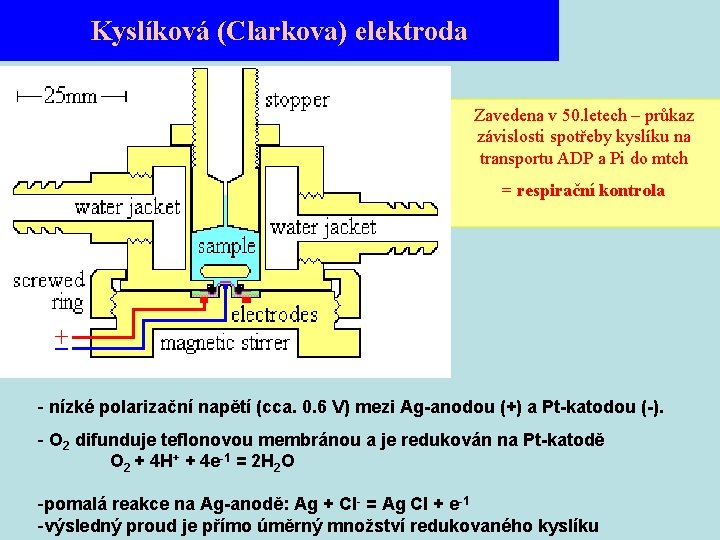
Kyslíková (Clarkova) elektroda Zavedena v 50. letech – průkaz závislosti spotřeby kyslíku na transportu ADP a Pi do mtch = respirační kontrola - nízké polarizační napětí (cca. 0. 6 V) mezi Ag-anodou (+) a Pt-katodou (-). - O 2 difunduje teflonovou membránou a je redukován na Pt-katodě O 2 + 4 H+ + 4 e-1 = 2 H 2 O -pomalá reakce na Ag-anodě: Ag + Cl- = Ag Cl + e-1 -výsledný proud je přímo úměrný množství redukovaného kyslíku
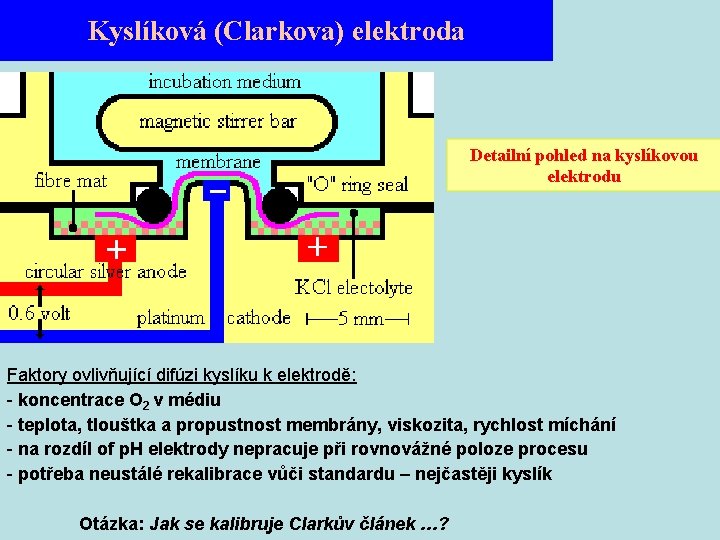
Kyslíková (Clarkova) elektroda Detailní pohled na kyslíkovou elektrodu Faktory ovlivňující difúzi kyslíku k elektrodě: - koncentrace O 2 v médiu - teplota, tlouštka a propustnost membrány, viskozita, rychlost míchání - na rozdíl of p. H elektrody nepracuje při rovnovážné poloze procesu - potřeba neustálé rekalibrace vůči standardu – nejčastěji kyslík Otázka: Jak se kalibruje Clarkův článek …?
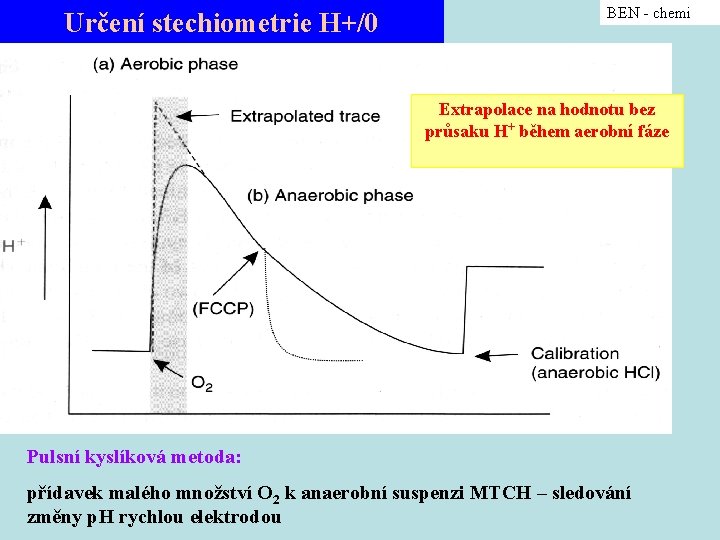
Určení stechiometrie H+/0 BEN - chemi Extrapolace na hodnotu bez průsaku H+ během aerobní fáze Pulsní kyslíková metoda: přídavek malého množství O 2 k anaerobní suspenzi MTCH – sledování změny p. H rychlou elektrodou

Inhibitory MTCH funkce BEN - meth Typy dle cílového místa: 1) Inhibitory dýchacího řetězce (např. KCN, antimycin, rotenone ) blokování dýchání v přítomnosti ADP nebo rozpojovačů 2) Inhibitory fosforylace (např. oligomycin) zrušení nárůstu spotřeby O 2 po přidávku x bez efektu na dýchání stimulované rozpojovači 3) Rozpojovače (např. dinitrofenol, CCCP, FCCP) zrušení spojení dýchacího řetězce a fosforylace v intaktních MTCH. 4) Inhibitory transportu (např. atractyloside, bongkrekát, NEM) inhibice exportu ATP nebo import substrátů do MTCH 5) Ionofory (např. valinomycin, nigericin) propustnost vnitřní membrány pro neprůchozí ionty 6) Inhibitory Krebsova cyklu (např. arsenitan, aminooxyacetát) inhibice enzymů TCA cyklu

Určení respirační kontroly a poměru P/O Rychlost spotřeby kyslíku ve stavu 4 je obvykle vyšší než ve stavu 2 před prvním přídavkem ADP Proč? Výpočet poměru P/O z grafu: pokles konc. O 2 (z grafu) = 0. 135 m. M objem reakční nádobky = 2. 5 ml O- atomy spotřebované ve stavu 3 = 0. 135 * 2. 5 = 0. 68. 10 -6 atomů (všimněte si faktoru 2) přídavek ADP (20 l 50 m. M roztoku) = vytvořené ATP = celkem 1 mol P: O = [ATP ] : [O 2] = 1. 48 (pro oxidaci sukcinátu) Hodnota pro NADH je vyšší (cca 2. 5) – Proč ? ?

Měření protonmotivní síly BEN - meth Měření p – zahrnuje oddělené stanovení a p. H Stanovení ~ rovnovážná distribuce permeabilních kationtů na každých 60 m. V = 10 x násobná akumulace iontů v příslušném kompartmentu (kationty v záporně nabitém apod. ) Stanovení p. H ~ rovnovážná distribuce permeabilních slabých kyselin na každých 60 m. V = 10 násobná akumulace kyseliny v basickém kompartmentu Důležité: - minimální koncentrace použité „sondy“ - p. H komponentu lze minimalizovat vysokou konc. Pi nebo nigericinem
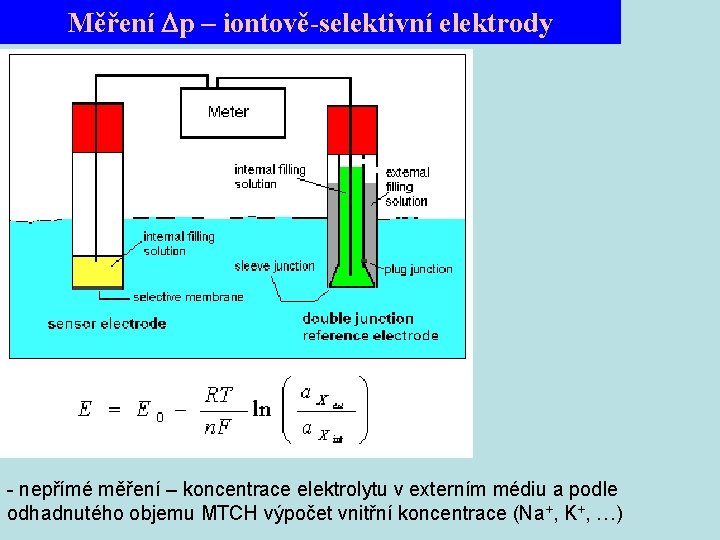
Měření p – iontově-selektivní elektrody - nepřímé měření – koncentrace elektrolytu v externím médiu a podle odhadnutého objemu MTCH výpočet vnitřní koncentrace (Na+, K+, …)

Měření p – vnitřní optické indikátory BEN - meth „Elektrochromismus“ -změna spektrálních vlastností membránových složek při vytvoření potenciálu na membráně = 200 m. V odpovídá elektrickému poli cca 300 000 V cm-1 Karotenoidy = nejvýznamnější indikátory - centrální hydrofóbní část s konjug. dvojnými vazbami - velice rychlá odpověď (řádově ns) - změny v abs. maximech do několika nm = nutnost duálních spekter - reagují pouze na změny potenciálu v bezprostřední blízkosti molekuly (výsledkem vyšší hodnoty než metodou distribuce iontů)
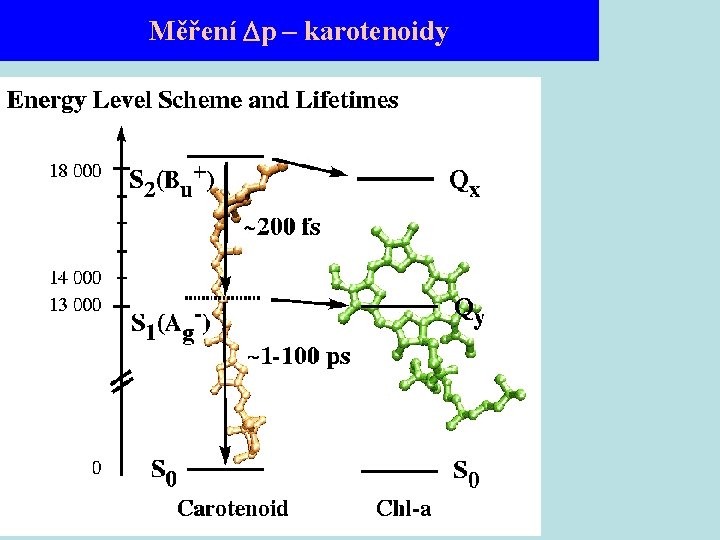
Měření p – karotenoidy
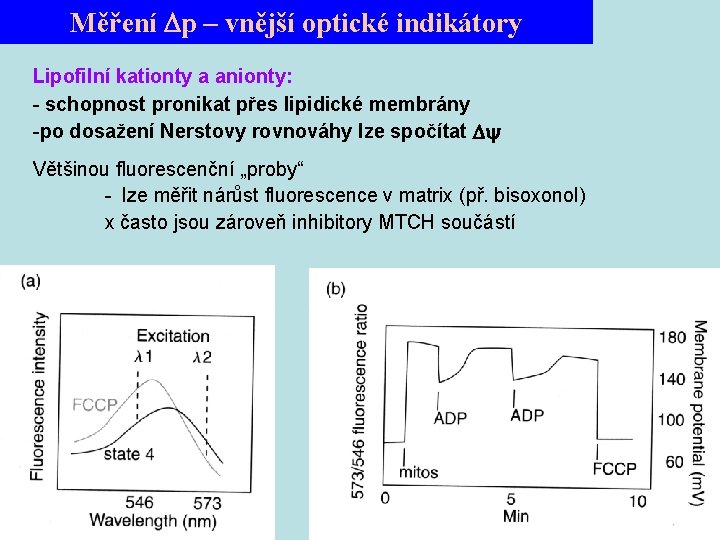
Měření p – vnější optické indikátory Lipofilní kationty a anionty: - schopnost pronikat přes lipidické membrány -po dosažení Nerstovy rovnováhy lze spočítat Většinou fluorescenční „proby“ - lze měřit nárůst fluorescence v matrix (př. bisoxonol) x často jsou zároveň inhibitory MTCH součástí

Měření p – 31 P-NMR BEN - meth Přímá metoda: Resonanční energie jádra fosforu v Pi je ovlivněna jeho protonizací p. Ka pro H 2 PO 4 -/HPO 4 2 - = 6. 8 …. možnost měření p. H v 6 -7. 6 -NMR signál je průměrem signálu obou protonovaných forem (výměna protonu je rychlá v měřítku NMR metody) -p. H lze vypočítat z konc. Pi uvnitř a vně MTCH Nevýhody: - nízká citlivost – cca m. M koncentrace Pi - vyžaduje husté suspenze MTCH x problémem s difúzí kyslíku a substrátů
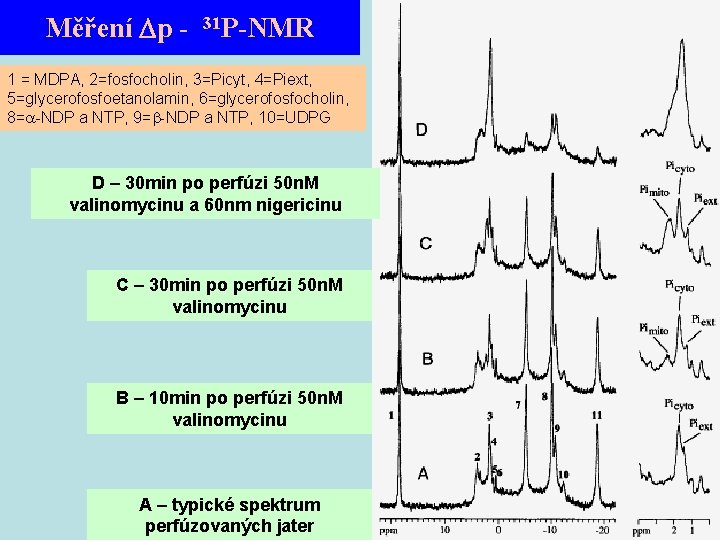
Měření p - 31 P-NMR 1 = MDPA, 2=fosfocholin, 3=Picyt, 4=Piext, 5=glycerofosfoetanolamin, 6=glycerofosfocholin, 8= -NDP a NTP, 9= -NDP a NTP, 10=UDPG D – 30 min po perfúzi 50 n. M valinomycinu a 60 nm nigericinu C – 30 min po perfúzi 50 n. M valinomycinu B – 10 min po perfúzi 50 n. M valinomycinu A – typické spektrum perfúzovaných jater

Děkuji vám za pozornost!
- Slides: 18