Experimente fr den PCB Unterricht V Modelle und

Experimente für den PCB- Unterricht V Modelle und Modellvorstellungen Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
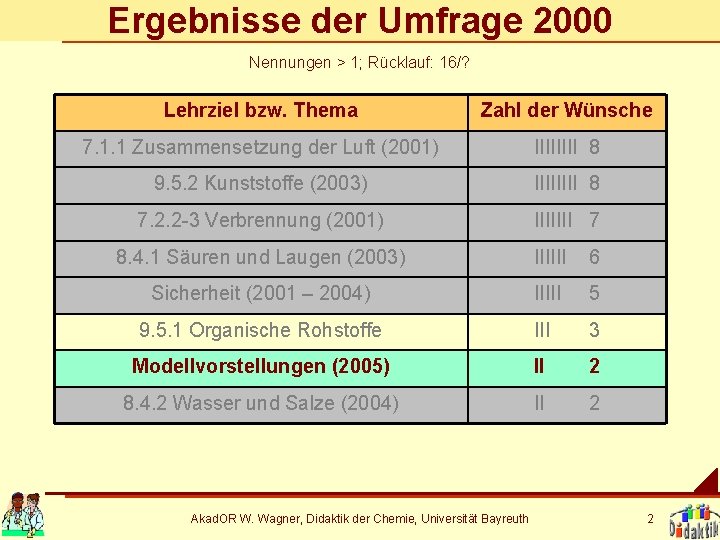
Ergebnisse der Umfrage 2000 Nennungen > 1; Rücklauf: 16/? Lehrziel bzw. Thema Zahl der Wünsche 7. 1. 1 Zusammensetzung der Luft (2001) IIII 8 9. 5. 2 Kunststoffe (2003) IIII 8 7. 2. 2 -3 Verbrennung (2001) IIIIIII 7 8. 4. 1 Säuren und Laugen (2003) IIIIII 6 Sicherheit (2001 – 2004) IIIII 5 9. 5. 1 Organische Rohstoffe III 3 Modellvorstellungen (2005) II 2 8. 4. 2 Wasser und Salze (2004) II 2 Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 2
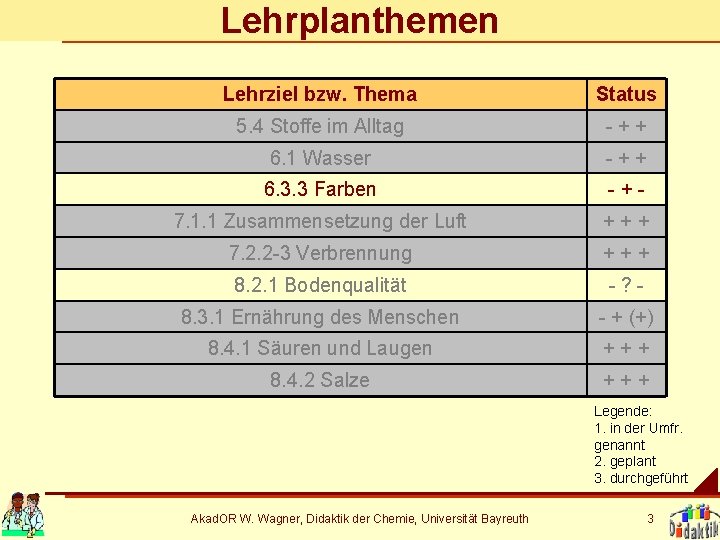
Lehrplanthemen Lehrziel bzw. Thema Status 5. 4 Stoffe im Alltag -++ 6. 1 Wasser -++ 6. 3. 3 Farben -+- 7. 1. 1 Zusammensetzung der Luft +++ 7. 2. 2 -3 Verbrennung +++ 8. 2. 1 Bodenqualität -? - 8. 3. 1 Ernährung des Menschen - + (+) 8. 4. 1 Säuren und Laugen +++ 8. 4. 2 Salze +++ Legende: 1. in der Umfr. genannt 2. geplant 3. durchgeführt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 3

Lehrplanthemen Lehrziel bzw. Thema Status 9. 3. 2 Aufbau der Materie (2005) -++ 9. 3. 3 Radioaktivität -? - 9. 5. 1 Organische Rohstoffe ++- 9. 5. 2 Kunststoffe +++ 10. 3. 2 Atome, Elemente, Bindungen (2005) -++ 10. 6. 1 Energie von der Sonne -+- 10. 6. 2 Energie aus Kernkraftwerken -? - Modellvorstellungen (2005) +++ Legende: 1. in der Umfr. genannt 2. geplant 3. durchgeführt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 4

Programm • • • 09. 00 – 09. 30 Uhr: Modelle (V) 09. 30 – 10. 30 Uhr: Selbstbau von Modellen I (P) 10. 30 – 11. 00 Uhr: Atombau (V) 11. 00 – 11. 30 Uhr: Selbstbau von Modellen II (P) 11. 30 – 12. 30 Uhr: Mittagspause 12. 30 – 13. 00 Uhr: Selbstbau von Modellen III (P) 13. 00 – 14. 00 Uhr: and. Selbstbaumodelle (De/Di) 14. 00 – 15. 00 Uhr: Chemische Bindung (V) 15. 00 – 15. 30 Uhr: Pause 15. 30 – 16. 30 Uhr: Schlussbesprechung (Di) Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 5

1. Modelle Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
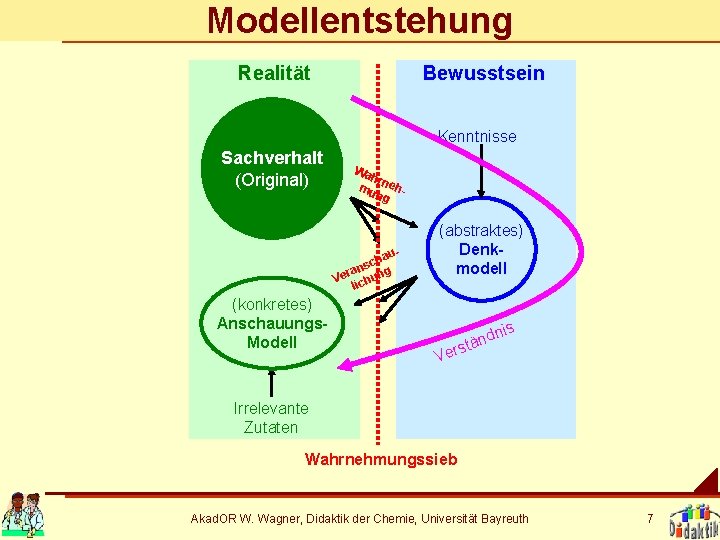
Modellentstehung Realität Bewusstsein Kenntnisse Sachverhalt (Original) Wa hr mu nehng auh c ans g Ver ichun l (konkretes) Anschauungs. Modell (abstraktes) Denkmodell nis d n rstä Ve Irrelevante Zutaten Wahrnehmungssieb Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 7

Bsp. : Modellexperiment Exo- und endotherme Reaktionen Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 8

Begriff: Modell http: //de. wikipedia. org/wiki/Modell : • Das Wort: aus Italien (Renaissance) • modello, aus modulo, dem Maßstab in der Architektur • bis 18. Jh. : Fachsprache der bildenden Künstler • um 1800: verdrängte im Deutschen das ältere, direkt vom lat. modulus entlehnte Model (Muster, Form, z. B. Kuchenform), das noch im Verb ummodeln fortlebt. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 9

Begriff: Modell 1. Abbildung natürlicher oder künstlicher Originale (die selbst wieder Modelle sein können). 2. Verkürzung. Erfasst nicht alle Seiten des Originals, sondern nur diejenigen, die dem Modellschaffer bzw. Modellnutzer relevant erscheinen. 3. Pragmatische Orientierung am Nützlichen. Frage Wozu? Ein Modell wird vom Modellschaffer bzw. Modellnutzer innerhalb einer bestimmten Zeitspanne und zu einem bestimmten Zweck für ein Original eingesetzt. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 10

Begriff: Modell Ein Modell zeichnet sich durch die bewusste Vernachlässigung bestimmter Merkmale aus, um die für den Modellierer oder den Modellierungszweck wesentlichen Modelleigenschaften hervorzuheben. Literatur: Stachowiak, Herbert (1973): „Allgemeine Modelltheorie“, Wien. Nach http: //de. wikipedia. org/wiki/Modell Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 11

Schlussfolgerungen 1. Ein Modell ist nie „richtig“, also mit der Wirklichkeit identisch (Bsp. : Kochsalz, Strukturmodelle). 2. Ein Modell ist nie endgültig (Bsp. : Atommodell). 3. Ein Modell ist nie falsch, aber es kann für den Zweck ungeeignet sein. 4. Die Wissenschaft verwendet i. d. R. nur ein Modell („die exakteste Beschreibung der Wirklichkeit“), die Schule viele (z. B. historische Stufen). Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 12
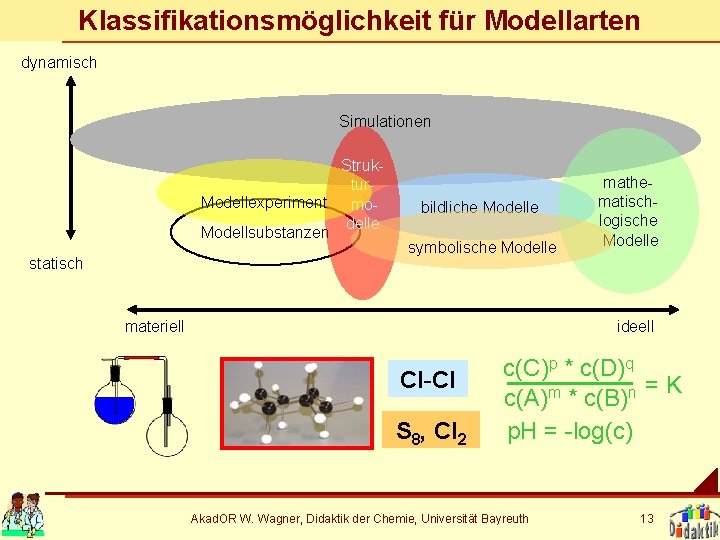
Klassifikationsmöglichkeit für Modellarten dynamisch Simulationen Struktur. Modellexperiment modelle Modellsubstanzen statisch bildliche Modelle symbolische Modelle materiell mathematischlogische Modelle ideell Cl-Cl S 8, Cl 2 c(C)p * c(D)q =K c(A)m * c(B)n p. H = -log(c) Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 13

Modellbau Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
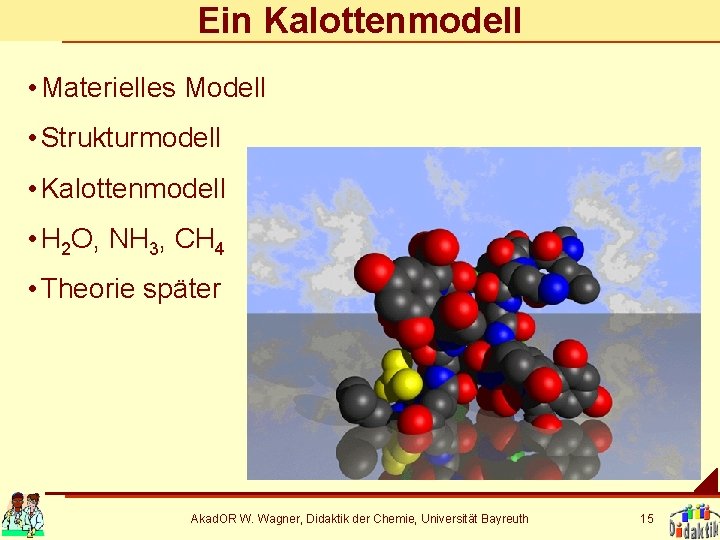
Ein Kalottenmodell • Materielles Modell • Strukturmodell • Kalottenmodell • H 2 O, NH 3, CH 4 • Theorie später Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 15

Anleitung: Kalottenmodell aus Styropor 1. Stecken Sie einen Zahnstocher möglichst senkrecht mitten in den Ring, der auf der großen Styroporkugel an den Polen zu sehen ist. 2. Stellen Sie die Styroporkugel so in das Loch der Schablone, dass der Zahnstocher möglichst senkrecht steht. 3. Markieren Sie mit dem Filzstift die Position der 120°Markierungen auf der Styroporkugel mit einem senkrechten Strich. 4. Binden Sie den Faden mit einem Ende an dem schon steckenden Zahnstocher fest. 5. Markieren Sie mit dem Filzstift die Entfernung von 109/360 U mit einem waagrechten Strich. U = d * π. 109/360=0, 30. An den entstehenden Kreuzungspunkten befinden sich die Positionen der Liganden. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 16

Anleitung 6. Markieren Sie an einem Zahnstocher von einem Ende her die Entfernung von 5 mm. Stecken Sie den Zahnstocher an jeder Ligandenposition bis zur Markierung hinein. 7. Schleifen Sie an jeder Markierung möglichst tangential so viel Styropor weg, dass das Loch nicht mehr zu sehen ist. 8. Streichen Sie die Kugel in der CPK-Farbe (Corey, Pauling, Koltun) des gewünschten Atoms (C = schwarz, H = weiß, O = rot, N = blau, S = gelb, Cl = grün. . . ) 9. Schleifen Sie die Wasserstoff-Kugeln nach 6 -7 auch an und kleben Sie sie einzeln mit etwas Styroporkleber auf; erst nach dem Trocknen folgt die nächste. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 17

2. Atombau und Bindung Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth

Aus dem Lehrplan 9. 3. 2 Aufbau der Materie: • Größenverhältnisse Zelle – Molekül – Atom – (Elementarteilchen) • Aufbau der Atome aus Kern (p, n) und Hülle (e) • Atommodelle: Kugelmodell – Kern-Hülle-Modell • Unterscheiden von Elementen, z. B. H, He, Na, Cl, C aufgrund der Zahl der Protonen • Unterscheidung von Isotopen aufgrund der Massezahl (p + n) Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 19

Größenverhältnisse • Durchmesser eines C-Atoms: 150 pm = 1, 5*10 -10 m • Größenunterschied zwischen Kirchturm (100 m) und einem Staubkorn (0, 1 mm) = 10 -6 • Das Kohlenstoffatom ist so viel mal kleiner als ein Staubkorn, wie ein Staubkorn kleiner ist als ein Kirchturm. • Von 100 m bis ~100 pm: Faktor 10 -12 = 10 -6 * 10 -6 Moleküle sind 1(-100) nm = 10 -9 m groß. C 60 = 1, 002 nm Bakterien sind 1 µm = 10 -6 m groß. Zellen sind 0, 1 mm = 10 -4 m groß. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 20

2. 1 Ein herkömmlicher Weg zum Atombau Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth

Ein wenig Geschichte -500 EMPEDOKLES: Luft, Feuer, Wasser, Erde DEMOKRIT: „Atomos“ EPIKUR: „Chem. Bindung“ ARISTOTELES: „ 4 Elemente: Feuer, Wasser, Erde, Luft“ 0 500 2000 Jahre „Kirchenvakuum“: 322 v. Chr. – 1632 n. Chr. Aristotelisches Weltbild wird dogmatisch übernommen, „Ketzer“ hingerichtet. 1000 1500 2000 GASSENDI, KEPLER, GALILEI DALTON: 1. und 2. Verbindungsgesetz AVOGADRO: Gase, Moleküle FARADAY: elektrische Natur der Atome RUTHERFORD: experimentelle Beweise Akad. OR W. Wagner, Didaktik. HEISENBERG: der Chemie, Universität Bayreuth BOHR; PLANCK, Orbitaltheorie 22
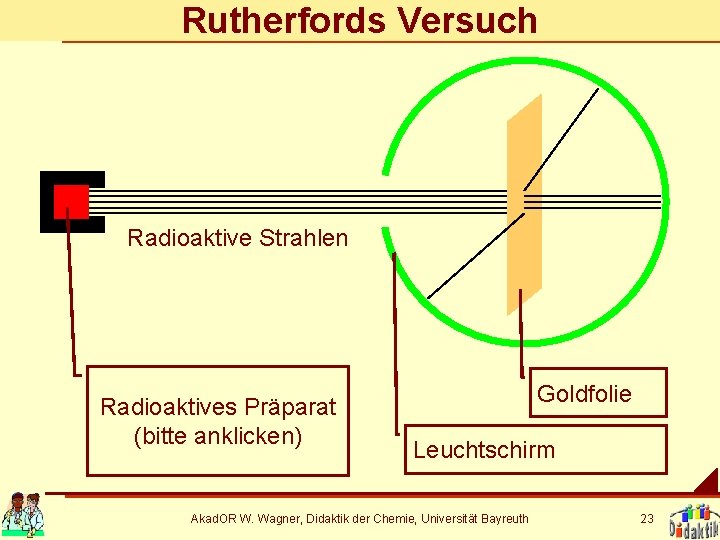
Rutherfords Versuch Radioaktive Strahlen Radioaktives Präparat (bitte anklicken) Goldfolie Leuchtschirm Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 23
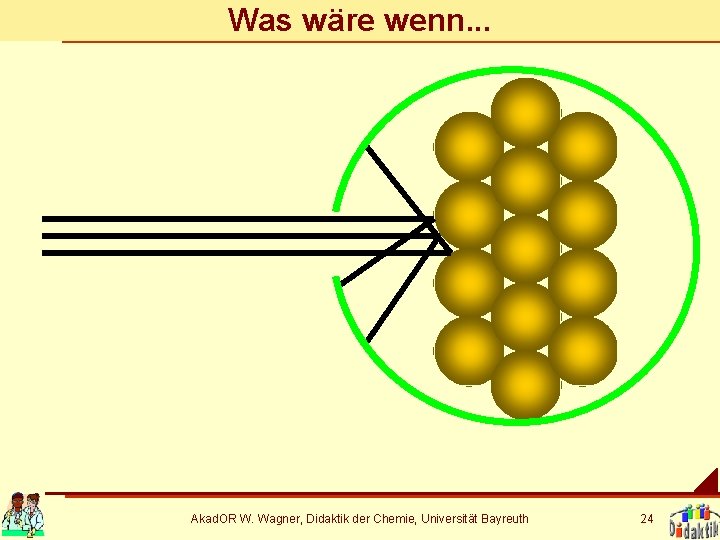
Was wäre wenn. . . Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 24
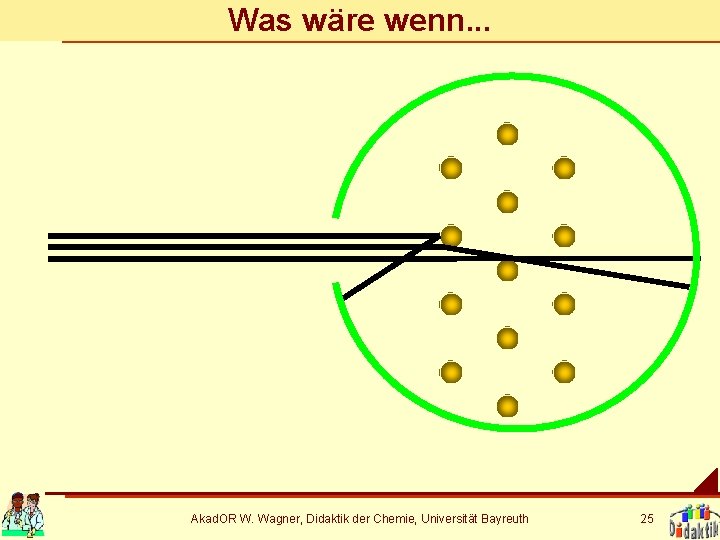
Was wäre wenn. . . Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 25
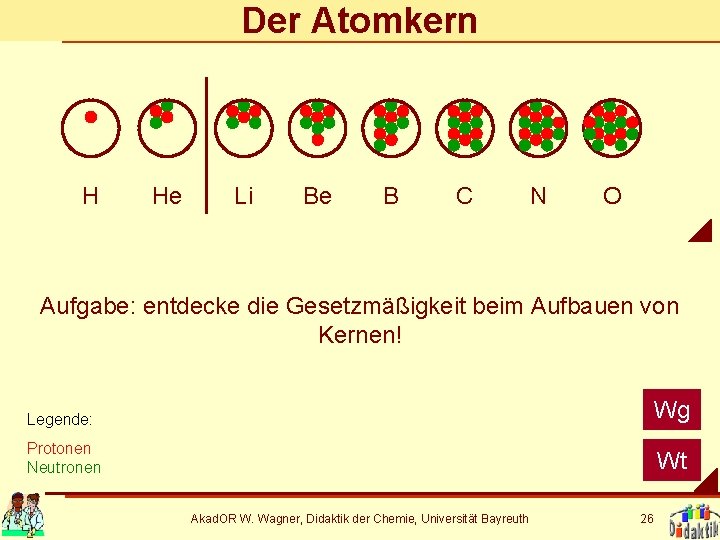
Der Atomkern H He Li Be B C N O Aufgabe: entdecke die Gesetzmäßigkeit beim Aufbauen von Kernen! Legende: Wg Protonen Neutronen Wt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 26

Die Bedeutung von Kernteilchen Elemente unterscheiden sich durch die Zahl ihrer Protonen. Neutronen spielen hierbei keine Rolle. Aufeinander folgende Elemente im PSE besitzen immer genau ein Proton mehr. Zu jedem Proton muss in der Schale ein Elektron existieren. Elektronen bestimmen die chemischen Eigenschaften eines Elementes. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 27

Die Bedeutung von Kernteilchen Mit Ausnahme des Wasserstoffs besitzt jedes Element auch Neutronen im Kern. Je Proton benötigt man mindestens ein Neutron, damit der Kern stabil ist. Bis zum Element 40 Ca gilt: je Proton genau ein Neutron, danach werden es mehr. Bsp. : 238 Nu - 92 p = 146 n : 92 p = 1, 6 Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 28

Eine Applikation D: ein selbst gebautes Atomkernmodell Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 29
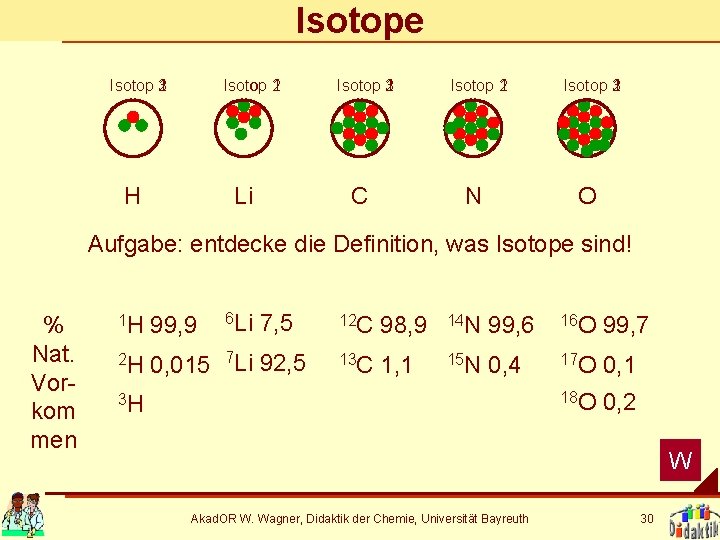
Isotope Isotop 3 1 2 Isotop 1 2 H Li Isotop 3 1 2 C Isotop 2 1 Isotop 3 1 2 O N Aufgabe: entdecke die Definition, was Isotope sind! % Nat. Vorkom men 6 Li 7, 5 1 H 99, 9 2 H 0, 015 7 Li 92, 5 12 C 98, 9 14 N 99, 6 16 O 99, 7 13 C 1, 1 15 N 0, 4 17 O 0, 1 18 O 0, 2 3 H W Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 30
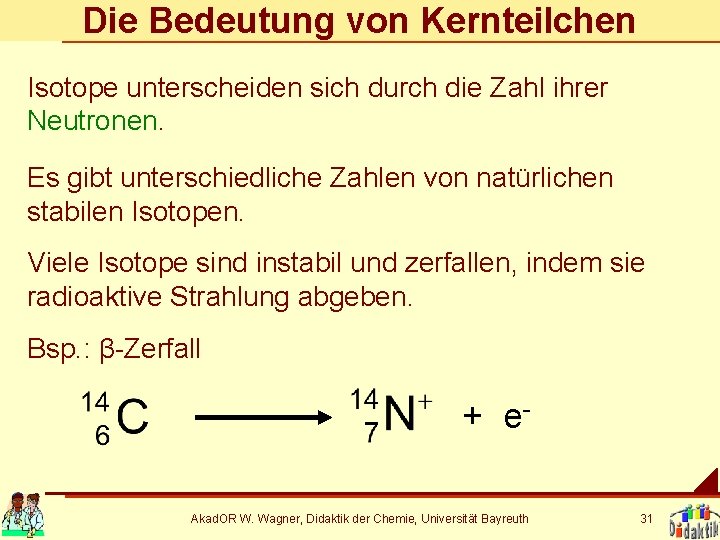
Die Bedeutung von Kernteilchen Isotope unterscheiden sich durch die Zahl ihrer Neutronen. Es gibt unterschiedliche Zahlen von natürlichen stabilen Isotopen. Viele Isotope sind instabil und zerfallen, indem sie radioaktive Strahlung abgeben. Bsp. : β-Zerfall + e. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 31
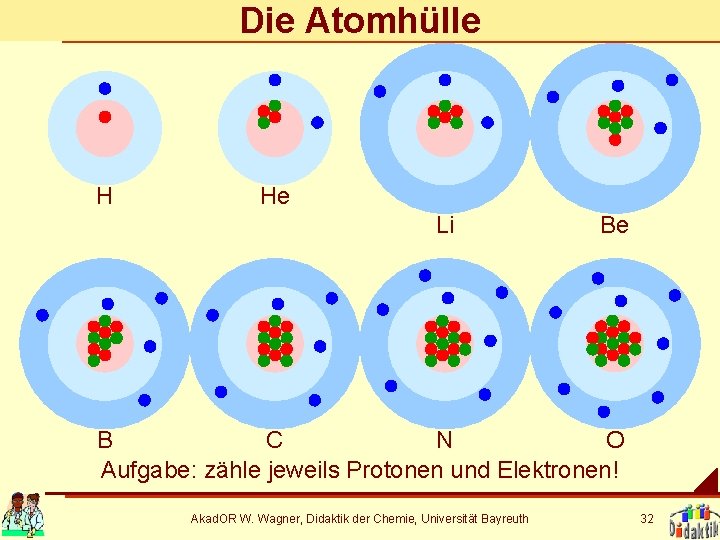
Die Atomhülle H He Li Be B C N O Aufgabe: zähle jeweils Protonen und Elektronen! Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 32

Aufbau der Elektronenhülle 1. Elektronen kommen in Schalen um den Kern vor. 2. In die erste Schale passen zwei Elektronen, in die zweite mehr. 3. Die Zahl der passenden Elektronen erhält man: 2 n 2, wobei n = Schalennummer n=1 2 Elektronen n=2 8 Elektronen n=3 18 Elektronen 4. Die Zahl der Protonen und Elektronen ist immer gleich. 5. Deshalb sind Atome immer neutral. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 33
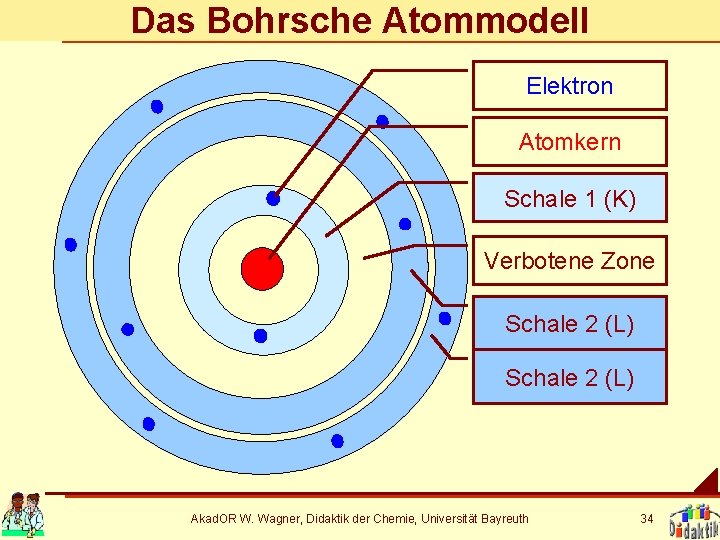
Das Bohrsche Atommodell Elektron Atomkern Schale 1 (K) Verbotene Zone Schale 2 (L) Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 34

Noch eine Applikation Ein selbst gebautes Atomhüllenmodell Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 35

2. 2 Probleme Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth

Aus dem Lehrplan 10. 3. 2 Atome, Elemente, Bindungen: • Atommodell: Kern-Schale („Hülle“); PSE als Erklärungshilfe für das Reaktionsverhalten chemischer Elemente • Ionenbindung, Elektronenpaarbindung, physikalischchemische Eigenschaften aufgrund der Bindungsart • Modelle und Formeln als Verständnishilfen für chemische Bindungen Verständnishilfen Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 37
Warum? Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 38

2. 3 Lösung: das Kugelwolkenmodell nach KIMBALL Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
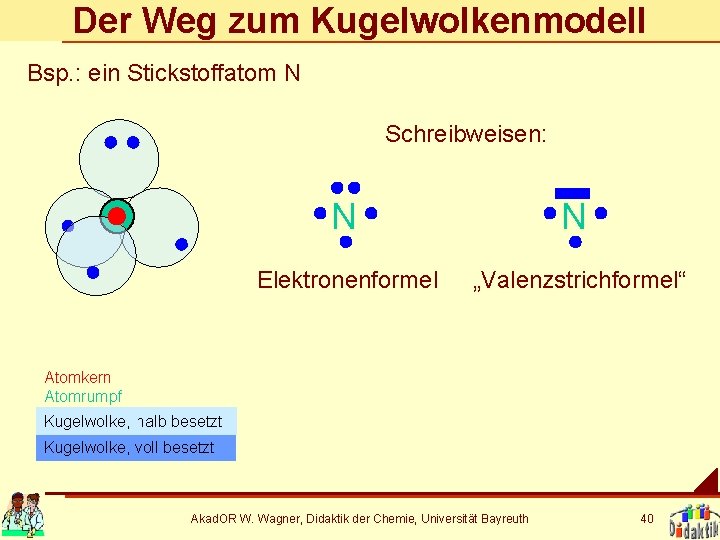
Der Weg zum Kugelwolkenmodell Bsp. : ein Stickstoffatom N Schreibweisen: N N Elektronenformel „Valenzstrichformel“ Atomkern Atomrumpf Kugelwolke, halb besetzt Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 40
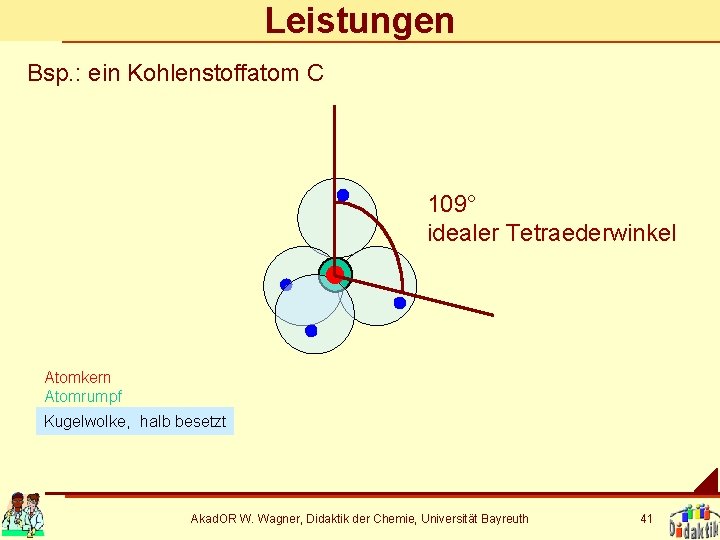
Leistungen Bsp. : ein Kohlenstoffatom C 109° idealer Tetraederwinkel Atomkern Atomrumpf Kugelwolke, halb besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 41
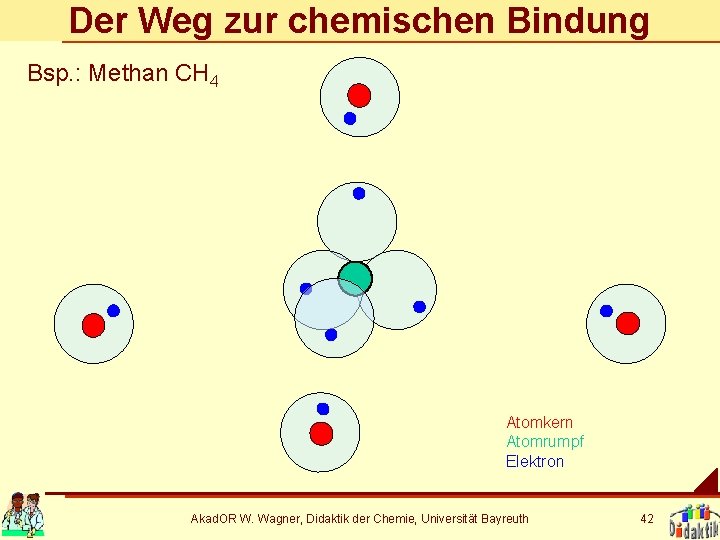
Der Weg zur chemischen Bindung Bsp. : Methan CH 4 Atomkern Atomrumpf Elektron Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 42
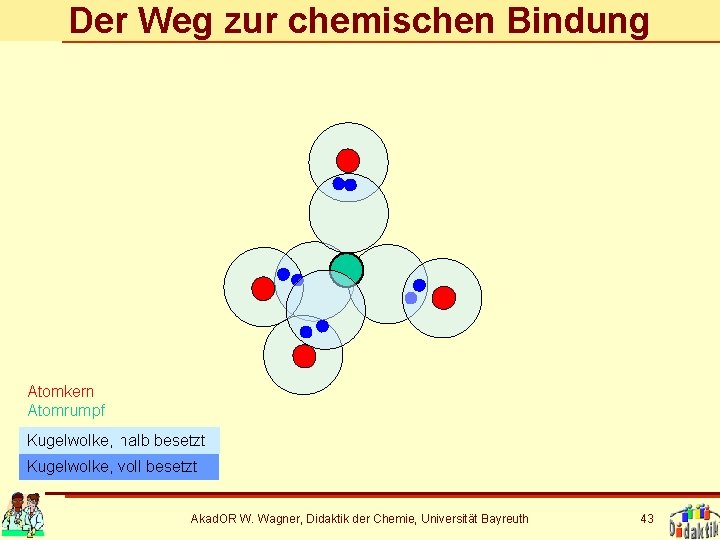
Der Weg zur chemischen Bindung Atomkern Atomrumpf Kugelwolke, halb besetzt Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 43
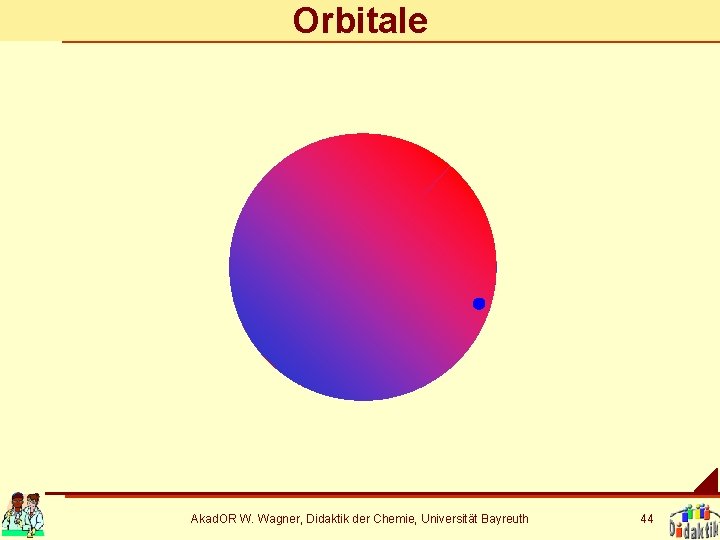
Orbitale Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 44
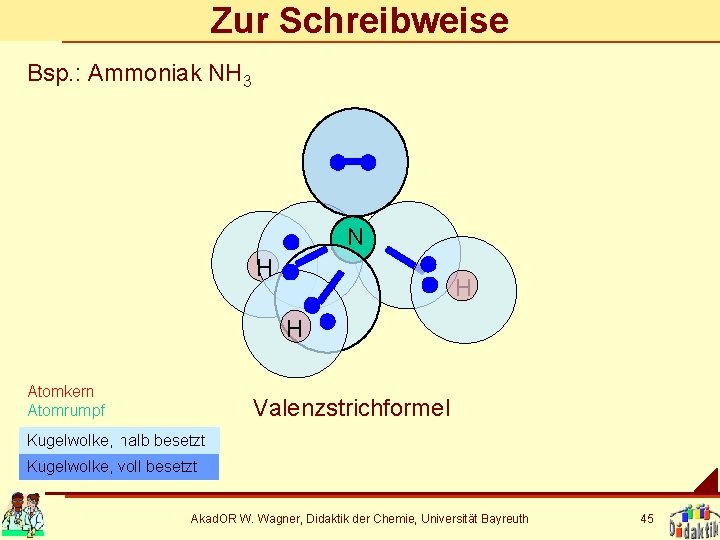
Zur Schreibweise Bsp. : Ammoniak NH 3 N H H H Atomkern Atomrumpf Valenzstrichformel Kugelwolke, halb besetzt Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 45
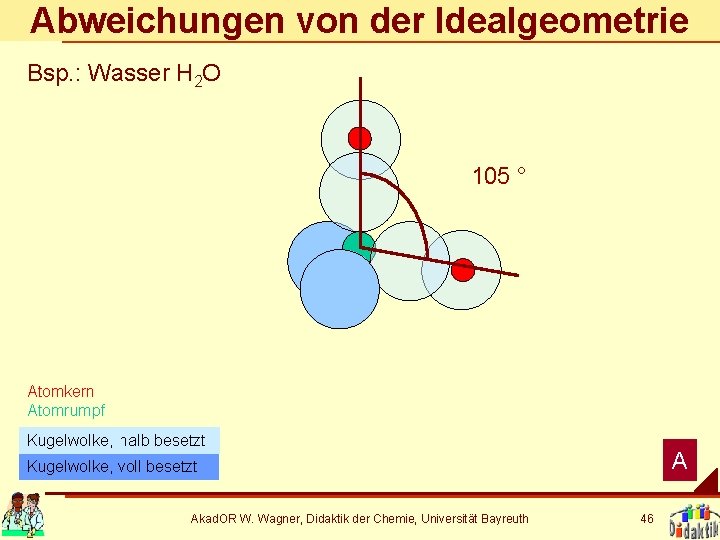
Abweichungen von der Idealgeometrie Bsp. : Wasser H 2 O 105 ° Atomkern Atomrumpf Kugelwolke, halb besetzt A Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 46
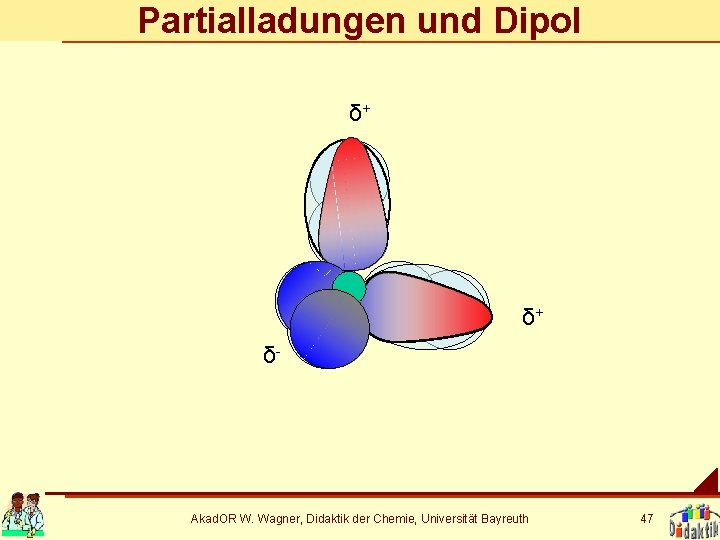
Partialladungen und Dipol δ+ δ+ δ- Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 47
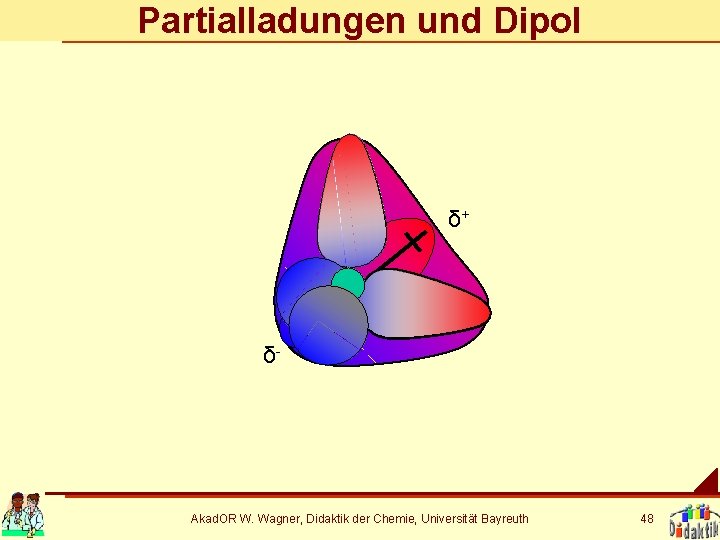
Partialladungen und Dipol δ+ δ- Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 48

Demonstration V: Nachweis des Dipolcharakters von Wasser Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 49

2. 4 Weitere Beispiele für die Anwendung des Kugelwolkenmodells Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
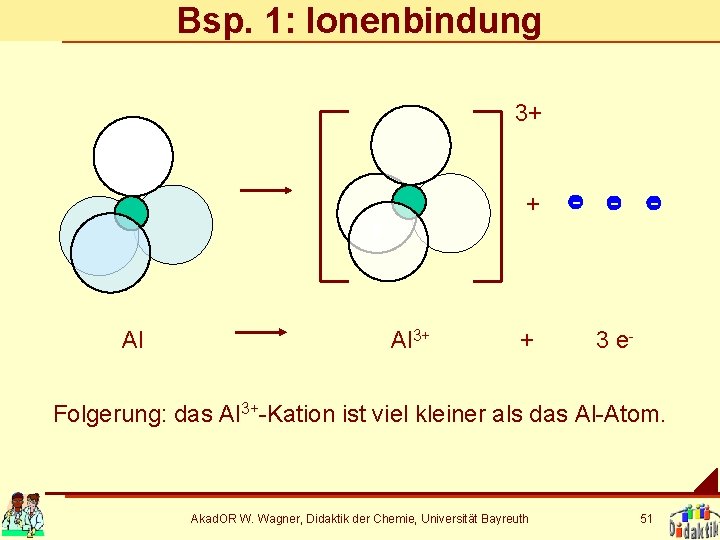
Bsp. 1: Ionenbindung 3+ + Al Al 3+ + - - - 3 e- Folgerung: das Al 3+-Kation ist viel kleiner als das Al-Atom. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 51
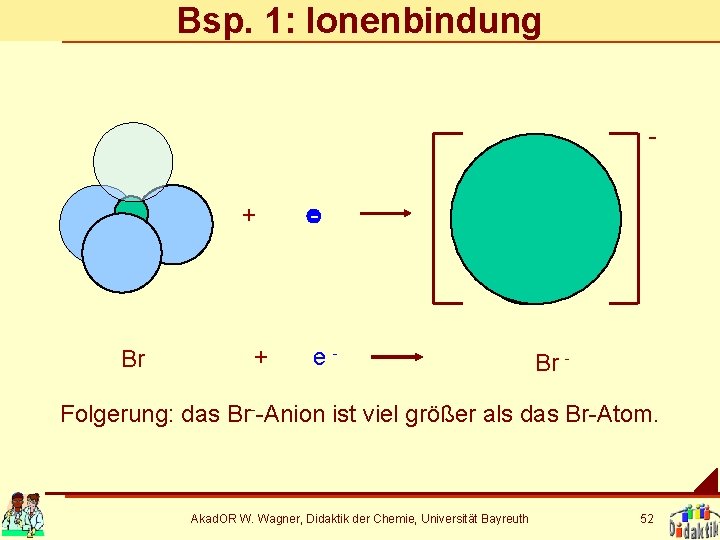
Bsp. 1: Ionenbindung + Br + - e- Br - Folgerung: das Br--Anion ist viel größer als das Br-Atom. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 52

Bsp. 2: Mehrfachbindungen Aus dem Lehrplan: 10. 5. 1 Kohlenwasserstoffe: • ungesättigte KW, z. B. Ethen, Propen; Modelle, Strukturformel, Summenformel • Chemische Vorgänge bei der Herstellung von Kunststoffen; Polymerisation, Polykondensation, Makromoleküle; Modelle • . . . Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 53
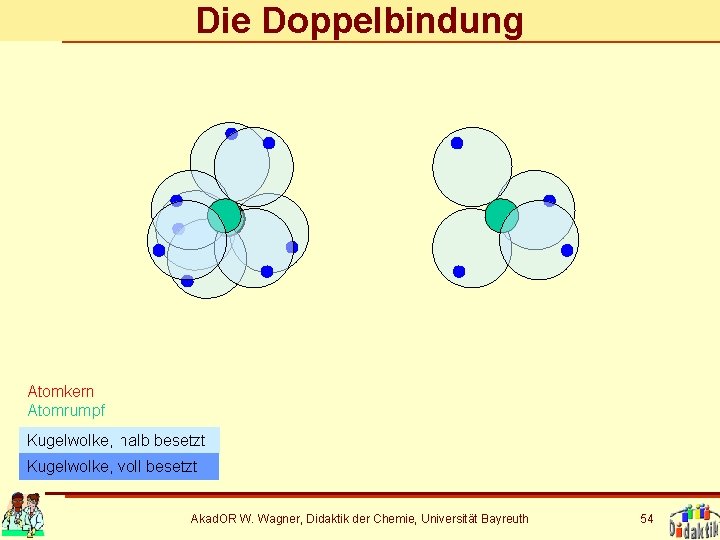
Die Doppelbindung Atomkern Atomrumpf Kugelwolke, halb besetzt Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 54
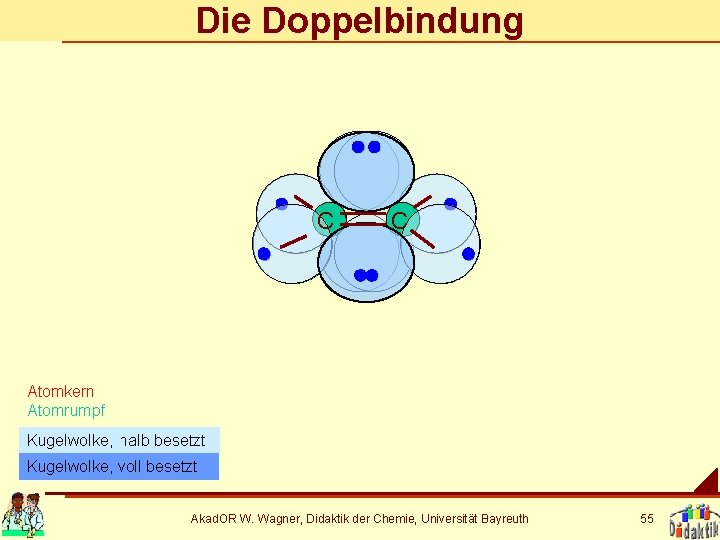
Die Doppelbindung C C Atomkern Atomrumpf Kugelwolke, halb besetzt Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 55
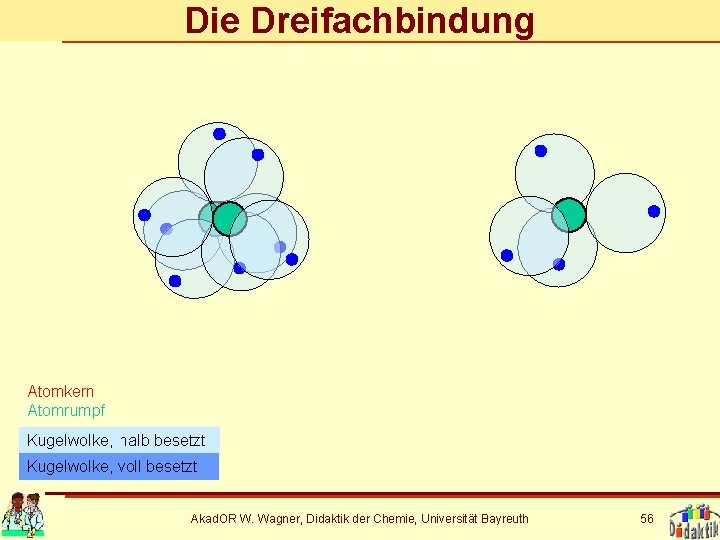
Die Dreifachbindung Atomkern Atomrumpf Kugelwolke, halb besetzt Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 56
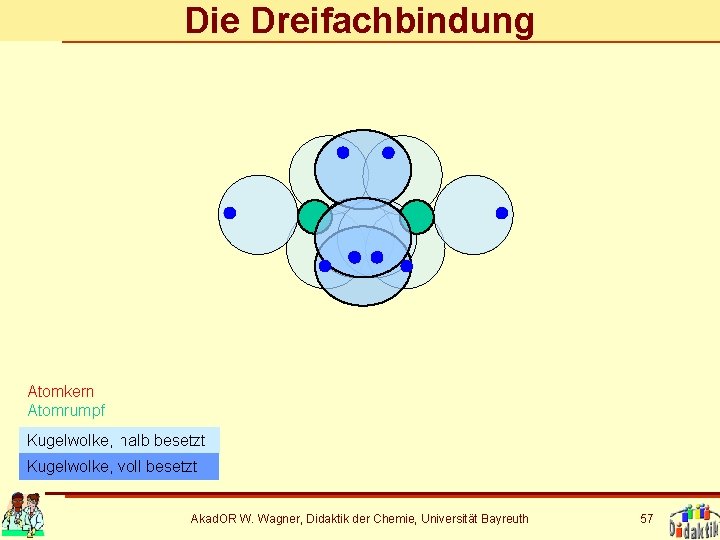
Die Dreifachbindung Atomkern Atomrumpf Kugelwolke, halb besetzt Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 57
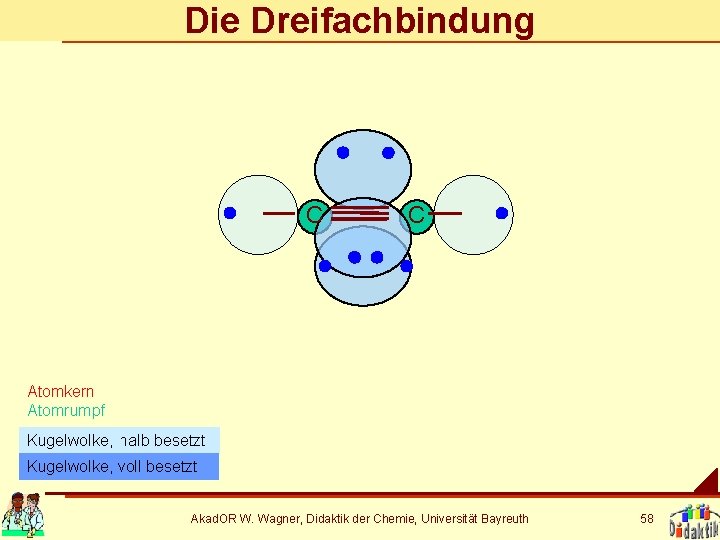
Die Dreifachbindung C C Atomkern Atomrumpf Kugelwolke, halb besetzt Kugelwolke, voll besetzt Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 58

Demonstration Ein Modell zur Polymerisation Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 59

2. 5 PSE und Bindung Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
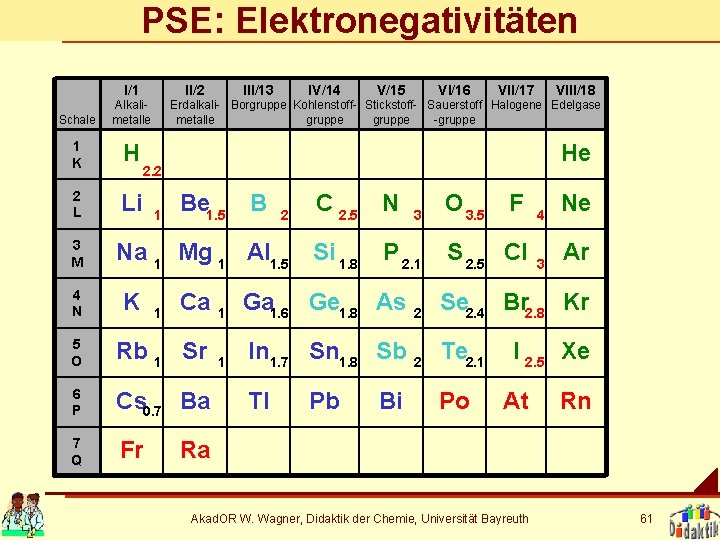
PSE: Elektronegativitäten I/1 II/2 Schale Alkalimetalle 1 K H 2 L Li 3 M 4 N III/13 IV/14 V/15 VI/16 VII/17 VIII/18 Erdalkali- Borgruppe Kohlenstoff- Stickstoff- Sauerstoff Halogene Edelgase metalle gruppe -gruppe He 2. 2 1 Be 1. 5 B 2 C 2. 5 N Na 1 Mg 1 Al 1. 5 Si 1. 8 P 2. 1 K 1 Ca 1 Ga 1. 6 Ge 1. 8 As 2 Se 2. 4 Br 2. 8 Kr 5 O Rb 1 Sr 1 In 1. 7 Sn 1. 8 Sb 2 Te 2. 1 6 P Cs 0. 7 Ba 7 Q Fr Tl Pb Bi 3 O 3. 5 F 4 S 2. 5 Cl 3 Po Ne Ar I 2. 5 Xe At Rn Ra Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 61
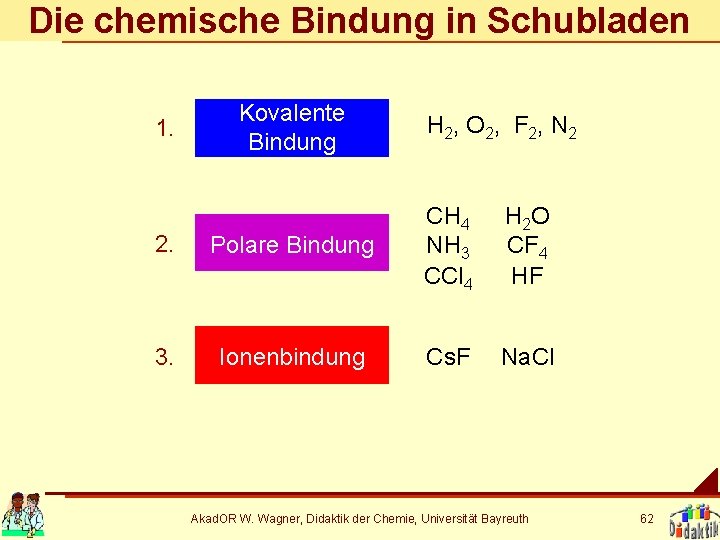
Die chemische Bindung in Schubladen 1. Kovalente Bindung H 2, O 2, F 2, N 2 2. Polare Bindung CH 4 NH 3 CCl 4 3. Ionenbindung Cs. F H 2 O CF 4 HF Na. Cl Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 62
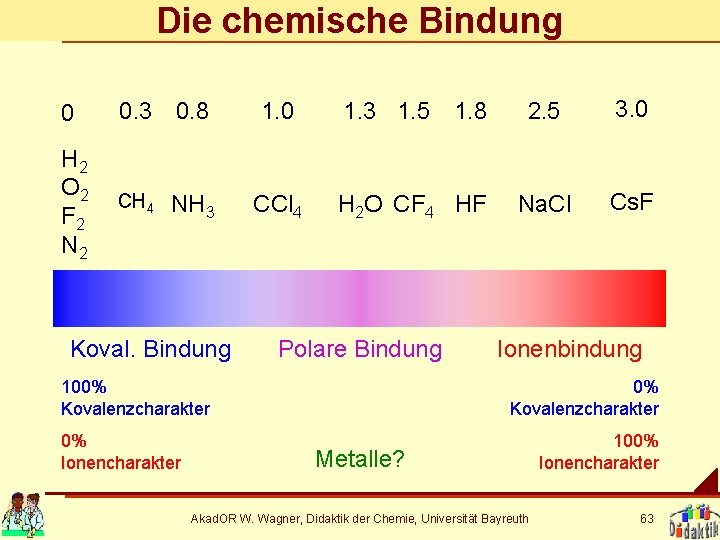
Die chemische Bindung 0 0. 3 0. 8 H 2 O 2 F 2 N 2 CH 4 NH 3 Koval. Bindung 1. 0 1. 3 1. 5 1. 8 2. 5 3. 0 CCl 4 H 2 O CF 4 HF Na. Cl Cs. F Polare Bindung 100% Kovalenzcharakter 0% Ionencharakter Ionenbindung 0% Kovalenzcharakter Metalle? Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 100% Ionencharakter 63
![Zusammenhänge zwischen Bindungstypen Cs ΔEN= 0 ΣEN~2 Mg Al Si P 4 [Na. Si] Zusammenhänge zwischen Bindungstypen Cs ΔEN= 0 ΣEN~2 Mg Al Si P 4 [Na. Si]](http://slidetodoc.com/presentation_image/11b6c1e1eede0f6b7d1ef879408ec526/image-64.jpg)
Zusammenhänge zwischen Bindungstypen Cs ΔEN= 0 ΣEN~2 Mg Al Si P 4 [Na. Si] Na 2 S S 8 ΣEN>2 ΔEN= 0 3 H 2, O 2, F 2 CH NH CCl H O CF HF Na. Cl Cs. F 4 3 4 2 4 Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 64

2. 6 Zwischenmolekulare Kräfte Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth

Van-der-Waals-Kräfte wirken zwischen unpolaren Molekülen (enthalten nur kovalente Bindungen). Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
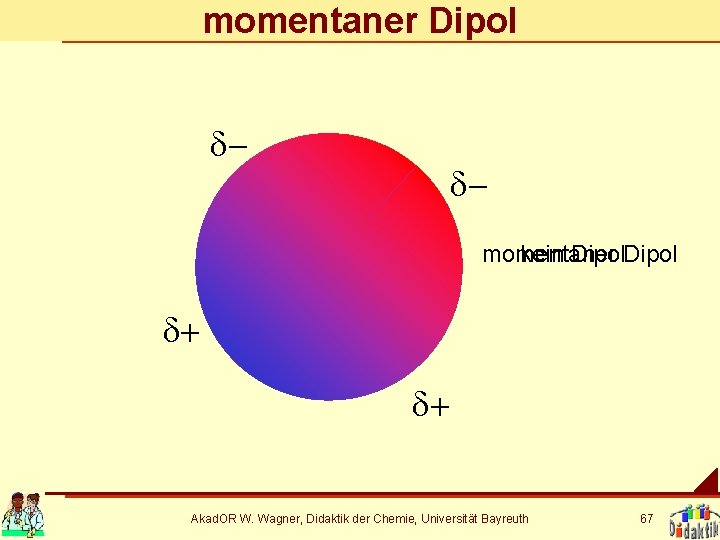
momentaner Dipol d- dmomentaner kein Dipol d+ d+ Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 67

induzierter Dipol momentaner Dipol z. B. Br 2 induzierter Dipol Br 2 Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 68

Dipolkräfte wirken zwischen Molekülen mit polaren Bindungen. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
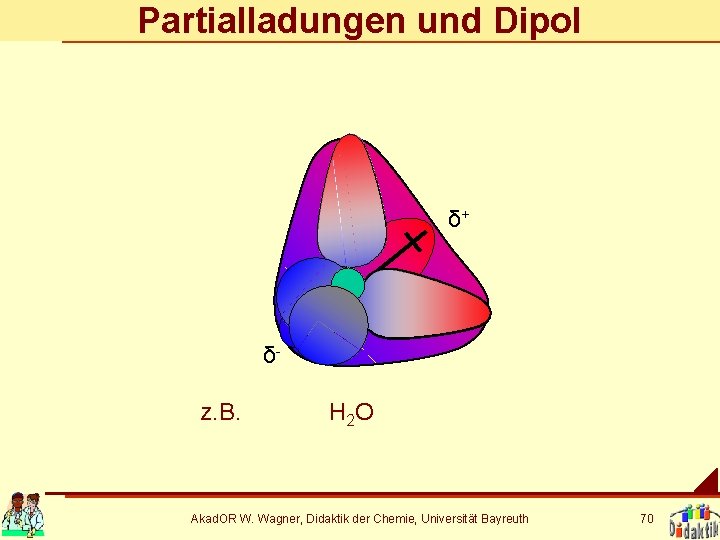
Partialladungen und Dipol δ+ δz. B. H 2 O Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 70

Elektrostatische Anziehung wirkt zwischen Ionen. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth
Elektrostatische Anziehung Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 72
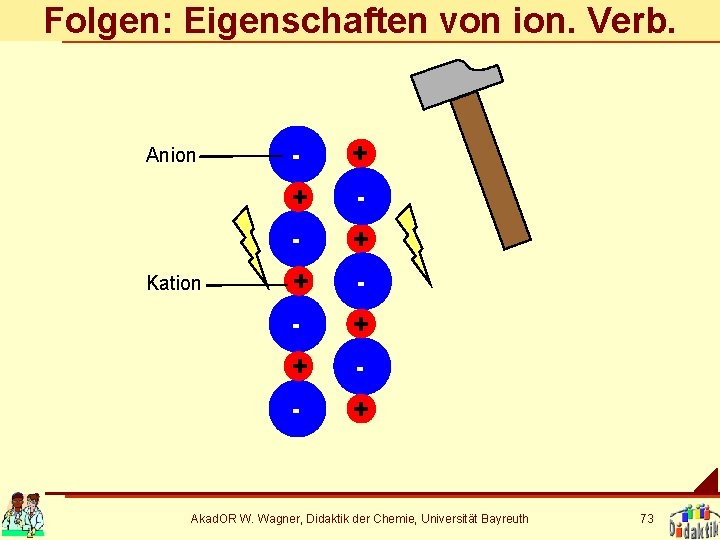
+ - - - + + - + Kation - + Anion + Folgen: Eigenschaften von ion. Verb. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 73
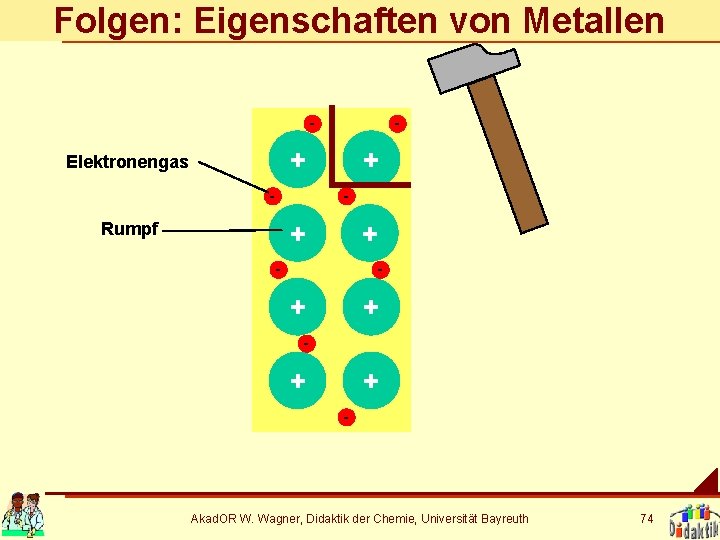
Folgen: Eigenschaften von Metallen + Elektronengas - - + Rumpf + - + - + + - - Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 74
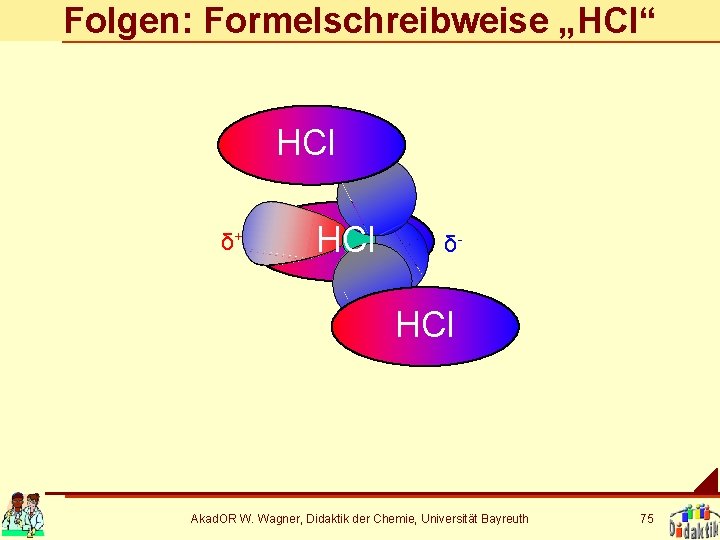
Folgen: Formelschreibweise „HCl“ HCl δ+ HCl δ- HCl Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 75

Die „Summenformel“ Die Schreibweise An. Bm bezeichnet bei kovalenten und polaren Bindungen Moleküle, weil • die Bindungen gerichtet sind und • die Zuordnung der Atome eindeutig ist. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 76
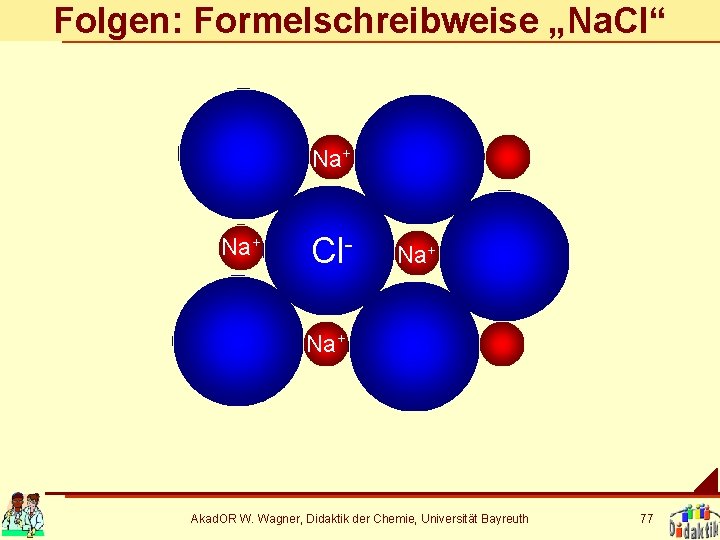
Folgen: Formelschreibweise „Na. Cl“ Na+ Cl- Na+ Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 77

Die „Summenformel“ Die Schreibweise An. Bm bezeichnet bei ionischen Bindungen das Zahlenverhältnis von Kationen zu Anionen, weil • die Bindungen nicht gerichtet sind und • die Zuordnung der Ionen zueinander nicht eindeutig ist. Diese Gleichbehandlung, wo keine Gleichheit herrscht, ist für Schüler in höchstem Maß irreführend. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 78
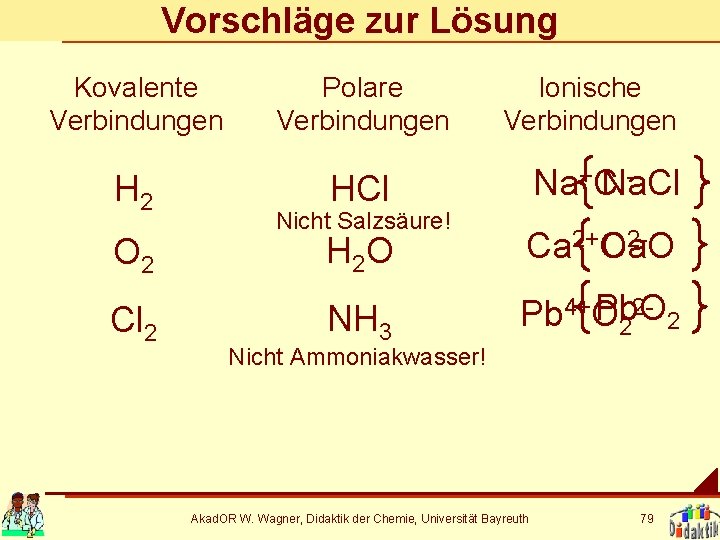
Vorschläge zur Lösung Kovalente Verbindungen H 2 O 2 Cl 2 Polare Verbindungen Ionische Verbindungen HCl Na+Cl H 2 O 2 Ca. O Ca 2+O NH 3 2 Pb. O Pb 4+O 2 2 Nicht Salzsäure! Nicht Ammoniakwasser! Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 79

Ein Modell für kovalente Bindungen Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 80

Modelle für ionische Bindungen • Na. Cl 1: käufliches Gittermodell • Na. Cl 2: Gittermodell „Wattekugeln“ • Na. Cl 3: Gittermodell „Glas“ • Magnetmodell / Overhead Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 81

Ein Selbstbau-PSE-Modell. . . und sein Einsatz im schülerzentrierten Unterricht Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 82

3. Schlussbesprechung • • Was haben Sie heute gelernt? Was ist ein Modell? Sind Modelle immer anfassbar? Wozu braucht ein Naturwissenschaftler Modelle? • Wozu braucht ein Chemiker Modelle? • Wozu brauchen wir in der Hauptschule Modelle? Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 83

Wir haben es geschafft. . . aber was sind schon 5 Folgen „Chemie für die HS“ seit dem Jahr 2000 gegenüber 1007 Folgen „Lindenstraße“ seit dem Jahr 1985 ? Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 84

Die Überlegungen der alten Griechen Kontinuums- vs. Diskontinuumssicht Experiment: LEGO-Steine und Knetmasse Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 85
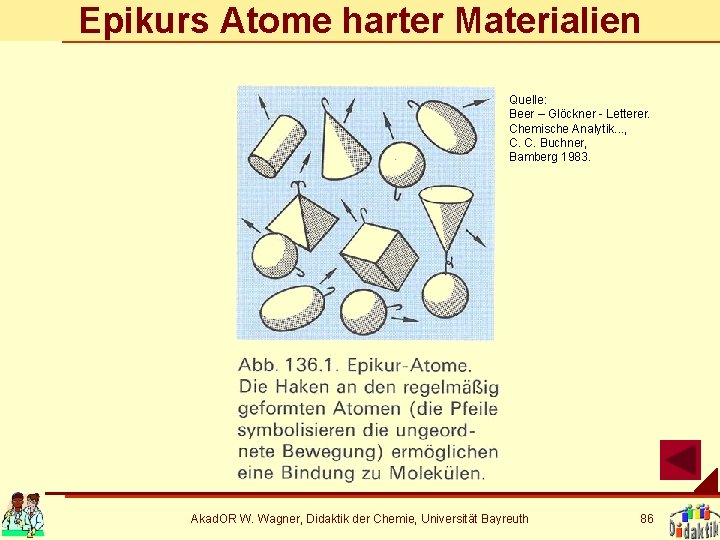
Epikurs Atome harter Materialien Quelle: Beer – Glöckner - Letterer. Chemische Analytik. . . , C. C. Buchner, Bamberg 1983. Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 86
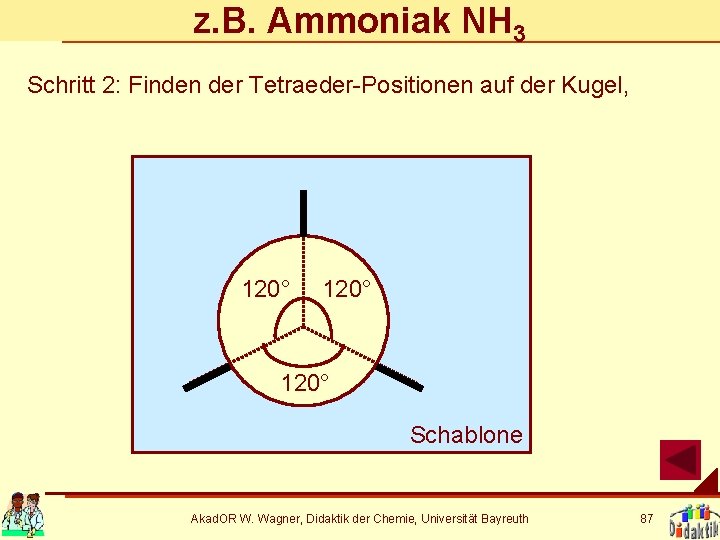
z. B. Ammoniak NH 3 Schritt 2: Finden der Tetraeder-Positionen auf der Kugel, 120° Schablone Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 87
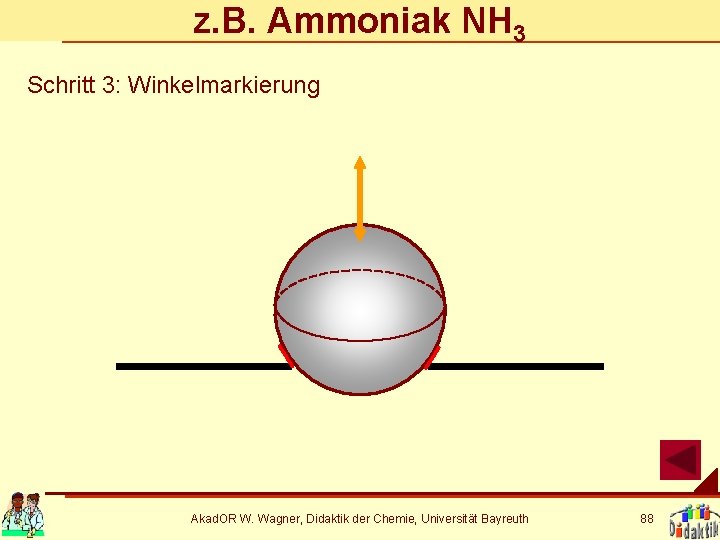
z. B. Ammoniak NH 3 Schritt 3: Winkelmarkierung Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 88
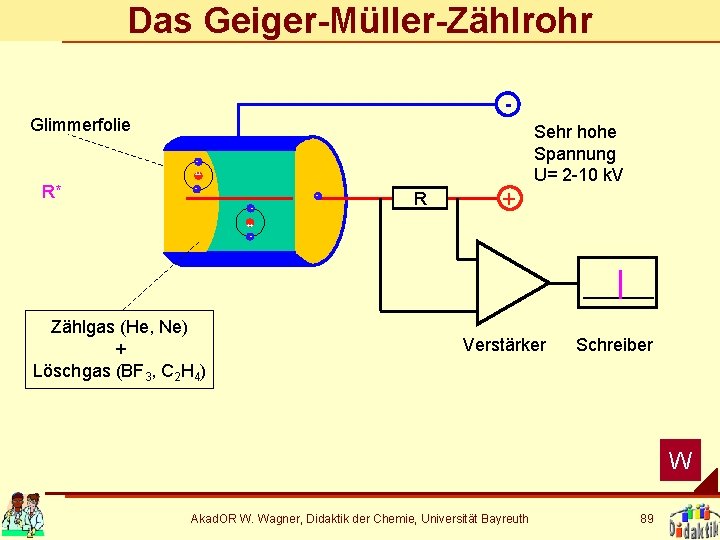
Das Geiger-Müller-Zählrohr Glimmerfolie ++ R* - - R + Sehr hohe Spannung U= 2 -10 k. V ++ - Zählgas (He, Ne) + Löschgas (BF 3, C 2 H 4) Verstärker Schreiber W Akad. OR W. Wagner, Didaktik der Chemie, Universität Bayreuth 89
- Slides: 89