Experimentalvortrag AC Silicium und seine Verbindungen SS 2009

Experimentalvortrag AC „Silicium und seine Verbindungen“ SS 2009 Meike Griesel

Gliederung 1. Einleitung 2. Silicium : Herstellung und Eigenschaften 3. Silane D 1, V 1 4. Kieselsäure und Silicate V 3, D 2, V 4 5. Silicone V 5 V 2 6. Schulrelevanz 7. Literatur 2

1. Einleitung 3
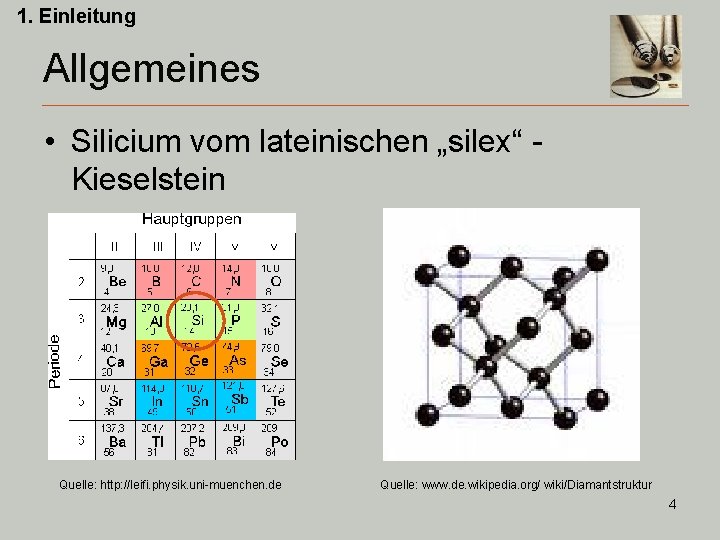
1. Einleitung Allgemeines • Silicium vom lateinischen „silex“ Kieselstein Quelle: http: //leifi. physik. uni-muenchen. de Quelle: www. de. wikipedia. org/ wiki/Diamantstruktur 4

1. Einleitung Allgemeines (2) • Träger des „anorganischen Lebens“ – 2. häufigstes Element der Erdkruste (Massenanteil ca. 26%) • Pflanzenreich: Si. O 2 Kristalle an Halmen und Gräsern • Tierreich – Schalen und Skelette von Aufgusstierchen » Kieselgur – essentielles Spurenelement für Wachstum und Knochenbau bei höheren Tieren 5

1. Einleitung Geschichte • vor 6000 Jahren: Glasherstellung in Syrien und Phönezien • Edelsteine als Schmuck und als Heilmittel – Topas: vergiftete Speisen erkennen, Sehkraft verbessern • 1823: J. J. Berzelius stellt erstmals amorphes Silicium dar 6

1. Einleitung Gegenwart • Si. O 2 als Trockenmittel in Tablettenröhrchen • Silicone (z. B. Schmiermittel, Beschichtungen) • Medizin – Kieselsäure • Reinsilicium ist „Grundwerkstoff“ des 21. Jahrhunderts – Energieversorgung – Information- und Unterhaltungstechnologie 7

2. Silicium: Herstellung und Eigenschaften 8

2. Silicium: Herstellung und Eigenschaften Demo 1: Labordarstellungen von amorphem und kristallinem Silicium 9

2. Silicium: Herstellung und Eigenschaften Auswertung: Demo 1 Darstellung von braunem, amorphem Silicium: + IV 0 0 +II Nebenreaktion: 0 0 +II -IV Mg. O + Mg 2 Si werden mit HCl (aq) umgesetzt: 10

2. Silicium: Herstellung und Eigenschaften Auswertung: Demo 1 (2) Darstellung von silbernem, kristallinem Silicium: +IV 0 0 + III Umsetzung von Al + Al 2 O 3 mit HCl (aq) : Hexaqua-aluminium-(III)-chlorid 11

2. Silicium: Herstellung und Eigenschaften Technische Darstellung • Lichtbogenreduktionsofen, 2000°C +IV 0 0 +II • 98% reines Silicium – Siliconherstellung – Legierungen von Leichtmetallen • Halbleitertechnik: 99, 9999999% reines Silicium 12

2. Silicium: Herstellung und Eigenschaften Technische Darstellung (2) • Wirbelschichtreaktor 0 +I +II 0 • Destillation: Trichlorsilan siedet bei 31, 8°C • Abscheidung des Si durch H 2 -Verdampfung • Tiegelziehverfahren / Zonenschmelzverfahren 13

2. Silicium: Herstellung und Eigenschaften Chemische Eigenschaften • Verhalten wie Nichtmetall • in seinen Verbindungen meist vierwertig • Zweiwertige bzw. dreiwertige Verbindungen (Si. O, Si. F 2) nur bei hohen Temperaturen stabil • in allen Säuren außer salpetersäurehaltiger HF praktisch unlöslich – Si. O 2 als Schutzschicht 14

2. Silicium: Herstellung und Eigenschaften Versuch 1: Halbleitereigenschaften des Siliciums 15
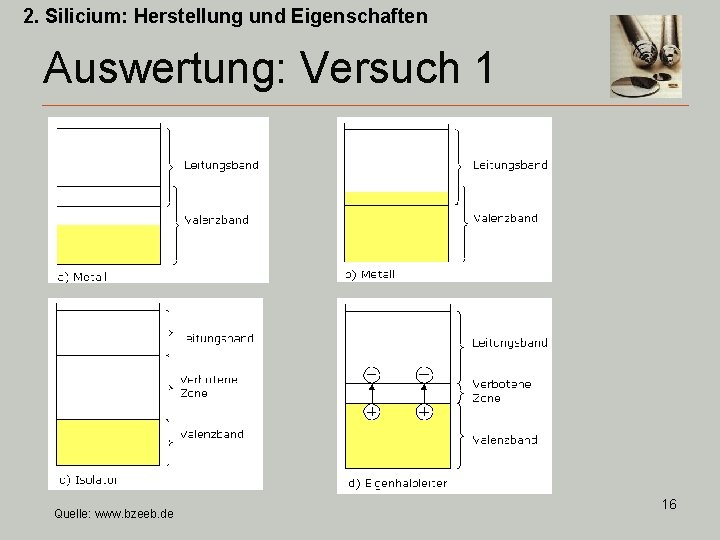
2. Silicium: Herstellung und Eigenschaften Auswertung: Versuch 1 Quelle: www. bzeeb. de 16
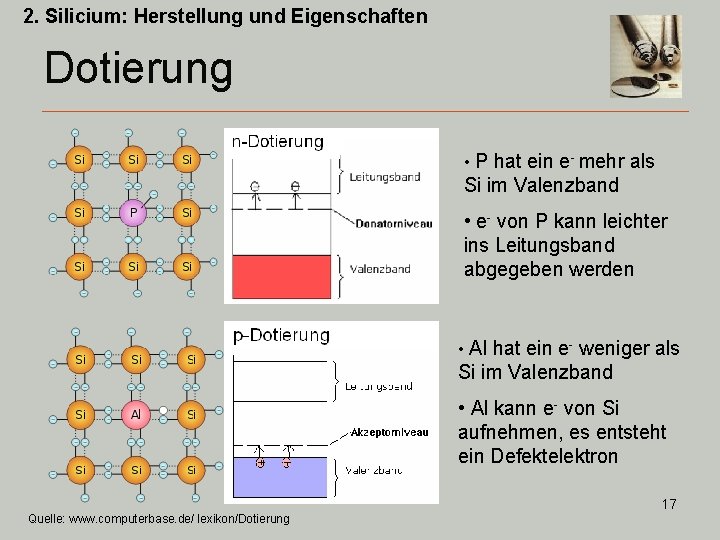
2. Silicium: Herstellung und Eigenschaften Dotierung • P hat ein e- mehr als Si im Valenzband • e- von P kann leichter ins Leitungsband abgegeben werden • Al hat ein e- weniger als Si im Valenzband • Al kann e- von Si aufnehmen, es entsteht ein Defektelektron 17 Quelle: www. computerbase. de/ lexikon/Dotierung

3. Silane 18

3. Silane Versuch 2: Herstellung von Monosilan 19

3. Silane Auswertung: Versuch 2 Darstellung von Monosilan: -IV +I +IV -I Monosilan reagiert mit Luftsauerstoff: -I 0 -II +I -II • es entsteht bei der Reaktion nicht nur Monosilan (Disilan, Trisilan) 20
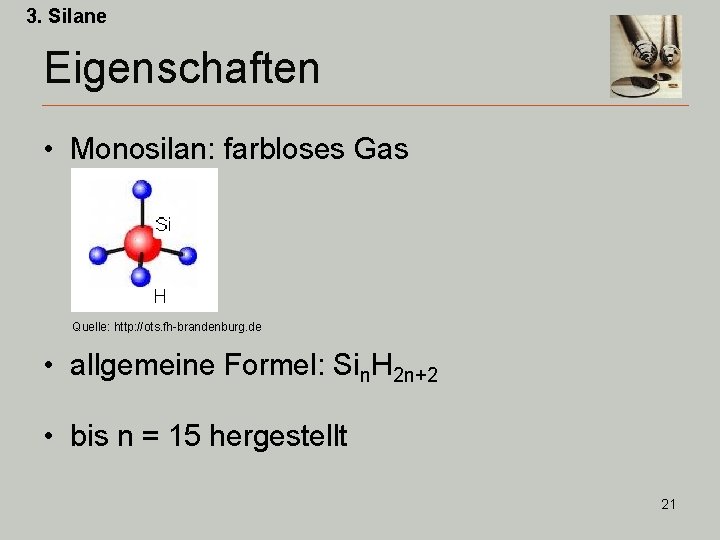
3. Silane Eigenschaften • Monosilan: farbloses Gas Quelle: http: //ots. fh-brandenburg. de • allgemeine Formel: Sin. H 2 n+2 • bis n = 15 hergestellt 21

3. Silane Technische Nutzung • in der Dünnschichtelektronik – Thermolyse: – Abscheidung von amorphem Silicium – dünne Schichten: bis 10 μm – genutzt wird dies für Photosensoren (z. B. Digitalkamera) 22

4. Kieselsäure und Silicate 23

4. Kieselsäure und Silicate Kieselsäure • Orthokieselsäure: H 4 Si. O 4 – Bildung: – nur in großer Verdünnung beständig (> 10 -3 mol/l) • bei höherer Konzentration: Polymerisation 24

4. Kieselsäure und Silicate Versuch 3: Ausfällen von Metakieselsäure aus Wasserglas 25
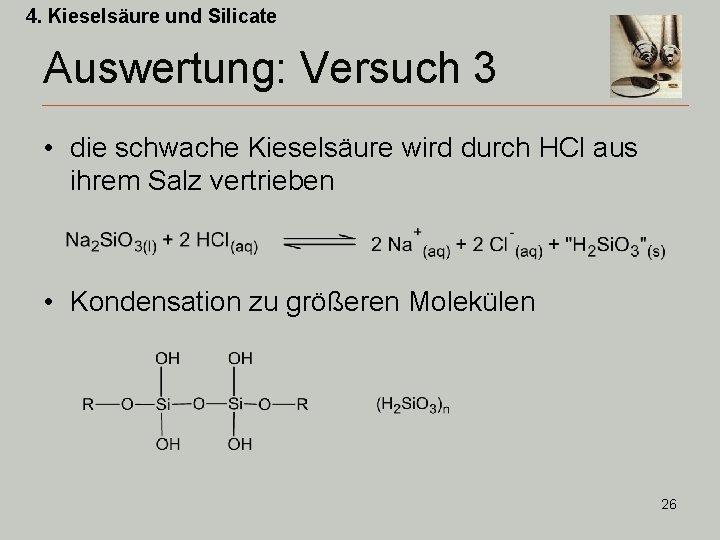
4. Kieselsäure und Silicate Auswertung: Versuch 3 • die schwache Kieselsäure wird durch HCl aus ihrem Salz vertrieben • Kondensation zu größeren Molekülen 26

4. Kieselsäure und Silicate Polykieselsäuren • das Endprodukt der Kondensation ist formal Si. O 2 • eine hochkondensierte, wasserreiche Polykieselsäure – Kieselgel – entwässertes Kieselgel (Silicagel) hat große spezifische Oberfläche – Absorption von Gasen und Dämpfen (Trockenmittel) 27

4. Kieselsäure und Silicate • Labordarstellung – Zusammenschmelzen von Quarz und Hydroxiden oder Carbonaten der Alkalimetalle • Silicate sind Salze der Kieselsäure • Si hat KZ = 4 – Tetraeder, eckenverknüpft 28

4. Kieselsäure und Silicate Demo 2: Der chemische Garten 29

4. Kieselsäure und Silicate Auswertung: Demo 2 • Schwermetallsalze bilden mit Silicat aus Wasserglas eine Haut aus Kupfersilicat, Cobaltsilicat etc. • die Haut ist semipermeabel – H 2 O diffundiert Richtung Kristall (Konzentrationsunterschied) – osmotischer Druck steigt • die Haut platzt und Salzlösung tritt aus, welche erneut eine Metallsilicatschicht bildet 30
![4. Kieselsäure und Silicate Silicatstrukturen Name: Inselsilicate Struktur: Beispiele: Zirkon Zr[Si. O 4] Gruppensilicate 4. Kieselsäure und Silicate Silicatstrukturen Name: Inselsilicate Struktur: Beispiele: Zirkon Zr[Si. O 4] Gruppensilicate](http://slidetodoc.com/presentation_image_h2/59aa942658bf9565bd343868530d32a8/image-31.jpg)
4. Kieselsäure und Silicate Silicatstrukturen Name: Inselsilicate Struktur: Beispiele: Zirkon Zr[Si. O 4] Gruppensilicate Ringsilicate Beryll Al 2 Be 3[Si 6 O 18] Kettensilicate Entsatit Mg 2[Si 2 O 6] Schichtsilicate Talk Mg 3[Si 4 O 10](OH)2 Gerüstsilicate Feldspat: Albit Na[Al. Si 3 O 8] 31

4. Kieselsäure und Silicate Zeolithe • kristalline, hydratisierte Aluminosilicate • enthalten Alkali- bzw. Erdalkalimetallkationen • in den Hohlräumen befinden sich Wasser und Kationen Quelle: www. chemieunterricht. de • Zeolith A „Sasil“: 32

4. Kieselsäure und Silicate Versuch 4: Die Ionenaustauschwirkung von Zeolithen 33
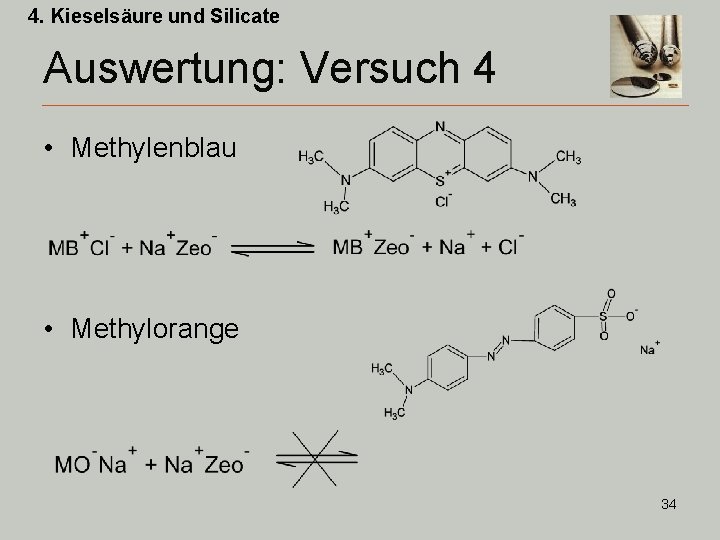
4. Kieselsäure und Silicate Auswertung: Versuch 4 • Methylenblau • Methylorange 34

5. Silcone 35

5. Silicone Herstellung / Eigenschaften • Kondensation von Silanolen (R 3 Si. OH), Silandiole (R 2 Si(OH)2) und Silantriole (RSi(OH)3) – Silanole etc. : Hydrolyse der entsprechenden Halogenverbindungen • Silcone sind thermisch stabil, oxidationsbeständig und inert gegenüber Wettereinflüssen 36

5. Silicone Versuch 5: Simethicon wirkt Schaumbildung entgegen 37

5. Silicone Auswertung: Versuch 5 • Dimethicon + Si. O 2 = Simethicon • wasserlösliches Silicon • erhöht Oberflächenspannung von Wasser / Seifenlauge – Schaumblasen zerplatzen – neuer Schaumbildung wird entgegen gewirkt 38

6. Schulrelevanz 39

6. Schulrelevanz Chemikalien Versuch: Chemikalien: Einstufung: 1 Siliciumscheibe S 1 2 Magnesiumsilicid Salzsäure c = 2 mol/L LV 3 Wasserglas S 1 Salzsäure c = 2 mol/L Zeolith A S 1 Methylorange, Methylenblau Simethicon S 1 4 5 40

6. Schulrelevanz Themen Thema Schulstufe elektrische Leitfähigkeit (fakultativ) Klasse 7 Umkehrung der Oxidbildung (Metallgewinnung aus Erzen) Metalle als Werkstoffe (fakulativ): Werkstoffe in der Technink, Energiefragen Synthetische Makromoleküle (fakultativ: Siloxane) Klasse 7 Klasse 10 Klasse 11 41

7. Literatur 42

Literatur • Häusler, Karl. et al. Experimente für den Chemieunterricht. 2. Aufl. . München: Oldenburg Schulbuchverlag, 1995. • Hollemann, A. F. ; Wiberg, E. Lehrbuch der anorganischen Chemie. Berlin: Walter de Gruyter, 1985. • Riedel, Dr. Erwin. Anorganische Chemie. 6. Auf. . Berlin: Walter de Gruyter, 2004. • Obendrauf, V. „CVD – Chemical Vapour Deposition“ Praxis der Naturwissenschaften. 1/54, 2005. • Bukatsch, Prof. Dr. F. et al. Experimentelle Schulchemie: Anorganische Chemie Nichtmetalle. Bd 2. Köln: Aulis Verlag Deubner & Co KG, 1969 • http: //www. axel-schunk. net/experiment/edm 0309. html im Juni 2009 • http: //www. kultusministerium. hessen. de/irj/HKM_Internet? uid=3 b 430 19 a-8 cc 6 -1811 -f 3 ef-ef 91921321 b 2 im Juli 2008 • Schmidkunz, Dorit. „Silicium Bedeutend für Mensch und Medizin“ Naturwissenschaften im Unterricht – Chemie. 10, 1991. 43
- Slides: 43