Experiment Nr 4 Extraktion von Menthol Allgemein Menthol




























- Slides: 52

Experiment Nr. 4 Extraktion von Menthol

Allgemein Menthol ist ein Stoff, den die Pfefferminzpflanze produziert. Allerdings nur zu 0. 2 %.

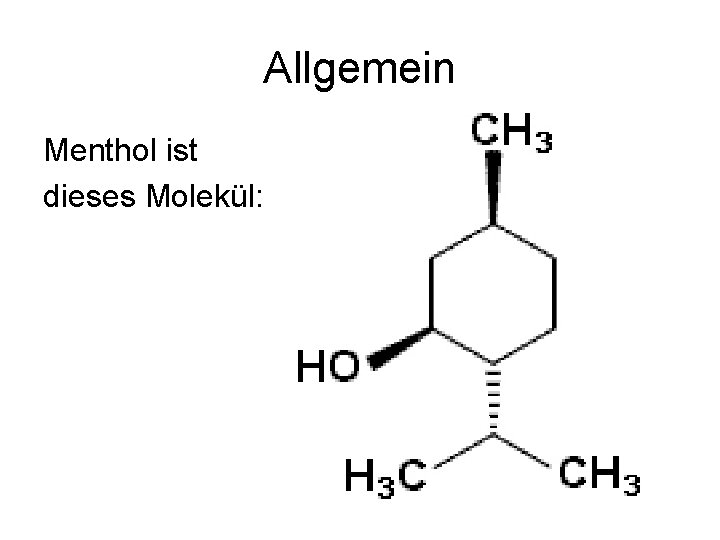
Allgemein Menthol ist dieses Molekül:

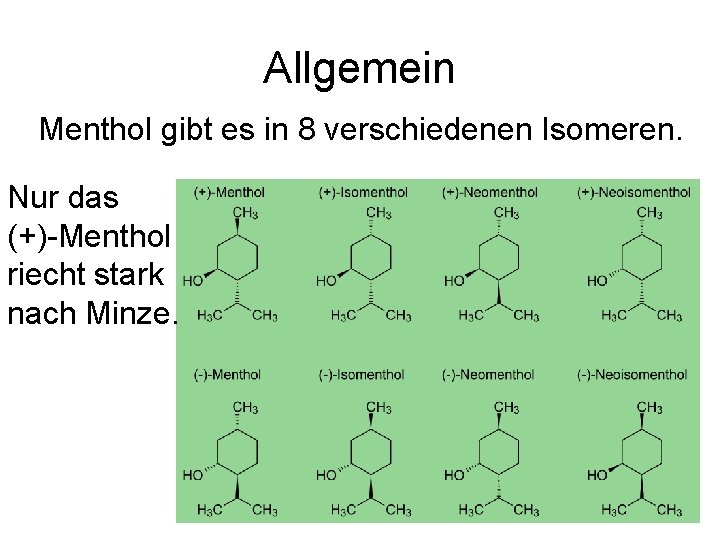
Allgemein Menthol gibt es in 8 verschiedenen Isomeren. Nur das (+) Menthol riecht stark nach Minze.

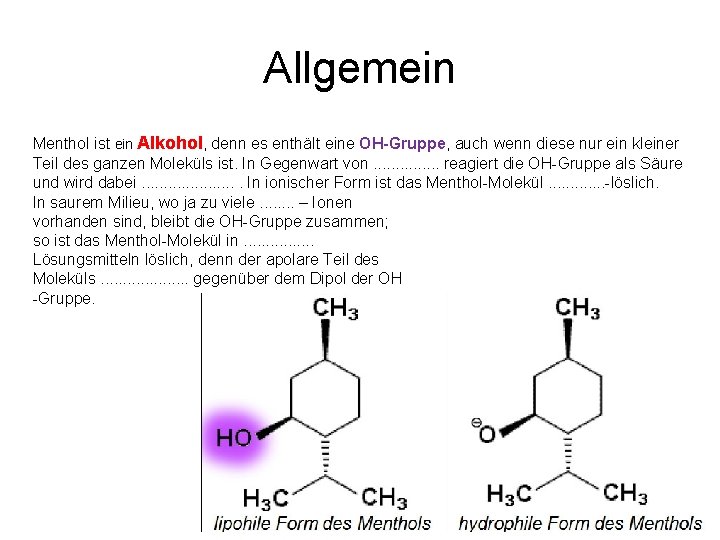
Allgemein Menthol ist ein. . . . , denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von. . . . reagiert die OH Gruppe als Säure und wird dabei. . . . . In ionischer Form ist das Menthol Molekül. . . löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

Allgemein Menthol ist ein. . . . , denn es enthält eine OH-Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von. . . . reagiert die OH Gruppe als Säure und wird dabei. . . . . In ionischer Form ist das Menthol Molekül. . . löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

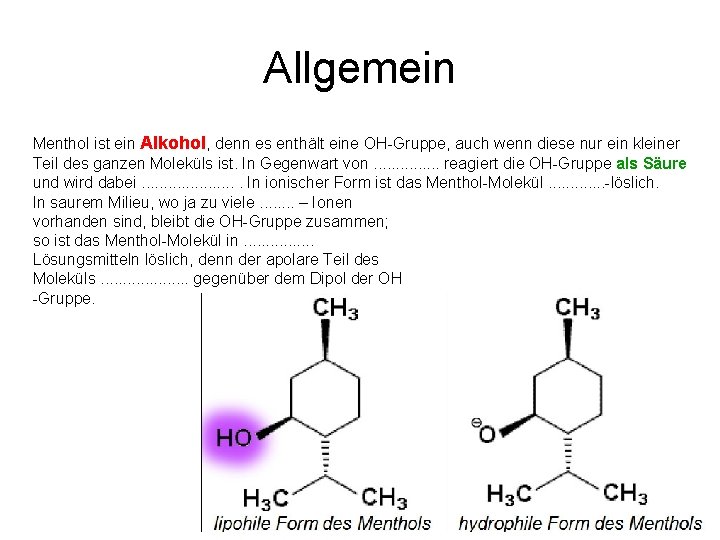
Allgemein Menthol ist ein Alkohol, denn es enthält eine OH-Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von. . . . reagiert die OH Gruppe als Säure und wird dabei. . . . . In ionischer Form ist das Menthol Molekül. . . löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von. . . . reagiert die OH Gruppe als Säure und wird dabei. . . . . In ionischer Form ist das Menthol Molekül. . . löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

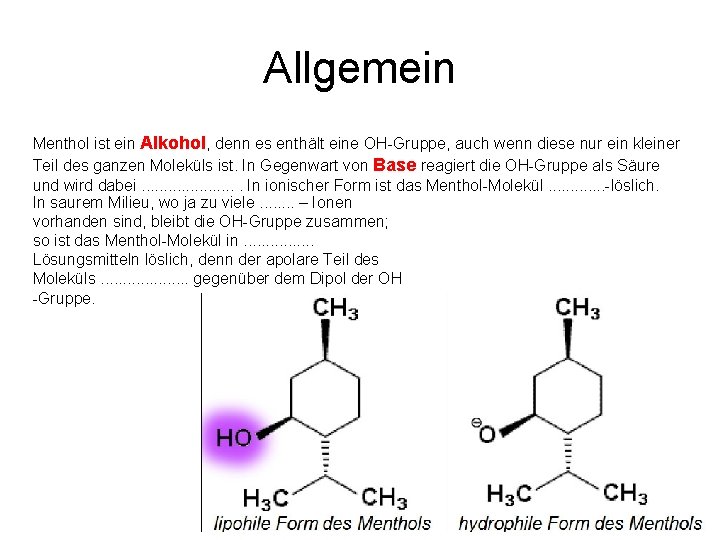
Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH Gruppe als Säure und wird dabei. . . . . In ionischer Form ist das Menthol Molekül. . . löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

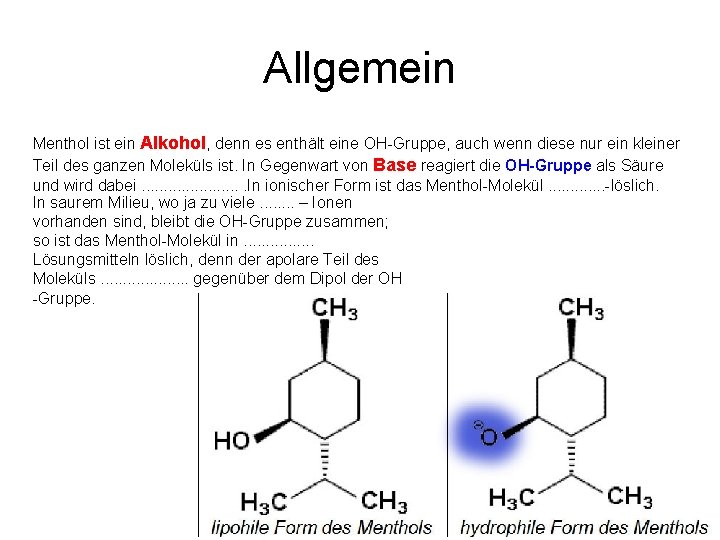
Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH-Gruppe als Säure und wird dabei. . . In ionischer Form ist das Menthol Molekül. . . löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

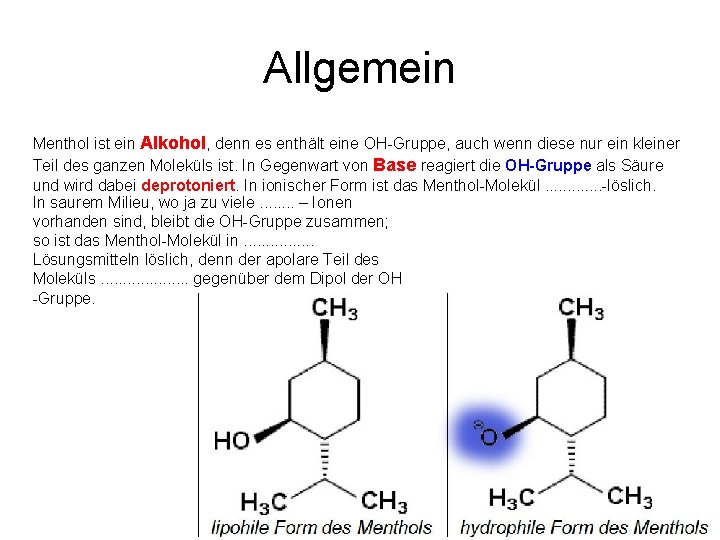
Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH-Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül. . . löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

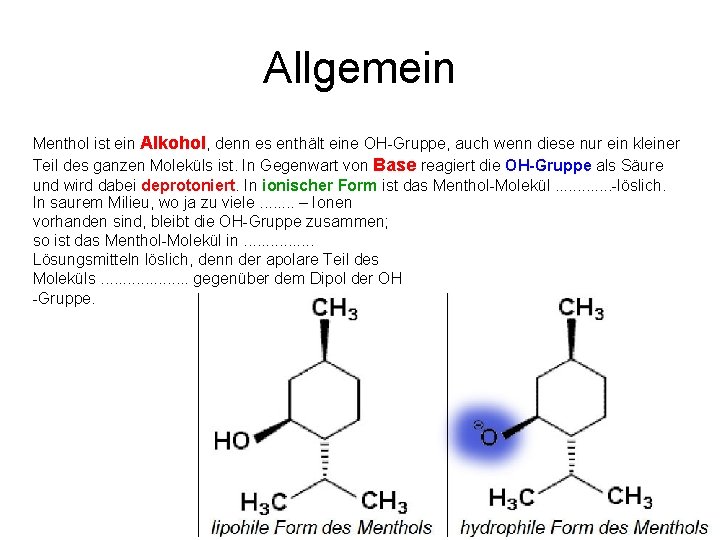
Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH-Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül. . . löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

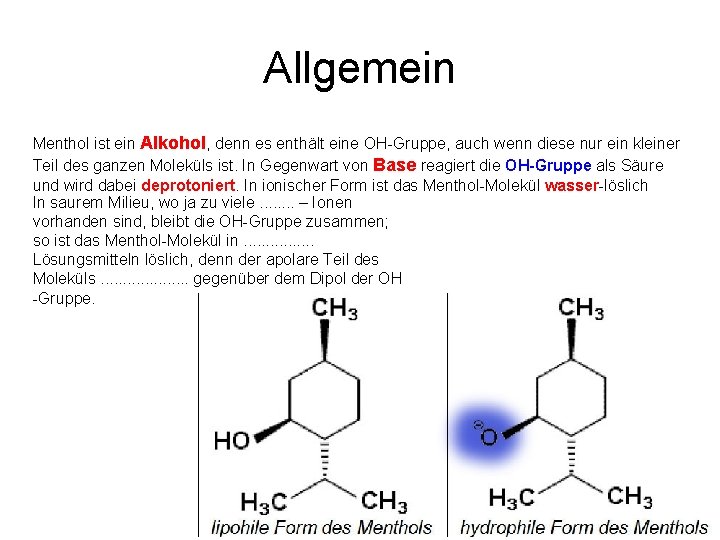
Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH-Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül wasser löslich In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

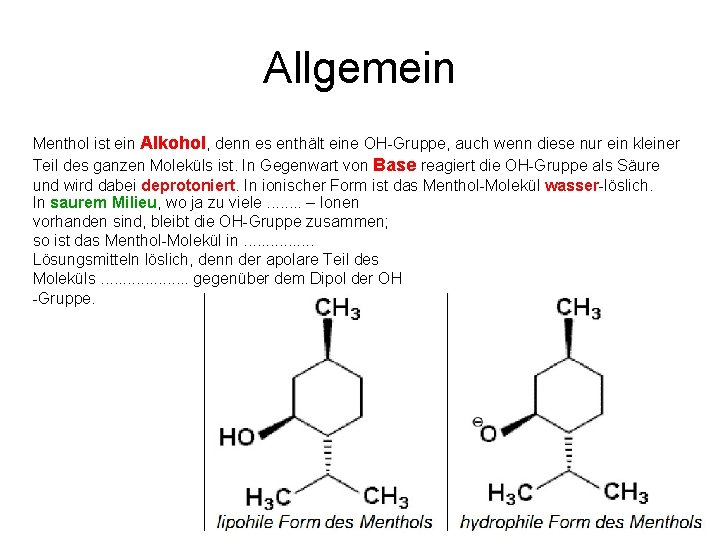
Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül wasser löslich. In saurem Milieu, wo ja zu viele. . . . – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül wasser löslich. In saurem Milieu, wo ja zu viele H+ – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül wasser löslich. In saurem Milieu, wo ja zu viele H+ – Ionen vorhanden sind, bleibt die OH-Gruppe zusammen; so ist das Menthol Molekül in. . . . Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül wasser löslich. In saurem Milieu, wo ja zu viele H+ – Ionen vorhanden sind, bleibt die OH-Gruppe zusammen; so ist das Menthol Molekül in apolaren Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül wasser löslich. In saurem Milieu, wo ja zu viele H+ – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in apolaren Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH Gruppe.

Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül wasser löslich. In saurem Milieu, wo ja zu viele H+ – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in apolaren Lösungsmitteln löslich, denn der apolare Teil des Moleküls. . . . . gegenüber dem Dipol der OH-Gruppe.

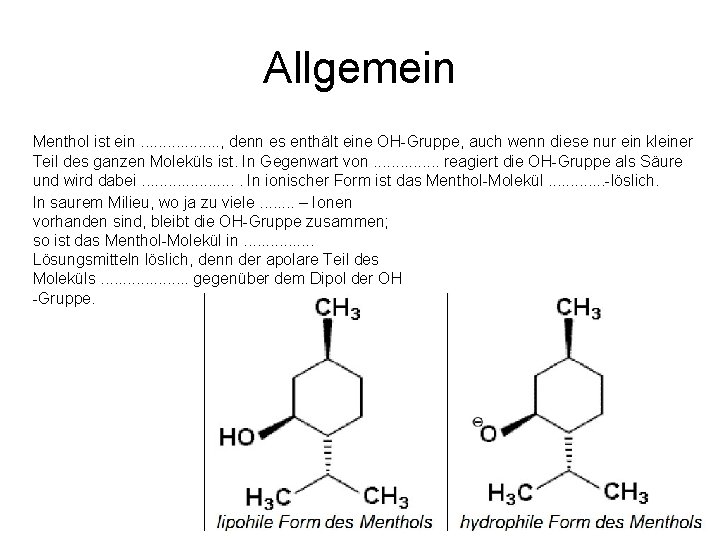
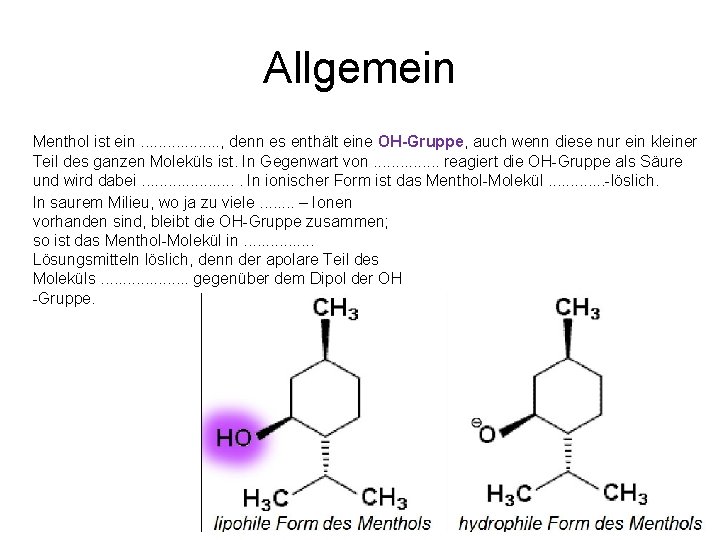
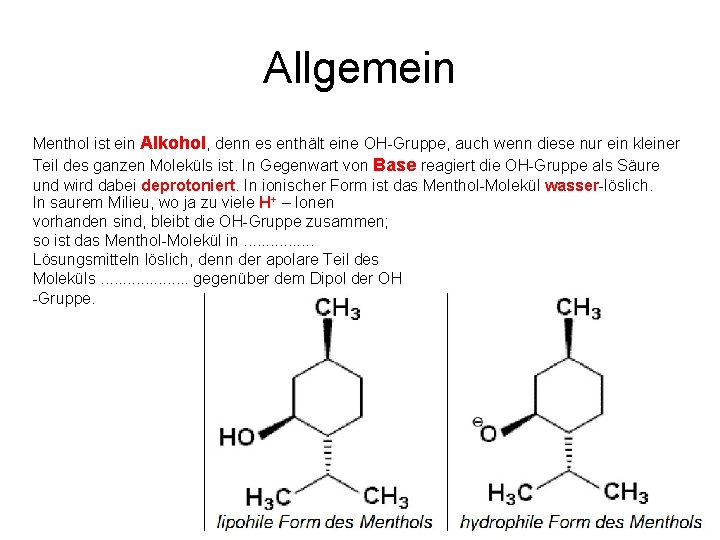
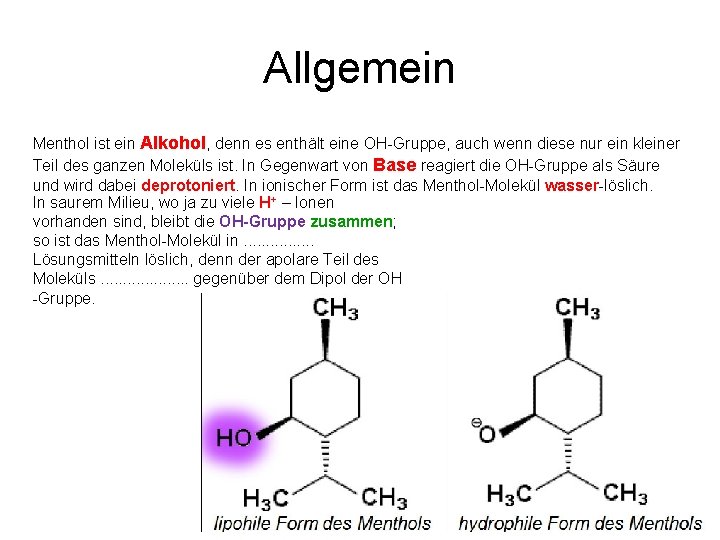
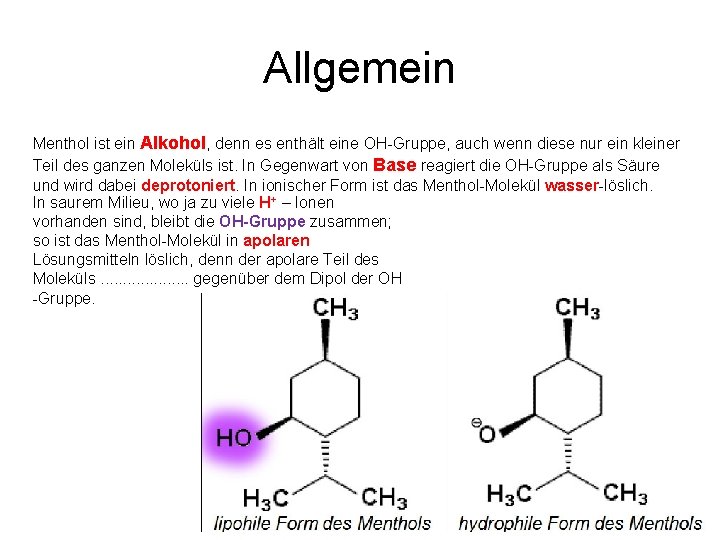
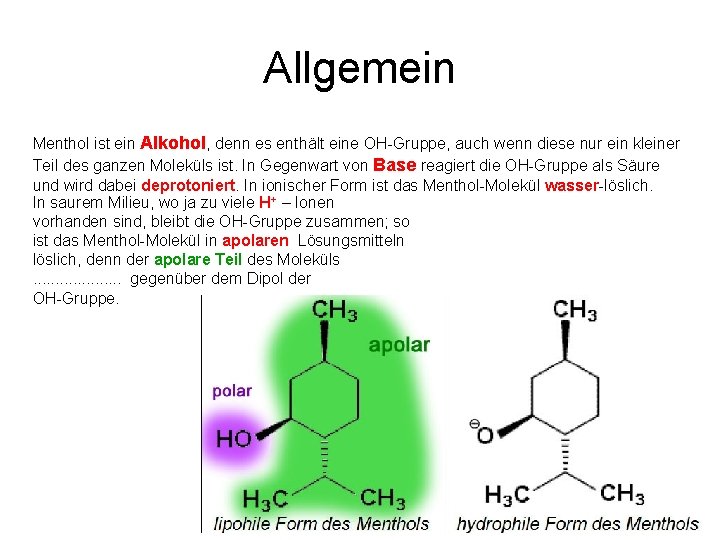
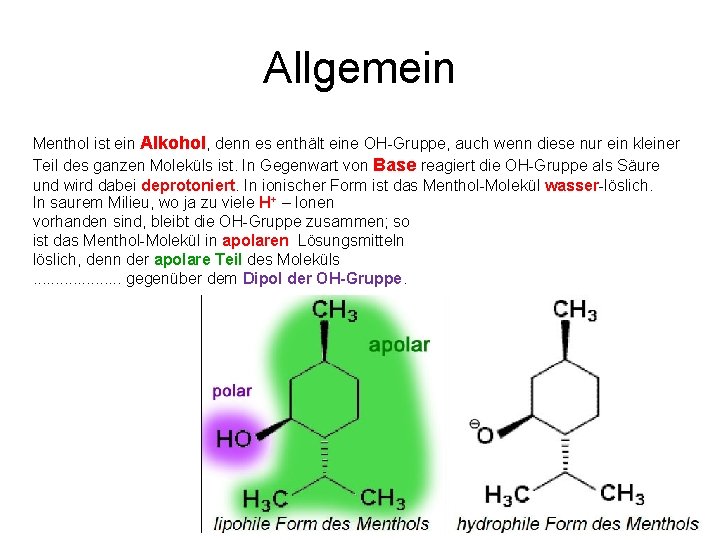
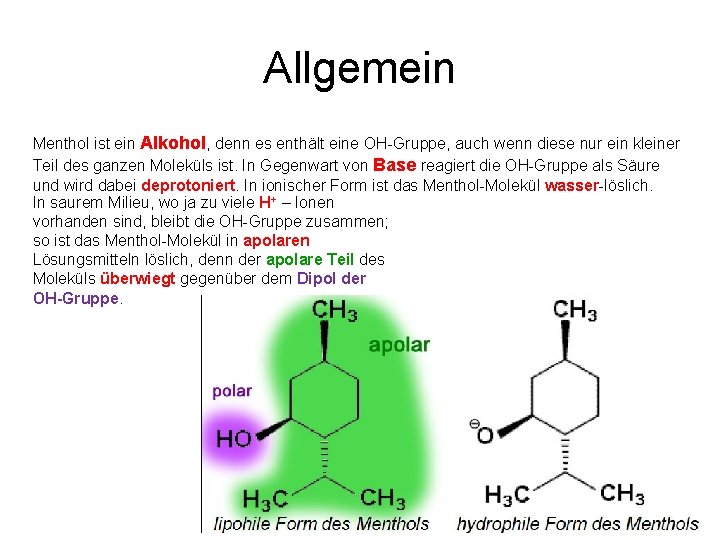
Allgemein Menthol ist ein Alkohol, denn es enthält eine OH Gruppe, auch wenn diese nur ein kleiner Teil des ganzen Moleküls ist. In Gegenwart von Base reagiert die OH Gruppe als Säure und wird dabei deprotoniert. In ionischer Form ist das Menthol Molekül wasser löslich. In saurem Milieu, wo ja zu viele H+ – Ionen vorhanden sind, bleibt die OH Gruppe zusammen; so ist das Menthol Molekül in apolaren Lösungsmitteln löslich, denn der apolare Teil des Moleküls überwiegt gegenüber dem Dipol der OH-Gruppe.

Durchführung • Verdünnte Natronlauge (ca. 5 ml) mit Wasser (ca. 40 ml) verdünnen. • 1 Teebeutel für ca. 5 min einlegen. • Teebeutel (ätzend) rausnehmen, in den Abfall.

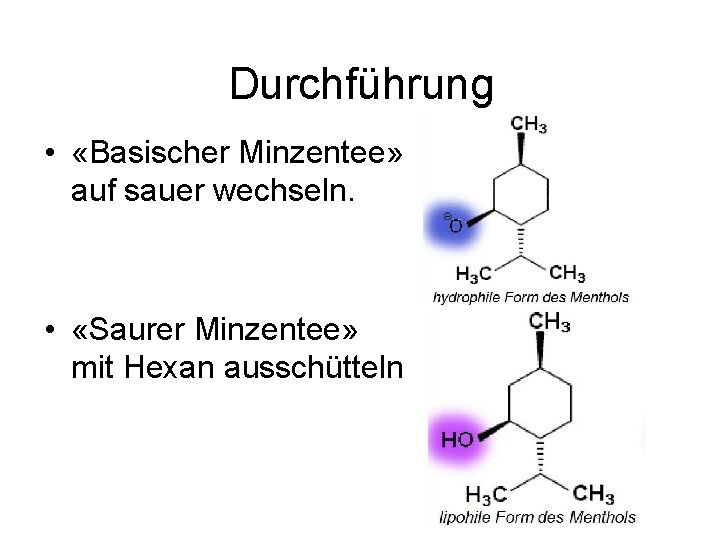
Durchführung • «Basischer Minzentee» auf sauer wechseln. • «Saurer Minzentee» mit Hexan ausschütteln

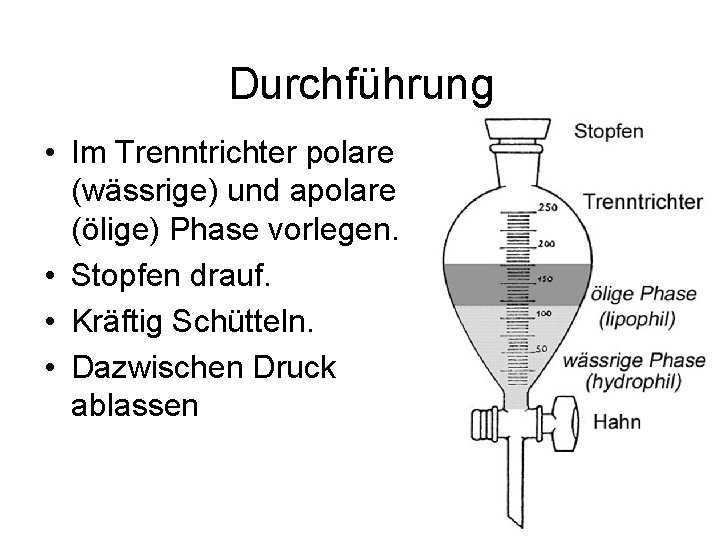
Durchführung • Im Trenntrichter polare (wässrige) und apolare (ölige) Phase vorlegen. • Stopfen drauf. • Kräftig Schütteln. • Dazwischen Druck ablassen

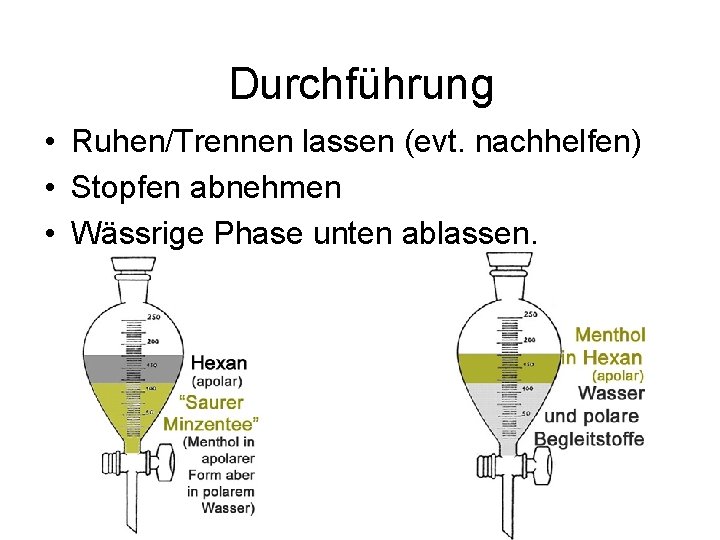
Durchführung • Ruhen/Trennen lassen (evt. nachhelfen) • Stopfen abnehmen • Wässrige Phase unten ablassen.

Durchführung • Hexan Menthol Lösung in ein breites Gefäss • mit Wärme (Wasserbad) Verdunstung beschleunigen.

Zur Durchführung Wasserbad

Zur Durchführung Bechergläser im Wasserbad befestigen (mit Draht oder Stativ)

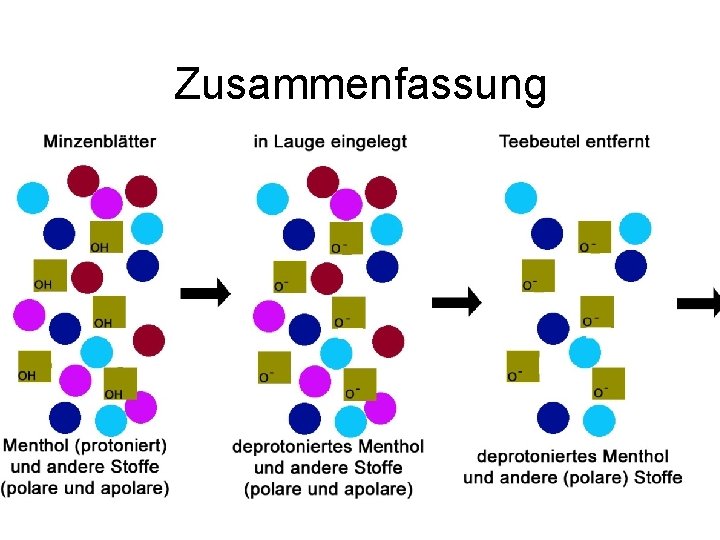
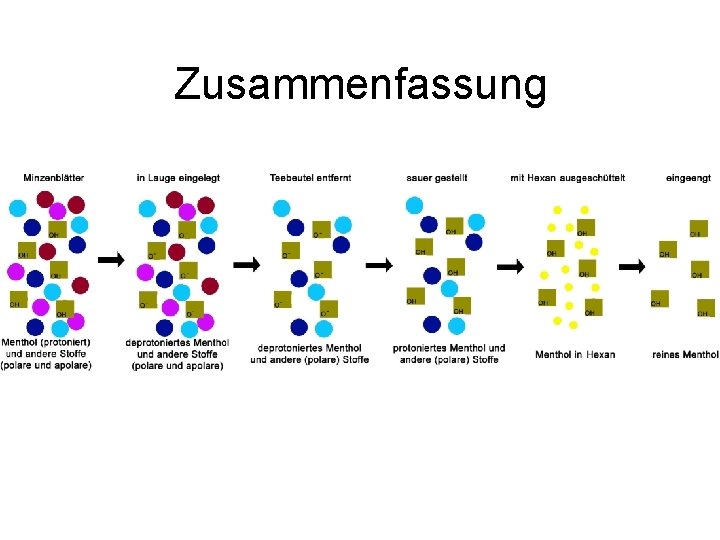
Zusammenfassung

Zusammenfassung

Entsorgung • Wässrige Lösungen in den Abfluss • Teebeutel in den Abfall

Sicherheitshinweise • Natronlauge: ätzend • Salzsäure: ätzend, reizend • Hexan: leichtentzündlich, gesundheits schädlich, reizend, umweltgefährlich. Schutzbrille tragen

Jetzt: Durchführung des Experiments Salzsäure: ätzend, reizend Später: Details zur Protokoll Führung (Sie kommen hierher zurück) Machen Sie Notizen vom Experiment.

Protokolle im Chemie Praktikum

Protokolle: Aufbau Ein wissenschaftliches Protokoll hat einen streng vorgegeben Aufbau. • • • Titel und einleitende Informationen Material Durchführung Resultate und Beobachtungen Interpretationen

Protokolle: Aufbau Ein wissenschaftliches Protokoll hat einen streng vorgegeben Aufbau. • Titel und einleitende Informationen: - Nummer und Titel - Datum der Durchführung - Ausführende - Hintergrund Informationen

Protokolle: Aufbau • Material - Geräte - Stoffe - Gefährliche Stoffe mit Gefahrensymbolen - Sicherheitshinweise • Durchführung: - Darf eine Zusammenfassung sein. - muss dem Verlauf Ihres Versuchs entsprechen (in der Vorlage anpassen). - Skizze willkommen.

Protokolle: Aufbau • Resultate und Beobachtungen: – Die Beobachtungen sind der wichtigste Teil des Protokolls; er muss umfassend sein. – Die Beobachtungen müssen vielseitig, verständlich und überzeugend formuliert und auf Ihren Versuch bezogen sein. – Alles beschreiben, was Ihnen auffällt, was besonders ist.

Protokolle: Aufbau • Resultate und Beobachtungen: – Veränderung an den Stoffen selbst (Farbe, Transparenz, Aggregatszustand, …) – Erscheinungen (Temperatur, Rauch, Geruch…) – Überraschungen, Pannen, Massnahmen… – Resultate (mit eindeutiger Kennzeichnung und Einheit) – Noch keine Interpretationen in diesem Teil

Protokolle: Aufbau • Interpretationen – Erklärungen der Beobachtungen – Schlussfolgerungen aus den Resultaten – Was Sie dazu denken • Beantwortung der Fragen – Integriert in den oberen Teilen – Die Fragen sind der „obligatorische Teil“ der Beobachtungen und Interpretationen.

Protokolle: Vorlagen Man kann das Protokoll verschieden verfassen, z. B. : • Ohne Vorlage: Handschriftlich, auf eigenen Blättern, während dem Praktikum. • Gedruckte Vorlage: Protokollvorlage ausgedruckt mitbringen, handschriftlich ausfüllen, während dem Praktikum. • Digitale Vorlage: Notizen während dem Praktikum, Protokollvorlage digital ausfüllen, nach dem Praktikum.

Protokolle: Vorlagen • Wenn Sie das Protokoll einer anderen Gruppe als Vorlage nehmen, ist es wichtig, dass Sie es vollständig auf Ihre Version anpassen.

Protokolle: Bewertung Bewertet wird am Protokoll: • Vollständigkeit • Umsetzung/Fülle • Richtigkeit der Protokollführung • Gestaltung/Layout Ob das Experiment gelungen ist, wird nicht bewertet.

Protokolle: Punkte • Ein gutes Protokoll wird mit 4 Punkten bewertet. • Ein Protokoll, welches den Anforderungen gerade genügt mit 3 Punkten. • 5 Punkte in der Bewertung sind für hervorragende, mustergültige Protokolle vorgesehen. • Wenn aus Ihrer Sicht etwas mit der Protokoll bewertung nicht stimmt, sollen Sie es innerhalb von 8 Tagen ansprechen.

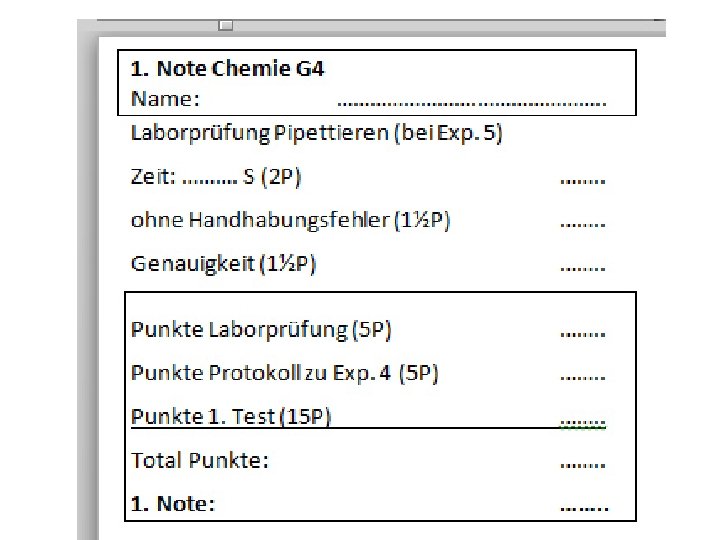
Protokolle: Bewertung Bewertet wird wie folgt:

Weitere Vorgaben • Schrift: Schrift, Gestaltung und Gliederung des Protokolls müssen ansprechend sein. • Details zur Gestaltung einer naturwissenschaftlichen Arbeit findet man auf www. reliefs. ch/chemie/gestaltung. docx • Umfang: 1 bis 2 Seiten. Mehrere Seiten zusammengeheftet. • Wer ein Experiment nicht gemacht hat, kann auch kein Protokoll darüber schreiben. • Nicht abgegebene Protokolle haben keinen Einfluss auf die Absenzen, jedoch auf die Bewertung/Praktikumsnote.

Protokolle: Bewertung Bewertet wird wie folgt:

Protokolle: Abgabetermine: 8 Tage nach Abschluss des Experiments. Wenn dieser Tag ganz unterrichtsfrei ist, am darauffolgenden Tag. Wenn dieser Tag in einer Ferien /Spezial woche liegt, eine Woche später. Die ersten 24 Stunden geben noch keinen Abzug. Danach 1 P Abzug pro angebrochenen Tag. Abgabe in Papier Form (nicht E mail)

Protokolle: Abgabe Meine Tipps zur Abgabe: • Vorlage herunterladen • Gute Notizen machen • Das Protokoll heute in einer Woche (gemeinsam) schreiben, ausdrucken und gleich abgeben. • Persönlich abgeben (Alternativen: Brief kasten Chemie oder Fach im Lehrerzimmer)

Protokolle: Rückgabe Die Protokolle erhalten Sie wieder zurück. Die Antworten zu den Fragen können dann besprochen werden. Inhalte zu grundlegenden Erkenntnissen aus den Experimenten können auch in einem Test vorkommen.


Laborprüfungen • Es finden total vier praktische Prüfungen statt: Bei den Experimenten Nr. 5, 6 und 12 (bei 10 als Zusatzprüfung). • Bei den Prüfungen ist eine Labortätigkeit, die Sie vorher geübt haben, unter Aufsicht und Kontrolle vorzuführen. • Bewertet wird dann die Genauigkeit, Zeit und/oder das Gelingen. • Bei jeder Prüfung sind max. 5 Punkte erreichbar. • Details zu den Prüfungen stehen auf www. reliefs. ch/praktikum/pruefungen. htm

Sicherheitshinweise • Natronlauge: ätzend • Salzsäure: ätzend, reizend • Hexan: leichtentzündlich, gesundheits schädlich, reizend, umweltgefährlich. Schutzbrille tragen