Exercice On dissout m2 g dun hydrocarbure non

Exercice On dissout m=2 g d’un hydrocarbure non volatil dans m’=100 g de benzène à 20°C. La tension de vapeur de ce dernier s’abaisse de 74, 66 à 74, 01 mm Hg. 1. Calculer la masse molaire de cet hydrocarbure 2. Donner sa formule brute sachant qu’il renferme 94, 4 % en masse de carbone. Benzène : M’=78 g. mol-1.

Exercice

Exemple 11 Un volume de 0, 1 L de sang à 0°C est en équilibre avec de l’azote gazeux pur à la pression 2 atm. 1. Calculer le volume gazeux d’azote dissous dans le sang. 2. Même question si on remplace l’azote pur par de l’air ( 80% d’azote , 20% d’oxygène) à la pression 2, 5 atm. Azote s = 0, 023 L. L-1 de sang. atm-1

Exemple 11 v = s Pi V = 0, 023. 2. 0, 1 = 4, 6 m. L 2. v’ = s P’i V P’i = 2, 5. 0, 8 = 2 atm ( Pression partielle) soit v’= 4, 6 m. L 1.

CHAP. 5 Solutions électrolytiques

1. Conductivité d’une solution

COMPORTEMENT DES SOLUTIONS ELECTROLYTIQUES q. Résistance électrique beaucoup plus faible que la résistance de l’eau pure q. Entre deux solutions de concentrations ioniques différentes apparaît une ddp
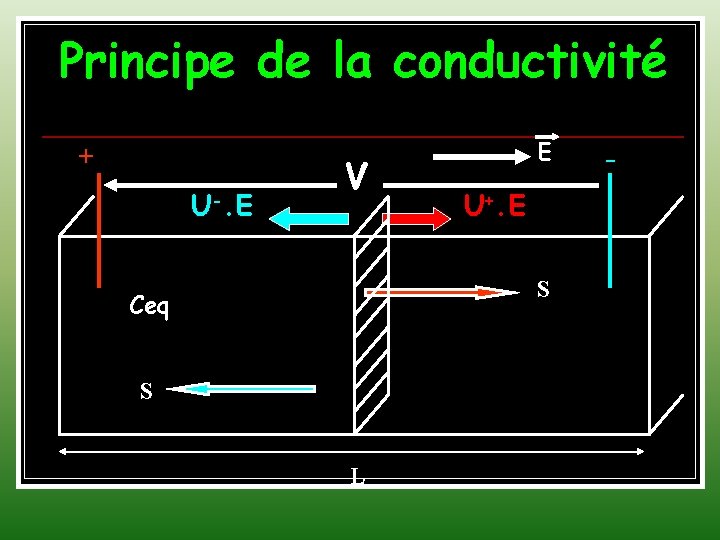
Principe de la conductivité + U-. E V E U+. E S Ceq S L -

Définition de la conductivité

Résistance et conductance

Formule générale de la conductivité

Remarques La conductivité dépend : 1. de la concentration molaire du soluté 2. de la nature des ions 3. de la température

Conductivité d’une solution

Exemple 1 Soit une solution d’acide chlorhydrique de 10 mmole/l. Les mobilités des ions H+ et Cl- sont respectivement égales à 35 m/s et 7, 63 m/s pour un champ de 1 V/cm , à une température de 25°C. Calculer la conductivité et la résistivité de cette solution.

Exemple 1

Conductivité équivalente

Exemple 2 La conductivité d’une solution aqueuse d’un électrolyte du type AB 2 de concentration 15 mmol. L-1 est σ = 24 Ω-1. m-1. Sa conductivité équivalente à dilution infinie est Λ∞=400 Ω-1. cm-2. Eq-1. Calculer son degré de dissociation et sa constante d’équilibre.

Exemple 2

QCM 1 Soit une solution électrolytique , sel d’un acide faible. Quel(s) élément(s) ne dépend(ent) pas de son coefficient de dissociation : A. La résistivité de la solution B. Le p. H C. La molarité D. L’abaissement cryoscopique E. L’osmolarité

QCM 2 La migration électrique : A. est un transport de type passif B. est en rapport avec un gradient de potentiel électrique C. entraîne un flux électrique de solvant D. est seule responsable du flux de la membrane cellulaire E. provoque un courant électrique dont le sens est toujours opposé au gradient de potentiel

QCM 3 Une membrane dialysante sépare deux solutions électrolytiques de concentration inégale. Dans l’un des compartiments se trouve une macromolécule neutre, l’état d’équilibre est tel que : A. L’électroneutralité de part et d’autre de la membrane B. L’égalité des concentrations de chaque ion de part et d’autre C. L’existence d’une ddp entre les côtés de la membrane rapidement résolutive D. L’établissement d’une contre-pression osmotique E. Un flux de migration négligeable
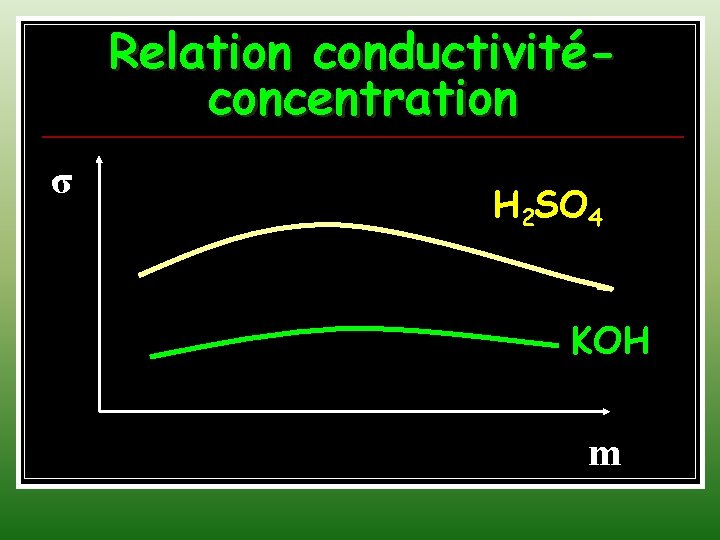
Relation conductivitéconcentration σ H 2 SO 4 KOH m
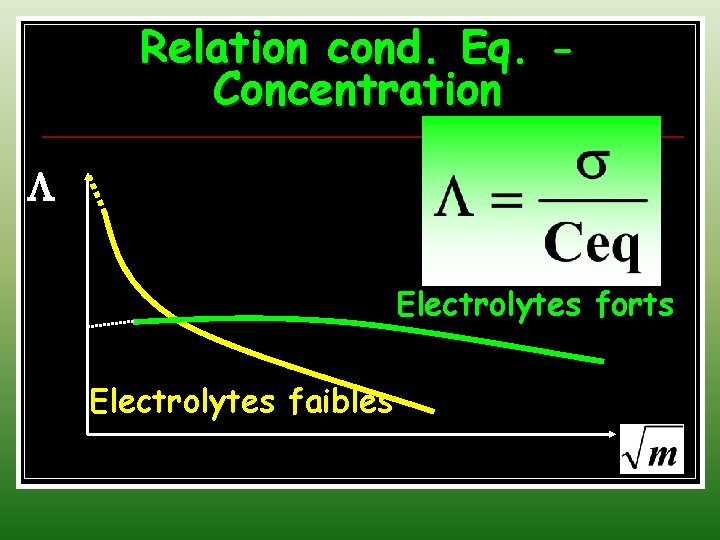
Relation cond. Eq. Concentration Electrolytes forts Electrolytes faibles

Interprétation de la relation cond. eq - concentration Deux interprétations possibles : m↑ ↓ Le nombre d’ions ↓ Λ ↓ ( Valable pour les électrolytes faibles) =1 Molécules complètement dissociées ; m↑ Activité ionique diminue↓ (cas des électrolytes forts)

Activité d’une solution Concentration d’une solution idéale qui présenterait la même conductivité que la solution réelle. a = m = Coefficient d’activité Faible concentration : = 1 Forte concentration : < 1

2. Mesure de la conductivité
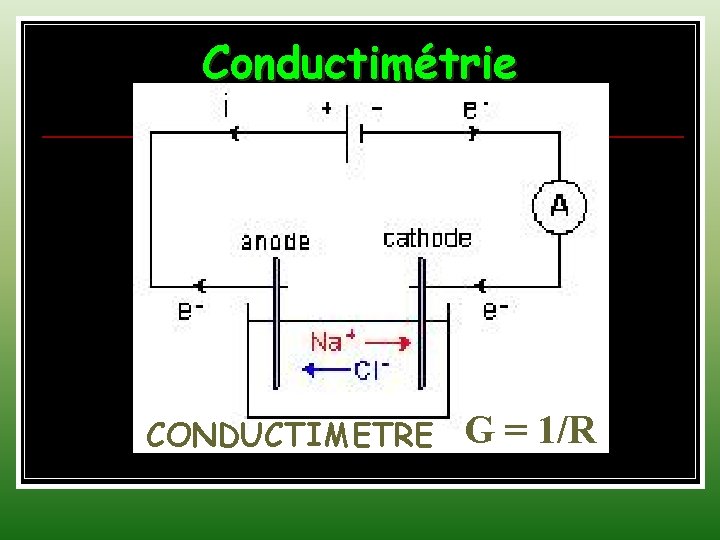
Conductimétrie CONDUCTIMETRE G = 1/R

QCM 5 Concernant la mobilité d’un ion soumis à l’action d’un champ électrique A. Elle est indépendante de la viscosité du milieu B. Elle est toujours identique pour deux ions de même charge C. Elle dépend de l’intensité du champ électrique D. Elle s’effectue toujours à vitesse croissante E. Elle génère une force de frottement

QCM 6 Concernant la membrane cellulaire : A. Les forces dues aux gradients transmembranaires de concentration et de potentiel électrique sont de même sens pour les ions K+ et Cl- , mais elles sont opposées pour l’ion Na+ B. Elle a une face interne toujours électronégative C. Elle a une face externe électropositive D. La ddp est supérieure à 50 m. V dans le cas des cellules excitables E. Les mécanismes de transport actif explique la constance des concentrations ioniques intra et extracellulaires
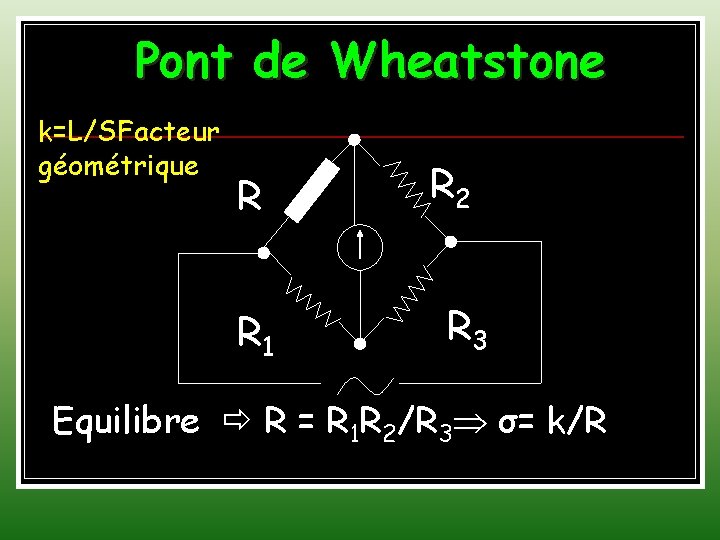
Pont de Wheatstone k=L/SFacteur géométrique R R 1 R 2 R 3 Equilibre R = R 1 R 2/R 3 σ= k/R

Conductivité du plasma

3. Mobilité ionique

Définition soit un ion dans un champ électrique E, qui se déplace dans un solvant ( avec frottements). Sa vitesse est constante en régime permanent. On définit la mobilité U+cation U+. E =v et U-anion U-. E =v

Exemple 3 Etablir la dimension de la mobilité U en l’exprimant en masse (M), temps (T) et intensité électrique (I).
Formule de la mobilité d’un ion

Aspects physico-chimiques de la mobilité La mobilité ionique est fonction de la nature de l’ion (Q et r) du milieu dans lequel il se déplace
Exemple 4

Ordres de grandeur Les mobilités ioniques : 2 à 10 microns/s pour un champ de 1 V/cm ( 2. 10 -8 à 10 -7 m 2. V-1. s-1) + Les ions OH et H sont beaucoup plus rapides : 20 et 30 microns/s.

QCM 4 A. Pour les électrolytes forts, est toujours égal à 1 mais l’activité diminue quand la concentration augmente B. L’intensité du courant augmente avec la concentration C. Pour un électrolyte faible, à forte dilution le coefficient d’activité tend vers 1 D. La force ionique caractérise l’environnement ionique E. La force ionique du plasma est de 0, 145

QCM 7 La mobilité d’un ion dans un champ électrique: A. dépend dans certains cas du p. H de la solution aqueuse B. dépend de la concentration C. est à la base de l’analyse par électrophorèse D. est fonction de la charge de l’ion E. est sa vitesse de migration

Exemple 4 Une protéine a une mobilité u= -7, 2 10 -7 m. s/V. m-1 dans un milieu tampon liquide de p. H=8, 6 et de viscosité η=0, 2 m. Pa. s. Cette particule est sphérique de rayon r=1 nm. 1. Situer son p. H isoélectrique et calculer la charge prise par cette particule à ce p. H. 2. Quelle tension faut-il appliquer entre les électrodes distantes de 10 cm pour qu’elle se déplace de 7 mm en 100 s?

Mobilité et courants ioniques Courant cationique Courant anionique

Exemple 5 Soit un acide AH dont l’ion A- a une mobilité de 5 m/s par volt/cm. Quelle est la proportion du courant cationique? t+ = 30/35 = 86 % par les ions H+

4. Potentiel d’électrode et loi de Nernst

Oxydation et réduction Oxydation = perte d’électrons : M =M z+ + ze. M z+= Forme oxydée Réduction = gain d’électrons M z+ + ze- = M M = Forme réduite

Exemple 3 Fe 2+ = Fe 3+ + e. Reducteur = Oxydant + ze. Réaction Redox

Potentiel d’électrode : Formule de Nernst Soit le couple rédox : Ox/Réd Ox + ne- = β Réd

Exemple 4 Vérifier qu’à 25°C, on a

Exemple 4 Sachant que ln. X=ln 10 x log. X et que pour 25°C , T = 298 °K

Les différents types d’électrodes 1. L’électrode métallique (M z+ /M) 2. L’électrode à hydrogène 3. L’électrode métallique inerte (solution contenant forme oxydée et forme réduite d’une même substance, exemple Fe 3+ / Fe 2+ )

L’électrode métallique Electrode métallique plongeant dans une solution d’un de ses sels ( Couple M z+ /M)

Exemple 5 Calculer le potentiel d’une lame d’argent plongeant dans une solution de Ag NO 3 de concentration m= 1 mmol. l-1. On donne E 0(Ag+/Ag) = 0, 80 V Ag=Ag++e- E = E 0 + 0, 059 log m = 626 m. V

L’électrode à hydrogène Couple H+/H 2 Une électrode en platine dans une solution acide contenant les ions H+ Au contact de l’électrode il y a échange d’e- entre H+ et H 2. 2 H 3 O+ + 2 e- = H 2 (g) + H 2 O

Exemple 6 Calculer le potentiel d’une électrode à hydrogène ( p. H 2 = 1 atm) plongée dans chacune des solutions suivantes à 20°C. 1. HCl 0, 1 mol. l-1 2. HCOOH 0, 15 mol. l-1 ( = 0, 03) 3. H 2 SO 4 0, 1 mol. l-1 4. Na. OH 0, 1 mol. l-1

Exemple 6

L’électrode métallique inerte

Exemple 7 1. 2. Calculer le potentiel d’une électrode inattaquable de platine plongée dans une solution de sels ferreux et ferrique à concentrations égales sachant que E(Fe 3+/Fe 2+)=0, 77 V Calculer le potentiel lorsque[Fe 3+]=2 [Fe 2+]

Exemple 7

Oxydo-réduction Une réaction d’oxydation ne s’effectue qu’en présence d’un accepteur d’électrons Couples : Ox 1/Réd 1 et Ox 2/Réd 2 Ox 1 + n 1 e- = Réd 1 Réd 2= Ox 2 + n 2 en 2 Ox 1 + n 1 Réd 2 = n 2 Réd 1+ n 1 Ox 2

Exemple 8 Oxydation du Cu+ ( cuivreux) par Fe 3+ ( Ferrique) Cu+ = Cu 2+ + e. Fe 3+ + e- = Fe 2+ Cu+ + Fe 3+ = Cu 2+ + Fe 2+
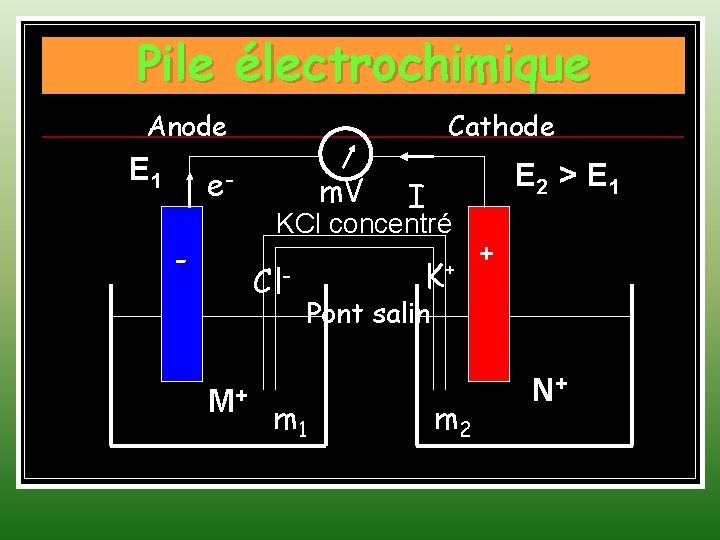
Pile électrochimique Anode E 1 Cathode e- m. V E 2 > E 1 I KCl concentré - Cl- M+ K+ + Pont salin m 1 m 2 N+

f. e. m d’une pile

Mesure du p. H Pile avec : -Electrode de référence impolarisable : E 2 -Electrode de mesure ( à hydrogène) dans une solution de concentration inconnue T=20°C E(V)= E 2 + 0, 058 p. H

Exemple 10 On considère la pile suivante : Données numériques : T=298°K; E 0(Fe 3+/Fe 2+)=0, 77 V; E 0(Ag+/Ag)=0, 80 V 1. Calculer la f. e. m E de cette pile 2. Quelle est la relation entre E 0 de la pile et la constante d’équilibre de la réaction chimique lorsque la pile débite. Calculer cette constante.

Exemple 10… 1. Couple Fe 3+/Fe 2+ : Fe 3++ e- = Fe 2+ E 1 = E 0 (Fe 3+/Fe 2+ )+ 0, 059 log[Fe 3+]/[Fe Couple Ag+/Ag : Ag++ e- = Ag E 2= E 0 (Ag+/Ag )+ 0, 059 log[Ag+] Réaction : Ag++ Fe 2+ = Ag + Fe 3+ 2+]

Exemple 12…

Exemple 12

A. Dans QCM 8 une pile électrochimique en fonctionnement, la réaction qui se produit est forcée B. La loi de Nernst dit que le potentiel pris par une électrode trempant dans une solution dépend : du couple étudié, et des concentrations (ou des pressions pour les gaz) des espèces intervenant dans le couple C. Lorsqu’une pile débite, la masse de l’électrode positive ne diminue jamais D. Le pont salin est nécessaire au fonctionnement de la pile E. Les ions se déplacent à l’intérieur des solutions et du pont salin

QCM 9 Données: E 0(H+/H 2)=0 V; E 0(Fe 2+/Fe)=-0, 44 V; ; E 0(Ag+/Ag)=0, 80 V A 25°C, par rapport à l’électrode normale d’hydrogène A. Le potentiel d’une lame de fer plongeant dans une solution centimolaire de sulfate de fer vaut -0, 38 V B. Le potentiel de la lame de fer vaut -0, 50 V C. Le potentiel d’une lame d’argent plongeant dans une solution de nitrate d’argent à 10 -3 mol. L-1 vaut 0, 62 V D. Le potentiel de la lame d’argent vaut 1, 32 V E. Le potentiel de la lame d’argent vaut 0, 62 V

QCM 10… On réalise la pile suivante : Zn/Zn 2+//Pb 2+/Pb Volume des solutions V=100 ml [Zn 2+]=5, 0. 10 -2 mol. L-1, [Pb 2+]= 1, 0. 10 -2 mol. L-1 La constante de réaction ayant pour réactifs les ions Zn 2+ et le métal Pb a pour valeur K=2. 10 -21. Un voltmètre est inséré dans le circuit extérieur, sa borne + est reliée à la lame de zinc et sa borne – à la lame de plomb

QCM 10 A. L’équation de réaction de la pile est : Pb 2+ + Zn= Zn 2++ Pb B. L’équation de réaction de la pile est : Zn 2++ Pb = Pb 2+ + Zn C. La valeur de la tension affichée au voltmètre est positive D. À l’intérieur de la pile, les électrons se déplacent de la lame de zinc vers la lame de plomb E. Quand la pile s’arrête de fonctionner, le quotient de réaction a pour valeur Qr=5.

Exemple 13 Solution 1 : Fe (NO 3)2 -Electrode en Fer Solution 2 : Ag(NO 3) - Electrode en Ag Solutions reliées par un conducteur Activité de Fe (NO 3)2 : a = 2 mol/l Molarité de Ag(NO 3) : c = 2 mol/l ddp mesurée entre les 2 solutions : 1241 mv Coefficient d’activité de Ag+ ?

Exemple 13

5 Transports et équilibres ioniques
![Potentiel de diffusion 1 2 m - A + B [A ]1 = - Potentiel de diffusion 1 2 m - A + B [A ]1 = -](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-75.jpg)
Potentiel de diffusion 1 2 m - A + B [A ]1 = - [A-] 2 + + [B ]1 = [B ]2
![Potentiel d’équilibre : Equ. Gibbs-Donnan [A-] [B+] 1 1 A- < [A-]2 > [B+]2 Potentiel d’équilibre : Equ. Gibbs-Donnan [A-] [B+] 1 1 A- < [A-]2 > [B+]2](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-76.jpg)
Potentiel d’équilibre : Equ. Gibbs-Donnan [A-] [B+] 1 1 A- < [A-]2 > [B+]2 B+ [A-]1. [B+]1 = [A-]2. [B+]2

Equation de Nernst

Condition d’équilibre

Exemple 14 Solution contenant des ions Cl, Na+, K+, CO 3 H-, Ca++, diffusibles à travers une membrane. Quel est le potentiel équilibre?

Exemple 14

Exemple 15 On considère 2 compartiments A et B séparés par une membrane perméable au K+. Les concentrations en A et B sont respectivement 0, 1 M et 0, 01 M. 1. Calculer la ddp VA-VB pour laquelle l’ion K+ est à l’équilibre? 2. Pour cette ddp, quelle est la valeur du flux net de K+?

Exemple 15 2. A l’équilibre le flux net d’ions K+ est nul.

Exemple 16 On considère 2 compartiments A et B séparés par une membrane perméable contenant HCO 3 - aux concentrations 1 M et 0, 1 M, respectivement. La ddp entre A et B est VA-VB = +100 m. V 1. L’ion est-il à l’équilibre ? Satisfait-il à l’équation de Nernst? 2. Si l’ion n’est pas à l’équilibre, dans quel sens la force électrochimique va-t-elle le faire migrer?

Exemple 16 Potentiel d’équilibre pour l’ion : (VA-VB) eq= +(60)log(1 / 0, 1)= +60 log 10 (VA-VB) eq= +60 m. V (VA-VB) eq est différent de VA-VB Pas d’équilibre électrochimique pour l’ion 2. z(VA-VB) <z (VA-VB) eq : Diff B A z(VA-VB) >z (VA-VB) eq : Diff A B Flux B A 1.

Macromolécule neutre : Phénomène de Donnan Membrane dialysante séparant deux solutions ioniques de concentrations différentes : dans un des compartiments se trouve une macromolécule électriquement neutre incapable de traverser la membrane Equilibre de Donnan

Etat d’équilibre de Donnan 1. 2. 3. 4. Electroneutralité de part et d’autre de la membrane Concentrations ioniques égales de part et d’autre ddp nulle entre les côtés de la membrane Contre pression osmotique liée à la concentration de la molécule neutre non diffusible

Macromolécule chargée : Phénomène de Donnan Membrane dialysante séparant deux solutions ioniques de concentrations différentes: dans un des compartiments une macromolécule non diffusible chargée électriquement ( Ex : RNaz Rz- + z Na+)
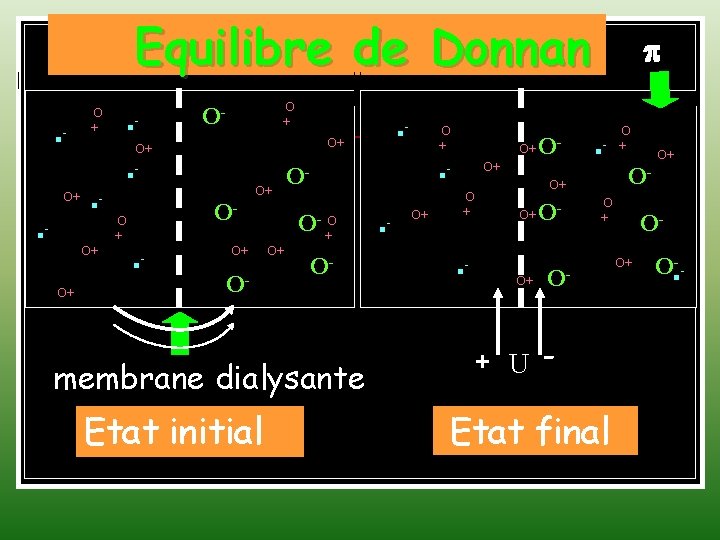
Equilibre de Donnan O + O+ O- O + O+ O+ O+ - O + O- O- membrane dialysante Etat initial O + OO- +O O+ - - O+ O+ O - - O+ O + O+ O- O+ O+ O + O- + U - Etat final OO+ O-

Etat d’équilibre de Donnan… 1. Electroneutralité de part et d’autre de la membrane ( ex : capillaire sanguin, glomérule rénal …) 2. La non égalité des concentrations de chaque ion diffusible ( Présence macro-ion) de part et d’autre de la membrane 3. ddp non nulle entre les côtés de la membrane 4. Pression osmotique plus forte que celle due au macro-ion ( Pression oncotique>Pression protéines)

Etat d’équilibre de Donnan 5. Le macro ion repousse les ions de son signe de l’autre côté de la membrane 6. Le potentiel de Donnan V 2 -V 1 est tel que le côté de la membrane où est présent le macro ion non diffusible se charge de son signe

Exemple 17 On considère 2 compartiments A et B, de volume constant, séparés par une membrane perméable aux ions K+ et Cl-, mais imperméable aux ions YCompartiment A : [K+]A = [Y-]A= 0, 1 M Compartiment B : [K+]B = [Cl-]B= 0, 1 M 1. En quoi la membrane est-elle de Donnan? 2. Les ions sont-ils à l’équilibre? 3. A l’équilibre, quelles sont les concentrations des différents ions dans chaque compartiment? Quelle sera la ddp entre A et B.

Exemple 17 … 1. Membrane de Donnan, puisqu’ elle est perméable à K+, Cl- , mais pas à Y-. 2. Au départ l’ion Cl- n’est pas à l’équilibre. Le flux Cl- va de B vers A (VA-VB) < 0 Flux K+ de B vers A.
![Exemple 17 … A l’équilibre : [K+]A [Cl-]A= [K+]B [Cl]B ( Eq. Gibbs-Donnan) (1) Exemple 17 … A l’équilibre : [K+]A [Cl-]A= [K+]B [Cl]B ( Eq. Gibbs-Donnan) (1)](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-93.jpg)
Exemple 17 … A l’équilibre : [K+]A [Cl-]A= [K+]B [Cl]B ( Eq. Gibbs-Donnan) (1) Electroneutralité [K+]A = [Cl-]A+[Y] (2) [K+]B = [Cl-]B (3) Conservation de la matiére [K+]A + [K+]B = 0, 2 M (4) [Cl-]A+ [Cl-]B=0, 1 M (5) [Y] = 0, 1 M (6) 3.
![Exemple 17 … + (3) [K+]A [Cl-]A= ([K+]B)2 (4) + (5) (0, 2 - Exemple 17 … + (3) [K+]A [Cl-]A= ([K+]B)2 (4) + (5) (0, 2 -](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-94.jpg)
Exemple 17 … + (3) [K+]A [Cl-]A= ([K+]B)2 (4) + (5) (0, 2 - [K+]B) (0, 1 - [Cl-]B)= ([K+]B)2 Ou (0, 2 - [K+]B) (0, 1 - [K+]B)= ([K+]B)2 (0, 2 x 0, 1)- [K+]B(0, 2+0, 1)+ ([K+]B)2 = ([K+]B)2 (0, 2 x 0, 1)= [K+]B (0, 2+0, 1) (1)
![Exemple 17 [K+]B =0, 02/0, 3=0, 066 M= [Cl-]B Exemple 17 [K+]B =0, 02/0, 3=0, 066 M= [Cl-]B](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-95.jpg)
Exemple 17 [K+]B =0, 02/0, 3=0, 066 M= [Cl-]B
![Exemple 17 : Autre méthode ([K+]A +x) x=([K+]B -x) ([Cl-]B -x) (0, 1+x) x=(0, Exemple 17 : Autre méthode ([K+]A +x) x=([K+]B -x) ([Cl-]B -x) (0, 1+x) x=(0,](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-96.jpg)
Exemple 17 : Autre méthode ([K+]A +x) x=([K+]B -x) ([Cl-]B -x) (0, 1+x) x=(0, 1 -x) x 2 +0, 1 x= x 2 -0, 2 x+0, 01 0, 3 x =0, 01 x = 0, 01/0, 3 =0, 033 M x=[Cl-]A=0, 033 M, [K+]A=x+0, 1 =0, 133 M [Cl-]B=0, 1 -0, 033=0, 066 M= [K+]B

QCM 11 De part et d’autre d’une membrane de dialyse, on a, à 27°C, 2 solutions à l’équilibre avec : P-10 en mmol/L HCO 3 - en mmol/L H+ en mmol/L Solution 1 1, 5 ? 16 Solution 2 0 ? ? A. [H+]2= 10 mmol/L B. [H+]2= 4 mmol/L C. [H+]2= 8 mmol/L D. [H+]2= 2 mmol/L E. Autre réponse

QCM 12 La différence de potentiel (V 1 -V 2) de part et d’autre de la membrane vaut : A. -24 m. V B. -18 m. V C. -10, 5 m. V D. -36 m. V E. Autre réponse
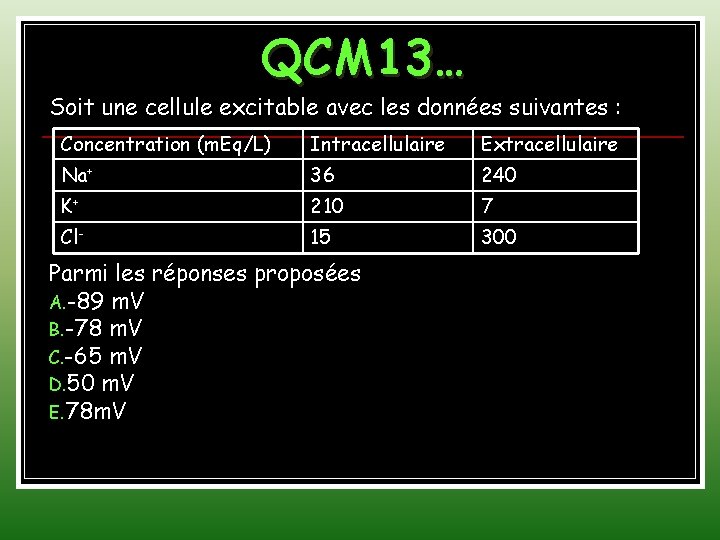
QCM 13… Soit une cellule excitable avec les données suivantes : Concentration (m. Eq/L) Intracellulaire Extracellulaire Na+ 36 240 K+ 210 7 Cl- 15 300 Parmi les réponses proposées A. -89 m. V B. -78 m. V C. -65 m. V D. 50 m. V E. 78 m. V

QCM 13 Choisir celle qui correspond à 27°C: 1. Au potentiel de repos 2. Au potentiel d’action 3. Au post-potentiel 4. Au potentiel d’équilibre des ions K+
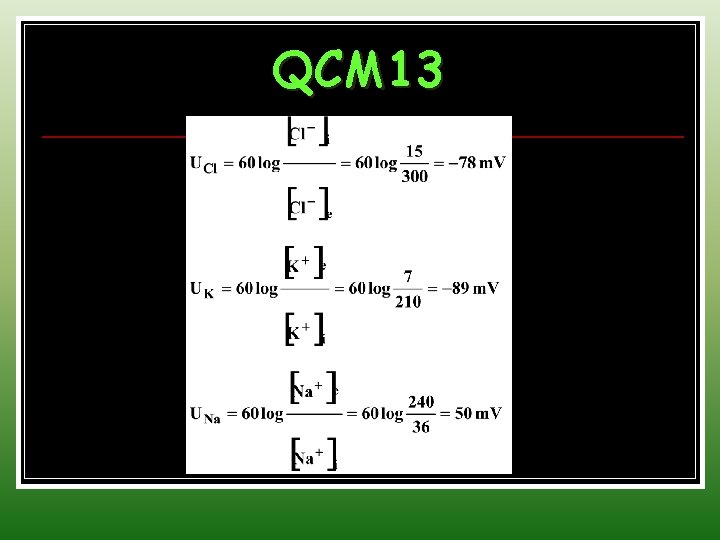
QCM 13

QCM 13 Potentiel de repos = -78 m. V Potentiel d’action = 50 m. V Post potentiel = -89 m. V Potentiel d’équilibre des ions K+ = -89 m. V

6 Diagramme de davenport et troubles acido-basiques

Définition On appelle diagramme de Davenport les graphes donnant l’évolution des ions carbonate HCO 3 - (aq) en fonction du p. H de l’organisme
![Lois de variation de [HCO 3 -] Lois de variation de [HCO 3 -]](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-105.jpg)
Lois de variation de [HCO 3 -]

Définitions • On appelle point normal, le point N représentant un état acido-basique normal soit [HCO 3 -]=24 mmol. L-1 et p. H=7, 40. • L’isobare passant par le point normal est appelé isobare normale. • La droite normale d’équilibration (DNE) correspond à la droite d’équilibration passant par N.
![Isobares et droites d’équilibration [HCO 3 -] mmol/L 24 >40 40 <40 PCO 2 Isobares et droites d’équilibration [HCO 3 -] mmol/L 24 >40 40 <40 PCO 2](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-107.jpg)
Isobares et droites d’équilibration [HCO 3 -] mmol/L 24 >40 40 <40 PCO 2 • N mm. Hg Isobare normale DNE p. H 7, 4

vi - ve (m. V) +50 UNa Potentiel d’action Activité électrique de la cellule 0 Stimulation UCl - 78 - 89 Perméabilité PNa+ Post Potentiel de repos t UK PK+ 50 ms t
![Mécanismes de compensation [HCO 3 -] mmol/L 24 II Acidose III P. I et Mécanismes de compensation [HCO 3 -] mmol/L 24 II Acidose III P. I et](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-109.jpg)
Mécanismes de compensation [HCO 3 -] mmol/L 24 II Acidose III P. I et III : compensation . P 2 II et IV : double agression 1 • N IV . M I . M 7, 4 métabolique et respiratoire 2 1 Alcalose p. H

Exemple 18 Placer sur le diagramme de Davenport le point représentatif d’un sujet: • A atteint d’une acidose respiratoire non compensée • B atteint d’une alcalose métabolique non compensée • C atteint d’une alcalose respiratoire partiellement compensée • D atteint d’une acidose mixte avec [HCO 3 -] normal • E atteint d’une agression totalement compensée par perfusion de bicarbonates
![Exemple 18 [HCO 3 -] mmol/L 24 . D . A . E. B Exemple 18 [HCO 3 -] mmol/L 24 . D . A . E. B](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-111.jpg)
Exemple 18 [HCO 3 -] mmol/L 24 . D . A . E. B • N . C p. H 7, 4

Exemple 19 … Soit le LEC d’un sujet avec un p. H de 7, 4, [HCO 3 -]=28 mmol. L-1, [CO 2]=1, 4 mmol. L-1 Loi d’Henderson-Hasselbach : p. H= 6, 1 + log 20 = 7, 4 1. Si on ajoute 14 mmol de HCl par litre de LEC : en absence de tampon carbonique ou autres 14 m. Eq/L de H+ p. H =1, 85

Exemple 19 … 2. Avec tampon carbonique : HCO 3 - + H+ CO 2 + H 2 O [HCO 3 -] =28 -14 = 14 m. Eq/L [CO 2]=1, 4 + 14 = 15, 4 m. Eq/L p. H = 6, 1 + log 14/15, 4 = 6, 06 ->[H+ ] 15000 fois plus faible que sans tampon Avec les autres tampons : p. H >6, 06
![Exemple 19 3. [CO 2] tend à rester en équilibre avec la PCO 2. Exemple 19 3. [CO 2] tend à rester en équilibre avec la PCO 2.](http://slidetodoc.com/presentation_image/1dc22c58adf8959b02906bf3209d6094/image-114.jpg)
Exemple 19 3. [CO 2] tend à rester en équilibre avec la PCO 2. Si PCO 2= Cte = 40 mm. Hg --> CO 2 éliminé et revient à 1, 4 mmol/L p. H= 6, 1 + log 14/1, 4 = 7, 1 4. Intervention du système respiratoire pour l’hypercapnie -> PCO 2 passe à 23 mm. Hg [CO 2] =0, 6 mmol/L p. H= 6, 1 + log 14 / 0, 7 = 7, 4 5. Le rein va finalement éliminer les 14 mmol en excès, et régénérer les bicarbonates et ramener [HCO 3 -] à sa valeur initiale , la ventilation diminue et PCO 2 revient à 40 mm. Hg.

CHAP. 6 Les Phénomènes de surface

1 Tension superficielle des liquides

Forces intermoléculaires Force d’interaction moléculaire Energie de surface δW= σ δS (σ >0)

Energie de cohésion C’est le travail à fournir pour vaincre les forces de cohésion

Exemple 1 Quel travail faut-il fournir ? 1. Pour casser un bâton de craie de section S en deux morceaux, σcr étant la tension superficielle de la craie 2. Pour pulvériser une goutte d’eau de surface S en n gouttelettes de surface s. On donne σE de l’eau.

Exemple 1 1. 2. Deux surfaces S sont nouvellement crées Wc = 2 σcr. S Surface initiale = Si Surface finale = Sf = n. s Wc = σE(Sf - Si)

Energie d’adhésion C’est le travail à fournir pour séparer deux phases ( liquide-solide par exemple) de surface S Wa = (σL+ σS – σL/S) S σL= Cte tension superficielle du liquide σS= Cte tension superficielle du solide σL/S = Cte tension superficielle du mélange liquide-solide

Potentiel d’électrode Métal plongé dans une solution contenant l’un de ses sels Potentiel d’électrode Ex : Fe (NO 3)2 et une électrode en Fer Ag(NO 3) et une électrode en Ag

Formule du potentiel d’électrode : Loi de Nernst 2 e- Zn Zn Zn++ Métal Solution Zn. SO 4 EM= Vmét-Vsol = EM 0= Potentiel 1 Normal Zn++ Zn/Zn++=-0, 76 2
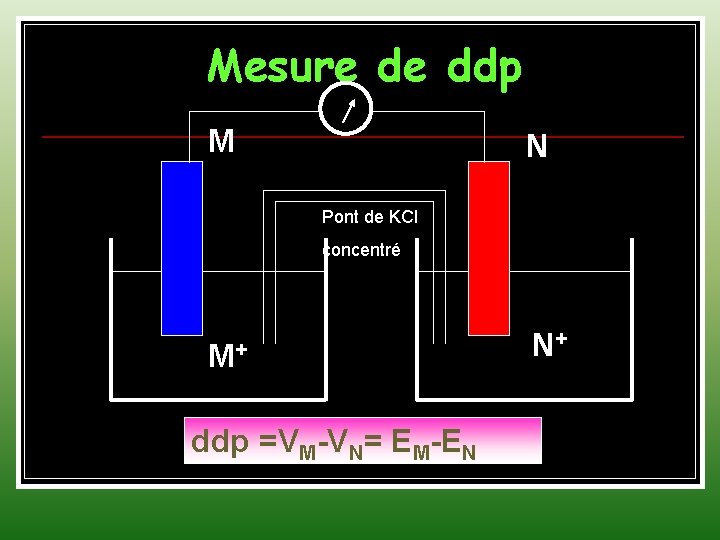
Mesure de ddp M N Pont de KCl concentré M+ ddp =VM-VN= EM-EN N+

Exemple 9 Solution 1 : Fe (NO 3)2 -Electrode en Fer Solution 2 : Ag(NO 3) - Electrode en Ag Solutions reliées par un conducteur Activité de Fe (NO 3)2 : a = 2 mol/l Molarité de Ag(NO 3) : c = 2 mol/l ddp mesurée entre les 2 solutions : 1241 mv Coefficient d’activité de Ag+ ?

Exemple 9

QCM 2 La mobilité d’un ion dans un champ électrique: A. est fonction de la ddp électrique B. dépend de la concentration C. est à la base de l’analyse par électrophorèse D. est fonction de la charge de l’ion E. est sa vitesse de migration

Réponses QCM 2 La mobilité d’un ion dans un électrique: champ A. dépend de la concentration C. est à la base de l’analyse par électrophorèse D. est fonction de la charge de l’ion B. E.

QCM 3 A. Un cristal de glace fond dans de l’eau pure à 0°C mais il ne fond pas dans une solution à 0°C B. Dans ce phénomène l’interface glace-liquide joue le rôle de la membrane hémiperméable C. Osmomètrie et cryoscopie sont de même nature mais ont des domaines d’applications différents D. Une solution de Na. Cl décimolaire à 27°C développe une pression osmotique équivalente de 5 m H 2 O et un T de 0, 37°C E. Le T cryoscopique du plasma est de 0, 56°C

Réponses QCM 3 A. B. Dans ce phénomène l’interface glace-liquide joue le rôle de la membrane hémiperméable C. Osmomètrie et cryoscopie sont de même nature mais ont des domaines d’applications différents D. E. Le T cryoscopique du plasma est de 0, 56°C

QCM 4 Les dosages sanguins d'un patient donnent les résultats suivants en mmol/l : Urée = 3. 5. Magnésium=1; Sodium=142; Chlore=103. Potassium=5. 4; Protéines=3; Glucose=3. 8; Calcium=1. 9. Si la masse molaire du glucose est de 180 g, on peut en déduire une glycémie de 684 g/l B. Céq(Ca++)=3. 8 m. Eq/l C. L'osmolarité réelle peut se mesurer par la méthode du cryoscopique D. Ceq(Na+)=142 Eq/l E. Les données ci-dessus nous permettent d'avoir une estimation de l'osmolarité de l'ordre de 296. 7 mosm. A.

Réponses QCM 4 Les dosages sanguins d'un patient donnent les résultats suivants en mmol/l : Urée = 3. 5. Magnésium=1; Sodium=142; Chlore=103. Potassium=5. 4; Protéines=3; Glucose=3. 8; Calcium=1. 9. A. B. Céq(Ca++)=3. 8 m. Eq/l C. L'osmolarité réelle peut se mesurer par la méthode du cryoscopique D. E. Les données ci-dessus nous permettent d'avoir une estimation de l'osmolarité de l'ordre de 296. 7 mosm.

QCM 5 Chez un sujet normal, suite à une restriction de la diète hydrique, on observe une augmentation de 10 m. Eq/l de la concentration plasmatique de l’ion Na+; les autres modifications cationiques peuvent être considérées comme négligeables, le cation principal étant l’ion sodium. Quelle est l’augmentation associée de l’osmolarité plasmatique (en m. Osm/l)? A. 0, 06 B. 0, 5 C. 1, 5 D. 10 E. 20

Réponses QCM 5 Chez un sujet normal, suite à une restriction de la diète hydrique, on observe une augmentation de 10 m. Eq/l de la concentration plasmatique de l’ion Na+; les autres modifications cationiques peuvent être considérées comme négligeables, le cation principal étant l’ion sodium. Quelle est l’augmentation associée de l’osmolarité plasmatique (en m. Osm/l)? A. B. C. D. E. 20

QCM 6 (suite QCM 5) Le delta cryoscopique du plasma lu au 1/100 de degré s’en trouve: A. réduit de 0, 56°C B. réduit de 0, 04°C C. réduit de 0, 02°C D. accru de 0, 04°C E. accru de 1, 86°C
Réponses QCM 6 Le delta cryoscopique du plasma lu au 1/100 de degré s’en trouve: A. B. C. D. E. accru de 0, 04°C

QCM 7 (suite QCM 5) La correction de cette anomalie pourra se faire par : A. une évolution vers l’hypernatrémie B. une sortie d’eau plasmatique vers l’espace interstitiel C. une hypervolémie à partir de l’eau interstitielle D. une fuite de protéines plasmatiques vers le secteur extravasculaire E. une hyperhydratation intracellulaire

Réponses QCM 7 (suite QCM 5) La correction de cette anomalie pourra se faire par : A. B. C. une hypervolémie interstitielle D. E. à partir de l’eau

QCM 8 Concernant la mobilité d’un ion soumis à l’action d’un champ électrique A. Elle est indépendante de la viscosité du milieu B. Elle est toujours identique pour deux ions de même charge C. Elle dépend de l’intensité du champ électrique D. Elle s’effectue toujours à vitesse croissante E. Elle génère une force de frottement

QCM 9 La technique d’électrophorèse A. Ne peut s’appliquer qu’à des molécules neutres sans charge électrique B. Nécessite l’application d’un champ électrique C. Permet l’analyse des protéines plasmatiques D. Sépare les molécules en fonction de leur solubilité dans les lipides E. Peut entraîner un déplacement dans l’albumine plasmatique

QCM 10 La présence d’un macro ion non diffusible d’un côté d’une membrane de dialyse A. Est responsable d’un phénomène d’osmose B. N’empêche pas l’homogénéisation des concentrations en ions diffusibles C. Entraîne l’apparition d’une ddp rapidement résolutive D. Aboutit à l’équilibre de Donnan E. Constitue une situation que l’on observe « in vivo » au niveau de la membrane capillaire

Exemple 4 On réalise l’électrophorèse sur papier d’une solution de 2 protéines A et B. Une goutte de solution déposée sur la ligne de départ détermine une tache de diamètre d=5 mm. Les conditions expérimentales sont U=100 V; distance entre les électrodes : l=10 cm; mobilités électrophorétiques : UA=4, 5. 10 -7 SI; UB=5, 5. 107 SI. Au bout de combien de temps et à quelle distance du point de départ peut-on considérer que les deux protéines sont séparées? Que se passe t-il si la diffusion n’est plus négligeable?

Exemple 4 Les distances parcourues par A et B au bout d’un temps t : l. A = v. A. t = u. A. E. t et l. B = v. B. t = u. B. E. t soit l. A = u. A. E. t 0 = 2, 25 cm ; l. B = u. B. E. t 0 = 2, 75 cm Si la diffusion n’est plus négligeable , elle augmente le diamètre de la tache au cours de sa migration, le temps pour séparer A et B est plus long (intérêt de la petite taille de la tache)

QCM 11 Concernant la membrane cellulaire : A. Elle est perméable au sodium B. Elle a une face interne électronégative C. Elle a une face externe électropositive D. Elle est imperméable à l’eau E. Elle est le siége de mécanismes de transport actif

QCM 12 L’équation de Nernst : A. Donne la ddp transmembranaire B. Concerne l’équilibre ionique C. Est vérifiée si le courant de filtration compense le courant de migration D. Donne la ddp qui annule le courant pour un ion donné E. S’applique au phénomène de Donnan

QCM 13 Une membrane dialysante sépare deux solutions électrolytiques de concentration inégale, dans l’un des compartiments se trouve une macromolécule neutre, l’état d’équilibre est tel que : A. L’électroneutralité de part et d’autre de la membrane B. L’égalité des concentrations de chaque ion de part et d’autre C. L’existence d’un potentiel de diffusion entre les côtés de la membrane D. L’établissement d’une contre-pression osmotique E. Identique à la membrane du glomérule rénal

QCM 13 L’équilibre de Donnan : A. Est dû à la présence d’un ion non diffusible B. Entraîne une pression supérieure à celle prévue par la loi de Van’t Hoff C. Entraîne une égalisation de la concentration des ions non diffusibles D. Entraîne une ddp de part et d’autre de la membrane E. Est dû à la présence d’une molécule neutre non diffusible
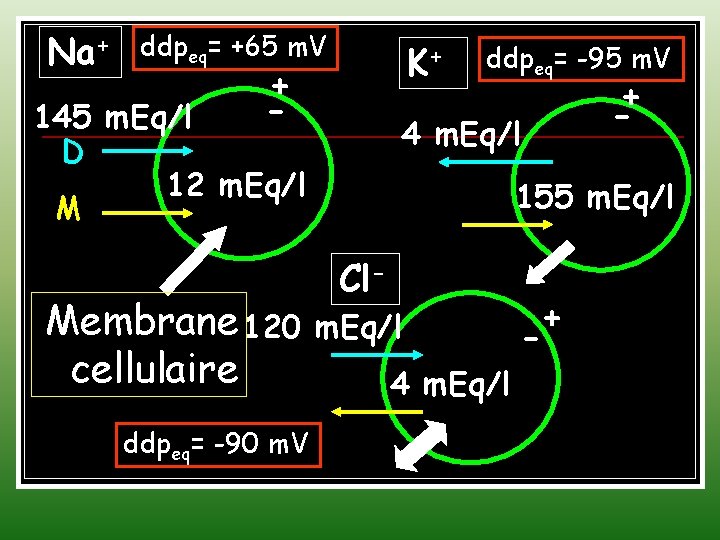
Na+ ddpeq= +65 m. V K+ + - 145 m. Eq/l D 12 m. Eq/l M Membrane 120 cellulaire ddpeq= -90 m. V ddpeq= -95 m. V 4 m. Eq/l + - 155 m. Eq/l Clm. Eq/l 4 m. Eq/l + -

QCM 14 Concernant une membrane de Donnan : A. Pour supprimer l’effet Donnan il suffit de travailler au p. H isoélectrique p. Hi du macro-ion B. On peut rendre l’effet négligeable si on dialyse le macro-ion contre une solution très concentrée d’électrolyte C. L’effet Donnan diminue avec le rapport de Donnan D. La pression osmotique due à l’effet Donnan est maximale si le macro-ion est opposé à de l’eau pure E. Lorsque le p. H de la solution est inférieure au p. Hi la protéine est chargée négativement

QCM 15 Concernant la membrane cellulaire les concentrations ioniques EC et IC en m. Eq/l sont : [Na+]e=140, [K+]e=4, [Cl-]e=120 [Na+]i=12, [K+]i=155, [Cl-]i=4 A. Na+ tend fortement à rentrer dans la cellule B. K+ tend à sortir de la cellule C. Cl- est à l’équilibre D. La perméabilité de Na+ est environ 50 fois celle de K+ E. La constance observée des concentrations ioniques EC et IC s’explique par le transport actif des ions.

QCM 15 Concernant la membrane cellulaire les concentrations ioniques EC et IC en m. Eq/l sont : [Na+]e=140, [K+]e=4, [Cl-]e=120 [Na+]i=12, [K+]i=155, [Cl-]i=4 A. Na+ tend fortement à rentrer dans la cellule B. K+ tend à sortir de la cellule C. Cl- est à l’équilibre D. La perméabilité de Na+ est environ 50 fois celle de K+ E. La constance observée des concentrations ioniques EC et IC s’explique par le transport actif des ions.
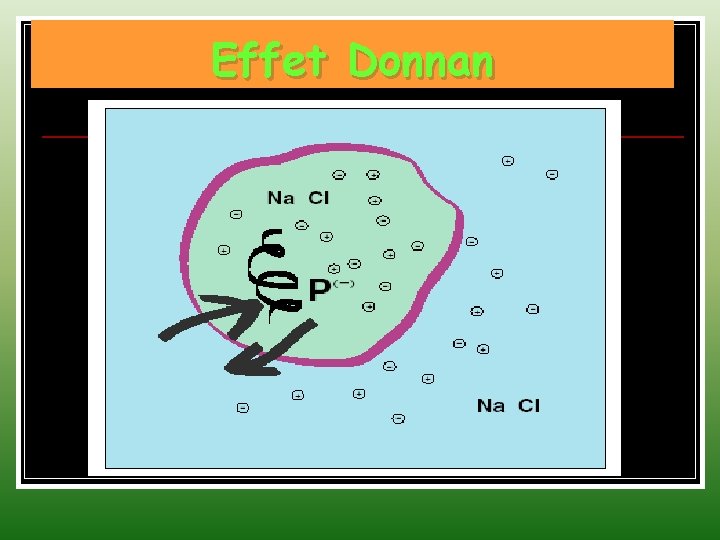
Effet Donnan

QCM 13 Une membrane cellulaire au repos, à 37°C, sépare 2 milieux dans lesquels les concentrations ioniques sont les suivantes: Intra : [Na+]i= 12 mmol/L; [K+]i=150 mmol/L Extra: [Na+]e=140 mmol/L; [K+]e=6 mmol/L Le potentiel de repos est égal à -78, 8 m. V. Le rapport des mobilités u. K/u. Na est de l’ordre de: A. 40 B. 50 C. 60 D. 70 E. Autre réponse

QCM 13 suite A un instant du potentiel d’action, la cellule étant en cours d’activité, le rapport des mobilités devient u. K/u. Na= 20 ( les concentrations sont considérées inchangées). La valeur du potentiel de membrane est de l’ordre de : A. +70, 5 m. V B. +59, 7 m. V C. +52, 7 m. V D. +48, 9 m. V E. Autre réponse
- Slides: 155