EVRE KMYASI I PROF DR GLFEM BAKAN 2018

ÇEVRE KİMYASI - I PROF. DR. GÜLFEM BAKAN 2018 -2019 1

ÇEVRE BİLİMLERİ ve ÇEVRE KİMYASI • Çevre mühendisliği eğitiminde, • Çevre bilimleri altında ağırlıklı olarak, • çevre kimyası ve çevre mikrobiyolojisi çalışılır. Çevre teknolojilerinin geliştirilmesinde temel alınan tüm parametreler ve bunların ölçüm yöntemleri ve bu yöntemlerin geliştirilmesi çevre kimyası ve mikrobiyolojisi içinde yer almaktadır. 2
ÇEVRE KİMYASI ÇEVRE; insanların ve diğer canlıların yaşamları boyunca ilişkilerini sürdürdükleri ve karşılıklı olarak etkileşim içinde bulundukları fiziki, biyolojik, sosyal, ekonomik ve kültürel ortamdır. Çevre Kimyası ; hava, su ve topraktaki kimyasal türlerin yok oluşlarını, etkilenmelerini, değişimlerini, tepkimelerini ve kaynaklarını inceleyen kimya dalıdır. 3

İnsan yaşamı çeşitli dengeler üzerine kurulmuştur. Bu denge insanlığın tarihi boyunca çeşitli etkileşimlerin sonucunda oluşmuştur. İnsanın çevresiyle oluşturduğu doğal dengeyi meydana getiren zincirin halkalarında meydana gelen kopmalar, zincirin tümünü etkileyip, bu dengenin bozulmasına sebep olmakta ve çevre sorunlarını oluşturmaktadır. 4

İnsanların çevre açısından karşıya kaldığı başlıca problemler şöyle özetlenebilir: Hava, su ve toprakların her geçen gün artan oranlarda kirlenmesi ve önemli bir kısmının kullanılamaz hale gelmesi, n Özellikle Büyükşehir ve sanayi bölgelerinin çevre kirliliği sebebiyle yaşanamaz hale gelmesi, n Ozon tabakasının delinmesi, n Yerkürenin giderek ısınması, n Kanser ve benzeri hastalıkların artması, n Doğal kaynakların hızla tüketilmesi, n 5

Hava, su ve toprak çevrenin fiziksel unsurlarını, insan, hayvan ve diğer mikroorganizmalar ise biyolojik unsurlarını teşkil eder. 6
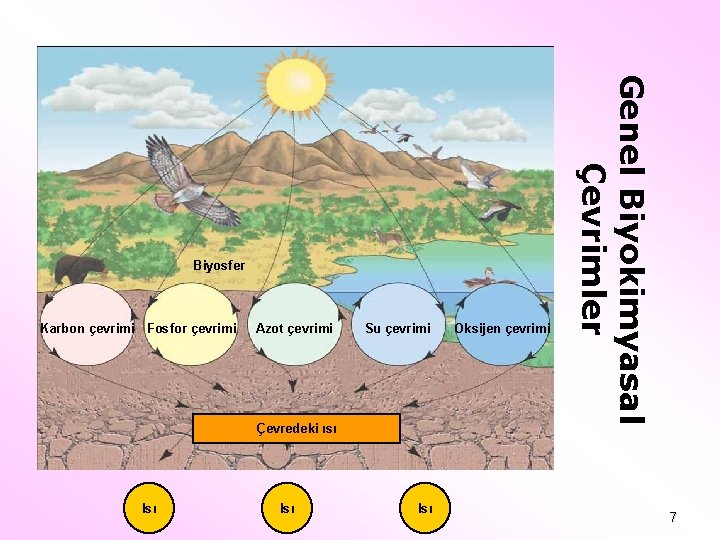
Karbon çevrimi Fosfor çevrimi Azot çevrimi Su çevrimi Çevredeki ısı Isı Isı Oksijen çevrimi Genel Biyokimyasal Çevrimler Biyosfer 7

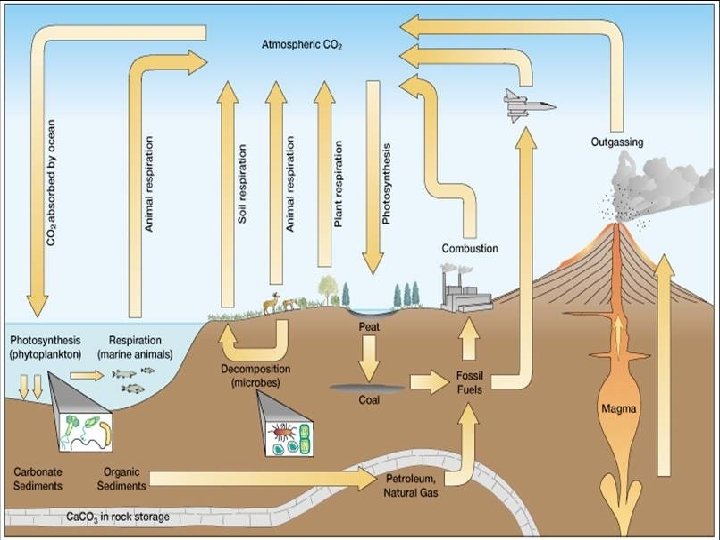
KARBON ÇEVRİMİ 8
9
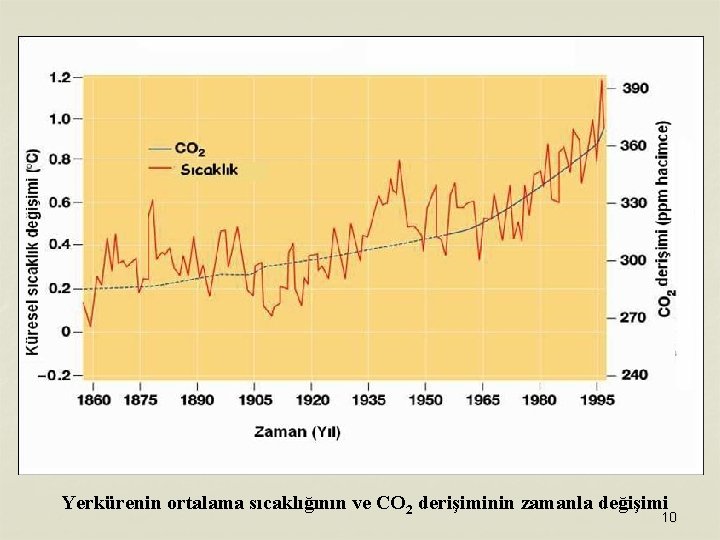
Yerkürenin ortalama sıcaklığının ve CO 2 derişiminin zamanla değişimi 10

P ÇEVRİMİ 11
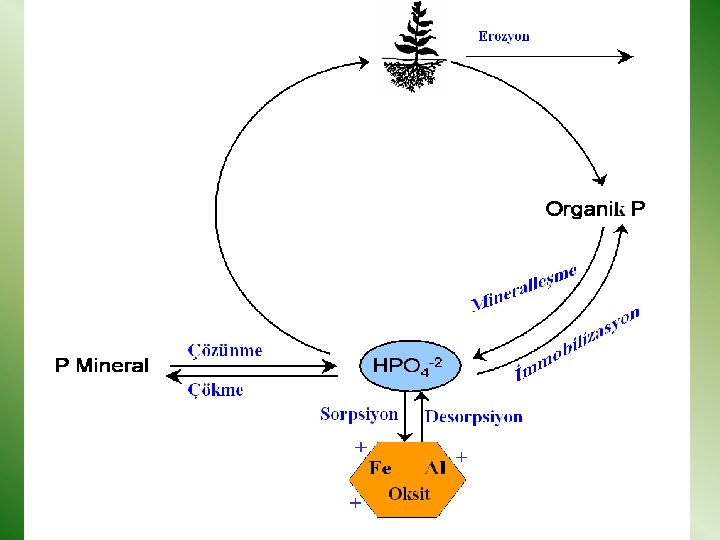
12
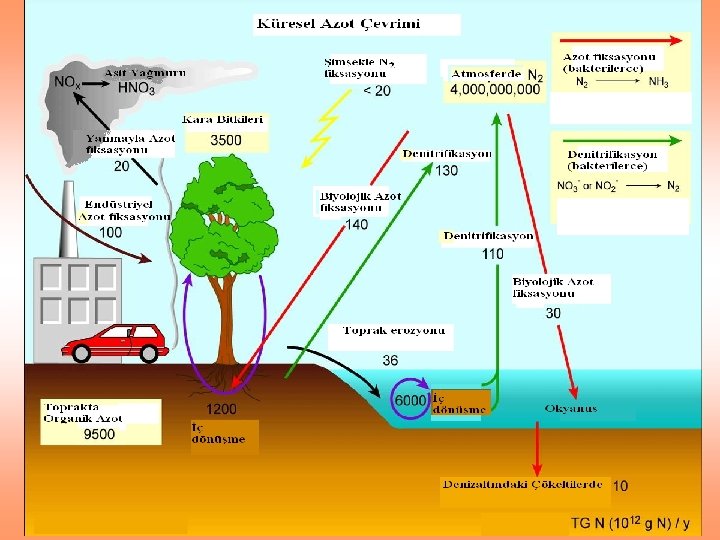
13
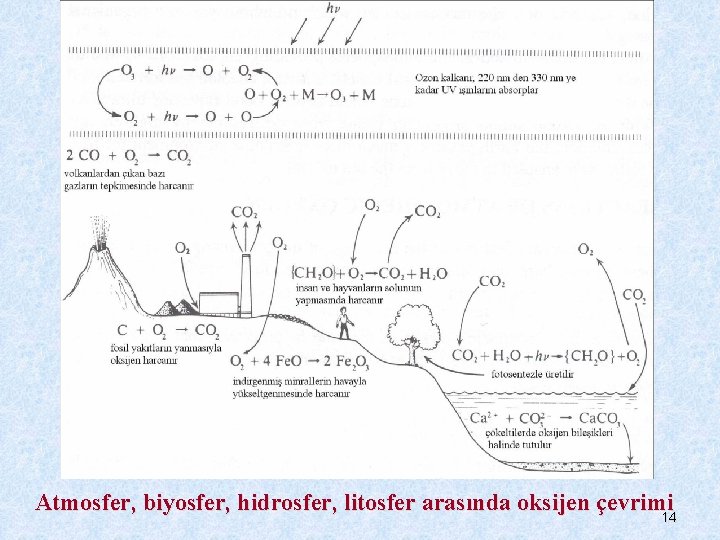
Atmosfer, biyosfer, hidrosfer, litosfer arasında oksijen çevrimi 14 14
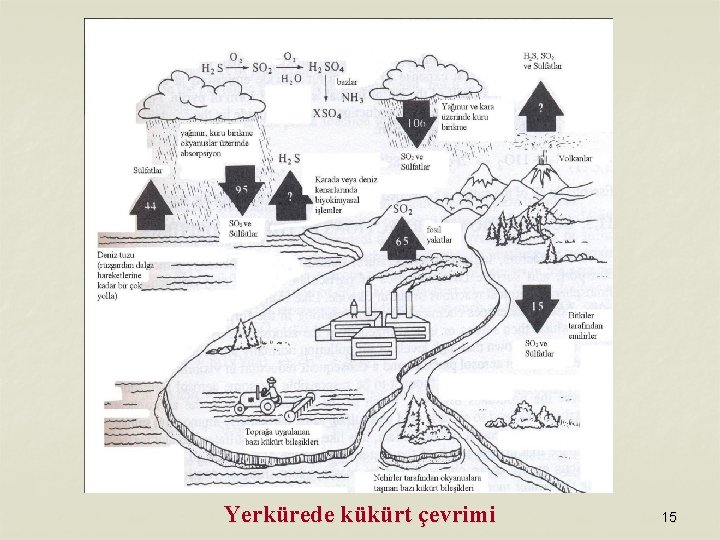
Yerkürede kükürt çevrimi 15

Çevre Kimyası Özde su, hava, toprak ve canlılarla, bu kesimlerin birbirleriyle etkileşimlerini inceleyen kimya dalı olarak tanımlanır. Klasik kimya ölçümlerinde, ölçüm örneği seçilen ölçüm yöntemine uygun olarak hazırlanıp uyarlanırken, çevresel kimya işlemlerinde, ölçüm yöntemi eldeki örneğe uyarlanmak zorundadır. 16

17

Çevre kimyasında ölçülecek parametreler için alınacak numunelerde, Numune alma zamanı, Numune alma yeri, Numune alma sıklığı ve numune sayısı, Seçilecek ölçüm yöntemleri ve hata düzeyleri, (çoğunlukla çevre kimyasında mg/l yada µg/l seviyesinde ölçümler) 18

Böylece sularda ölçüm planlamasına girişenler, Amaca yarayacak yeterli sayıdaki numuneyi, Amaca yararlı duyarlılık düzeyinde, yürüttüklerinde yeterli faydalı bilgi sahibi olacaklardır. 19

Örnek Alma ve Saklama Koşulları “ Su Kirliliği Kontrolü Yönetmeliği” uyarınca, su ortamında kalitenin belirlenmesi, evsel ve endüstriyel atıksuların atıksu altyapı tesislerine boşaltımında veya alıcı ortamlara deşarjda atıksulardan ve/veya su ortamlarından sürekli veya aralıklı olarak su örneklerinin alınması ve Yönetmelikte denetimi istenen kalite parametrelerinin ölçülmesi gerekmektedir. 20

Bu örneklerde yapılacak analizler için sürekli veya aralıklı örnek alma esaslarını ve kullanılabilecek analiz metodlarını tanıtma amacı ile “ Numune Alma ve Analiz Metodları Tebliğ” hazırlanmıştır. 21

Çevre Mevzuatının, Su Kirliliği Kontrolü Yönetmeliğinin ilgili bu tebliğinden “ Numune Alma ve Analiz Metodları “ ile ilgili gerekli ayrıntılı bilgiler edinilebilir. Burada ise, 1. örnek almada dikkat edilecek noktalar, 2. örnek alma esasları, 3. örnek alma teknikleri ve çeşitleri 4. hakkında kısa bilgiler verilmektedir. 22

n n n Öncelikle, çevre konusunda alınan örneklerin, tanımlayıcı ve geçerli olması gerekir. Örneğin tanımlayıcı olması, ölçülecek parametrelerin ölçüm yeri için tanımlayıcı veriler üretebilecek şekilde örnek alınması olarak tanımlanır. Örneklerin geçerli olması ise, ölçüm anında örnek alınan noktanın özelliklerini kaybetmeden taşıyacak şekilde örnek alınması, şeklinde tanımlanır. 23

Örneğin tanımlayıcı özelliği, Ø Örnek noktasının yanlış seçilmesi, Ø Ölçüm kabının yapısı ve temizliğinin yeterli olup, olmamasına göre değişebilir. 24

Örneğin geçerliliği ise, Ø Örnek kabından alınan ara örneğin yanlış alınması, Ø Örnek laboratuara getirilirken içinde gelişen bazı reaksiyonlar sonucu özelliğinin bozulması veya örnek yapısına bağlı olarak (örneğin endüstriyel toksik atıksu gibi) içinde farklı reaksiyonların oluşmasından değişebilir. 25

Örnek almanın amacı analiz edilecek su kütlesinin küçük bir hacimde temsil edilmesidir. Bu nedenle; 1) Laboratuara kolayca taşınabilecek yeterli miktarda örnek alınması, 2) Su kütlesine ait özelliklerin alınan örnekte de aynı olması ( örneğin tanımlayıcı olması) , 3) Örneğin testten önce bileşimi bozulmayacak şekilde laboratuara getirilmesi ( örneğin geçerli olması) gerekmektedir. 26

Ancak bu koşullarda, laboratuarda analiz edilen örnekte ölçülen parametreler, • eğer istenen hassasiyet ve duyarlılık seviyesinde de ölçüm yapılmışsa, • başta belirlenen amaca yarar bilgileri sağlayacak ve • analizci bu ölçüm sonuçlarını kullanarak ölçüm yapılan yer için doğru kararlar verebilecektir. 27

Toplanan her bir örnek için, örnek alma kabı üzerinde gerekli açıklamaların yazılacağı bir etiket olmalıdır. Örneğin daha sonra laboratuara getirildiğinde kolayca tanınabilmesi için örneğin alanın adı, alındığı tarih ve saat, örneğin alındığı yer, suyun sıcaklığı, su seviyesi, debi, hava koşulları vb. bilgiler kaydedilmelidir. 28

Basınç altında toplanmış sıcak örnekler, basınç altında korunmalı ancak ölçümden önce soğutulmalıdır. Su dağıtım sistemlerinden örnek almadan önce, suyun iyi bir şekilde temsil edilebilmesi için bir süre akıtılması gerekir. Suyun ne kadar akıtılacağı borunun çapı, uzunluğu ve suyun akış hızı ile ilgilidir. 29

Kuyulardan numune alınırken; örneğin yeraltı suyunu temsil ettiğinden emin olmak için pompa ile bir süre su çekilir ve daha sonra numune alınır. Akarsulardan numune alındığında, analitik değerler; derinlik, akış hızı, kıyıdan mesafe vb. ölçülür. Eğer cihaz varsa, su derinliğinin orta değerinden numune alınır. Göller ve rezervuarlar; mevsimsel tabakalaşma, yağmurlar, taşmalar ve rüzgar gibi nedenlerle kalite değişimlerine maruz kalırlar. 30

Dolayısıyla, örnek alınan yerdeki koşullar, çalışmanın amacı, örnek sayısını, yerini ve sıklığını belirlemede önemli kriterlerdir. Genellikle, su kütlesinin bütününü tanımlamak için dört mevsim değişimi sergileyecek sıklıkta, belirlenecek optimum sayıda örnek, amaca uygun yerlerden rutin olarak toplanmalıdır. 31

Örnek alma şekilleri ve örnek alma sıklığı, amaca ve örneğin alındığı kaynağa göre farklılıklar gösterir. Belli zamanda ve belli bir yerden örnek alındığında bu örnek sadece o yeri ve zamanı temsil eder. Bununla beraber, bileşiminde zamanla büyük değişiklik göstermeyen kaynaklardan alınan örnekler, daha uzun bir zaman periyodunu veya daha büyük bir hacmi temsil eder. Kaynağın zamana bağlı olarak büyük ölçüde değiştiği durumlarda, uygun zaman aralıklarında alınan numuneler ayrı analiz edilirler. Böylece bu değişimin frekansı, süresi, büyüklüğü belirlenir. Değişimlerin beklendiği zaman periyoduna göre numune alma aralığı seçilir. 32

Ani, özel, değişken veya düzensiz deşarjların ve işlemlerin olduğu tesislerde, bu tür deşarjların içinde bulunduğu periyodu temsil eden kompozit (karışık) örneklerin hazırlanması gerekir. Bu da evsel ve endüstriyel atıksularda belirli zaman aralıklarında atıksu debisi ile orantılı olarak alınan karışık örneği tanımlar. Kompozit örnekler çok sayıda örneğin analizi yerine ortalama özellikle bir tek numune ile çalışmaya olanak verir. 33

Özelliklerinde ve miktarlarında zamanla değişim gösteren parametrelerin analizlerinde kompozit örnekler kullanılmamalıdır. Bu gibi analizlerin, örnek alma noktasında ve/veya toplanan örneklerde hemen yapılması gerekir. Tüm çözünmüş gazların analizleri, kalıntı klor, çözünmüş sülfür, sıcaklık, p. H tayinleri ve mikrobiyolojik analizler bu kapsamdadır. 34

Eğer örnek alma sırasında bazı koruyucu maddeler ilave edilecekse, bunlar en başından örnek kabına konur ve kompozit örnek bu kapta hazırlanır. Genişlik ve derinliğe bağlı olarak suyun bileşiminin çok değiştiği nehirlerde ve akarsularda; Çok çeşitli ve ayrık atıksu akımlarının birlikte arıtılmasının önerildiği durumlarda; Farklı örnek alma noktalarından alınan örneklerin karışımının analizi gereklidir. Ancak, doğal sularda çoğunlukla yerel değişimler, toplam veya ortalama değerlerden çok daha önemli olduğu için örneklerin ayrı alınıp incelenmesi gerekir. 35

u Bazı örnekler bir defa alınır, bu örneklere ”Grab Örnek" denir. temsil eder. Grab örnekler ayrı, karıştırılmadan analiz edilir. Bir kez alınan grab örnekler şu koşullarda yeterli olabilir: 1. Su kalitesi uniform olan bir derin kuyudan bir kez örnek alınması, 2. Su kalitesindeki değişimi yavaş olan büyük su kütlelerinden, günde bir kez örnek alınması , 3. 24 saat içinde su kütlesi değişimi belirgin olan büyük su kütlelerinden düzgün aralıklarla birer kez alınan örnekler. 36

Örneklerin saklanmasında genelde dikkat edilmesi gerekmektedir: şunlara v 37

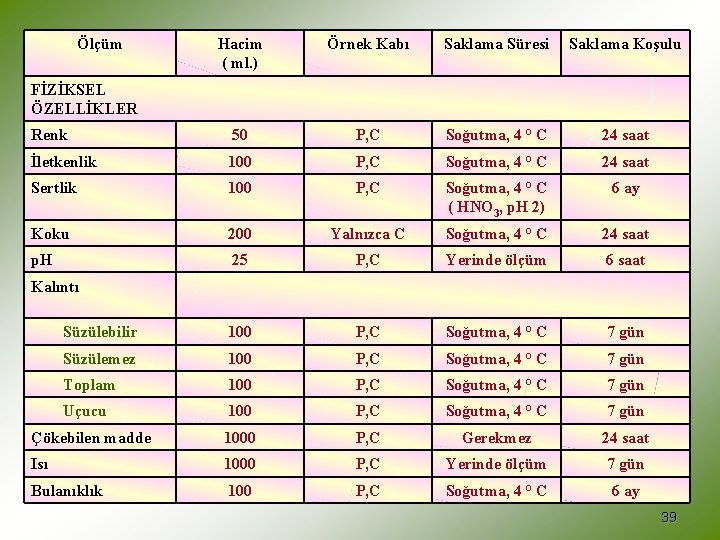
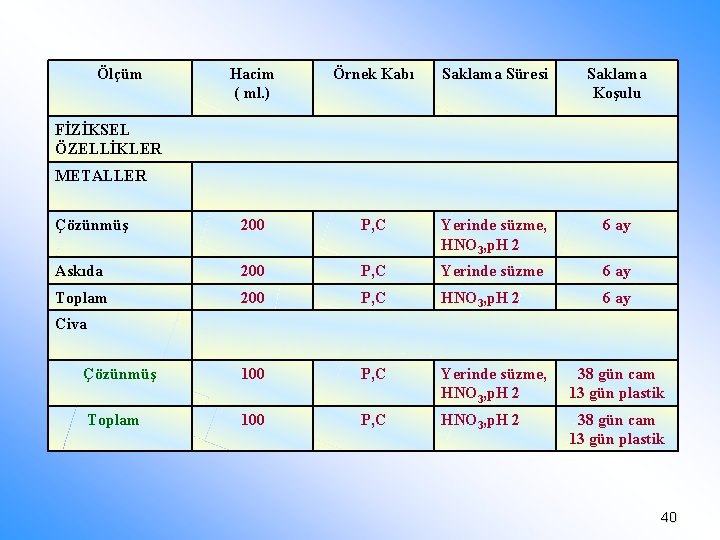
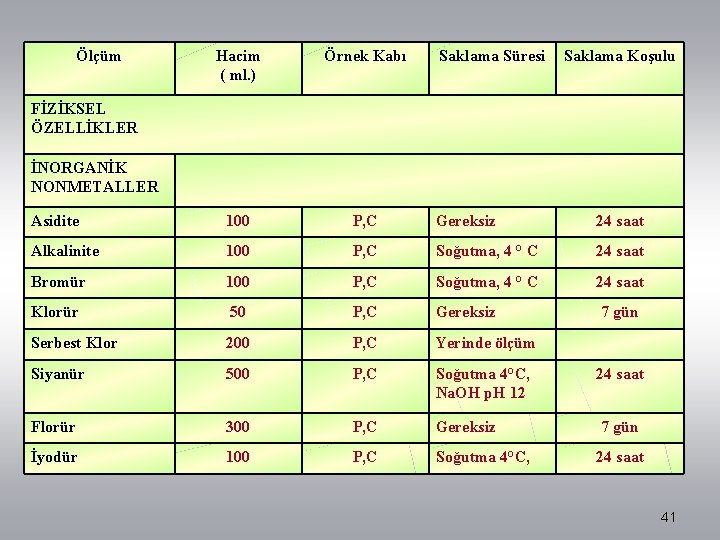
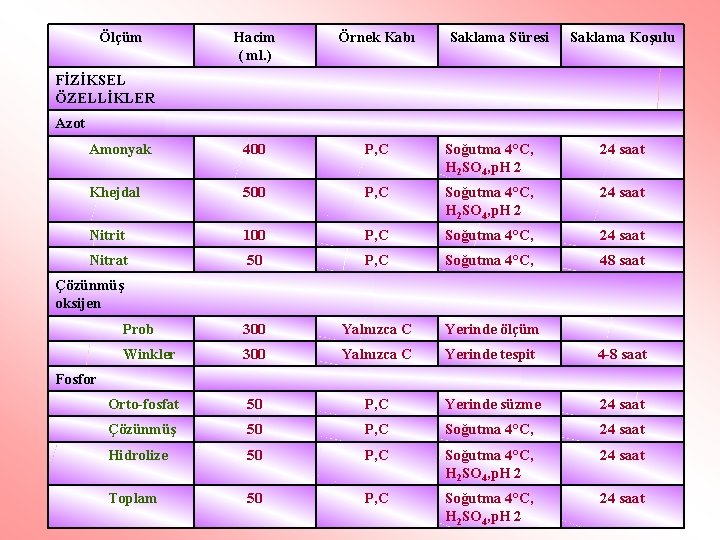
n n Sulardan alınabilecek örnekler ve bu örneklerde uygulanacak genel saklama yöntemleri Tabloda sunulmaktadır. Tablodan açıkça görüleceği üzere örnek saklama yöntemlerinden biri de uygun kimyasal maddelerin analiz öncesi örneğe katılışıdır. Bu noktada, kullanılan ve örneğe katılan her maddenin, örnekte ölçülen determinanta etkisinin tartışma konusu edilmesi ve ayrıca şahit örnekler, standart ilaveler yöntemi vb. analitik özellikler ile ölçülmesi gereklidir. 38
Ölçüm Hacim ( ml. ) Örnek Kabı Saklama Süresi Saklama Koşulu Renk 50 P, C Soğutma, 4 ° C 24 saat İletkenlik 100 P, C Soğutma, 4 ° C 24 saat Sertlik 100 P, C Soğutma, 4 ° C ( HNO 3, p. H 2) 6 ay Koku 200 Yalnızca C Soğutma, 4 ° C 24 saat p. H 25 P, C Yerinde ölçüm 6 saat Süzülebilir 100 P, C Soğutma, 4 ° C 7 gün Süzülemez 100 P, C Soğutma, 4 ° C 7 gün Toplam 100 P, C Soğutma, 4 ° C 7 gün Uçucu 100 P, C Soğutma, 4 ° C 7 gün Çökebilen madde 1000 P, C Gerekmez 24 saat Isı 1000 P, C Yerinde ölçüm 7 gün Bulanıklık 100 P, C Soğutma, 4 ° C 6 ay FİZİKSEL ÖZELLİKLER Kalıntı 39
Ölçüm Hacim ( ml. ) Örnek Kabı Saklama Süresi Saklama Koşulu Çözünmüş 200 P, C Yerinde süzme, HNO 3, p. H 2 6 ay Askıda 200 P, C Yerinde süzme 6 ay Toplam 200 P, C HNO 3, p. H 2 6 ay Çözünmüş 100 P, C Yerinde süzme, HNO 3, p. H 2 38 gün cam 13 gün plastik Toplam 100 P, C HNO 3, p. H 2 38 gün cam 13 gün plastik FİZİKSEL ÖZELLİKLER METALLER Civa 40
Ölçüm Hacim ( ml. ) Örnek Kabı Saklama Süresi Saklama Koşulu Asidite 100 P, C Gereksiz 24 saat Alkalinite 100 P, C Soğutma, 4 ° C 24 saat Bromür 100 P, C Soğutma, 4 ° C 24 saat Klorür 50 P, C Gereksiz Serbest Klor 200 P, C Yerinde ölçüm Siyanür 500 P, C Soğutma 4°C, Na. OH p. H 12 Florür 300 P, C Gereksiz İyodür 100 P, C Soğutma 4°C, FİZİKSEL ÖZELLİKLER İNORGANİK NONMETALLER 7 gün 24 saat 41
Ölçüm Hacim ( ml. ) Örnek Kabı Saklama Süresi Saklama Koşulu Amonyak 400 P, C Soğutma 4°C, H 2 SO 4, p. H 2 24 saat Khejdal 500 P, C Soğutma 4°C, H 2 SO 4, p. H 2 24 saat Nitrit 100 P, C Soğutma 4°C, 24 saat Nitrat 50 P, C Soğutma 4°C, 48 saat Prob 300 Yalnızca C Yerinde ölçüm Winkler 300 Yalnızca C Yerinde tespit 4 -8 saat Orto-fosfat 50 P, C Yerinde süzme 24 saat Çözünmüş 50 P, C Soğutma 4°C, 24 saat Hidrolize 50 P, C Soğutma 4°C, H 2 SO 4, p. H 2 24 saat Toplam 50 P, C Soğutma 4°C, H 2 SO 4, p. H 2 24 saat FİZİKSEL ÖZELLİKLER Azot Çözünmüş oksijen Fosfor 42
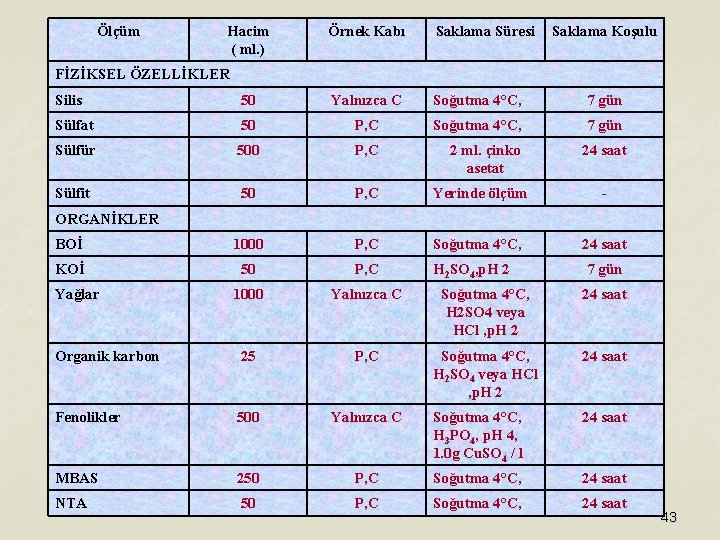
Ölçüm Hacim ( ml. ) Örnek Kabı Saklama Süresi Saklama Koşulu FİZİKSEL ÖZELLİKLER Silis 50 Yalnızca C Soğutma 4°C, 7 gün Sülfat 50 P, C Soğutma 4°C, 7 gün Sülfür 500 P, C 2 ml. çinko asetat Sülfit 50 P, C Yerinde ölçüm - BOİ 1000 P, C Soğutma 4°C, 24 saat KOİ 50 P, C H 2 SO 4, p. H 2 1000 Yalnızca C Soğutma 4°C, H 2 SO 4 veya HCl , p. H 2 24 saat Organik karbon 25 P, C Soğutma 4°C, H 2 SO 4 veya HCl , p. H 2 24 saat Fenolikler 500 Yalnızca C Soğutma 4°C, H 3 PO 4, p. H 4, 1. 0 g Cu. SO 4 / l 24 saat MBAS 250 P, C Soğutma 4°C, 24 saat NTA 50 P, C Soğutma 4°C, 24 saat ORGANİKLER Yağlar 7 gün 43

Bildiğiniz gibi, toplumların endüstrileşmesiyle birlikte doğaya yapay sentetik maddeler atılmaya başlanmıştır. Genellikle alıcı ortam dediğimiz toprak ve yüzey suları doğal atıkları kolayca asimile edip, mikroorganizmalar aracılığı ile son ürünlere dönüştürebilir. Ancak bu dönüşümünde bir sınırı vardır ve kirlenme hızı mikroorganizmal asimilasyon hızının üzerine çıkacak olursa atıklar doğada birikmeye başlamakta ve çevre kirlenmesine neden olmaktadır. 44

SUYUN YAPISI, KİMYASI VE ÇEVRE KİMYASINDAKİ ÖNEMİ Yeryüzünü saran ve okyanuslarda, denizlerde, göllerde, akarsularda ve yeraltısularında bulunan sularla atmosferdeki su buharının tümüne hidrosfer (su küresi) adı verilir. 45
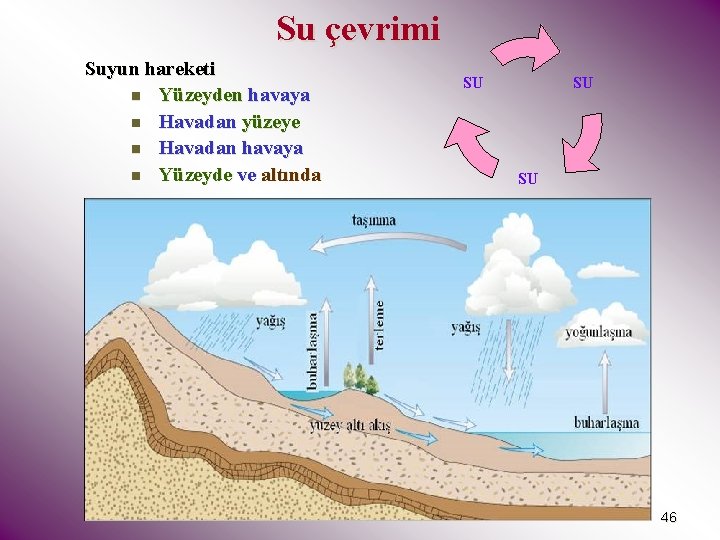
Su çevrimi Suyun hareketi n Yüzeyden havaya n Havadan yüzeye n Havadan havaya n Yüzeyde ve altında SU SU SU 46

Suyun Fiziksel Özellikleri 47

Su renksiz ve kokusuzdur. Suları renkli gösteren içerdikleri maddelerdir. Geçiş metallerinden özellikle Fe; Mn ve Cr bileşiklerinin suda bulunması suyun renkli görünmesine neden olur. Suyun kokusu ve tadının kaynağı sularda çözünen inorganik, organik maddeler ile mikroorganizmalardır. İçme sularında koku istenmez ancak lezzet istenir. Genellikle amonyak, sülfürler siyanürler, fenoller, serbest klor, petrol atıkları, bitki ve hayvani atıklar suya hoş olmayan kokular verir. 48

İçme sularında bulanıklık istenmez, berrak olması istenir. Ayrıca yerüstü sularında bulanıklık güneş ışınlarının suların alt kısımlarına ulaşmasını engeller. Suların çözünen madde miktarının fazlalığı iletkenlikle doğru orantılıdır. Maden suları iletkenlikleri en fazla sulardandır. Suyun +4°C de ki yoğunluğu 1 g/ml dir. Su donunca yoğunluğu azalır. 0, 9 g/ml olur. Bu da buzun neden suyun üzerinde yüzdüğünü açıklar. 49

Suyun Kimyasal Özellikleri 50

n n n Doğal suların p. H değerleri içerdikleri maddelere göre değişir. Normal suların p. H sı genellikle 6, 5 – 7, 5 arasında değişir. Asit yağmurlarında p. H nın 2, 3 e düştüğü görülmüştür. Yeraltı sularında CO 3 -2, HCO 3 -2, CO 2 daha fazla çözündüğünden p. H yı da bunlar belirler. Ayrıca sularda çözünmüş Fe+2, Mn+2, Cr+3 iyonları sulara asitlik sağlar. 51
Sularda Mg+2 ve Ca+2 iyonları sertliğe neden olur. Suların sertliği FS: 10 mg Ca. CO 3 /L, AS: 10 mg Ca. O /L olarak birimlendirilir. Sularda ana bileşen olarak Ca+2, Na+; Mg+2; K+, Cl-, SO 4 -2, HCO 3 - iyonları bulunur. Ayrıca Fe, Cu+2, Mn, Ni, Zn, Co, Cd, Cr, Pb, Hg, Be; Al, As, Se, Rb, Li, I, PO 4 -3, NO 3 -, B, CN-, H 2 S, Pestisitler eser miktarda bulunabilir. 52

Su doğada katı, sıvı ve gaz olmak üzere her üç fazda da bulunur (buz, su ve su buharı). Bilinen tüm sıvılar içinde en yüksek yüzey gerilimine sahiptir. (20 °C ‘de 0. 0728 N/m 2) Bu özelliği, yağmur damlacıklarının oluşumu açısından önem taşımaktadır. Yine tüm sıvılar içinde suyun buharlaşma ısısı en yüksektir. 53

Su, amonyaktan sonra en yüksek erime ısısına (0 °C) sahip olan bileşiktir. Yüksek özgül ısısıyla birlikte bu özellikler, suyu yeryüzündeki iklimsel farklılıkların belirleyici unsuru durumuna getirir. 54
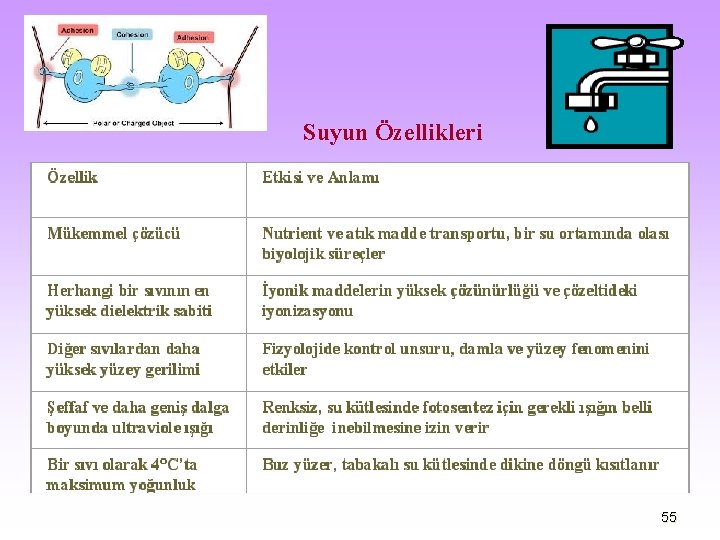
Suyun Özellikleri 55

56

57

Yeryüzünde bulunan toplam su miktarı yaklaşık 1. 600. 000 x 1023 km 3 su veya 54 x 1045 su molekülüdür (H 2 O). Bunun 220 000 x 1023 km 3' ü kimyasal olarak bağlı sudur, geriye kalan 1 380 000 x 1023 km 3 su ise serbest sudur. 58

Ancak toplam su miktarının %97. 6 'sı denizlerdeki tuzlu sulardır ve bu sular insanların gereksinimlerini karşılamak açısından uygun niteliklere sahip değildir. Karalardaki toplam su miktarı, yeryüzündeki suların %2. 4 'ünü oluşturmaktadır. 59

n Karalardaki suyun ancak %10 'u kadarı teorik kullanılabilir tatlı su potansiyelini oluşturmaktadır (3 4 milyon km 3). Bu miktar yeryüzündeki toplam su potansiyelinin %0. 3 'ü kadardır. n Nüfusla birlikte gelecekte artacak olan su gereksinmesinin karşılanmasının giderek daha büyük boyutlarda sorunlar yaratacağını ortaya koymaktadır. Ancak susuz yaşam mümkün değildir. n İnsan gıda almadan haftalarca yaşayabilir, fakat su içmeden ancak birkaç gün yaşamını sürdürebilir. Bu yüzden içme ve kullanma suyu sürekli ve güvenilir şekilde temin edilebilmelidir. 60

Suyun Fiziksel ve Kimyasal Özellikleri Kimyasal formülü H 2 O olan su, ağırlıkça % 11. 1 hidrojen ve % 88. 9 oksijenden meydana gelir. Bu iki elementin birbiriyle olan reaksiyonu ekzotermiktir. H 2 + ½ O 2 → H 2 O Renksiz, kokusuz ve tatsız olan su, H 2 O, tüm canlıların yaşamı için gereklidir ve kimyasal çözeltilerde geniş olarak kullanılır. 61

Erime noktası 0°C (32 ° F ) Kaynama noktası 100 °C (212 ° F ) Özgül ağırlığı (4 ° F ) 'de 1. 000, Galon başına ağırlığı (15 °F )'de 8. 337 lb. (pound) Suyun farklı değişik formları vardır; örneğin-yağmur. Ayrıca, farklı su kütleleri vardır; örneğin-deniz, göl, nehir. 62

Genelde, su moleküler ağırlığı 18'dir. Ancak H ve O 'nin her birinin 3 izotopu vardır ve su için 18 değişik mümkün olabilen moleküler ağırlık mevcuttur. Su moleküllerinde 2 hidrojen atomu aynı tarafta yer alarak bu tarafın pozitif yük oluşuna neden olur, oksijen atomu ise negatif yükle yüklüdür. 63

Yüklerin bu şekilde dağılımı, suyu kuvvetli bir dipolar (iki kutuplu) moleküler haline getirir. Su molekülleri birbirini çeker ve hidrojen bağları yardımıyla kümeleşme olur. Sudaki hidrojen bağları, suyun pek çok olağan dışı özelliklerinin sorumlusudur. Su, periyodik çizelgedeki oksijene benzer diğer maddelerin dihüdrürleriyle kıyaslandığında büyük farklılıklar gösterdiği görülür. 64

Su Molekülü n n n Su molekülü bir oksijen atomuna bağlanan iki hidrojen atomundan oluşur. Bu üç atom düz bir sıra oluşturmak yerine yukarıda gösterildiği şekilde 105 ’lik açı teşkil ederler. Bu eğik yapı ve oksijen atomunun hidrojen atomlarına göre negatif elektronları daha kuvvetli etkilemesinden dolayı su molekülü her iki ucunda zıt elektrik taşıyan bir dipol gibi davranır. 65
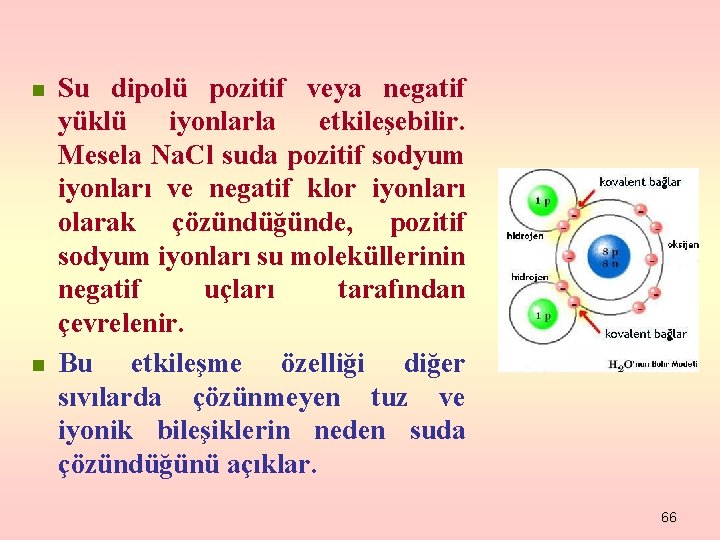
n n Su dipolü pozitif veya negatif yüklü iyonlarla etkileşebilir. Mesela Na. Cl suda pozitif sodyum iyonları ve negatif klor iyonları olarak çözündüğünde, pozitif sodyum iyonları su moleküllerinin negatif uçları tarafından çevrelenir. Bu etkileşme özelliği diğer sıvılarda çözünmeyen tuz ve iyonik bileşiklerin neden suda çözündüğünü açıklar. 66
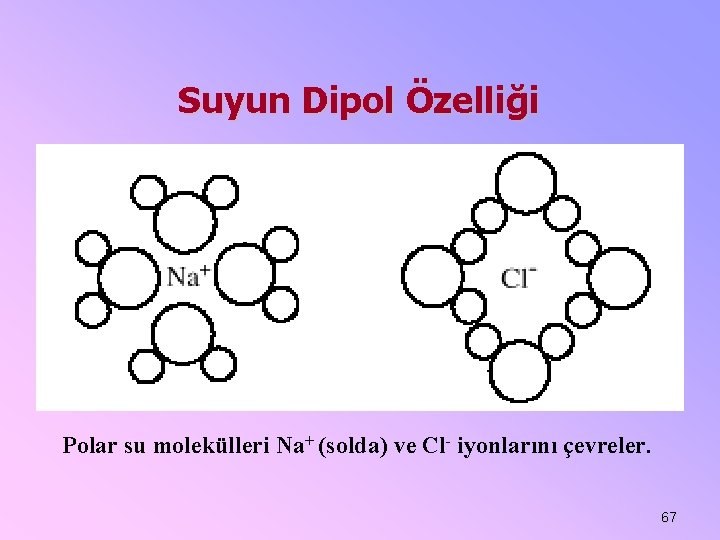
Suyun Dipol Özelliği Polar su molekülleri Na+ (solda) ve Cl- iyonlarını çevreler. 67
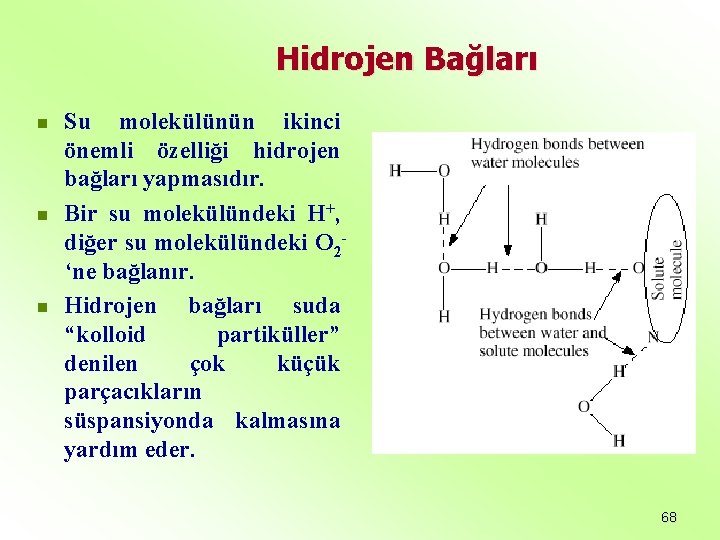
Hidrojen Bağları n n n Su molekülünün ikinci önemli özelliği hidrojen bağları yapmasıdır. Bir su molekülündeki H+, diğer su molekülündeki O 2‘ne bağlanır. Hidrojen bağları suda “kolloid partiküller” denilen çok küçük parçacıkların süspansiyonda kalmasına yardım eder. 68

Atmosferik basınç ve oda sıcaklığında (25° C) , daha ağır moleküller örneğin H 2 S (m. a. 30), H 2 Se (m. a. 81) ve H 2 Te (m. a. 130) tümü gaz halinde iken su sıvı olup ancak sıcaklık 100 °C 'ye çıkarıldığında gazlaşmaktadır. Herhangi bir sıcaklıkta su benzerlerinden daha yoğundur ve maksimum yoğunluğu 4 °C 'dedir. Yüzey gerilimi ve dielektrik sabiti, diğer dihüdrürlerle kıyaslandığında çok büyüktür. Donma noktası beklenenden çok daha düşük olup, donduğunda daha az yoğun bir yapı oluşturur. Tüm bu özellikler, sudaki hidrojen bağlarından kaynaklanmaktadır. 69

Yüzey gerilimi ve dielektrik sabiti, diğer dihüdrürlerle kıyaslandığında çok büyüktür. Donma noktası beklenenden çok daha düşük olup, donduğunda daha az yoğun bir yapı oluşturur. Tüm bu özellikler, sudaki bağlarından kaynaklanmaktadır. hidrojen 70

Eğer katı su, sıvı sudan daha yoğun olsaydı; doğal sularda, buz yüzeyde değil, dipte oluşurdu. Ve göller, örneğin, aşağıdan yukarı doğru donardı ve sucul (aquatik) sistemlerden olan yaşam olmazdı ve bu sular suyun donma derecesinin altına düşer düşmez donardı. 71

Suyun çözücü özelliklerini belirlemekte su polaritesinin önemi büyüktür. Yeryüzünün katı kütlesinde bulunan mineraller, genelde inorganik katılardır ve pozitif değerlikli ve negatif değerlikli iyonlar lattice yapısındadırlar; birbirlerine elektrostatik bağlarla bağlanırlar. 72

Su, dipolar karakterleriyle, pozitif değerlikli bir iyonu, molekülünün negatif değerlikli kısmıyla sarar (veya tam tersi), böylece bu iyon çevresindeki iyonlardan izole olur ve kristal yapısının integrasyonunu sağlayan itme güçlerini nötralize eder. Böylece bu iyon; su molekülleri tarafından sarılan veya hidrat olan; kristal yapısını bırakır ve solüsyona geçer, böylece çözünmüş iyon olur. Su, az veya çok temas haline geçtiği her katıyı veya gazı biraz çözer. 73

Dünyadaki, global su çemberinde (hidrolojik çember), su, atmosferdeki gazlarla temas halindedir (ki bunların içinde hava kirleticileri ve volkanik emisyonlarda vardır) ve ayrıca yeryüzü kütlesinin ilk birkaç km' sindeki minerallerle de temas halindedir. 74

Küçük ölçekte ise, su, tüm insan yapımı sistemlerin çevresindedir (kanallar, sentetik minerallerden yapılmış borular; örneğin, beton veya rafine metaller, demir , bakır, gibi ). Suyun çözücü özelliği bu sistemlerde korozyon ve kireçlenme gibi problemlere neden olurlar. 75
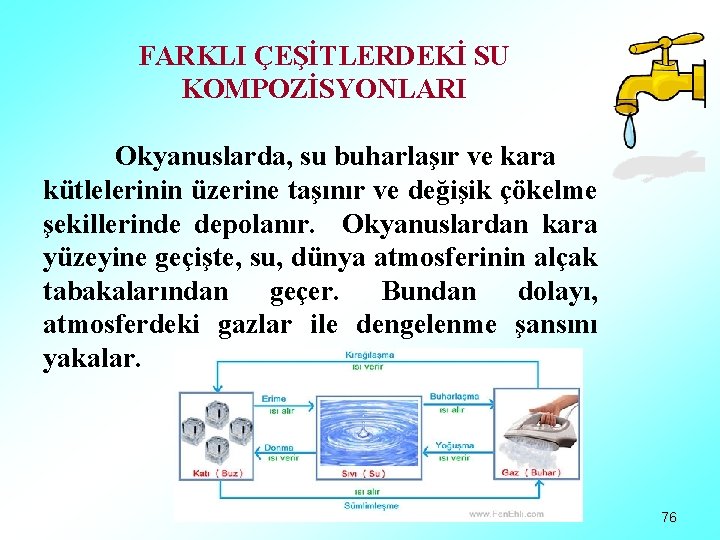
FARKLI ÇEŞİTLERDEKİ SU KOMPOZİSYONLARI Okyanuslarda, su buharlaşır ve kara kütlelerinin üzerine taşınır ve değişik çökelme şekillerinde depolanır. Okyanuslardan kara yüzeyine geçişte, su, dünya atmosferinin alçak tabakalarından geçer. Bundan dolayı, atmosferdeki gazlar ile dengelenme şansını yakalar. 76
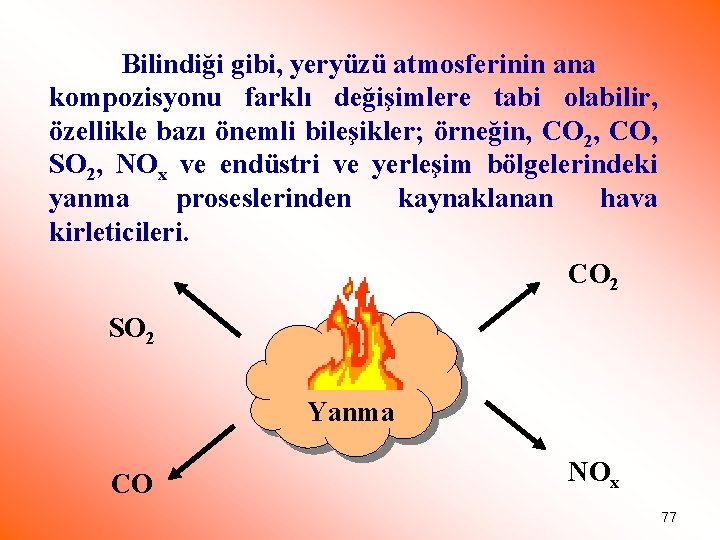
Bilindiği gibi, yeryüzü atmosferinin ana kompozisyonu farklı değişimlere tabi olabilir, özellikle bazı önemli bileşikler; örneğin, CO 2, CO, SO 2, NOx ve endüstri ve yerleşim bölgelerindeki yanma proseslerinden kaynaklanan hava kirleticileri. CO 2 SO 2 Yanma CO NOx 77

Atmosferin ana bileşikleri N 2 ve O 2, suda belirli bir ölçüde çözünür ancak bazı minor bileşikler örneğin CO 2 ve SO 2 suda çok çözünürler. Böylece çökeltinin ( yağışın ) kompozisyonu çok değişken ve atmosferik kirleticiler tarafından etkilenebilir durumdadırlar. 78

Okyanus yakınındaki yağışlarda daha çok SO 4 -2, Cl-, Na+ ve Mg+2 iyonları bulunur. İçinde, çok fazla yanmadan kaynaklanan SO 2 içeren, atmosfer ortamlarında oluşan yağmur ve kar kütleleri genelde asidiktir. 79

Kirlenmemiş bir yağışın p. H'sı 5. 5 - 6. 5 civarındadır ki bu p. H, yağışın kaynaklandığı deniz suyu p. H'sından daha düşüktür. Bu, atmosferdeki CO 2 ile denizden yükselen su kütlesinin denge durumunun yağışa yansımasıdır. 80

Ancak yağmur suyunun tampon özelliği düşük olduğundan, asit üreten gazlarla karşılaştığında kendisinin bu nötr p. H özelliğini saklayamaz. Yağmur suyunun asiditesi kayalardaki bazları titre ederler. Okyanuslarda bu reaksiyonun tersi olur ve dibindeki kayalar dikkate alınmalıdır. 81

Okyanusun dibindeki; katyonlar, bikarbonat iyonları ve çözünmüş silika ve kil mineralleri, yeni kayaların oluşumunu sağlayan reaksiyonlara neden olurlar. Dolayısıyla okyanustaki bu iyonların (Si. O 2, K+, CO 3 -) konsantrasyonları, bu reaksiyonlarda etkilidir. 82

Bu reaksiyonların, okyanus p. H'sını 8. 0 civarında tutmayı sağladığı düşünülmektedir. Ayrıca, bu reaksiyonlar atmosferdeki CO 2 içeriğini de dengelemeye yarar. 83
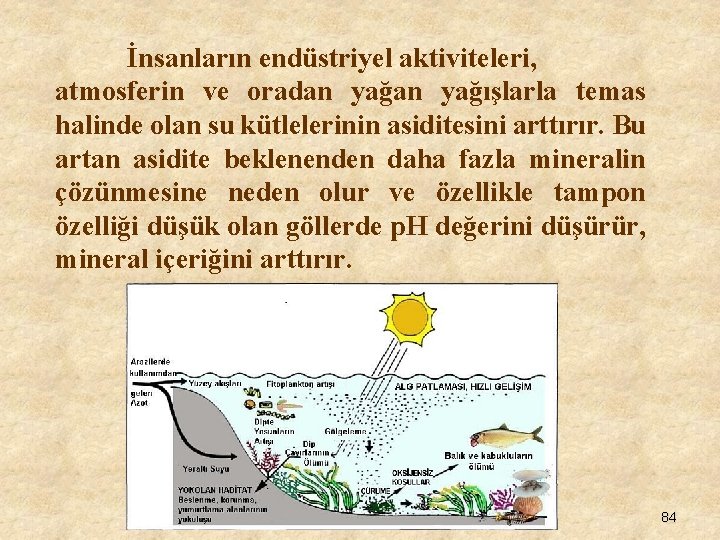
İnsanların endüstriyel aktiviteleri, atmosferin ve oradan yağışlarla temas halinde olan su kütlelerinin asiditesini arttırır. Bu artan asidite beklenenden daha fazla mineralin çözünmesine neden olur ve özellikle tampon özelliği düşük olan göllerde p. H değerini düşürür, mineral içeriğini arttırır. 84

Böylece insan aktiviteleri çok farklı yollarla su kalitesini etkiler; örneğin evsel, endüstriyel, tarımsal atıkların yüzey ve yeraltı sularına karışımı ile. Ayrıca, fazla miktarda tarımsal sulama sularından oluşan çözünmüş tuzlarda bu ortamlara karışırlar. 85

Atıksuların ulaştıkları alıcı ortamlardaki seyrelmesi çok önemlidir çünkü seyrelmemiş atıksuların içindeki biyolojik parçalanabilir organik madde konsantrasyonunun ihtiyacı olan, (aerobik parçalanma için) oksijen miktarı, oksijene doymuş Ç. O. su kütlesinden çok daha fazladır. 86

Doğal sulardaki organizmaların önemi, katalize ettikleri kimyasal transformasyonlarla ilgilidir. Bu aktiviteleri 2 çeşide ayırabiliriz: Organizma için, kullanılabilir enerji veren (katabolizm) Organizmadaki enerjiyi harcayandır (anabolizm). 87
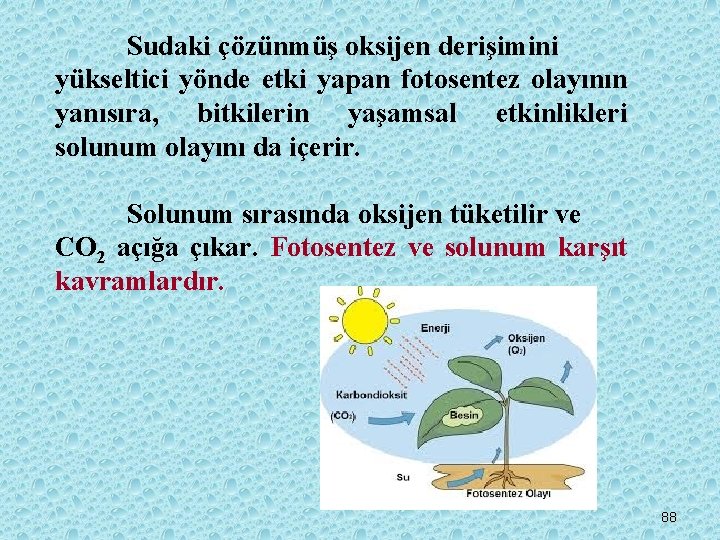
Sudaki çözünmüş oksijen derişimini yükseltici yönde etki yapan fotosentez olayının yanısıra, bitkilerin yaşamsal etkinlikleri solunum olayını da içerir. Solunum sırasında oksijen tüketilir ve CO 2 açığa çıkar. Fotosentez ve solunum karşıt kavramlardır. 88

Fotosentez sırasında CO 2 ve sudan organik madde üretilir. bu süreç içinde su ; enzimler tarafından kontrol edilen bir dizi reaksiyon sonucunda serbest kalan oksijen ile organik bileşenler oluşturan hidrojene ayrıştırılır. 6 CO 2 + 6 H 2 O C 6 H 12 O 6 + 6 O 2 2815. 7 k. J Solunum sırasında ise, bitkisel metabolizmanın gerektirdiği enerjinin üretilmesi için ortamdan oksijen alınır. 89
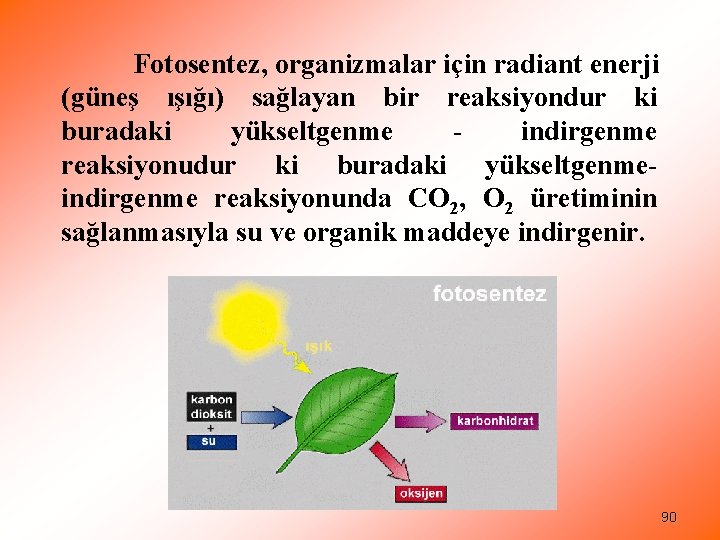
Fotosentez, organizmalar için radiant enerji (güneş ışığı) sağlayan bir reaksiyondur ki buradaki yükseltgenme indirgenme reaksiyonudur ki buradaki yükseltgenmeindirgenme reaksiyonunda CO 2, O 2 üretiminin sağlanmasıyla su ve organik maddeye indirgenir. 90

Doğal sistemlerde bu reaksiyon önemlidir çünkü bunun oluşumu gösterir ki doğal sistemler, kapalı sistemler olarak tanımlanamazlar. Ayrıca, fotosentez reaksiyonları sonucu, doğal su sistemlerini, denge sistemleri olarak incelenip ve sistemin sabit konumunu bulunmalıdır. 91

Fotosentez, yeryüzündeki ve doğal sulardaki birçok organik maddenin oluşumundan sorumludur ve diğer bir çok biyolojik reaksiyonlar gibi o da su kalitesini etkilemektedir. Çünkü fotosentez ile organizmalar çözelti içindeki inorganik karbon bileşiklerine (CO 2, HCO 3 -, CO 3 -2) ihtiyaç duyarlar; 92

Böylece sistemin alkalinitesini düşürür ve büyüdükleri ortamlarda sistemin p. H'sını arttırırlar. p. H'sı çözünürlüğü ile ters orantılı olan maddeler (Mg(OH)2(k) ve Ca. CO 3(k)), fotosentezlenen doğal sularda çökerler. İçinde aktif fotosentez organizmalar içeren suların oxıc konumda olması beklenir çünkü fotosentez oksijen tüketir. 93

Özet olarak, atmosferdeki kimyasal reaksiyonlar ve kara yüzeyindeki kayalarda oluşan katı maddeler, seyrelmiş mineral çözeltiler oluştururlar ki bunlara yüzey suları ve yeraltı suları denir. Bu sular ve parçalanmış mineraller, okyanuslara ulaşırlar ki burada bu reaksiyonların tersi oluşur. 94

İnsan aktiviteleri ve bu doğal suların etrafında büyüyen organizmaların aktiviteleri, bu su kütlelerinin hem inorganik, hem de organik kompozisyonlarını etkiler. 95

Gazların Sıvılardaki Çözünürlükleri Suyun içinde gazlar nasıl ve neden çözünür. Gazlar temas ettikleri sıvılarda genelde yapısı bozulmadan moleküler halde çözünürler. Çözünme miktarları sıcaklığa ve basınca bağlıdır. Gazların sıvılardaki çözünürlükleri Henry Yasası ile verilir. 96

Sıcaklığın Etkisi n Gazların sıvılarda yoğunlaşarak sıvılaşmaları ısıalan bir tepkime gerektirdiğinden sıvılaşmazlar. n Gazların sıvılarda çözünmeleri ısı veren bir işlem olduğundan tercih edilen bir olaydır. n Bu yüzden sıcaklık arttıkça çözünmeleri azalır. Isıtılan sudan hava, gaz kabarcıklarının çıkması sıcaklık artışıyla çözünmenin azalmasına örnektir. n Soğuk sularda çözünmüş oksijen miktarı, ılık sulardakinden daha fazladır. 97
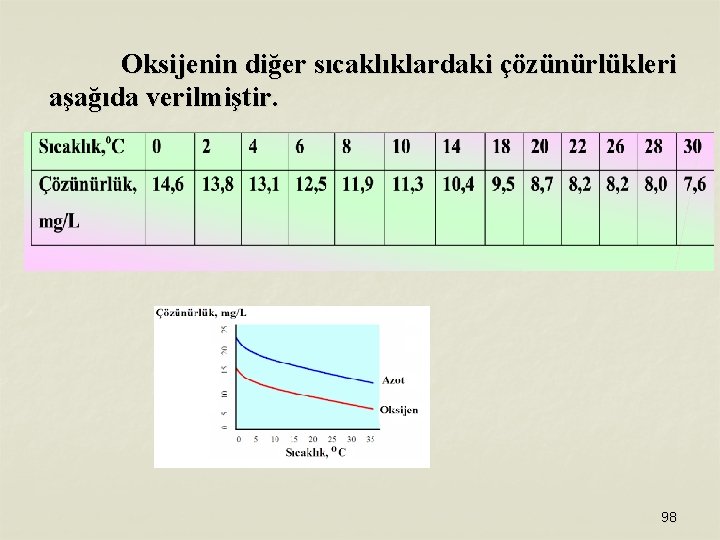
Oksijenin diğer sıcaklıklardaki çözünürlükleri aşağıda verilmiştir. 98

Basıncın Etkisi Bir gazın sıvı içerisindeki çözünürlüğüne basıncın etkisi, sıcaklığınkinden çok daha fazladır. Bir gazın çözünürlüğü gaz basıncıyla doğru olarak artar Bu Henry Yasası olarak bilinir ve C=k. Pgaz ve Pgaz = Xgaz. k şeklinde ifade edilir. Pgaz: doymuş çözeltinin üstündeki gazın kısmi basıncı, Xgaz; gazın mol kesri, k; Henry sabiti(sıcaklığa bağlı) Henry yasası yüksek basınçlarda ve gazın sıvıda iyonlaşması ya da tepkimeye girmesi durumlarında geçerli değildir. 99

100
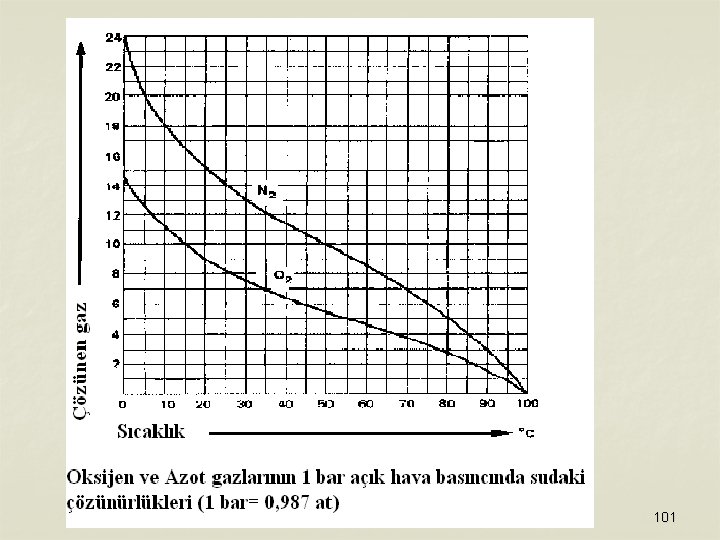
101

Örnek ; 0 ºC ve 1 atm açık hava basıncında N 2 ( g ) gazının sudaki çözünürlüğü 23, 54 m. L N 2 / L dir. N 2 (g) gazının çözünürlüğünü 100 m. L N 2 / L yapmak için, N 2 ( g ) basıncı 0 ºC da ne olmalıdır. k sabit = C / P gaz 102
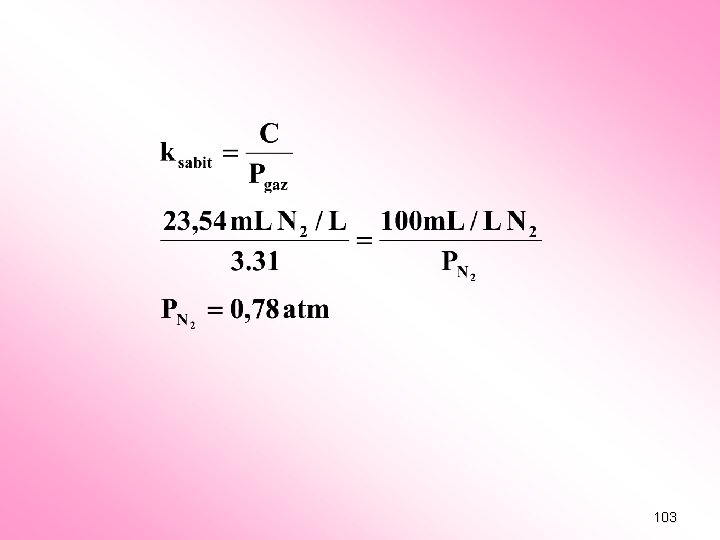
103

Örnek: 0 ºC ve 1 atm O 2 basıncındaki O 2 (g) çözünürlüğü 48, 9 m. L / L dir. Oksijenin havadaki normal kısmi basıncında (0, 2095 atm) sudaki doygun çözeltinin molar derişimi nedir? 0 ºC da 1 atm de O 2 48, 9 m. L O 2 / L çözelti. 1 mol gaz 0 ºC da x x = 2, 18. 10 -3 mol 22, 4 L 48, 9. 10 -3 L 104

1 L çözeltide 2, 18. 10 -3 mol O 2 varsa = 2, 18. 10 -3 M C=k. P k = C/ P 105

10 °C de CO 2(g) nin sulu çözeltisi için k= 1, 04. 103 at dir. Çözelti üzerindeki CO 2 nin kısmi basıncı 1 atm ise 900 g suda kaç mol CO 2 çözünür? Çözünen gazın miktarı kaç g dır? Gazın Çözünürlüğünü M ve mg/L cinsinden bulunuz. 106
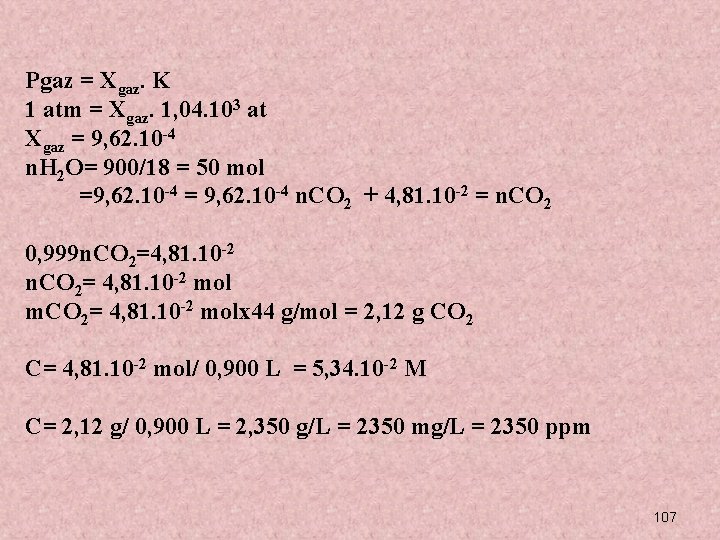
Pgaz = Xgaz. K 1 atm = Xgaz. 1, 04. 103 at Xgaz = 9, 62. 10 -4 n. H 2 O= 900/18 = 50 mol =9, 62. 10 -4 = 9, 62. 10 -4 n. CO 2 + 4, 81. 10 -2 = n. CO 2 0, 999 n. CO 2=4, 81. 10 -2 n. CO 2= 4, 81. 10 -2 mol m. CO 2= 4, 81. 10 -2 molx 44 g/mol = 2, 12 g CO 2 C= 4, 81. 10 -2 mol/ 0, 900 L = 5, 34. 10 -2 M C= 2, 12 g/ 0, 900 L = 2, 350 g/L = 2350 mg/L = 2350 ppm 107

Örnek: Havanın hacimce %0, 035 CO 2 içerdiği bilinmektedir. Bu gazın 20°C de sudaki çözünürlüğünü hesaplayınız. 20 °C de k. CO 2 = 1, 720 mg/L. atm dir. Havanın açık hava basıncı 1 at dir. CO 2 basıncı = y. CO 2. P = 0, 035/100. 1= 3, 5. 10 -4 atm C = k. P = 1, 720 mg/L. atm. 3, 5. 10 -4 atm= 0, 6 mg/L 108
- Slides: 108