Evaluation et renforcement des Autorits Nationales de Rglementation
















- Slides: 23

Evaluation et renforcement des Autorités Nationales de Réglementation pharmaceutique (ANRP) Séminaire sur les Politiques Pharmaceutiques Nationales OMS, Genève, Suisse 13 -17 Juin 2011 l Alain PRAT, Conseiller technique, HSS/EMP/QSM/MRS l OMS Siège- Genève

Glossaire AMM ANRP BPD BPF EC OMS PFP PQP PV SAP 2 | Autorisation de mise sur le marché Autorité nationale de réglementation pharmaceutique Bonnes pratiques de distribution Bonnes pratiques de fabrication Essai clinique Organisation mondiale de la Santé Produit fini pharmaceutique Programme de préqualification de l'OMS Pharmacovigilance Substance active pharmaceutique Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Plan de la session l L'évaluation des Autorités proprement dite – Le procédé d'évaluation – Le contenu de l'outil l Les principales observations l Les modalités du renforcement – la logique – les méthodes et les outils 3 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Les étapes du procédé d'évaluation l Expression du besoin l Validation de la demande l Composition de l'équipe l Planification et préparation de la visite l Evaluation proprement dite – Réunion d'ouverture – Conduite de la visite – Réunion de clôture l Gestion des suites 4 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Cartographie des processus l Processus de production de services – Autorisation, License, Retrait, Suspension, . . . l Processus généraux à toute organisation – Management de la vision-mission, des stratégies et des objectifs de l’organisation – Gestion des ressources humaines et matérielles (les activités des services de ressources humaines, des achats, d’approvisionnement. . . ) – Gestion de la relation client, processus de détermination du besoin et de la satisfaction des clients (les activités de communication) – Gestion et traitement de l’information – Amélioration continue ( audits, actions correctives et préventives, analyse des mesures faites) l Processus connexes (faisant intervenir l'organisation) 5 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

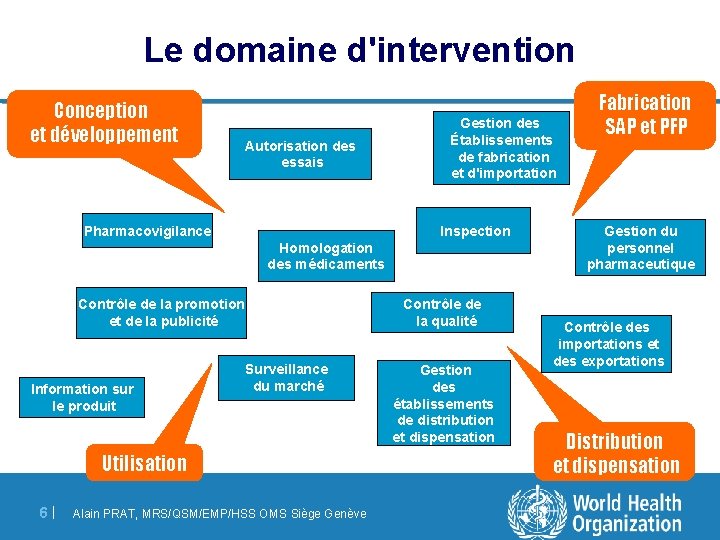
Le domaine d'intervention Conception et développement Autorisation des essais Gestion des Établissements de fabrication et d'importation Inspection Pharmacovigilance Homologation des médicaments Contrôle de la qualité Contrôle de la promotion et de la publicité Information sur le produit Surveillance du marché Utilisation 6 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève Gestion des établissements de distribution et dispensation Fabrication SAP et PFP Gestion du personnel pharmaceutique Contrôle des importations et des exportations Distribution et dispensation

Evaluation de la structure institutionelle l Base légale de l'institution l Structure de gouvernance (DG, Président, Secrétaire général, etc…) l Organisation en place l Système de gestion de la qualité l Ressources financières l Gestion des ressources humaines 7 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Evaluation de la structure institutionelle / 2 l Indépendance et impartialité l Transparence et confidentialité l Gestion des comités et de l'expertise externe l Infrastructure et équipements l Modalités de surveillance et pour rendre compte l Gestion des technologies de l'information 8 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

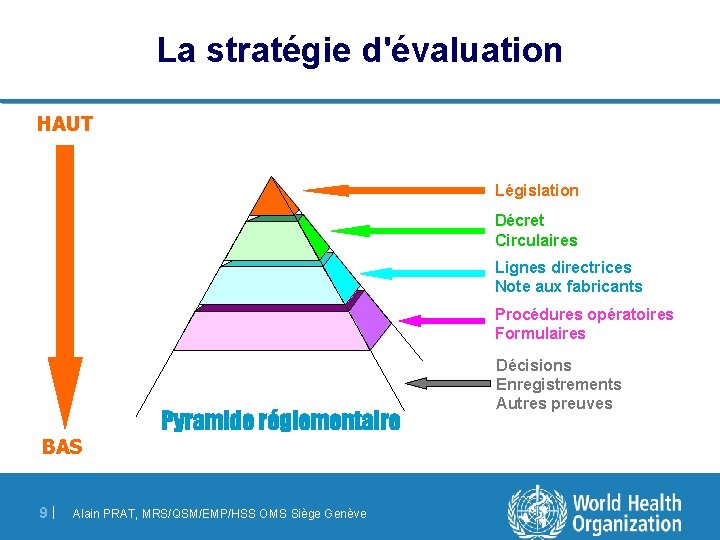
La stratégie d'évaluation HAUT Législation Décret Circulaires Lignes directrices Note aux fabricants Procédures opératoires Formulaires BAS 9 | Pyramide réglementaire Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève Décisions Enregistrements Autres preuves

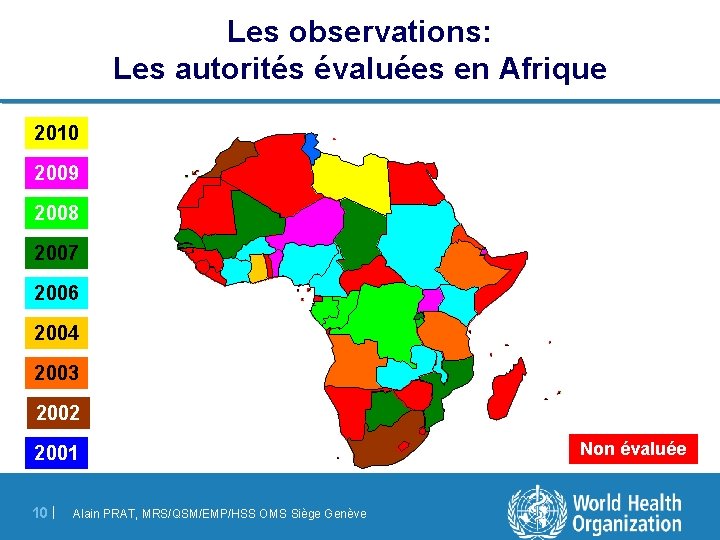
Les observations: Les autorités évaluées en Afrique 2010 2009 2008 2007 2006 2004 2003 2002 2001 10 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève Non évaluée

Les observations: La multiplicité des acteurs Fonctions Réglementaires Acteurs ou Institutions Autorisation des fabricants, importateurs Ministère de la santé et distributeurs Directions régionales Autorisation des pharmacies et du personnel pharmaceutique Ministère de la santé Ordre des pharmaciens Homologation des médicaments Direction du Ministère Inspection pharmaceutique Inspection générale de la santé Pharmacovigilance Centre national de pharmacovigilance Programmes verticaux Importations Inspection des Douanes Essais cliniques Comité d'éthique Ministère de la santé 11 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

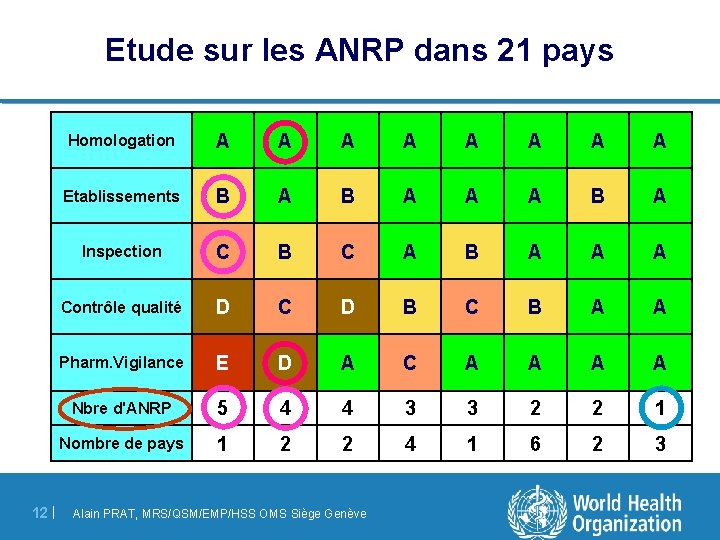
Etude sur les ANRP dans 21 pays 12 | Homologation A A A A Etablissements B A A A B A Inspection C B C A B A A A Contrôle qualité D C D B C B A A Pharm. Vigilance E D A C A A Nbre d'ANRP 5 4 4 3 3 2 2 1 Nombre de pays 1 2 2 4 1 6 2 3 Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

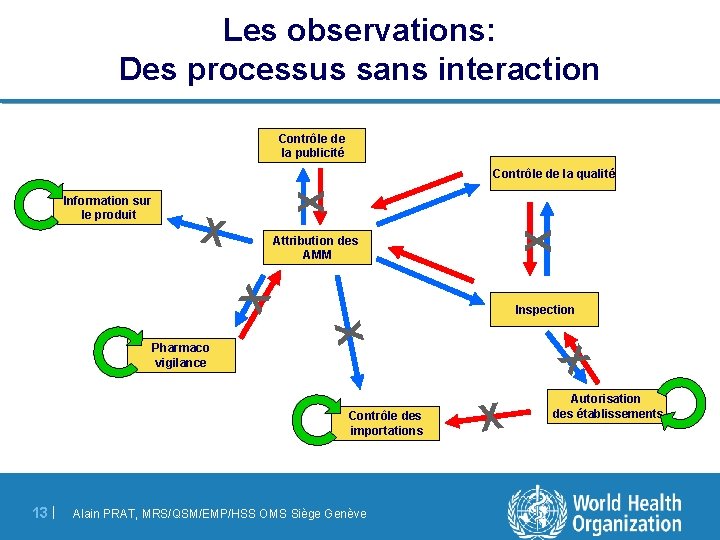
Les observations: Des processus sans interaction Contrôle de la publicité X X Attribution des AMM X Information sur le produit X Contrôle de la qualité X X Pharmaco vigilance Inspection Contrôle des importations 13 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève X Autorisation des établissements

Les observations: Le cadre réglementaire l La loi est obsolète ou est absente RARE sauf PV, EC l La loi est promulguée • Mais la réglementation nécessaire est absente SOUVENT PV, EC l La loi et les règlements sont publiés • Mais ne sont pas appliqués • Mais aucune ligne directrice (LD) n'est publiée TRES SOUVENT sauf BPF l Les lignes directrices sont publiées • Mais elles sont obsolètes ou non-conformes à l'état de l'art SOUVENT l Les lignes directrices sont appliquées • Mais sans base légale ou sans publication préalable ASSEZ SOUVENT l Les décisions administratives sont prises et publiées • Mais sans base légale CELA ARRIVE 14 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Exemples de défisciences observées : Cas de l'inspection l Ressources humaines – Absence de compétence technique des inspecteurs (BPF, Ster. ) – Ressources humaines limitées au regard du nombre des établissements à inspecter – Pas les compétences judiciaires pour réaliser leurs missions. l Indépendance/Impartialité – Pas de code de conduite – Pas de mécanisme ou de ligne directrice pour gérer les conflicts d'intérêt 15 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Exemples de défisciences observées : Cas de l'inspection / 2 l Système de management de la qualité – Pas de système de management de la qualité et en particulier pas de procédure documentée pour la gestion de la documentation, pas d'audit interne périodique – Les procédures documentés pour la planification, la préparation , l'inspection et le suivi des inspection ne sont pas finalisées – Pas de procédure pour la qualification des inspecteurs et du responsable de l'équipe d'inspection – Aucune checklist ou plan pour la réalisation des inspections des fabricants ou des distributeurs n'est disponible – Pas de procédure pour effectuer le suivi des déficiences observées durant les inspection 16 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Exemples de défisciences observées : Cas de l'inspection / 3 l Equipement / Technologies de l'Information – Accès limité à internet, à des banques de données – Logistique inadéquate i. e. outils de communication, véhicules et ordinateurs l Organisation – Pas de coordination, de collaboration ou d'échange sur les programmes d'inspection et les établissements inspectés avec les inspecteurs régionaux – Pas de mécanisme pour démontrer que tous les inspecteurs suivent les procédures identiques sur l'ensemble du territoire l Enregistrements et données de sorties – Pas de listes consolidées des activités d'inspection 17 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Les activités de soutien Etablir ou réorganiser une structure Réglementation pharmaceutique Lignes directrices scientifiques et techniques Développer et mettre en oeuvre des procédures et formulaires Etude comparative de bonnes pratiques Activités de plaidoyer Diagnostic situationnel par évaluation des ANRP Activités de conseil Normes et guides développés par l'OMS Guide sur les système qualité Procédure existantes développées par l'OMS ou la PQP Qualification à la fonction Nombreuses formations dispensées (inspection, homologation, vigilance) Gestion de l'information Système informatique OMS / SIAMED 18 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

19 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

20 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Les activités annexes l Encourager l'harmonisation des pratiques l Faciliter les échanges d'information réglementaire l Promouvoir dans certains cas des standards internationaux globalement identifiés et reconnus 21 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

22 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève

Merci de votre attention 23 | Alain PRAT, MRS/QSM/EMP/HSS OMS Siège Genève