Evaluacin de tecnologas sanitarias y Regulacin de precios














- Slides: 23

Evaluación de tecnologías sanitarias y Regulación de precios de medicamentos X Encuentro de la Red de Evaluación de Tecnologías en Salud de las Américas Buenos Aires Agentina 07/11/2018 Adriana Granizo M. Directora Nacional de Inteligencia de la Salud

Contenido Antecedentes Normativa y Metodología Decreto Ejecutivo Nro. 400

Constitución (2008) Art. 3. - Deber primordial del estado, garantizar la salud. Art. 32. - La salud es un derecho. Art. 37. - Atención gratuita, acceso gratuito medicinas. Art. 363. Numeral 7: “El Estado será responsable de garantizar la disponibilidad y acceso a medicamentos de calidad, seguros y eficaces, regular su comercialización y promover la producción nacional y la utilización de medicamentos genéricos que respondan a las necesidades epidemiológicas de la población. ” “Y que en el acceso a medicamentos, los intereses de la salud pública prevalecerán sobre los económicos y comerciales. ”

Perspectiva: Salud Pública Perspectiva: Mercado

“ Los medicamentos no son un producto comercial, sino un elemento esencial en el seno de la atención de salud, que se le confiere la clasificación de un bien público, y un elemento La Regulación en el Ecuador parte de 1964 imprescindible para el respeto y garantía del derecho a la salud” Un bien público y no un bien de mercado. (CNMB-9 NA edición) Un derecho que garantiza el Estado. Es un mercado imperfecto. Es altamente influenciado por terceros.

MERCADO ALTAMENTE INFLUENCIADO POR TERCEROS

MEDICAMENTO “BIEN PÚBLICO” NO ES UN BIEN DE MERCADO

COMPORTAMIENTO ANORMAL DEL MERCADO

DISTORSIONES PROPIAS DEL MERCADO

A nivel internacional se ha evidenciado la necesidad de que los países regulen el precio de los medicamentos a través de métodos directos o indirectos. El objetivo máximo es garantizar que estos sean asequibles y lograr que los ciudadanos tengan acceso a tratamientos que mejoren su calidad de vida. Estas regulaciones han sido implementadas ya en varios países europeos, la India y Brasil, entre otros. No obstante no existe una metodología única para fijar precios a un medicamento.

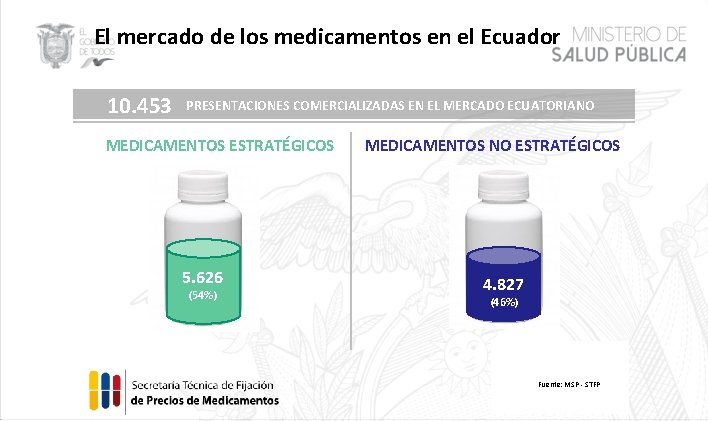
El mercado de los medicamentos en el Ecuador 10. 453 PRESENTACIONES COMERCIALIZADAS EN EL MERCADO ECUATORIANO MEDICAMENTOS ESTRATÉGICOS 5. 626 (54%) MEDICAMENTOS NO ESTRATÉGICOS 4. 827 (46%) Fuente: MSP - STFP

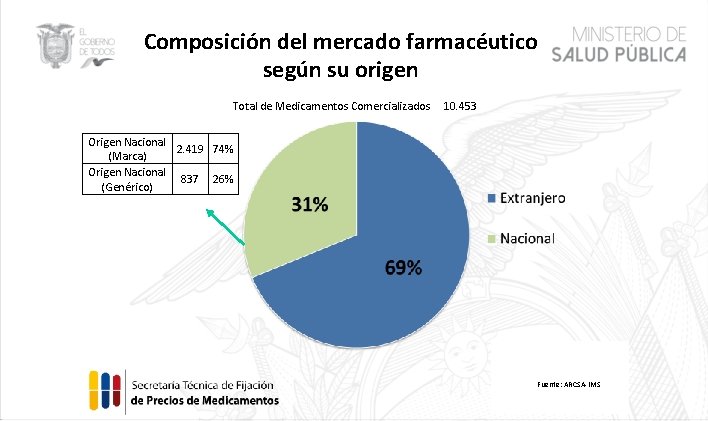
Composición del mercado farmacéutico según su origen Total de Medicamentos Comercializados 10. 453 Origen Nacional 2. 419 74% (Marca) Origen Nacional 837 26% (Genérico) Fuente: ARCSA-IMS

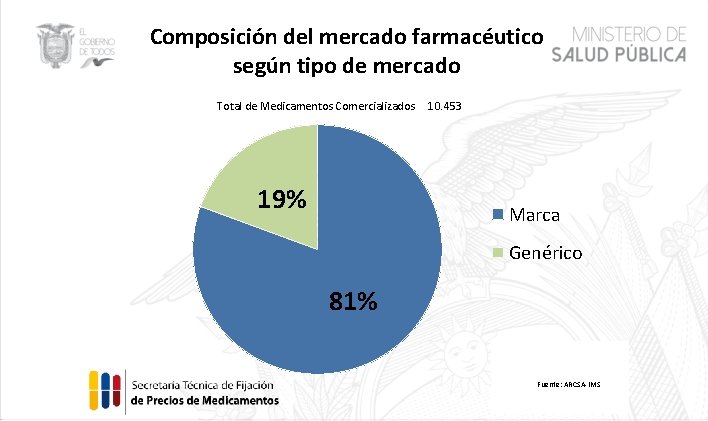
Composición del mercado farmacéutico según tipo de mercado Total de Medicamentos Comercializados 10. 453 19% Marca Genérico 81% Fuente: ARCSA-IMS

Normativa y Metodología Decreto Ejecutivo Nro. 400

Art. 1. : Establecer y regular los procedimientos para la fijación, revisión y control de precios de venta al consumidor final de medicamentos de uso y consumo humano, que se comercialicen dentro del territorio ecuatoriano.

Regímenes de Fijación de Precios Medicamentos estratégicos y nuevos. RÉGIMEN REGULADO Sujetos a control mediante notificación periódica RÉGIMEN LIBERADO RÉGIMEN DE FIJACIÓN DIRECTA De excepción por incumplimiento de la ley o por emergencia sanitaria

Régimen Regulado RÉGIMEN REGULADO Medicamentos estratégicos 1346 Criterios según Resolución del Consejo Nro. 07 -2014 1. 2. 3. 4. Pertenecientes al CNMB, incluyendo sus combinaciones, siempre que no sean considerados de venta libre. Medicamentos para enfermedades de las estrategias de salud colectiva y medicamentos para enfermedades raras Monopólicos o con restricciones relevantes a la competencia. Medicamentos nuevos, sin codificación ATC, sometidos a Régimen Regulado. Además, por resolución del MSP (prioridades de salud) o pedido de la SCPM

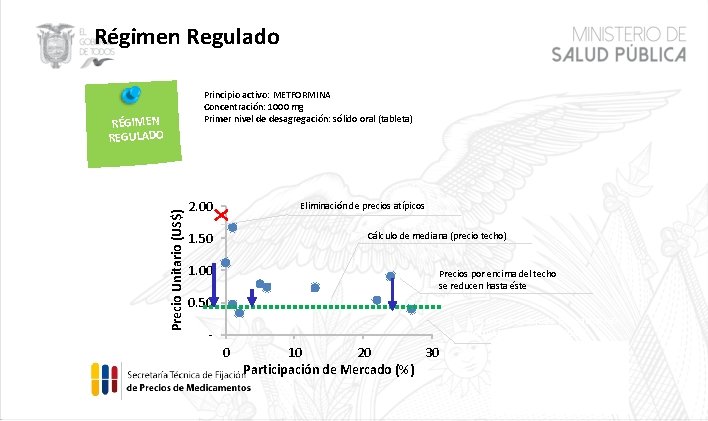
Régimen Regulado Principio activo: METFORMINA Concentración: 1000 mg Primer nivel de desagregación: sólido oral (tableta) Precio Unitario (US$) RÉGIMEN REGULADO 2. 00 Eliminación de precios atípicos 1. 50 Cálculo de mediana (precio techo) 1. 00 Precios por encima del techo se reducen hasta éste 0. 50 Precios por debajo de la mediana NO PODRÁN SUBIR SUS PRECIOS. 0 10 20 30 Participación de Mercado (%)

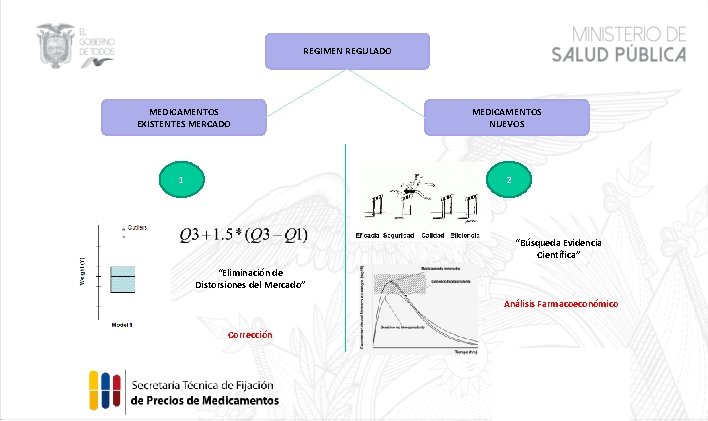
REGIMEN REGULADO MEDICAMENTOS EXISTENTES MERCADO MEDICAMENTOS NUEVOS 1 2 “Búsqueda Evidencia Científica” “Eliminación de Distorsiones del Mercado” Análisis Farmacoeconómico Corrección

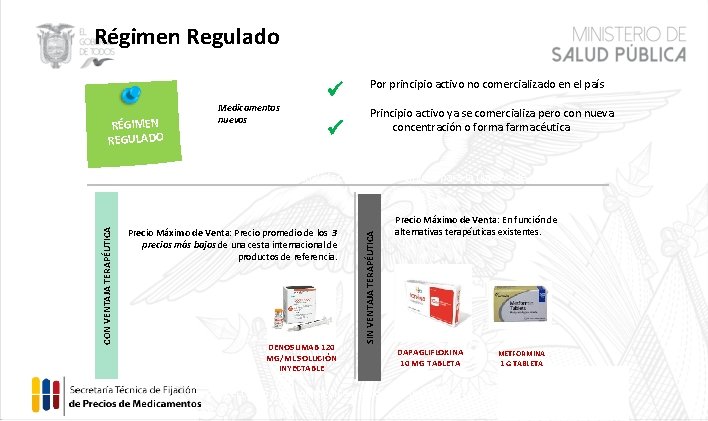
Régimen Regulado RÉGIMEN REGULADO Medicamentos nuevos Por principio activo no comercializado en el país Principio activo ya se comercializa pero con nueva concentración o forma farmacéutica. Precio Máximo de Venta: Precio promedio de los 3 precios más bajos de una cesta internacional de productos de referencia. DENOSUMAB 120 MG/ML SOLUCIÓN INYECTABLE SIN VENTAJA TERAPÉUTICA CON VENTAJA TERAPÉUTICA En un plazo de 60 días se realizan los análisis clínico y económicos para la fijación de precios. Precio Máximo de Venta: En función de alternativas terapéuticas existentes. DAPAGLIFLOXINA 10 MG TABLETA METFORMINA 1 G TABLETA El precio fijado será el techo para los medicamentos que ingresen a competir en el segmento correspondiente

RÉGIMEN REGULADO Criterio para la Selección de Medicamentos Análisis Clínico CON VENTAJA TERAPÉUTICA • Se debe dar prioridad a los fármacos con eficacia y seguridad probadas, evitando la duplicidad innecesaria de fármacos y formas farmacéutica. • Sólo se deben seleccionar los fármacos para los que se dispone de suficiente información científica, y para los que se disponga de pruebas de efectividad de su uso en diferentes contextos. • Los fármacos de reciente comercialización sólo deben incluirse si tienen ventajas que los distingan de los utilizados actualmente. Fuente: Guía de la Buena Prescripción - OMS. Programa de Acción Sobre los Medicamentos Esenciales. MBE Preferencias del Paciente Mejor Evidencia Disponible

CON VENTAJA TERAPÉUTICA RÉGIMEN REGULADO Análisis económico de Precios de Referencia Internacional de medicamentos nuevos Artículo 18 literal b. - En el caso de que el nuevo producto tenga aporte terapéutico a los tratamiento existentes para la indicación correspondiente, la Secretaria Técnica pondrá en consideración del Consejo, como referencia, los precios de comercialización del mismo medicamento de una cesta de productos de países que incluirán: miembros y asociados del Mercado Común del Sur (MERCOSUR), y la Alianza Bolivariana para los Pueblos de Nuestra América (ALBA). De igual forma, y si se considera pertinente, la cesta de precios de referencia podrá también incluir a los países Miembros de UNASUR, Estados Unidos de América, Unión Europea y el resto del mundo. El Consejo determinará como precio máximo de venta al público, el equivalente en moneda nacional al precio promedio de los tres (3) precios más bajos de esta cesta de productos de referencia, ajustado por la paridad de poder adquisitivo. Para cada análisis se deberá considerar el precio del mismo medicamento en al menos 3 países distintos.

GRACIAS POR SU ATENCIÓN martes, 06 de noviembre de 2018