Evaluacin de la Contaminacin Ambiental Tema 3 Procesos

Evaluación de la Contaminación Ambiental Tema 3. - Procesos físicos y químicos en la atmósfera → Reacciones de fotoionización y fotodisociación en la atmósfera → La oxidación en la atmósfera → Smog fotoquímico → La lluvia ácida → La pérdida de ozono estratosférico → El balance de radiación de la Tierra y el efecto invernadero

Interacción de la luz con la atmósfera Atmósfera sujeta al bombardeo de radiación y de partículas con gran energía provenientes del sol y de radiación cósmica del espacio exterior Esta energía tiene efectos químicos importantes, especialmente en los límites exteriores de la atmósfera La alta atmósfera, de baja densidad, constituye la defensa externa contra la radiación y las partículas de alta energía → sus componentes experimentan cambios químicos Las propiedades de las moléculas atmosféricas son muy importantes para nuestro planeta La cantidad de energía que absorbe una molécula depende de: - la naturaleza de la propia molécula - la energía, E, de la luz que le llega (que depende de la frecuencia, n, ó de la longitud de onda, l) 2
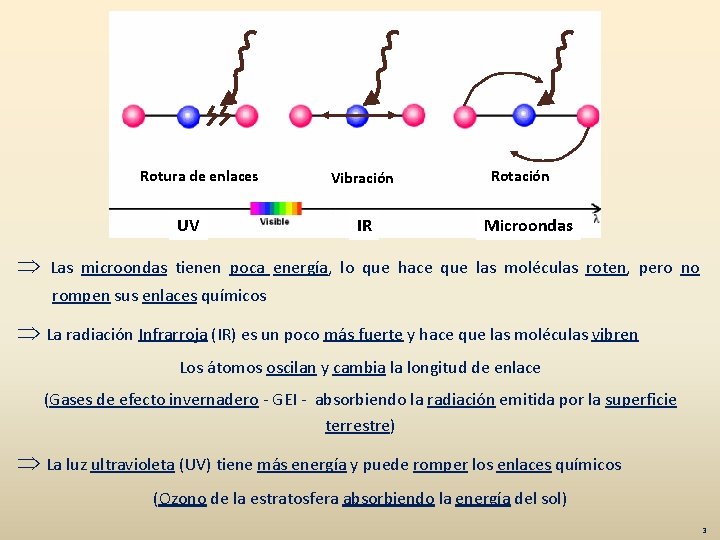
Rotura de enlaces UV Vibración IR Rotación Microondas Las microondas tienen poca energía, lo que hace que las moléculas roten, pero no rompen sus enlaces químicos La radiación Infrarroja (IR) es un poco más fuerte y hace que las moléculas vibren Los átomos oscilan y cambia la longitud de enlace (Gases de efecto invernadero - GEI - absorbiendo la radiación emitida por la superficie terrestre) La luz ultravioleta (UV) tiene más energía y puede romper los enlaces químicos (Ozono de la estratosfera absorbiendo la energía del sol) 3

La interacción de la luz con la atmósfera: reacciones de fotodisociación y fotoionización Para que ocurra un cambio químico cuando la radiación llega a la atmósfera de la Tierra, se deben de satisfacer dos condiciones 1. - Debe haber fotones con suficiente energía para llevar a cabo un proceso químico determinado 2. - Las moléculas deben ser capaces de absorber estos fotones Cuando la radiación atraviesa un gas, este absorbe unas determinadas l (fotones) El resultado es su espectro de absorción característico, donde faltan las bandas absorbidas, apareciendo en su lugar bandas negras 4

Fotodisociación * Es la ruptura de un enlace químico debida a la absorción de un fotón por una molécula Fotodisociación del oxígeno es uno de los procesos más importantes que ocurren en la atmósfera superior, por arriba de los 120 km (Termosfera o ionosfera) O 2(g) + h n (fotón) 2 O(g) La energía mínima del fotón es la energía de disociación del O 2 , 495 k. J/mol Para que la disociación se lleve a cabo el fotón debe ser absorbido por el O 2: necesita longitudes de onda del fotón inferiores a 242 nm (radiación UV-C) O 2 absorbe gran parte de la radiación solar de alta energía (l corta) antes de que llegue a la atmósfera inferior y así se forma el oxígeno atómico, O A grandes altitudes, la disociación del O 2 es muy importante: * 400 km: el 1% del oxígeno es oxígeno diatómico; el 99% es oxígeno atómico * 130 km, O 2 y O son igualmente abundantes * Por debajo de esta altura el oxígeno diatómico es el más abundante 5

Fotodisociación del nitrógeno Debido a que la energía de disociación del enlace de N 2 es muy elevada (1495 k. J/mol), solamente los fotones de l muy corta poseen suficiente energía para disociarlo Además, el N 2 no absorbe fácilmente los fotones, aun cuando éstos tengan suficiente energía El resultado es que en la atmósfera superior se forma muy poco nitrógeno atómico a causa del proceso de disociación Fotoionización Arrancar un electrón de una molécula o átomo (ionización) por acción de un fotón de energía suficiente (l alta energía del UV) electrones de Ionosfera Ej. : N 2 + h n (fotón) = N 2+ + e- necesita un fotón de l < 80 nm Como resultado de su absorción en la atmósfera superior, estas l son filtradas completamente de la radiación que llega a la Tierra 6

No todas las radiaciones UV son absorbidas en las capas altas ventana (200 -320 nm) ninguna sustancia salvo el O 3 absorbe radiación sin el O 3 llegaría a la superficie En las capas más altas fotoionización filtra los fotones más energéticos A medida que descendemos en la atmósfera adquiere más importancia la fotodisociación, porque disminuye la proporción de fotones ionizantes En la baja atmósfera la fotodisociación pierde también importancia y comienzan las reacciones de recombinación de sustancias químicas reacciones de oxidación - reducción 7
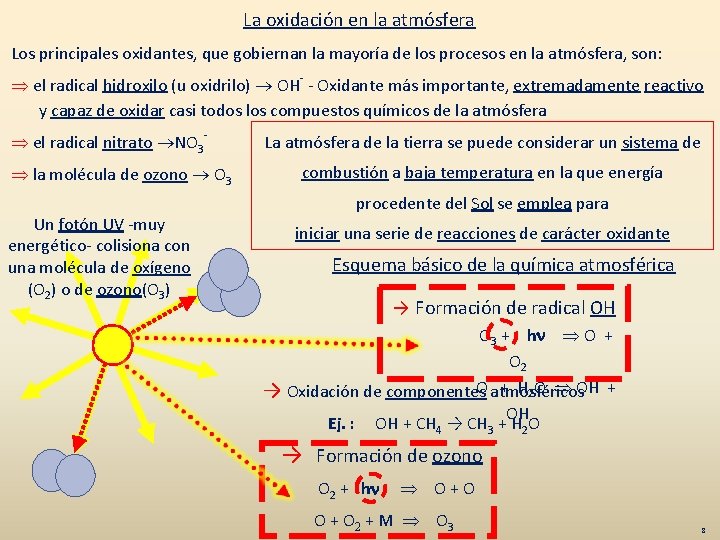
La oxidación en la atmósfera Los principales oxidantes, que gobiernan la mayoría de los procesos en la atmósfera, son: el radical hidroxilo (u oxidrilo) OH- - Oxidante más importante, extremadamente reactivo y capaz de oxidar casi todos los compuestos químicos de la atmósfera el radical nitrato NO 3 la molécula de ozono O 3 Un fotón UV -muy energético- colisiona con una molécula de oxígeno (O 2) o de ozono(O 3) La atmósfera de la tierra se puede considerar un sistema de combustión a baja temperatura en la que energía procedente del Sol se emplea para iniciar una serie de reacciones de carácter oxidante Esquema básico de la química atmosférica → Formación de radical OH O 3 + hn O + O 2 O + H 2 O OH + → Oxidación de componentes atmosféricos OH Ej. : OH + CH 4 → CH 3 + H 2 O → Formación de ozono O 2 + hn O + O 2 + M O 3 8

La oxidación en la atmósfera Sólo algunos compuestos, ej. CFCs, N 2 O ó CO 2 son muy estables y no reaccionan del todo con el OH o reaccionan muy lentamente ¿Cómo se forma el radical OH? El OH gobierna la química atmosférica durante el día porque su formación depende fundamentalmente de la radiación solar La reacción inicial de formación del OH en la atmósfera es la ruptura del ozono por la luz del sol (fotolisis) a l < 310 nm, seguido de la reacción del átomo de O formado con agua O 3 + hn O + O 2 (l < 310 nm) O + O 2 + M * O 3 + M* O + H 2 O 2 OH (3%) (97%) → M es una molécula ( Ej. N 2) necesaria para eliminar el exceso de energía pero que no reacciona Formación de OH: > 97% de los átomos de O formados por la fotolisis del ozono reaccionan formando de nuevo ozono y sólo < 3% inicia la formación del radical más importante de la atmósfera, el OH 9

Otras fuentes de OH son la fotólisis del ácido nitroso HNO 2 (HNO 2 + hn NO + OH) el peróxido de hidrógeno H 2 O 2 el peroxi metano CH 3 O 2 H la reacción del NO con el radical hidroperoxi HO 2 (HO 2 + NO 2 + OH) Todas estas reacciones constituyen el llamado ciclo diurno del OH ya que todas ellas necesitan la radiación solar para producirse Dado que el OH es un radical extremadamente reactivo, nada más formarse reacciona (vida de 1 s o menos) lo que implica que su concentración es muy baja (105 - 107 moléc cm-3) Como su formación depende de la disponibilidad de vapor de agua O + H 2 O 2 OH También disminuye con la latitud porque a medida que nos acercamos a los polos no solo disminuye la concentración de vapor de agua sino también la intensidad y la duración de la luz solar 10

El OH presenta una fuerte tendencia a la reacción con radicales RH (R= radical orgánico): RH + OH R • + H 2 O A continuación el radical R • reacciona con oxígeno dando lugar a peróxidos orgánicos (que participan en el ciclo de formación del ozono troposférico) Gases que contribuyen a la eliminación del OH (40 %) CO: El principal gas que reacciona con el OH (30 %) Gases orgánicos (15 %) CH 4: la más importante y pequeña de las moléculas orgánicas (15 %) O 3, radicales peroxi HO 2 y el hidrógeno H 2 El CO y el metano (CH 4) representan los principales sumideros de OH (55 %) Otros compuestos reactivos están disponibles en muy pequeñas cantidades del orden de pptv, mientras que el CO alcanza niveles medios de 120 ppb en el hemisferio norte (más procesos de combustión) y 60 ppb en el hemisferio sur 11

Aunque el OH es el oxidante más importante de la atmósfera, su concentración durante la noche ≈ 0, ya que para formarse necesita radiación solar durante la noche la química del nitrato (NO 3) y el ozono (O 3) adquieren más importancia La química nocturna se inicia con la presencia de un agente oxidante como el ozono capaz de oxidar el NO 2 a NO 3 O 3 + NO 2 NO 3 + O 2 Dado que el NO 3 sufre con facilidad reacciones fotolíticas, su concentración solo es apreciable durante la noche El NO 3 reacciona de nuevo con NO, por lo que nunca pueden coexistir altas concentraciones de NO y NO 3 Los radicales nitrato, igual que el radical OH, sustraen un átomo de hidrógeno de los compuestos orgánicos (RH) NO 3 + RH HNO 3 + R • Los radicales alquilo R • reaccionan con el O 2 del aire y forman radicales peróxido RO 2 • R • + O 2 RO 2 • Al llegar la luz del día, el NO 3 se rompe por fotolisis produciendo principalmente NO 2 y O, y de nuevo domina la química del OH (O + H 2 O 2 OH) Los peróxidos que provienen de las reacciones de los radicales OH, NO 3 u ozono experimentan numerosos y complicados procesos en la atmósfera produciendo alcoholes, aldehídos, nitratos y ácidos carboxílicos 12

El ozono, el tercer oxidante más importante de la atmósfera, no reacciona con alcanos (HC con enlaces simples C-C) pero, si disminuye la concentración de OH, sí que reacciona con alquenos (HC con doble enlace C-C) bajo condiciones de relativa oscuridad (invierno o tarde-noche) Más adelante se tratarán las reacciones del ozono Contaminación fotoquímica ó Smog fotoquímico Smog (de smoke: humo y fog: niebla) La causa de la formación de esta neblina contaminante urbana, principal problema de contaminación en muchas ciudades, es la acción de la radiación UV que produce la fotólisis de moléculas de contaminantes, generándose sustancias altamente oxidantes como el ozono y el PAN (Nitrato de peroxiacilo) Condiciones para que se produzca smog fotoquímico en una ciudad 1) Trafico importante suficiente NO, HC y otros COVs 2) Tiempo cálido (mucho sol) muchas reacciones fotoquímicas 3) Poco movimiento de aire acumulación de reactivos Época más favorable: Verano Julio-Septiembre (Hemisferio N); Enero – Marzo (H S) Meteorología idónea: Inversión de temperatura Orografía, como obstáculo para la dispersión de contaminantes, puede favorecer que ciudades con densidades de población elevadas y soleadas sufran mayores episodios de smog Ej. : Los Ángeles, Denver, Ciudad de Méjico, Tokyo, Atenas, Sao Paulo y Roma 13

En la formación del smog fotoquímico se pueden distinguir 3 tipos de procesos: 1) Formación de O 3 en el ciclo fotolítico del NO 2 + UV (< 380 nm) NO + O (muy inestable) # O + O 2 O 3 Si en la atmósfera no hay HC que se combinen con el ozono, éste vuelve a descomponerse: NO + O 3 NO 2 + O 2 (ciclo fotolítico del NO 2) Reacciones parecidas forman también ozono troposférico a partir de otros contaminantes 2) Formación de radicales libres activos Si en la atmósfera hay HC (radicales hidrogenados RH), éstos tienen fuerte tendencia a formar radicales oxigenados muy reactivos: RH + O RO • # RO • + O 2 RO 3 • 3) Formación de productos finales Los radicales libres ( • ) reaccionan con otros contaminantes y con los constituyentes normales del aire, originando una mezcla de productos oxidantes entre los que se encuentran los “peroxiacetilnitratos o nitratos de peroxiacilo” (PANs) provenientes de los HC alifáticos o los “nitratos de peroxibenzoilo” (PBNs) derivados de los HC aromáticos RO 3 • + O 2 O 3 + RO 2 # RO 3 • + NO RO 2 + NO 2 RO 3 • + NO 2 RCO 3 NO 2 (PAN, PBN, . . ) El más importante es el PAN(Es tóxico y cancerígeno) 14

El ozono troposférico es el más abundante de los productos de alto poder oxidante que se generan en el smog Indicador de este tipo de contaminación El O 3 no se emite directamente por ninguna fuente contaminante, sino que se forma en la atmósfera (contaminante secundario) El ozono existe de forma natural en la troposfera nivel de fondo (no es una concentración peligrosa) debido a intercambios con la estratosfera y a procesos naturales que tienen lugar en la biosfera a partir de la emisión de NOx y COVs procedentes de la vegetación, de procesos de fermentación y de los volcanes o el que se forma en las descargas eléctricas de una tempestad Sin embargo, es el aumento en la generación de NOx, de origen antropogénico, la que provoca que la reacción se desplace hacia la formación de ozono, aumentando su concentración NO 2 + UV (< 380 nm) NO + O # O + O 2 O 3 15

Nota: Radicales libres Son átomos o grupos de átomos que tienen un electrón desapareado (con capacidad de aparearse) por lo que son muy reactivos Estos radicales intentan robar un electrón de las moléculas estables, con el fin de alcanzar su estabilidad electroquímica Una vez que el radical libre ha conseguido robar el electrón que necesita para aparear su electrón libre, la molécula estable que se lo cede se convierte a su vez en un radical libre, por quedar con un electrón desapareado, iniciándose así una verdadera reacción en cadena Para escribir las ecuaciones químicas, los radicales libres se escriben poniendo un punto situado inmediatamente a la derecha del símbolo atómico o de la fórmula molecular: H 2 + hν → 2 H· CFCl 3 + hn CFCl 2· + Cl· 16

Lluvia ácida Los compuestos químicos más relacionados con las lluvias ácidas son los ácidos carbónico, sulfúrico y nítrico La acidez de la lluvia se mide con la escala de p. H = - log[H+] = - log[H 3 O+] (cuanto más fuerte es el ácido mayor será [H+] y más pequeño es el p. H) Las precipitaciones normales en atmósferas no contaminadas son algo ácidas ya que el CO 2 que existe de forma natural en el aire se disuelve, creando una solución de ácido carbónico (H 2 CO 3) lluvias con un p. H alrededor de 5. 6 Esto es debido a que el ácido carbónico formado por el CO 2 y el agua atmosféricos CO 2 + H 2 O H 2 CO 3 no es estable y se disocia al disolverse en agua formando iones hidronio y bicarbonato: H 2 CO 3+ H 2 O HCO 3 - + H 3 O+ Así pues, la lluvia limpia es ligeramente ácida por la disociación del ácido carbónico Hablamos de lluvia ácida cuando su p. H es menor que 5. 6 aunque algunos científicos consideran lluvia ácida las precipitaciones con p. H < 5. 0 (más acida) Característica importante sus efectos se pueden observar a miles de km de las fuentes de emisión Problema transfronterizo 17

La contribución más importante del hombre a la lluvia ácida: emisión de oxidos de S y N SO 2 y NOx pasan por una serie de complejas reacciones químicas antes de convertirse en los ácidos sulfúrico (H 2 SO 4) o sulfuroso (H 2 SO 3) y nítrico (HNO 3) o nitroso (HNO 2) respectivamente que se encuentran en la lluvia ácida El ácido sulfúrico procede de compuestos sulfurosos: 2 SO 2 + O 2 2 SO 3 el SO 3 y el agua reaccionan dando ácido sulfúrico: SO 3 + H 2 O H 2 SO 4 También el SO 2 reacciona directamente con el agua dando ácido sulfuroso SO 2 + H 2 O H 2 SO 3 La reacción de NO 2 con agua produce ácido nítrico y óxido nítrico o bien ácido nítrico y ácido nitroso, según la cantidad de NO 2 presente en la atmósfera para reaccionar con agua: 3 NO 2 (g) + H 2 O (v) 2 HNO 3 (l) + NO (g) 2 NO 2 (g) + H 2 O (v) HNO 3 (l) + HNO 2 (l) El p. H de una nube ácida puede llegar a ser menor de 2. 6 En regiones muy industrializadas ≈ 4. 0 (nieblas Los Ángeles (USA), p. H < 3) Sin embargo, no siempre las precipitaciones ácidas tienen origen antropogénico en algunas zonas, ej. Norte de Australia, las emisiones orgánicas naturales de la vegetación producen, por si solas, un p. H ≈ 4. 4 18

¿Qué procesos originan la lluvia ácida? Principalmente efecto de las emisiones del hombre Las centrales térmicas generan los óxidos precursores de la lluvia ácida en gran cantidad así como los procesos de quema de combustibles fósiles (transporte) Fuentes naturales NOx: volcanes, descomposición biológica, etc SO 2: volcanes, océanos, descomposición biológica e incendios forestales Efectos de la lluvia ácida Lagos y ecosistemas acuáticos: Disminución del p. H de las masas de agua donde se deposita (más ácidas) modificación de las condiciones de vida acuática muerte de especies Plantas y suelos: Cuando el suelo se acidifica, se filtran los nutrientes esenciales (calcio y magnesio) a capas más profundas antes de que los árboles y las plantas puedan usarlos para crecer (Lixiviación de nutrientes) Edificios y monumentos: Los hechos de piedra caliza o mármol (carbonato cálcico, Ca. CO 3), que se disuelve fácilmente en los ácidos que forman parte de la lluvia ácida, se van deteriorando y perdiendo sus formas y detalles Otros materiales Con la lluvia ácida se corroen los metales, las pinturas, algunos plásticos, el cuero o las telas Los materiales más resistentes son el acero inoxidable y el aluminio 19

Efectos de la lluvia ácida La acidez puede causar daños severos a los árboles Muerte de bosques en el oeste de West Karkonosze Range (las Mts. Sudety), en la frontera Checo-polaca Autor: Witold Goraczko Daños provocados por la lluvia ácida Estatua del año 1702 de arenisca fotografiada en 1908 (izquierda) y en 1969 (derecha) 20
- Slides: 20