Evaluacin de la Contaminacin Ambiental Tema 3 Procesos

Evaluación de la Contaminación Ambiental Tema 3. - Procesos físicos y químicos en la atmósfera Parte II → La pérdida de ozono estratosférico
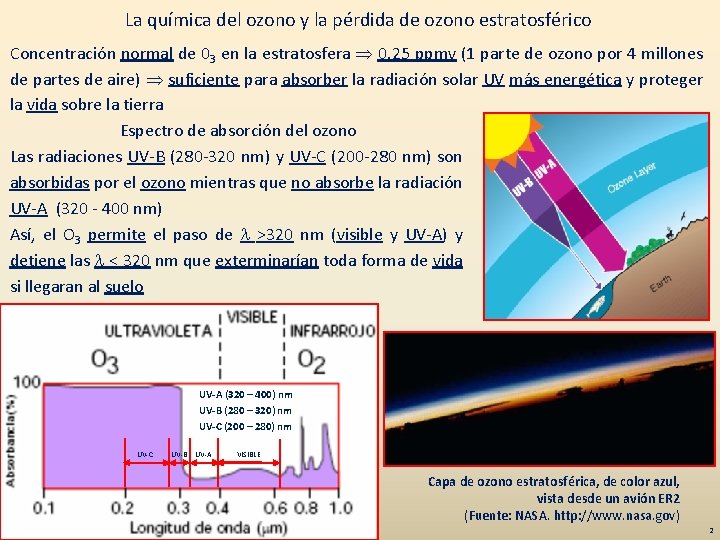
La química del ozono y la pérdida de ozono estratosférico Concentración normal de 03 en la estratosfera 0. 25 ppmv (1 parte de ozono por 4 millones de partes de aire) suficiente para absorber la radiación solar UV más energética y proteger la vida sobre la tierra Espectro de absorción del ozono Las radiaciones UV-B (280 -320 nm) y UV-C (200 -280 nm) son absorbidas por el ozono mientras que no absorbe la radiación UV-A (320 - 400 nm) Así, el O 3 permite el paso de l >320 nm (visible y UV-A) y detiene las l < 320 nm que exterminarían toda forma de vida si llegaran al suelo UV-A (320 – 400) nm UV-B (280 – 320) nm UV-C (200 – 280) nm UV-C UV-B UV-A VISIBLE Capa de ozono estratosférica, de color azul, vista desde un avión ER 2 (Fuente: NASA. http: //www. nasa. gov) 2
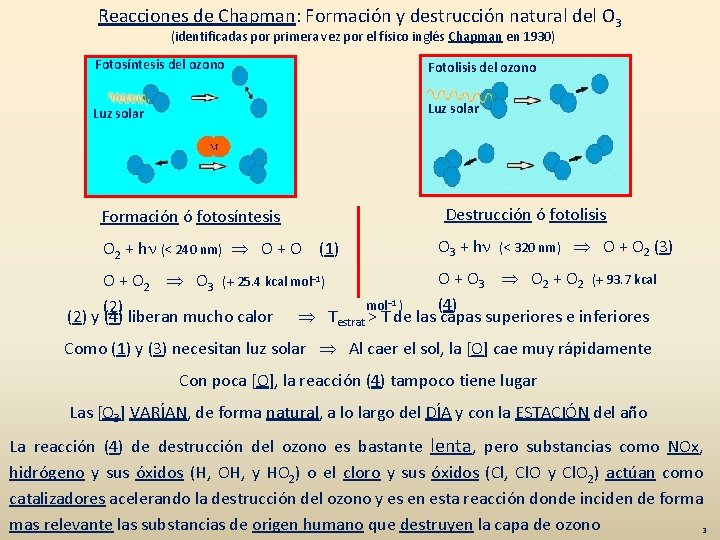
Reacciones de Chapman: Formación y destrucción natural del O 3 (identificadas por primera vez por el físico inglés Chapman en 1930) Fotosíntesis del ozono Fotolisis del ozono Luz solar Destrucción ó fotolisis Formación ó fotosíntesis O 2 + hn (< 240 nm) O + O (1) O 3 + hn (< 320 nm) O + O 2 (3) O + O 3 O 2 + O 2 (+ 93. 7 kcal O + O 2 O 3 (+ 25. 4 kcal mol− 1) mol− 1 ) (4) (2) y (4) liberan mucho calor Testrat > T de las capas superiores e inferiores Como (1) y (3) necesitan luz solar Al caer el sol, la [O] cae muy rápidamente Con poca [O], la reacción (4) tampoco tiene lugar Las [O 3] VARÍAN, de forma natural, a lo largo del DÍA y con la ESTACIÓN del año La reacción (4) de destrucción del ozono es bastante lenta, pero substancias como NOx, hidrógeno y sus óxidos (H, OH, y HO 2) o el cloro y sus óxidos (Cl, Cl. O y Cl. O 2) actúan como catalizadores acelerando la destrucción del ozono y es en esta reacción donde inciden de forma mas relevante las substancias de origen humano que destruyen la capa de ozono 3

Distribución vertical de ozono observada (valores inferiores) y estimada usando las ecuaciones de Chapman En la década de 1970 comenzó a observarse que las concentraciones medidas de ozono estratosférico no podían explicarse simplemente con las sencillas reacciones de Chapman Medidas de ozono estratosférico muestran que disminuye la concentración en cierta época del año especialmente (pero no exclusivamente) sobre los polos Crutzen, Molina, Rowland (Premios Nobel de Química en 1995) y otros científicos desarrollaron la teoría acerca de la implicación de productos químicos emitidos a la atmósfera por la actividad humana (compuestos halogenados que contienen cloro, bromo y también NOx, entre otros) en la química del ozono Zona del Agujero de ozono: región polar en la que la cantidad de ozono total < 220 UD 4
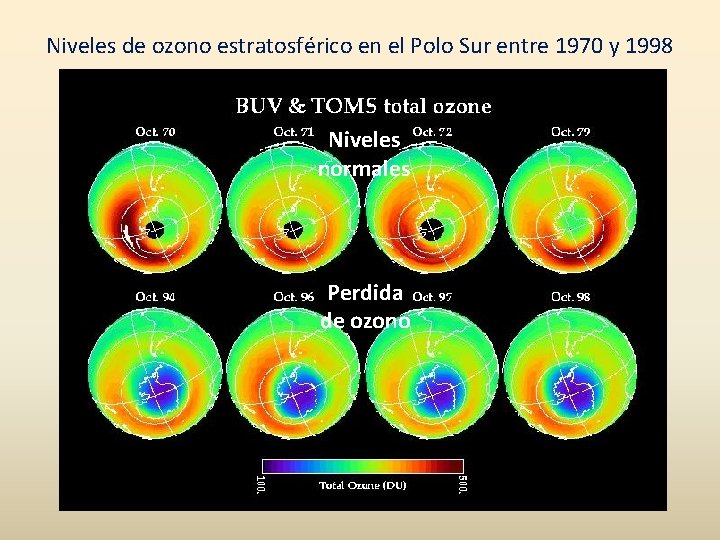
Niveles de ozono estratosférico en el Polo Sur entre 1970 y 1998 Niveles normales Perdida de ozono

Preguntas: → ¿De dónde sale el ozono y CFCs que hay en los polos si sus zonas de producción son las latitudes bajas o medias? → ¿De qué forma pueden destruir el ozono de la estratosfera, unas moléculas tan estables y poco reactivas como los CFCs? → ¿Por qué desaparece tanto ozono, si tenemos muchas más moléculas de ozono que de CFCs? → ¿Por qué desaparece el ozono de la estratosfera sobre las regiones polares principalmente? → ¿Por qué solo se produce destrucción en determinada época del año ? 6
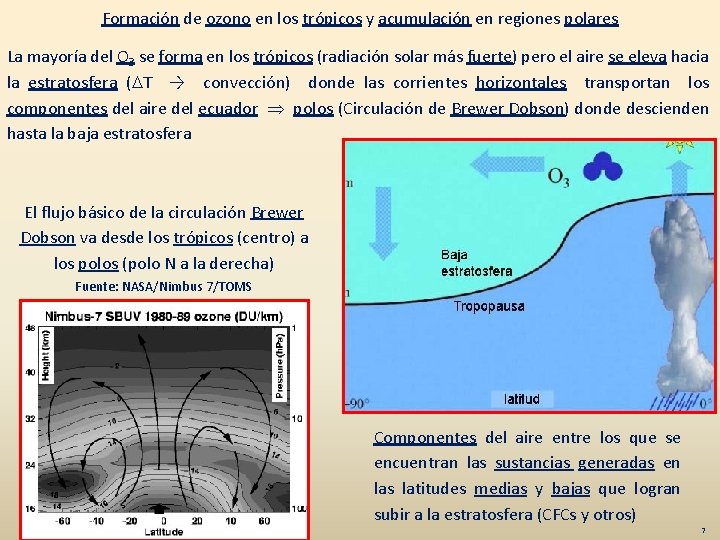
Formación de ozono en los trópicos y acumulación en regiones polares La mayoría del O 3 se forma en los trópicos (radiación solar más fuerte) pero el aire se eleva hacia la estratosfera (DT → convección) donde las corrientes horizontales transportan los componentes del aire del ecuador polos (Circulación de Brewer Dobson) donde descienden hasta la baja estratosfera El flujo básico de la circulación Brewer Dobson va desde los trópicos (centro) a los polos (polo N a la derecha) Fuente: NASA/Nimbus 7/TOMS Componentes del aire entre los que se encuentran las sustancias generadas en las latitudes medias y bajas que logran subir a la estratosfera (CFCs y otros) 7
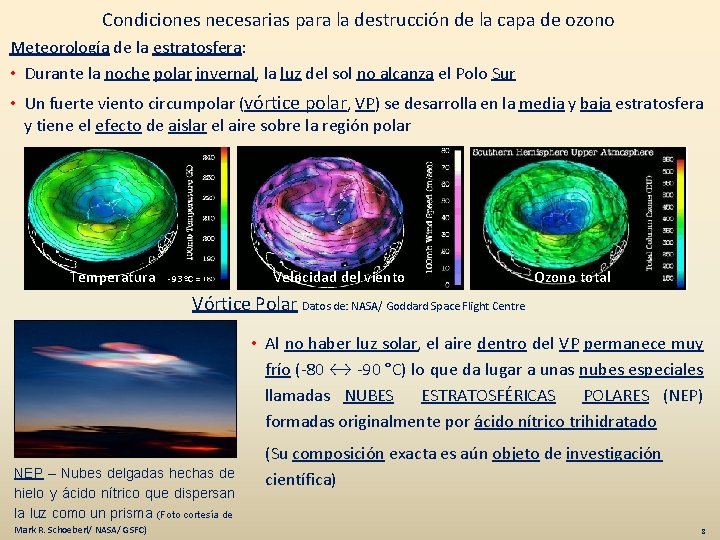
Condiciones necesarias para la destrucción de la capa de ozono Meteorología de la estratosfera: • Durante la noche polar invernal, la luz del sol no alcanza el Polo Sur • Un fuerte viento circumpolar (vórtice polar, VP) se desarrolla en la media y baja estratosfera y tiene el efecto de aislar el aire sobre la región polar Temperatura -93 ºC = Velocidad del viento Ozono total Vórtice Polar Datos de: NASA/ Goddard Space Flight Centre • Al no haber luz solar, el aire dentro del VP permanece muy frío (-80 ↔ -90 °C) lo que da lugar a unas nubes especiales llamadas NUBES ESTRATOSFÉRICAS POLARES (NEP) formadas originalmente por ácido nítrico trihidratado NEP – Nubes delgadas hechas de hielo y ácido nítrico que dispersan la luz como un prisma (Foto cortesía de Mark R. Schoeberl/ NASA/ GSFC) (Su composición exacta es aún objeto de investigación científica) 8

En la química del agujero de ozono tratamos con reacciones químicas poco comunes ya que sólo tienen lugar si en la atmósfera se presentan las condiciones A Invierno polar con la formación del VP y B Temperaturas lo suficientemente frías para la formación de NEP Las especies que son reservas de cloro (pero no destruyen el ozono), cloruro de hidrógeno (HCl) y nitrato de cloro (Cl. NO 3) -y sus equivalentes de bromo- se convierten en formas más activas en la superficie de las NEP La descomposición de los CFCs lleva a la obtención de radicales de cloro (Cl. O·), los cuales reaccionan con NO 2 y forman Cl. NO 3 (ó con NO y CH 4 y forman HCl) Cl. O + NO 2 → Cl. NO 3. . . Cl. O + NO → Cl + NO 2 # Cl + CH 4 → HCl + CH 3 En la superficie de estas nubes de hielo el HCl y Cl. NO 3 reaccionan entre sí y forman HNO 3 y cloro puro (Cl 2) que es una molécula estable y no reacciona con el ozono, pero es fácilmente fotolizado por la radiación UV dando lugar a 2 radicales de Cl, que atacan al ozono 9

Las reacciones más importantes (pero no las únicas) que se desarrollan en la superficie de las NEP (necesitan bajas temperaturas para que se den) llamadas reacciones heterogéneas (aquéllas que tienen lugar sobre superficies) y que conducen a la destrucción de O 3 son: Cl. NO 3 + HCl HNO 3 + Cl 2 (1) Cl. NO 3 + H 2 O HNO 3 + HOCl (2) HCl + HOCl H 2 O + Cl 2 (3) N 2 O 5 + HCl HNO 3 + Cl. NO 2 (4) N 2 O 5 + H 2 O 2 HNO 3 (5) Neto: 3 HCl + 2 Cl. NO 3 + H 2 O + 2 N 2 O 5 2 Cl 2 + 5 HNO 3 + Cl. NO 2 Estas reacciones son muy rápidas y sólo tienen lugar en la superficie de las NEP, razón por la cuál el agujero de O 3 fue una sorpresa Las reacciones heterogéneas no eran tenidas en cuenta en química atmosférica (al menos en la estratosfera), antes del descubrimiento del agujero de ozono ¡¡ Otra condición para que se destruya el ozono !! Que se den las reacciones heterogéneas que permiten que especies de reserva de Cl (y Br) sean rápidamente convertidas a formas más activas El HNO 3 formado en esas reacciones permanece en las partículas de las NEP, de tal manera que disminuye la concentración en fase gaseosa de los NOx (necesarios para formar el ácido) 10

Pero al producirse las reacciones heterogéneas (1) - (5) sólo tenemos cloro molecular (Cl 2) Para destruir ozono necesitamos cloro atómico El Cl 2 se fotodisocia fácilmente: Cl 2 + hn Cl· + Cl· Esquema de destrucción del O 3 Cl· + O Cl. O + O 3 2 Cl. O + O Cl· + O 2 Neto: O 3 + O O 2 + O 2 Esta es la clave para explicar el desarrollo temporal del agujero de ozono Durante el oscuro invierno polar (junio, julio y agosto), las temperaturas frías que tienen lugar en el vórtice conducen a la formación de NEP Las reacciones heterogéneas convierten las sustancias que representan formas de reserva de especies destructoras de ozono (cloro y bromo) en sus formas moleculares preparadas para la fotodisociación bajo la luz solar ¡cuando aparezca! En la primavera antártica (sept, oct y nov), retorna la luz del sol a la región polar y el Cl 2 se transforma rápidamente en cloro atómico → destrucción inmediata del ozono Las medidas de las especies químicas sobre el polo muestran altos niveles de formas activas de Cl, pero hay muchos más átomos de O 3 que de Cl activo, ¿cómo es posible que se destruya casi totalmente el O 3 en algunos periodos? 11
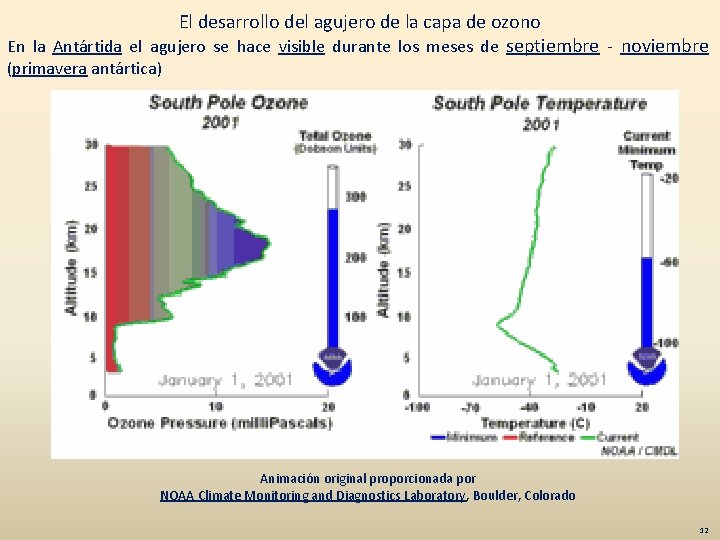
El desarrollo del agujero de la capa de ozono En la Antártida el agujero se hace visible durante los meses de septiembre - noviembre (primavera antártica) Animación original proporcionada por NOAA Climate Monitoring and Diagnostics Laboratory, Boulder, Colorado 12
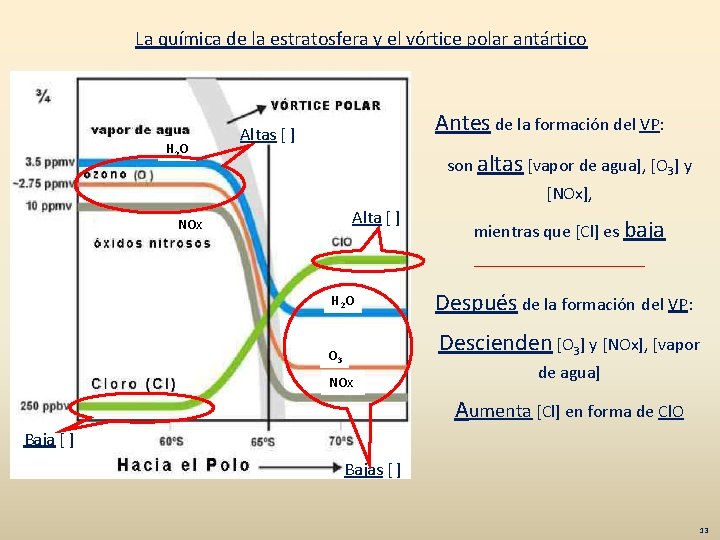
La química de la estratosfera y el vórtice polar antártico H 2 O Antes de la formación del VP: Altas [ ] son altas [vapor de agua], [O 3] y [NOx], Alta [ ] NOx H 2 O mientras que [Cl] es baja Después de la formación del VP: Descienden [O 3] y [NOx], [vapor O 3 NOx de agua] Aumenta [Cl] en forma de Cl. O Baja [ ] Bajas [ ] 13

La respuesta está en lo que conocemos como “ciclos catalíticos” ya que se realizan con la intervención de sustancias que resultan inalteradas, es decir, sustancias que actúan como catalizadores de las reacciones Ciclo catalítico II Cl. O + M Cl 2 O 2 + M* Cl. O + Br. O Br. Cl + O 2 · · Cl 2 O 2 + hn Cl· + Cl. O 2 Br. Cl + hn Br + Cl Cl. O 2 + M Cl· + O 2 + M* Cl· + O 3 Cl. O + O 2 2 x (Cl· + O Cl. O + O ) Br· + O Br. O + O 3 2 3 Global: 2 O 3 3 O 2 2 Global: 2 O 3 3 O 2 M es un componente atmosférico que absorbe la energía de las especies formadas y que se encuentran en un estado excitado El dímero del radical monóxido de cloro (Cl 2 O 2) involucrado en el Ciclo Catalítico (I) es térmicamente inestable y el ciclo es más efectivo a bajas temperaturas - Nuevamente, las bajas temperaturas en el vórtice polar durante el invierno vuelven a ser importantes – Ciclo Catalítico I - (70%) de la pérdida de ozono en la Antártida Ciclo Catalítico II – gobierna la pérdida en el Ártico (mucho menor que PN – más caliente) Con el aumento de temperatura, el cloro pierde actividad y los niveles de ozono aumentan También se han observado pérdidas de ozono en Canadá, Siberia y el Nde Europa 14
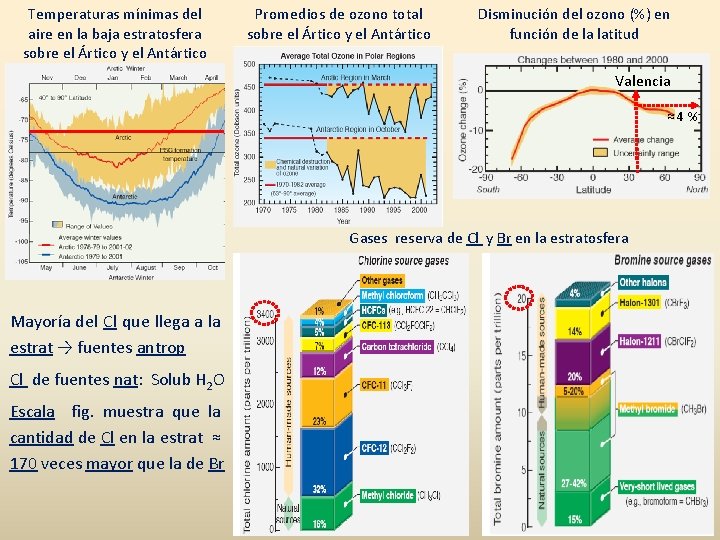
Temperaturas mínimas del aire en la baja estratosfera sobre el Ártico y el Antártico Promedios de ozono total sobre el Ártico y el Antártico Disminución del ozono (%) en función de la latitud Valencia ≈ 4 % Gases reserva de Cl y Br en la estratosfera Mayoría del Cl que llega a la estrat → fuentes antrop Cl de fuentes nat: Solub H 2 O Escala fig. muestra que la cantidad de Cl en la estrat ≈ 170 veces mayor que la de Br
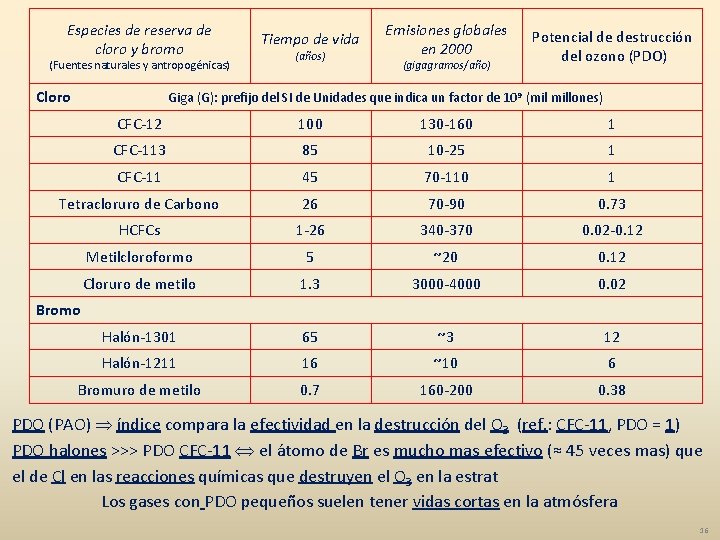
Especies de reserva de cloro y bromo (Fuentes naturales y antropogénicas) Cloro Tiempo de vida (años) Emisiones globales en 2000 (gigagramos/año) Potencial de destrucción del ozono (PDO) Giga (G): prefijo del SI de Unidades que indica un factor de 109 (mil millones) CFC-12 100 130 -160 1 CFC-113 85 10 -25 1 CFC-11 45 70 -110 1 Tetracloruro de Carbono 26 70 -90 0. 73 HCFCs 1 -26 340 -370 0. 02 -0. 12 Metilcloroformo 5 ~20 0. 12 Cloruro de metilo 1. 3 3000 -4000 0. 02 Halón-1301 65 ~3 12 Halón-1211 16 ~10 6 Bromuro de metilo 0. 7 160 -200 0. 38 Bromo PDO (PAO) índice compara la efectividad en la destrucción del O 3 (ref. : CFC-11, PDO = 1) PDO halones >>> PDO CFC-11 el átomo de Br es mucho mas efectivo (≈ 45 veces mas) que el de Cl en las reacciones químicas que destruyen el O 3 en la estrat Los gases con PDO pequeños suelen tener vidas cortas en la atmósfera 16

Resumen Las condiciones para la disminución del ozono estratosférico son: La circulación general transporta el ozono y los contaminantes desde su lugar de producción a los polos El invierno polar lleva a la formación del vórtice polar que aísla el aire (con las sustancias contaminantes) en su interior y deja los contaminantes en la baja estratosfera Las temperaturas frías que se dan dentro del VP permiten la formación de Nubes Estratosféricas Polares (NEP) que persisten mientras se mantiene aislado el aire en el VP En las NEP, tienen lugar las reacciones heterogéneas que convierten las reservas inactivas de cloro y bromo en formas más activas (cloro y bromo diatómicos) No hay pérdida de ozono hasta que el sol ilumina el aire dentro del VP y permite la producción de cloro y bromo activos (atómicos) e inicia los ciclos de destrucción catalítica 17
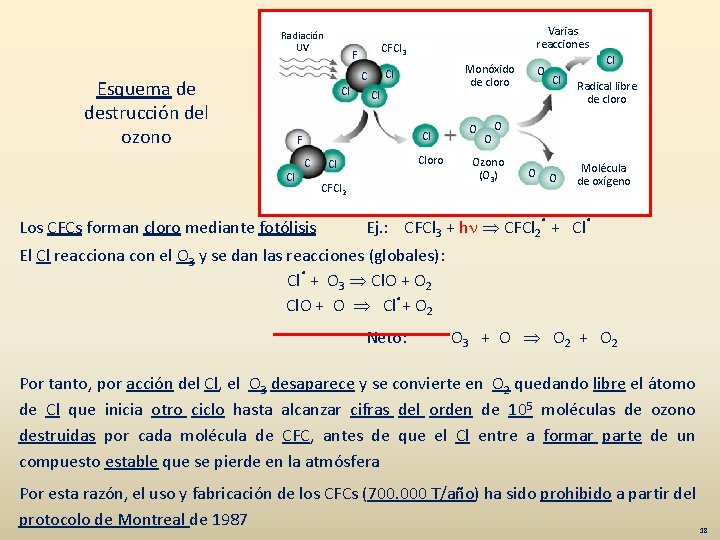
Radiación UV CFCl 3 F Cl Cl Cl F Cl Monóxido de cloro Cl C Esquema de destrucción del ozono Varias reacciones C Los CFCs forman cloro mediante fotólisis Cloro Cl CFCl 2 O O O Cl Cl Radical libre de cloro O Ozono (O 3) O O Molécula de oxígeno Ej. : CFCl 3 + hn CFCl 2· + Cl· El Cl reacciona con el O 3 y se dan las reacciones (globales): Cl· + O 3 Cl. O + O 2 Cl. O + O Cl·+ O 2 Neto: O 3 + O O 2 + O 2 Por tanto, por acción del Cl, el O 3 desaparece y se convierte en O 2 quedando libre el átomo de Cl que inicia otro ciclo hasta alcanzar cifras del orden de 105 moléculas de ozono destruidas por cada molécula de CFC, antes de que el Cl entre a formar parte de un compuesto estable que se pierde en la atmósfera Por esta razón, el uso y fabricación de los CFCs (700. 000 T/año) ha sido prohibido a partir del protocolo de Montreal de 1987 18
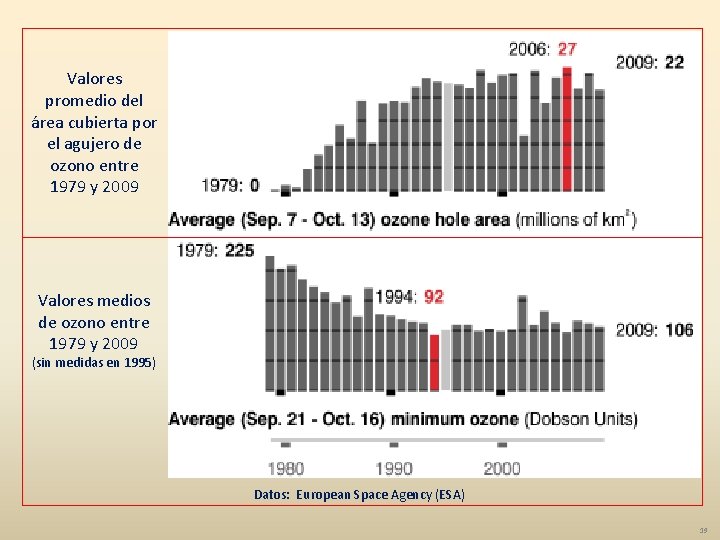
Valores promedio del área cubierta por el agujero de ozono entre 1979 y 2009 Valores medios de ozono entre 1979 y 2009 (sin medidas en 1995) Datos: European Space Agency (ESA) 19

El protocolo de Montreal En prevención de los riesgos que conlleva la destrucción de la capa de ozono, se elaboró en 1985 el Convenio de Viena para la Protección de la Capa de Ozono En 1987 se firmó el Protocolo de Montreal, relativo a las sustancias que afectan a la capa de ozono que entró en vigor en 1989 En 1997 se acordó un calendario para la eliminación del uso del bromuro de metilo (uno de los compuestos con mayor PDO) en Equivalente en cloro (compuestos de cloro y bromo globales) Disminución como consecuencia de los acuerdos contenidos en el Protocolo de Montreal el que se establece que los países desarrollados deben eliminar su consumo para el año 2005 (menos en aquellas actividades donde no exista desarrollo tecnológico que lo sustituya); los países en vías de desarrollo deberán eliminarlo en el año 2015 y se ratificó para el año 2030 la eliminación de los hidroclorofluorocarbonos También se creó un sistema de control del comercio de CFC's y otras sustancias que afectan a la capa de ozono, con el fin de prevenir su tráfico ilegal 20
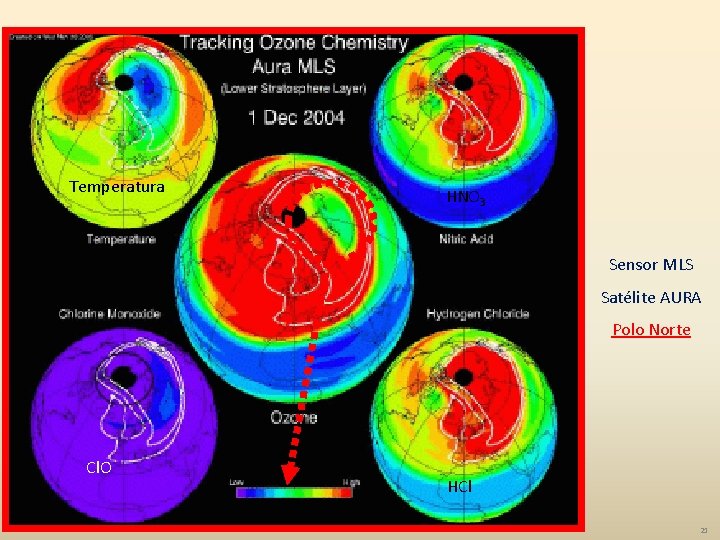
Temperatura HNO 3 Sensor MLS Satélite AURA Polo Norte Cl. O HCl 21
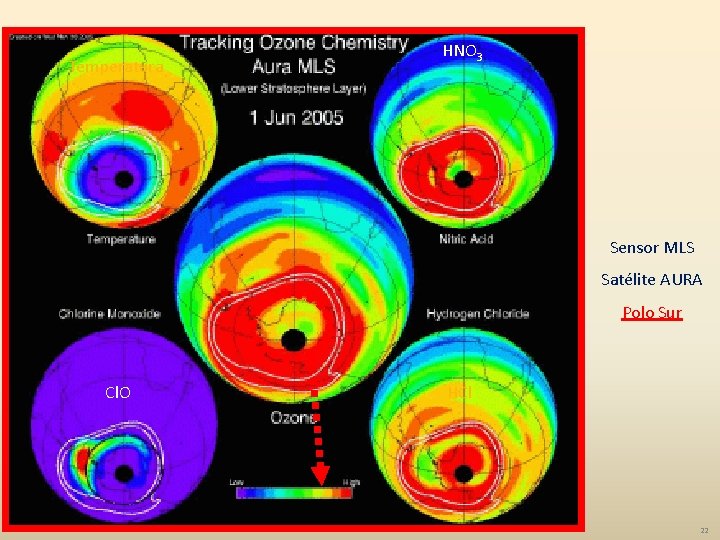
Temperatura HNO 3 Sensor MLS Satélite AURA Polo Sur Cl. O HCl 22
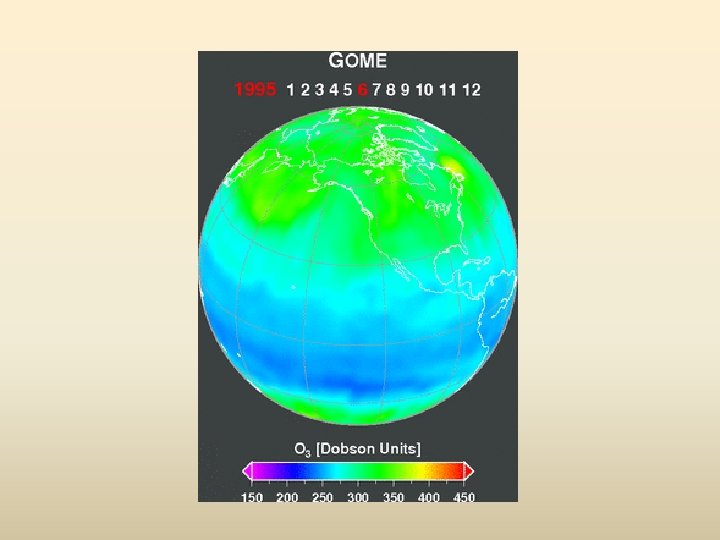
- Slides: 23