Estrutura Atmica tomo 3 partculas Quais so Descoberta

Estrutura Atômica

Átomo – 3 partículas Quais são? Descoberta o elétron – século XIX por Thomsom Próton - - século XX por Rutherford Neutron – 1932 por Chadwick Modelo atômico Núcleo – prótons e neutros Elétrons cercam o núcleo (como? )

Átomo identificado pelo número atômico (Z) e pelo número de massa (A) Z = número de prótons no núcleo A= número de prótons + nêutrons no núcleo A Ex: 16 ZX 8 O Todos os átomos de um mesmo elemento tem o mesmo número de prótons no núcleo Entretanto podem ter diferentes números de nêutrons em seu núcleo - Esses átomos são chamados de isótopos Ex: – 1 próton; 0 nêutron e 1 elétron 2 H – 1 próton; 1 nêutron e 1 elétron 1 3 H – 1 próton; 2 nêutron e 1 elétron 1 1 1 H

Massas Atômicas São expressas em unidade de massa atômica (u), é definida como 1/12 da massa de um átomo de carbono. A abundância isotópica maioria dos elementos é encontrada como uma mistura de isótopos Massas e abundâncias de isótopos são determinadas por espectrometria de massa A massa atômica de um elemento é calculada pela média das massas dos Isótopos destes elementos Massa atômica é diferente de número de massa Número de massa – número de partículas no núcleo Massa atômica – média das massas de todos os seus isótopos

1902 – Lewis propôs que os elétrons estão arranjados em níveis de energia começando próximo do núcleo e crescendo para fora Mas, onde estão localizados? Possuem energia? A elucidação da estrutura do átomo seria encontrada na natureza da luz emitida pelas substâncias a temperaturas altas ou sob influência de uma descarga elétrica. Luz é produzida quando elétrons nos átomos sofrem alterações de energia Luz, microondas, raios X sinais de rádio etc são chamados de radiações eletromagnéticas ou energia radiante
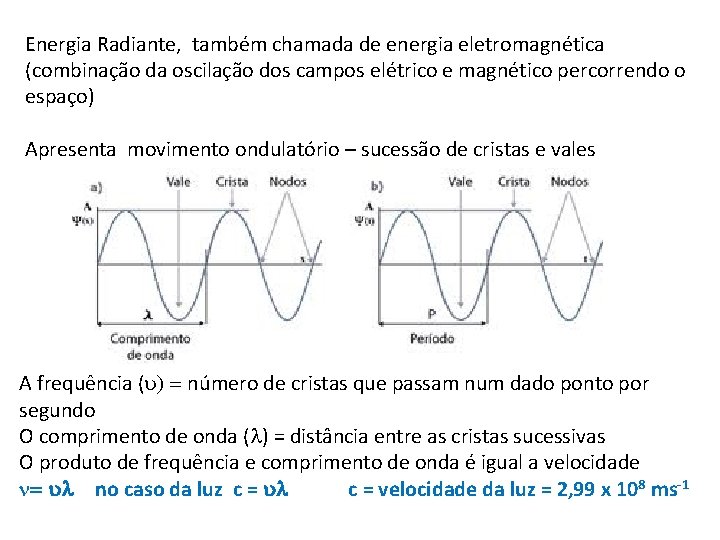
Energia Radiante, também chamada de energia eletromagnética (combinação da oscilação dos campos elétrico e magnético percorrendo o espaço) Apresenta movimento ondulatório – sucessão de cristas e vales A frequência (u) = número de cristas que passam num dado ponto por segundo O comprimento de onda (l) = distância entre as cristas sucessivas O produto de frequência e comprimento de onda é igual a velocidade n= ul no caso da luz c = ul c = velocidade da luz = 2, 99 x 108 ms-1

Quando eletricidade passa através do gás hidrogênio ou quando o gás é aquecido a alta temperatura, o hidrogênio emite luz Quando a luz atravessa um prisma não temos um espectro contínuo e sim uma linha espectral Linha espectral – conjunto de linhas distintas cada uma Produzida pela luz de um comprimento de onda discreta
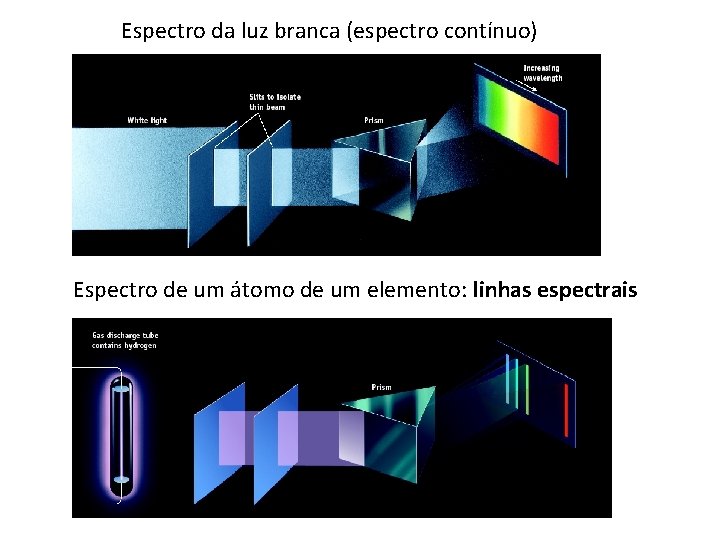
Espectro da luz branca (espectro contínuo) Espectro de um átomo de um elemento: linhas espectrais

Espectro da luz branca Espectro de emissão do H Espectro de emissão do Fe

Átomo de Bohr (1913) Elétrons num átomo emitem luz quando absorvem energia (eletricidade ou calor) e posteriormente liberam aquela energia na forma de luz A radiação emitida é limitada a certos comprimentos de onda o elétron Não está livre para qualquer quantidade de energia, ou seja, a energia de um elétron em um átomo é quantizada Início século XX – Planck e Einstein independentemente mostraram que Todas as radiações eletromagnéticas comportavam-se como pequenos Pacotes de energia denominados Fótons e que cada fóton tinham energia proporcional à frequência da radiação Efóton = hu Mas, c = ul então Efóton = hc /l
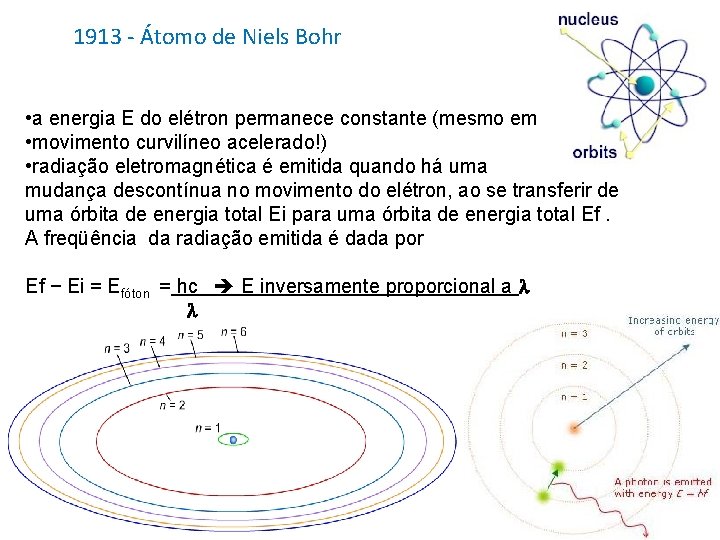
1913 - Átomo de Niels Bohr • a energia E do elétron permanece constante (mesmo em • movimento curvilíneo acelerado!) • radiação eletromagnética é emitida quando há uma mudança descontínua no movimento do elétron, ao se transferir de uma órbita de energia total Ei para uma órbita de energia total Ef. A freqüência da radiação emitida é dada por Ef − Ei = Efóton = hc E inversamente proporcional a l l

Ao receber energia o elétron é excitado a um nível de energia mais elevado e quando retorna emite energia, muitas vezes na forma de luz Estado fundamental – estado de mais baixa energia Estado excitado – estado de mais alta energia (instável) A teoria de Bohr explicou muito bem o átomo de hidrogênio e ao fazê-lo foi capaz de obter a equação de Rydberg ΔE = Rhc/nf 2 − Rhc/ni 2 R = cte de Rydberg = 1, 097 x 107 m-1 h = cte de Planck c = velocidade da luz n = número quântico principal ΔE = Ef – Ei
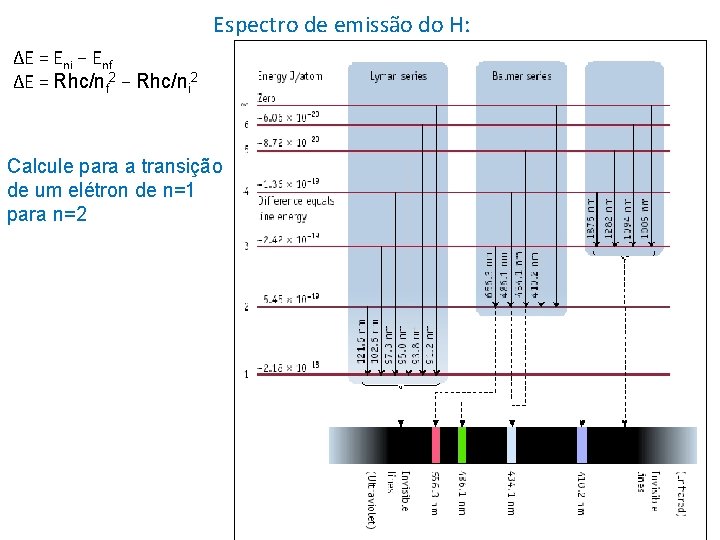
Espectro de emissão do H: ΔE = Eni − Enf ΔE = Rhc/nf 2 − Rhc/ni 2 Calcule para a transição de um elétron de n=1 para n=2

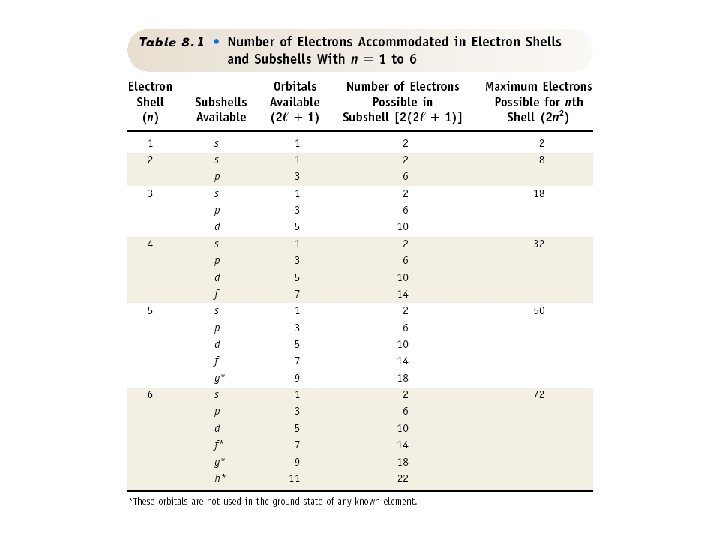
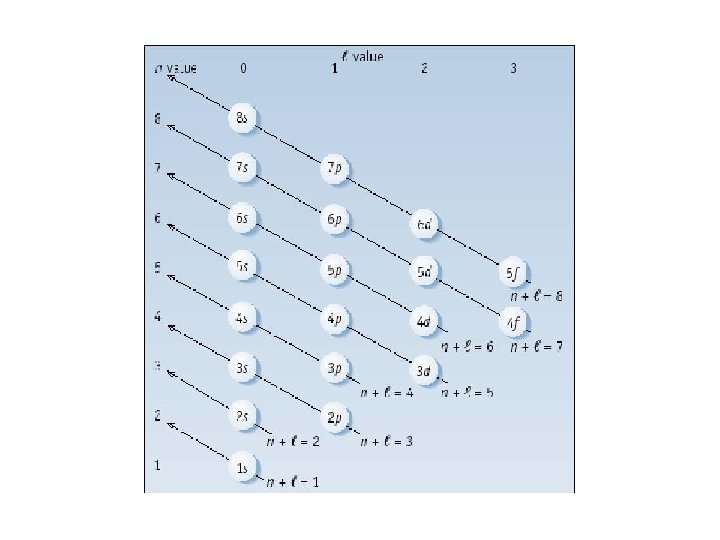
Modelo da mecânica quântica A quantização de energias eletrônicas são descritas em termos de orbitais Os orbitais são agrupados em subníveis de energia ou subcamadas – s, p, d, f Os subníveis de energia são agrupados em níveis de energia ou camadas – K, L, M. N. . Para denominar a camada, a subcamada e o orbital podemos usar quatro números quânticos

Os números quânticos são n, l e m 1. Número quântico principal, n. Este é o mesmo n de Bohr. Tem valores n=1, 2, 3, 4, … Representa fisicamente o nível de energia (camada) principal em que o elétron se encontra. 2. O número quântico azimutal, l. Podem assumir os valores: l = 0, 1, 2, 3, (n-1) Normalmente utilizamos letras para l (s, p, d, f ) Representam fisicamente o sub-nível do elétron e sua forma geométrica no espaço. 3. O número quântico magnético, m. Tem os valores: m = -l , 0 , +l Representa fisicamente a orientação espacial do orbital do elétron, a quantidade de valores possíveis para l determina o número de orbitais existentes em um sub-nível l.

Spin Eletrônico 1920 – demonstração experimental que o elétron comporta-se como se tivesse uma rotação Esta rotação é representada por um quarto número quântico – número Quântico magnético de spin eletrônico ms Uma orientação é associada com um valor do número quântico spin do elétron ms = +½ e outra com um valor de ms = -½

Princípio da Exclusão de Pauli em princípio, nada impediria que todos os elétrons de um átomo ficassem no mais baixo nível de energia (1 s). O que aconteceria ? se assim fosse, as ligações químicas não existiriam dois elétrons de um mesmo átomo não podem ter o mesmo conjunto de números quânticos (n, l, ml , ms) em outras palavras, nenhum orbital atômico pode conter mais que 2 elétrons

Representação dos Orbitais s • os orbitais s são esféricos. • À medida que n aumenta, os orbitais s ficam maiores.
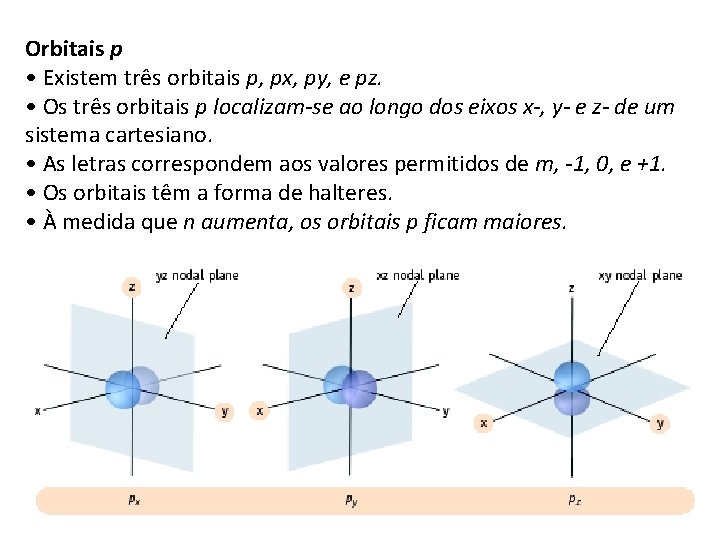
Orbitais p • Existem três orbitais p, px, py, e pz. • Os três orbitais p localizam-se ao longo dos eixos x-, y- e z- de um sistema cartesiano. • As letras correspondem aos valores permitidos de m, -1, 0, e +1. • Os orbitais têm a forma de halteres. • À medida que n aumenta, os orbitais p ficam maiores.
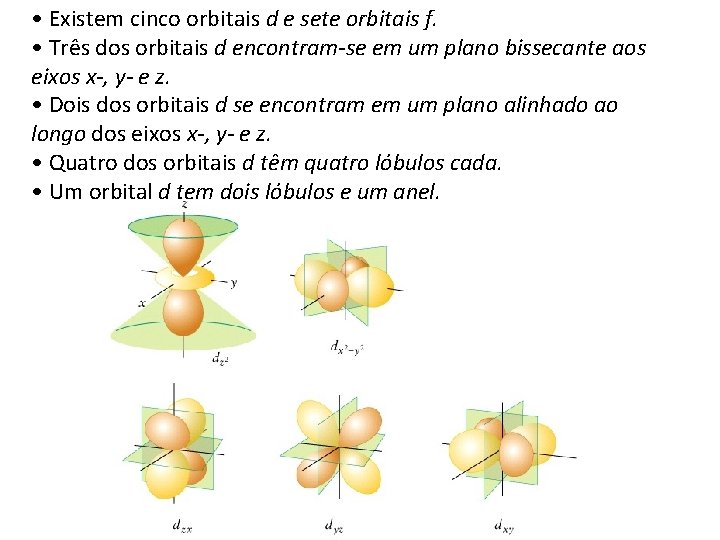
• Existem cinco orbitais d e sete orbitais f. • Três dos orbitais d encontram-se em um plano bissecante aos eixos x-, y- e z. • Dois dos orbitais d se encontram em um plano alinhado ao longo dos eixos x-, y- e z. • Quatro dos orbitais d têm quatro lóbulos cada. • Um orbital d tem dois lóbulos e um anel.
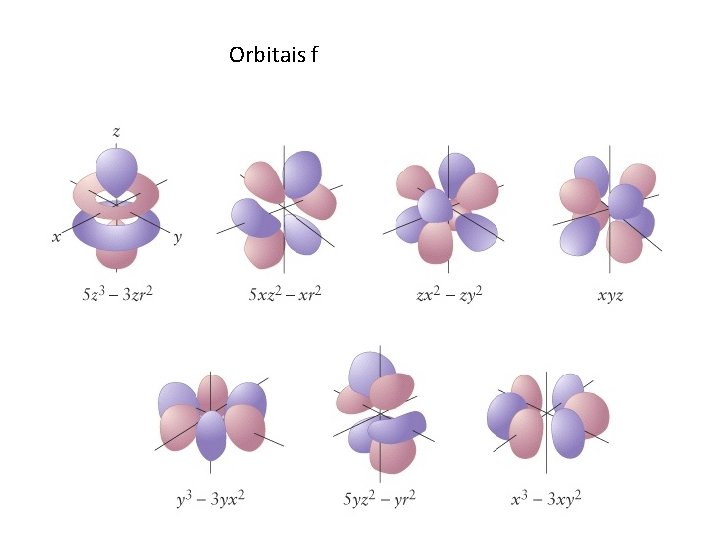
Orbitais f
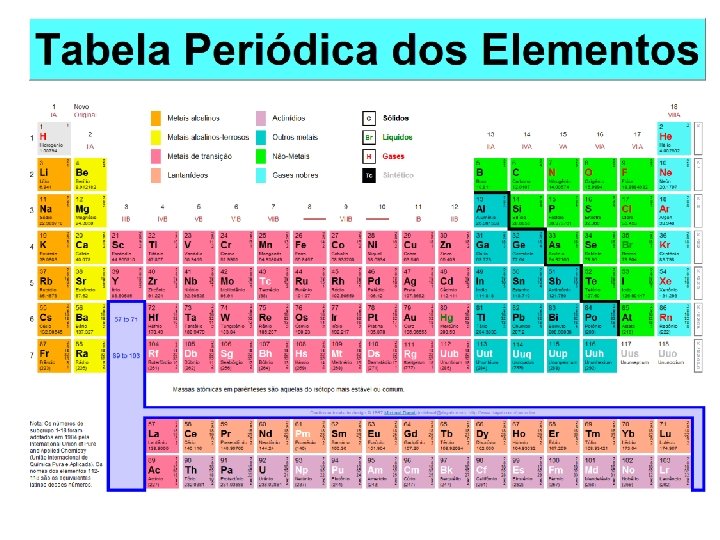
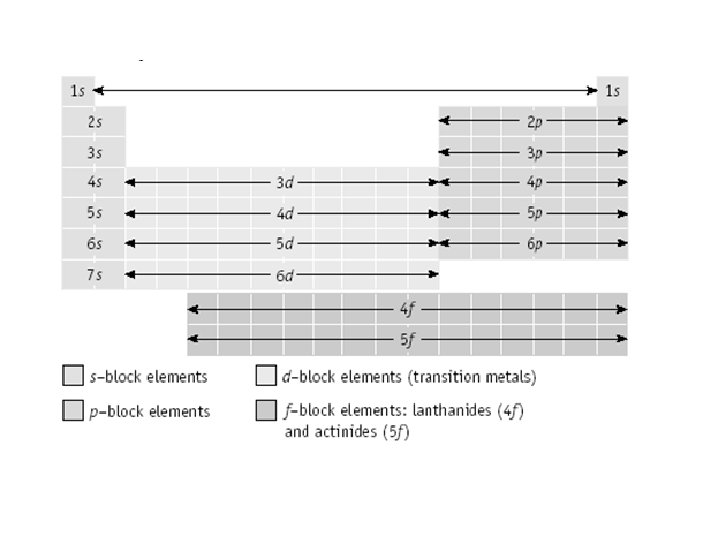

Tabela Periódica e a configuração eletrônica • A tabela periódica pode ser utilizada como um guia para as configurações eletrônicas. • O número do periodo é o valor de n. • Os grupos 1 e 2 têm o orbital s preenchido. • Os grupos 13 - 18 têm o orbital p preenchido. • Os grupos 3 - 12 têm o orbital d preenchido. • Os lantanídeos e os actinídeos têm o orbital f preenchido. Há vários modos de representar as configurações, os principais são: Notação s p d f Notação de caixas Exemplos das duas notações

Configurações eletrônica condensadas • O neônio tem o subnível 2 p completo. • O sódio marca o início de um novo período. • Logo, escrevemos a configuração eletrônica condensada para o sódio como Na: [Ne] 3 s 1 • [Ne] representa a configuração eletrônica do neônio. • Elétrons mais internos: os elétrons no [Gás Nobre]. • Elétrons de valência: os elétrons fora do [Gás Nobre].

Metais de Transição • Depois de Ar, os orbitais d começam a ser preenchidos Depois que os orbitais 3 d estiverem preenchidos, os orbitais 4 p começam a ser preenchidos Metais de transição são os elementos nos quais os elétrons d são os elétrons de valência

Lantanídeos e actinídeos Do Ce em diante, os orbitais 4 f começam a ser preenchidos. Observe: La: [Kr]6 s 25 d 14 f 1 Os elementos Ce -Lu têm os orbitais 4 f preenchidos e são chamados lantanídeos ou elementos terras raras. Os elementos Th -Lr têm os orbitais 5 f preenchidos e são chamados actinídeos. A maior parte dos actinídeos não é encontrada na natureza.

TENDÊNCIAS PERIÓDICAS X CONFIGURAÇÃO ATÔMICA

Tendências Periódicas Gerais • Raios atômico e iônico • Energia de ionização • Afinidade eletrônica
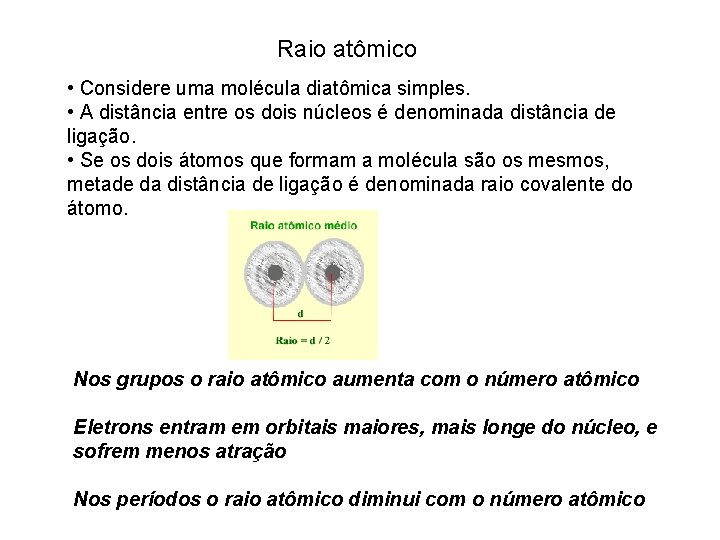
Raio atômico • Considere uma molécula diatômica simples. • A distância entre os dois núcleos é denominada distância de ligação. • Se os dois átomos que formam a molécula são os mesmos, metade da distância de ligação é denominada raio covalente do átomo. Nos grupos o raio atômico aumenta com o número atômico Eletrons entram em orbitais maiores, mais longe do núcleo, e sofrem menos atração Nos períodos o raio atômico diminui com o número atômico

Z* aumenta e- externos mais fortemente atraídos n aumenta tamanho do orbital mais externo aumenta
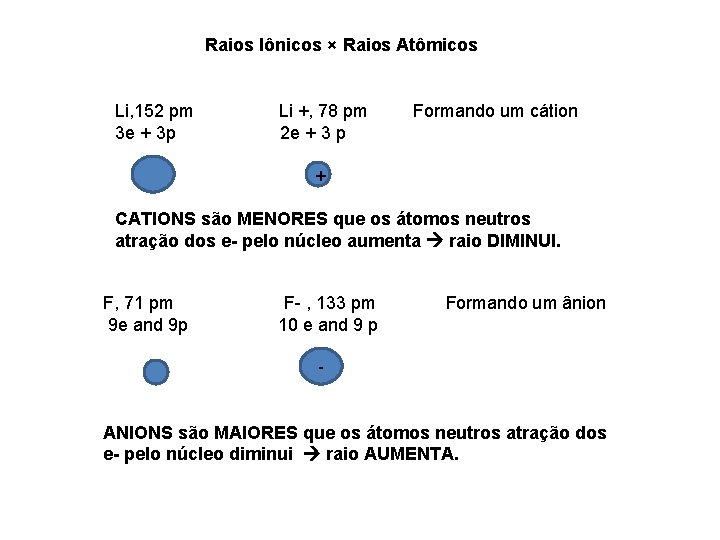
Raios Iônicos × Raios Atômicos Li, 152 pm 3 e + 3 p Li +, 78 pm 2 e + 3 p Formando um cátion + CATIONS são MENORES que os átomos neutros atração dos e- pelo núcleo aumenta raio DIMINUI. F, 71 pm 9 e and 9 p F- , 133 pm 10 e and 9 p Formando um ânion ANIONS são MAIORES que os átomos neutros atração dos e- pelo núcleo diminui raio AUMENTA.
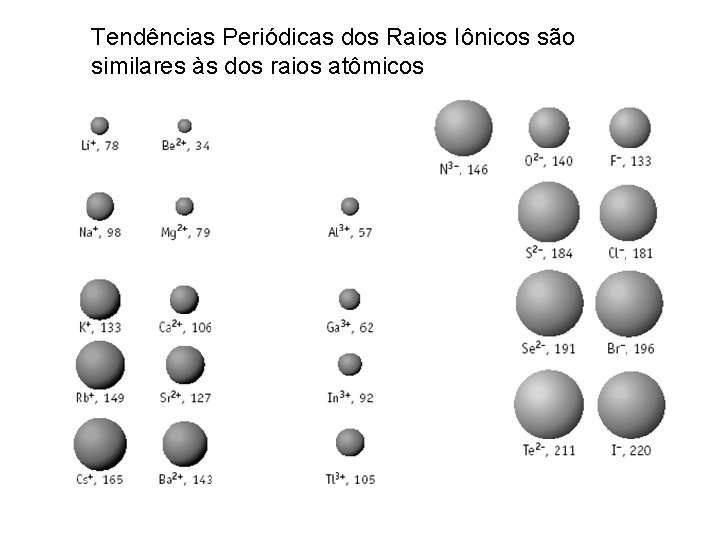
Tendências Periódicas dos Raios Iônicos são similares às dos raios atômicos

Energia de Ionização (E. I) - uma medida da tendência a formar cátions - quantidade de energia necessária para retirar (energia gasta) 1 mol de elétrons de 1 mol de átomos no estado gasoso Seu valor tem sinal +. exemplo: Cu(g) Cu+(g) + e−(g), I 1 = +785 k. J · mol− 1 (primeira energia de ionização) Cu+(g) Cu 2+(g) + e−(g), I 2 = +1955 k. J · mol− 1 (segunda energia de ionização Carga positiva Aumenta EI aumenta energia de ionização baixa =) elementos formam cátions (metais; bons condutores elétricos) Correlacionar com raio
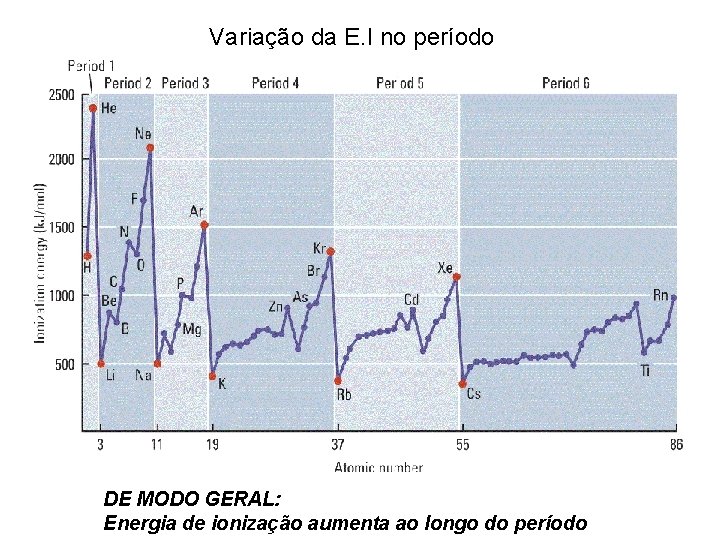
Variação da E. I no período DE MODO GERAL: Energia de ionização aumenta ao longo do período

EI aumenta no período porquê o raio diminue. • Metais perdem eletrons mais facilmente que não metais. • Metais são agentes redutores fortes. Variação da Energia de Ionização no Grupo • EI diminui com o número atômico no grupo • Raio atômico aumenta, facilitando a remoção de eletrons. • Elementos se tornam agentes redutores mais fortes.

Afinidade Eletrônica (A. E) Energia perdida ou ganha quando um átomo recebe um eletron formando um ânion A(g) + e- A-(g) A. E. = ΔE da reação O (g) + e- O-(g) O [He]2 s 22 p 4 O- [He]2 s 22 p 5 AE = - 141 k. J/mol Δ E é Exotérmica = energia da atração (e- + núcleo) maior que a da repulsão entre 2 e- no mesmo orbital p Comparar com raio - é uma medida da tendência a formar ânions estáveis - é o negativo da variação de energia de quando um elétron é aceito por um átomo no estado gasoso, para originar um ânion - afinidade eletrônica grande e positiva =) ânion é estável (não-metais)
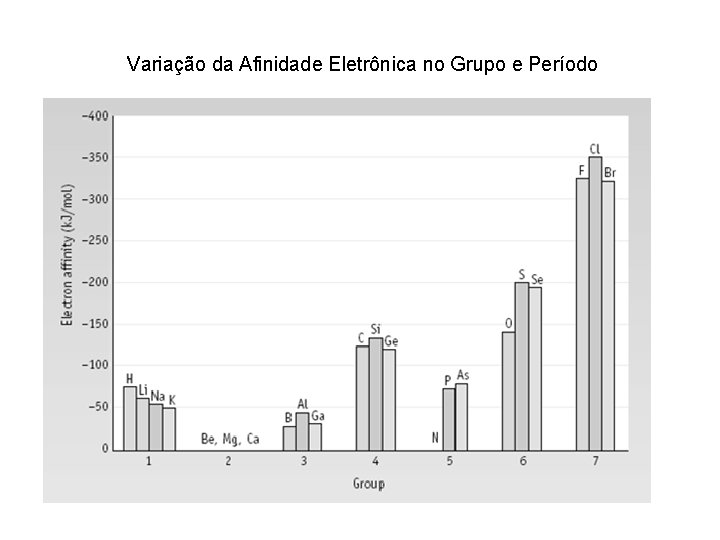
Variação da Afinidade Eletrônica no Grupo e Período

• Afinidade eletrônica aumenta com número atômico no período (devido o raio diminuir) • Afinidade eletrônica diminui com número atômico nos grupos (aumento do raio atômico = menor interação com o núcleo) Seu valor tem sempre sinal negativo (libera energia) Átomo F Cl Br I AE -328 k. J -349 k. J -325 k. J -295 k. J
- Slides: 41