ESTRUCTURAS DE LEWIS FORMULAS DE PUNTOS Escriba La

ESTRUCTURAS DE LEWIS (FORMULAS DE PUNTOS): Ø Ø Ø Escriba La fórmula de Lewis para el Na. HSO 4 Escriba La fórmula de Lewis para el CO 3 -2 Escriba La fórmula de Lewis para el Na 3 PO 4 Escriba La fórmula de Lewis para el SCl 2 Excepciones regla del octeto: PCl 5 , NO

FUERZAS INTERIONICAS: Øla fuerza de atracción entre iones con carga opuesta

FUERZAS INTRAMOLECULARES: ØSon las fuerzas que existen dentro de la molécula debido a sus enlaces

FUERZAS INTERMOLECULARES: ØSon las fuerzas de atracción que existe entre las moléculas

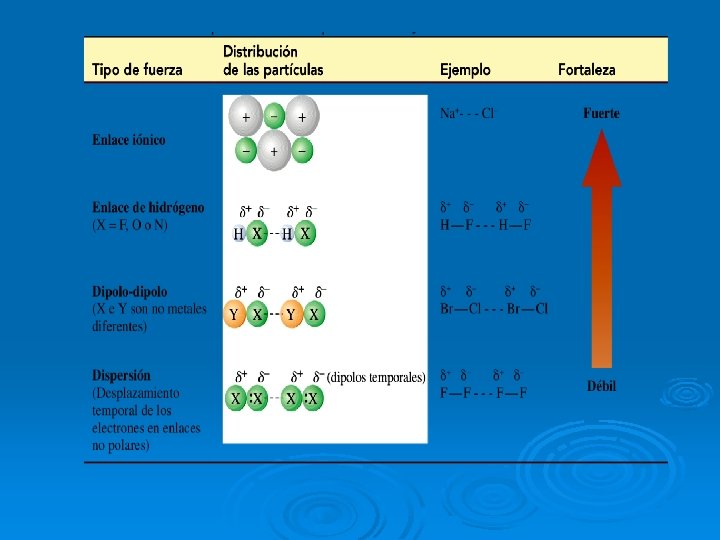
FUERZAS INTERMOLECULARES: Ø Reciben el nombre de Fuerzas de Van Der Waals Ø Contribuyen a determinar las propiedades físicas de las sustancias. Ø Existen 3 tipos: Fuerzas Dipolares, Puentes de Hidrógeno y Fuerzas de dispersión
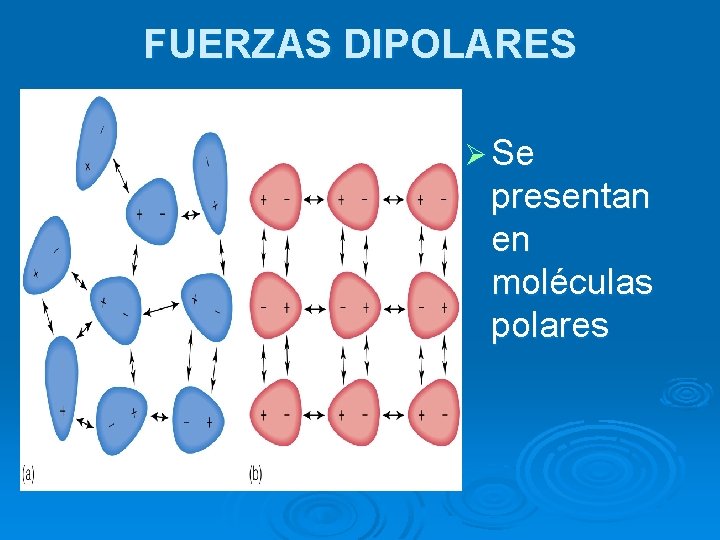
FUERZAS DIPOLARES Ø Se presentan en moléculas polares

FUERZAS DIPOLARES Las moléculas que tienen centros separados y no equilibrados de carga opuestas reciben el nombre de dipolos (ej: HCl). Ø Las moléculas polares se atraen como resultado de las fuerzas que ejercen los centros de carga parcial: el extremos negativo de una molécula atrae al extremo positivo de otra molécula. Ø
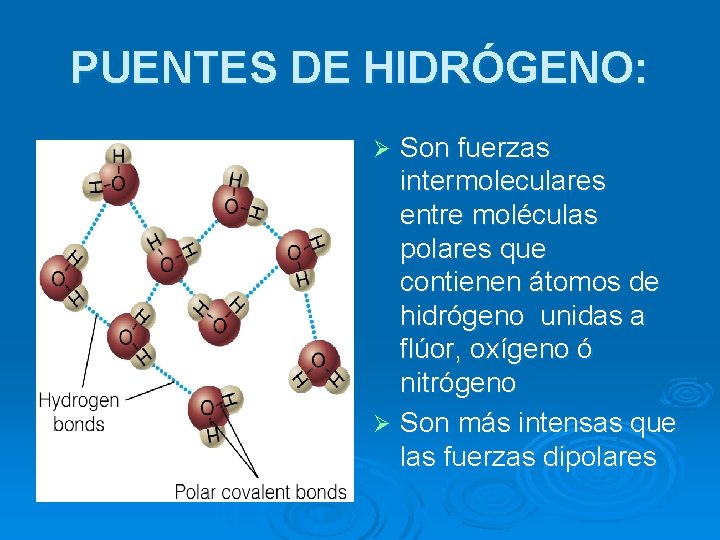
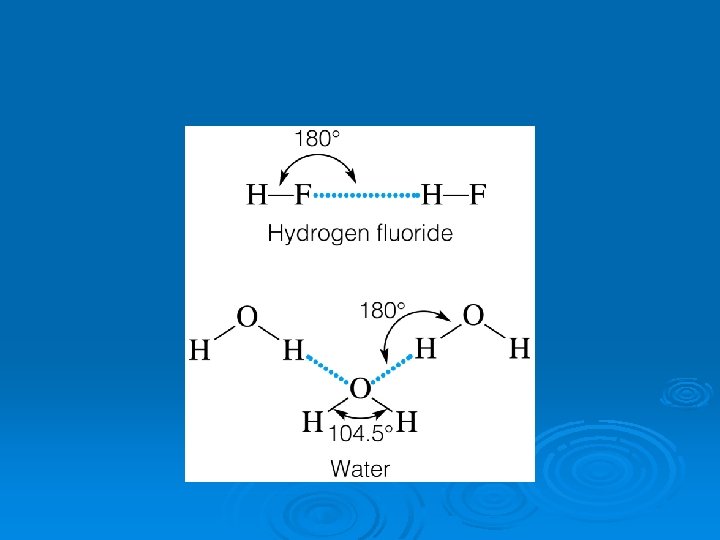
PUENTES DE HIDRÓGENO: Son fuerzas intermoleculares entre moléculas polares que contienen átomos de hidrógeno unidas a flúor, oxígeno ó nitrógeno Ø Son más intensas que las fuerzas dipolares Ø

CARACTERÍSTICAS: Ø Se presentan en compuestos en los cuales el hidrógeno está enlazado a elementos muy electronegativos (fluor , oxígeno ó nitrógeno) Ø El átomo más electronegativo adquiere carga parcial negativa, el hidrógeno queda con carga parcial positiva.
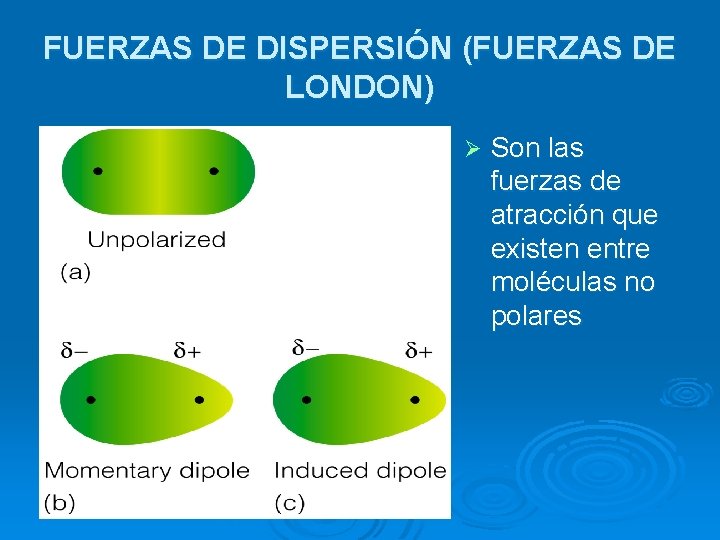
FUERZAS DE DISPERSIÓN (FUERZAS DE LONDON) Ø Son las fuerzas de atracción que existen entre moléculas no polares

FUERZAS DE DISPERSIÓN (FUERZAS DE LONDON) Ø Estas fuerzas se originan debido a dipolos momentáneos, que son inducidas por el movimiento de los electrones: la nube electrónica de la molécula puede distorcionarse y se produce un dipolo en el cual una parte de la molécula es ligeramente más negativa que el resto.

Ø Son más intensas en moléculas no polares más grandes que en las pequeñas: debido a que los átomos más grandes tienen nubes electrónicas de mayor tamaño, los electrones están más lejos del núcleo y por consiguiente son más polarizables.

Diga que tipo de fuerzas mantienen unidos a los siguientes compuestos: 1. 2. 3. 4. 5. 6. 7. HCl _________ H 2 O_________ Cl 2_________ NH 3______________ Na. Br______________ Ba. H 2____________ KCl____________
- Slides: 15