ESTRUCTURA ATOMICA QUIMICA GENERAL CONTENIDO Estructura Atmica Numero







- Slides: 10

ESTRUCTURA ATOMICA QUIMICA GENERAL

CONTENIDO » Estructura Atómica. » Numero y Peso atómico. » Isotopos. » Evolución de la teoría atómica. » Principio de Incertidumbre de Heinsemberg. .

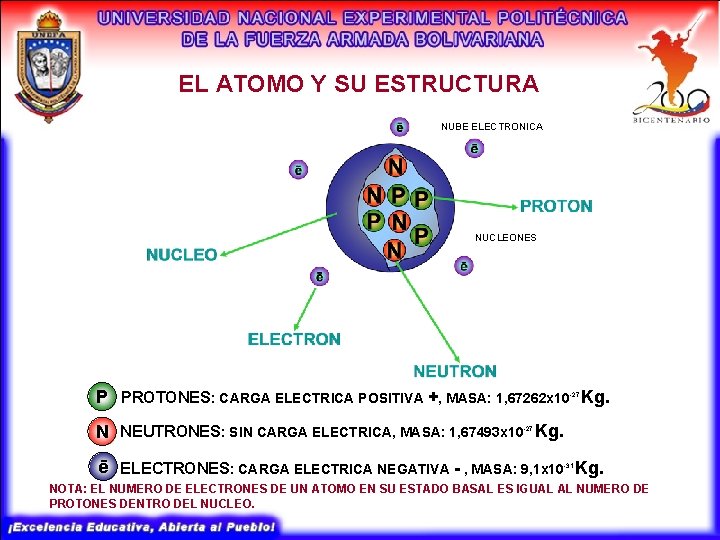
EL ATOMO Y SU ESTRUCTURA NUBE ELECTRONICA NUCLEONES P PROTONES: CARGA ELECTRICA POSITIVA +, MASA: 1, 67262 x 10 Kg. -27 N NEUTRONES: SIN CARGA ELECTRICA, MASA: 1, 67493 x 10 Kg. -27 ē ELECTRONES: CARGA ELECTRICA NEGATIVA - , MASA: 9, 1 x 10 Kg. -31 NOTA: EL NUMERO DE ELECTRONES DE UN ATOMO EN SU ESTADO BASAL ES IGUAL AL NUMERO DE PROTONES DENTRO DEL NUCLEO.

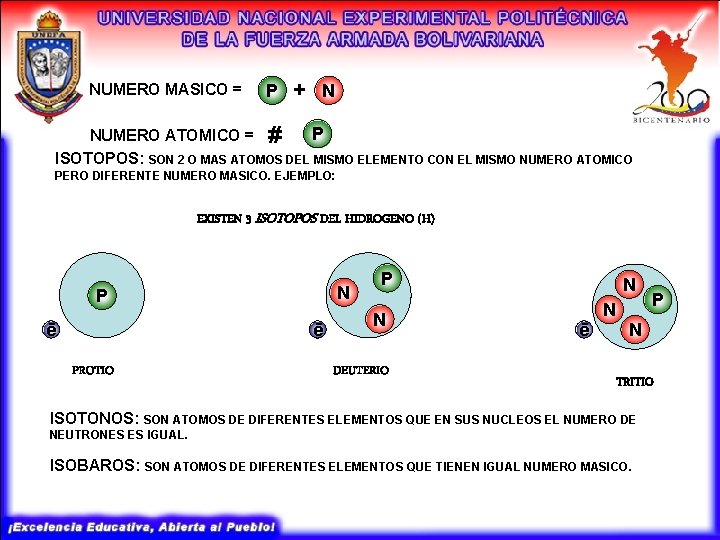
NUMERO MASICO = P + N P NUMERO ATOMICO = # ISOTOPOS: SON 2 O MAS ATOMOS DEL MISMO ELEMENTO CON EL MISMO NUMERO ATOMICO PERO DIFERENTE NUMERO MASICO. EJEMPLO: EXISTEN 3 ISOTOPOS DEL HIDROGENO (H) N P ē ē PROTIO P N DEUTERIO N ē N P N TRITIO ISOTONOS: SON ATOMOS DE DIFERENTES ELEMENTOS QUE EN SUS NUCLEOS EL NUMERO DE NEUTRONES ES IGUAL. ISOBAROS: SON ATOMOS DE DIFERENTES ELEMENTOS QUE TIENEN IGUAL NUMERO MASICO.

¤ LA CARGA ELECTRICA DE UN ATOMO ES DE 0 (CERO) YA QUE SE EQUILIBRAN ENTRE LOS PROTONES Y ELECTRONES. ¤ LA MAYOR MASA DE UN ATOMO SE CONCENTRA EN EL NUCLEO, FORMADO POR LOS PROTONES Y NEUTRONES. ē 1 NEUTRON ES DE 1838 VECES MAS GRANDE QUE UN ē ¤ 1 PROTON ES DE 1836 VECES MAS GRANDE QUE UN ¤ EL TAMAÑO O VOLUMEN EXACTO DE UN ATOMO ES DIFICIL CALCULARLO YA QUE LA NUBE ELECTRONICA EN SU BORDE ES IREGULAR GEOMETRICAMENTE. . PERO APROXIMADAMENTE -27 ES DE 1, 0586 x 10 m DE RADIO. ¤ EL NUCLEO ES 100. 000 VECES MENOR EN TAMAÑO QUE EL RESTO DEL ATOMO.

EVOLUCION DEL MODELO ATOMICO De LAVOSIER DEMOCRITO DE ABDERA: FUE EL PRIMER MODELO SUGERIDO (460 AÑOS A/C) ESTABLECIO QUE EL ATOMO COMPONE LA MATERIA Y QUE EL MISMO ES INDIVISIBLE, INVISIBLE E INDESTRUCTIBLE. (ENTRE 500 Y 700 AÑOS A/C) POSTULO BASICAMENTE LO MISMO QUE DEMOCRITO, PERO AGREGO QUE EL ATOMO Y/O LA MATERIA NO SE PUEDEN DESTRUIR PERO SE PUEDEN TRANSFORMAR. JOHN DALTON (1820) CONSIDERO QUE ERAN DIMINUTAS ESFERAS RIGIDAS, TODAS DE PESO FIJO, UNA PROPIEDAD QUE SE PODIA MEDIR EXPERIMENTALMENTE. CON ESTO EXPLICO: • LA DIFUSION DE LOS GASES • ESTRUCTURA DE LA MATERIA • COMBINACION QUIMICA POSTULO: • EL ATOMO ES INDIVISIBLE • ATOMOS DE DIFERENTES ELEMENTOS TIENEN CARACTERISTICAS DIFERENTES • COMBINACION • LOS COMPUESTOS ESTAN FORMADOS POR LA UNION DE ATOMOS DE DIFERENTES ELEMENTOS EN PROPORCIONES NUMERICAS SIMPLES; 1: 1, 1: 2, 2: 1, 2: 3, ………. ENTRE OTROS. • LOS PESOS DE COMBINACION DE LOS ELEMENTOS REPRESENTAN LOS PESOS DE COMBINACION DE LOS ATOMOS. LIMITACIONES: NO TOMO EN CUENTA QUE LAS DESCARGAS ELECTRICAS PONEN DE MANIFIESTO LA NATURALEZA ELECTRICA DE LA MATERIA.

JUAN JOSE THOMPSON (1856 - 1940) DETERMINO LA NATURALEZA DE LA CARGA POSITIVA A LO QUE LLAMO RAYOS CANAL (HOY PROTONES). CONSIDERO AL ATOMO COMO UNA ESFERA RIGIDA DE CARGA POSITIVA EN LA CUAL SE ENCONTRABAN INSCRUSTADOS Y DISTRIBUIDOS LOS ELECTRONES DE CARGA NEGATIVA Y EN NUMERO SUFICIENTE COMO PARA EQUILIBRAR Y HACER UN CONJUNTO NEUTRO. THOMPSON LO COMPARO CON UN PASTEL DE PASAS SUS POSTULACIONES PERMITIERON EXPLICAR: • LOS RAYOS CANAL QUE PRODUCEN LOS ATOMOS PIERDEN ELECTRONES AL PASAR POR LOS TUBOS DE RAYOS CATODICOS. • EL PROCESO DE FORMACION DE IONES. • EL FENOMENO DE LA ELECTROLISIS. LIMITACIONES: • LA ESFERA SÓLIDA DE CARGA POSITIVA. • RUTHERFORD DEMOSTRO QUE LA TEORIA DEL PASTEL DE PASAS ERA FALSA. • EL MISMO THOMPSON RECONOCIO COMO INSUFICIENTE SUS ESTUDIOS.

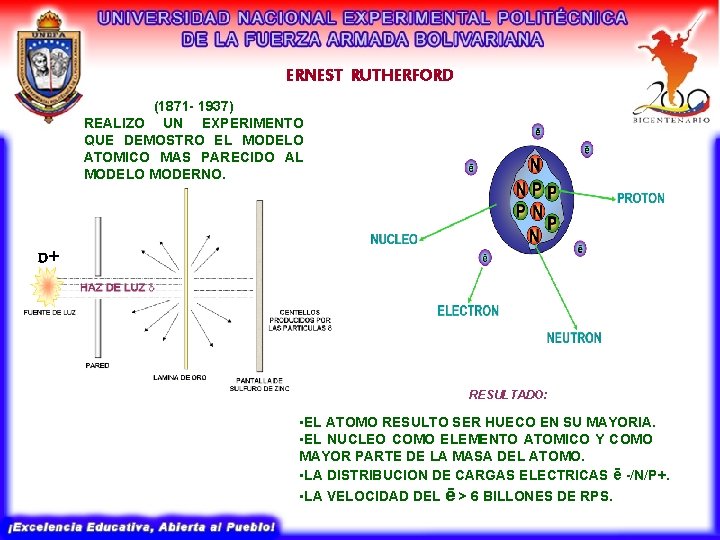
ERNEST RUTHERFORD (1871 - 1937) REALIZO UN EXPERIMENTO QUE DEMOSTRO EL MODELO ATOMICO MAS PARECIDO AL MODELO MODERNO. D+ RESULTADO: • EL ATOMO RESULTO SER HUECO EN SU MAYORIA. • EL NUCLEO COMO ELEMENTO ATOMICO Y COMO MAYOR PARTE DE LA MASA DEL ATOMO. • LA DISTRIBUCION DE CARGAS ELECTRICAS ē -/N/P+. • LA VELOCIDAD DEL ē > 6 BILLONES DE RPS.

NEILS BOHR • REALIZO EXPERIMENTOS PROPAGACION DE LA LUZ. (1939) RELACIONADOS CON LA EMISION Y • DEMOSTRO QUE LA NATURALEZA DE LA LUZ NO ES VIAJAR EN LINEA RECTA, PUES LAS PARTICULAS TIENEN MOVIMIENTOS ONDULATORIOS Y EN LOTES Y ESTOS SI VIAJAN EN LINEA RECTA. • RESUMIO LA VELOCIDAD DE LA LUZ A UNA ECUACION: V=nλ V, VELOCIDAD DE LA LUZ EN cm. /s n λ, , FRECUENCIA X SEGUNDO LONGITUD DE ONDA EN cm.

PRINCIPIO DE INCERTIDUMBRE DE HEISENBERG WERNER HEISENBERG (1901 -1976) FUE ASISTENTE DE NEILS BOHR. v USANDO LA FISICA CLASICA PODEMOS CALCULAR LA VELOCIDAD Y LA UBICACIÓN EN UN TIEMPO X, CON UN SOLO EXPERIMENTO, POR EJEMPLO EL DE UNA PELOTA CON MOVIMIENTO ONDULATORIO SOBRE UNA RAMPA x NUCLEO ē PERO UN ē TAMBIEN PRODUCE UN MOVIMIENTO ONDULATORIO ALRREDEDOR DEL NUCLEO, PERO UNA ONDA SE EXTIENDE EN EL ESPACIO Y SU POCISION NO ESTA DEFINIDA EN CON PRECISION, ASI SE COMPORTAN LAS PARTICULAS SUBATOMICAS. DEBIDO A ESTO, HEINSENBERG DEMOSTRO QUE EXISTE INSERTIDUMBRE SI SE DESEA CALCULAR SIMULTANEAMENTE LA POSICION Y VELOCIDAD DE UN ē EN UN SOLO EXPERIMENTO.