Estructura Atmica y Tabla Peridica SEMANA 01 2016

Estructura Atómica y Tabla Periódica SEMANA 01 ---- 2016 Isabel Fratti de Del Cid DIAPOSITIVAS CON IMÁGENES, E ILUSTRACIONES, CORTESÍA DE LCDA. : LILIAN GUZMÁN 2016

ATOMO 2 2 2 Es la partícula mas pequeña de un elemento que mantiene sus características. Todos los átomos de un elemento son característicos de ese elemento y diferentes de los otros elementos. Los modelos atómicos han variado y han sido modificados a través del tiempo.
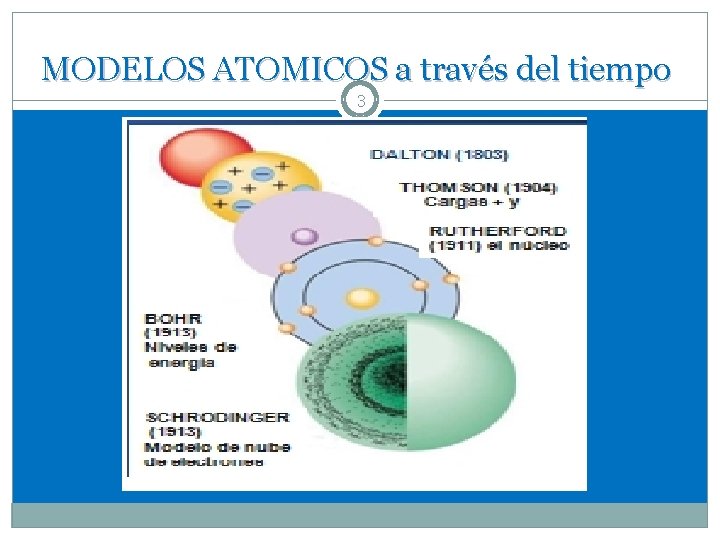
MODELOS ATOMICOS a través del tiempo 3

Estructura básica del átomo 4 Núcleo: parte central muy pequeña, posee carga positiva, y prácticamente toda la masa del átomo. Aquí hallamos Protones (+) y neutrones sin carga(o); por eso la carga del núcleo es positiva. Nube de electrones: región extranuclear en ella se hallan los electrones (-) a altas velocidades. Esta región tiene carga negativa. Recordar que el átomo tiene igual número de protones (+) que electrones (-), por eso el átomo es NEUTRO.

PARTICULAS SUB-ATOMICAS 6 El átomo esta formado de muchas partículas sub atómicas, Entre las principales tenemos: PROTONES(p, p+): Partículas que tienen una carga positiva y una masa que es aproximada de 1 uma ( se halla en el núcleo). NEUTRONES (n, no): Partículas neutras con una masa un poco mayor 1 uma(se halla en el núcleo) ELECTRONES(e-): Partículas con carga negativa y una masa muy pequeña (respecto al protón, y el neutrón, por eso para efectos prácticos se considera despreciable ) se hallan fuera del núcleo.

Partículas subatómicas fundamentales partícula Símbolo Protón p ó p+ Neutrón n ó n 0 Electrón e- Carga Masa (uma) + 1. 007 (positiva) 0 (neutra) 1. 008 0. 00055 (negativa) Ubicación En el átomo núcleo Fuera del núcleo
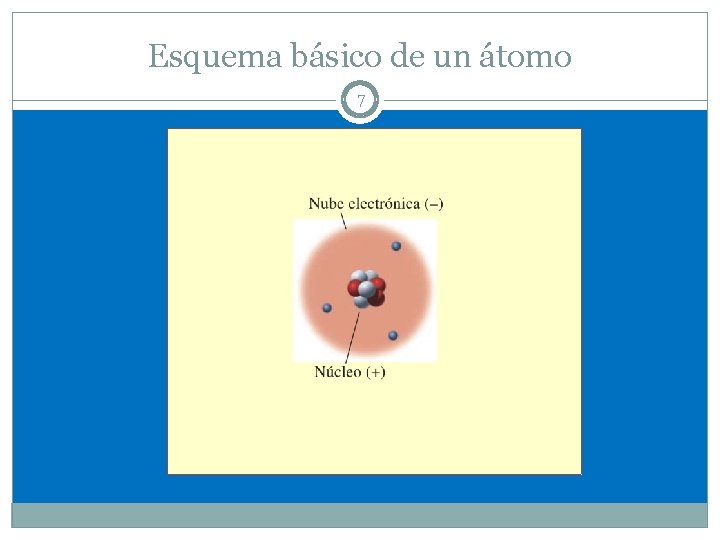
Esquema básico de un átomo 7

Número atómico y número de masa 8 NÚMERO ATÓMICO: ATÓMICO Es igual al número de protones en el núcleo de un átomo. Es igual al número que 0 cupa en la tabla periódica. Este número identifica al elemento. Debido a que el átomo es eléctricamente neutro el número atómico también corresponde al número de electrones que el átomo posee. NÚMERO DE MASA: Es la suma del número de protones mas el número de neutrones en un átomo. ( tanto protones como neutrones se hallan en el núcleo).
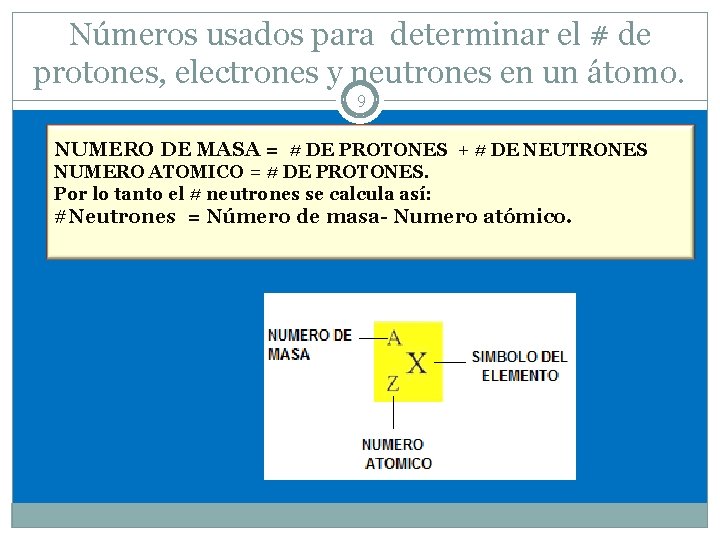
Números usados para determinar el # de protones, electrones y neutrones en un átomo. 9 NUMERO DE MASA = # DE PROTONES + # DE NEUTRONES NUMERO ATOMICO = # DE PROTONES. Por lo tanto el # neutrones se calcula así: #Neutrones = Número de masa- Numero atómico.

ISOTOPOS 10 Átomos del mismo elemento que tienen el mismo número atómico pero diferente número de masa, lo que se debe a que poseen diferente número de neutrones.

Ejemplo de el # de protones, electrones y neutrones en isotopos de un mismo elemento. 11 Isotopo Note: 24 No cambia Mg Ni el Número De Protones 12 Ni electrones 25 SOLO el Número de Mg Neutrones PROTO NES ELECTRO NES NEUTRONES 12 12 12 13 12 14 12 26 12 Mg 12

REPRESENTACIÓN DE LOS ISOTOPOS 12 Los isotopos se pueden representar de las siguientes maneras: 24 Mg 12 Magnesio-24 Mg-24 Note que se hace énfasis en indicar la masa del isótopo (24) ya que el número atómico es el mismo (12) para todos los isótopos del Mg, no es necesario indicarlo en todas las representaciones.
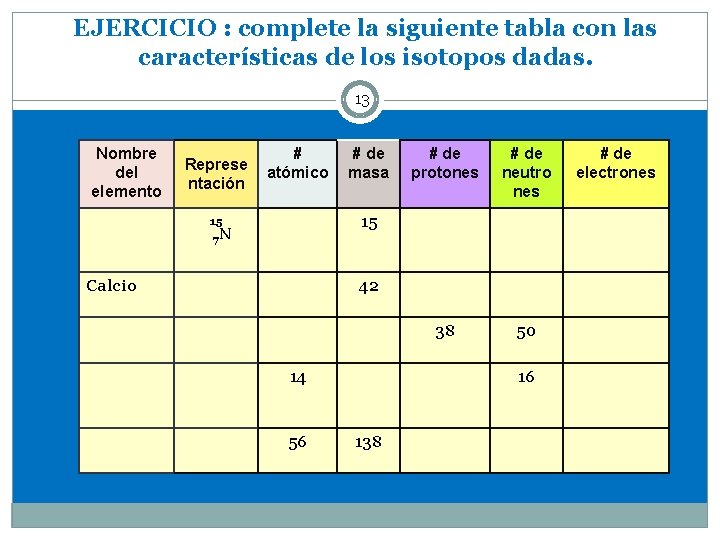
EJERCICIO : complete la siguiente tabla con las características de los isotopos dadas. 13 Nombre del elemento Represe ntación # atómico # de masa # de protones # de neutro nes 38 50 15 15 7 N Calcio 42 14 56 16 138 # de electrones

EJERCICIOS para realizar en clase. 14 1 -Los dos isotopos mas abundantes del estaño tienen números de masa 120 y 118. Escriba la representación de cada isótopo y calcule ¿Cuántos protones y neutrones tiene cada isotopo? . 2. Escriba la representación para isotopos que posen: a) 4 protones y 5 neutrones b) 26 electrones y 30 neutrones c) Un número de masa 24 y 13 neutrones
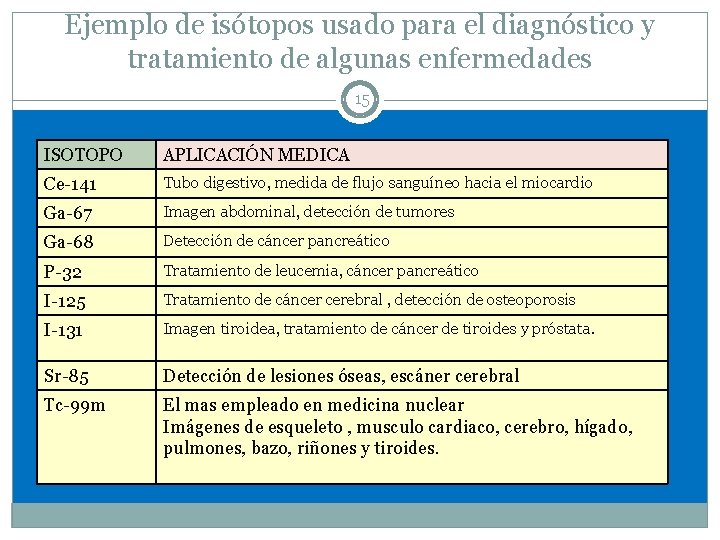
Ejemplo de isótopos usado para el diagnóstico y tratamiento de algunas enfermedades 15 ISOTOPO APLICACIÓN MEDICA Ce-141 Tubo digestivo, medida de flujo sanguíneo hacia el miocardio Ga-67 Imagen abdominal, detección de tumores Ga-68 Detección de cáncer pancreático P-32 Tratamiento de leucemia, cáncer pancreático I-125 Tratamiento de cáncer cerebral , detección de osteoporosis I-131 Imagen tiroidea, tratamiento de cáncer de tiroides y próstata. Sr-85 Detección de lesiones óseas, escáner cerebral Tc-99 m El mas empleado en medicina nuclear Imágenes de esqueleto , musculo cardiaco, cerebro, hígado, pulmones, bazo, riñones y tiroides.

PESO ATÓMICO 16 Es la masa de un átomo expresada en uma (unidades de masa atómica). Se calcula obteniendo el promedio de los pesos de sus isotopos según el % de su existencia en la naturaleza. Esta es la razón por que en la tabla periódica, la mayoría de los pesos atómicos, no son números enteros sino poseen fracciones. Ej: Hidrogeno (H): 1. 00797 Cloro (Cl) : 35. 453 Antimonio (Sb): 121. 75

Tabla periódica actual 17 Los más de 100 elementos reconocidos ( entre los hallados en la naturaleza y los sintetizados en el laboratorio), se distribuyen en una tabla que posee: A) 18 columnas ( Bloques verticales) conocidos como grupos, identificados con números romanos : I al VIII ó con números Arábigos ( 1 a la 18). Aquí están agrupados elementos con propiedades físicas , químicas y configuración electrónica similares. B) 7 Periodos ( Hileras Horizontales). Los elementos están colocados en orden creciente a sus números atómicos.
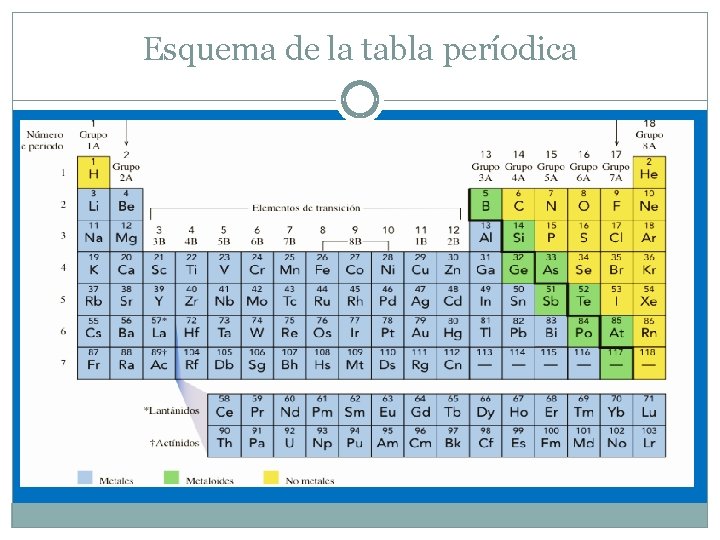
Esquema de la tabla períodica
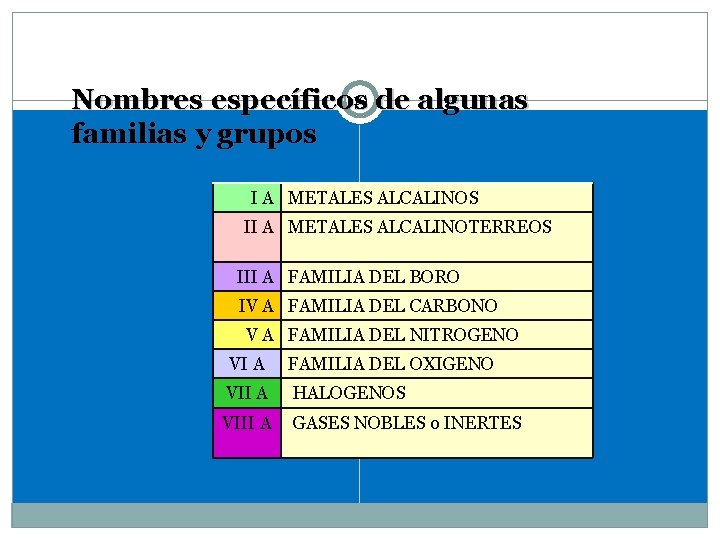
19 de algunas Nombres específicos familias y grupos I A METALES ALCALINOS II A METALES ALCALINOTERREOS III A FAMILIA DEL BORO IV A FAMILIA DEL CARBONO V A FAMILIA DEL NITROGENO VI A FAMILIA DEL OXIGENO VII A HALOGENOS VIII A GASES NOBLES o INERTES

CLASIFICACION DE LOS ELEMENTOS POR METALES, NO METALES Y METALOIDES 20 METALES: Constituyen más del 75 % de los elementos, se localizan a la izquierda de la línea gruesa escalonada. En su mayoría son sólidos ( excepto Ga, Hg, Cs, Fr), brillantes, dúctiles, maleables, buenos conductores del calor y electricidad. NO METALES: Se sitúan a la derecha de la línea escalonada, poseen poco o ningún brillo, malos conductores del calor y la electricidad. Se pueden hallar en estado líquido, solido o gas. Metaloides ( «Semiconductores» ) Presentan propiedades tanto de metales como de no metales. se encuentran en la región intermedia de la línea escalonada que separa metales y no metales. Ejemplo: Ge- As Sb-Te Po-At. Todos son sólidos.

ELEMENTOS DIATOMICOS 21 Se les encuentra en la naturaleza formando moléculas diatómicas ( uniones entre dos átomos iguales) : Son siete : H 2, N 2, O 2, F 2, Cl 2, Br 2, I 2 Observe que todos corresponden a No Metales.
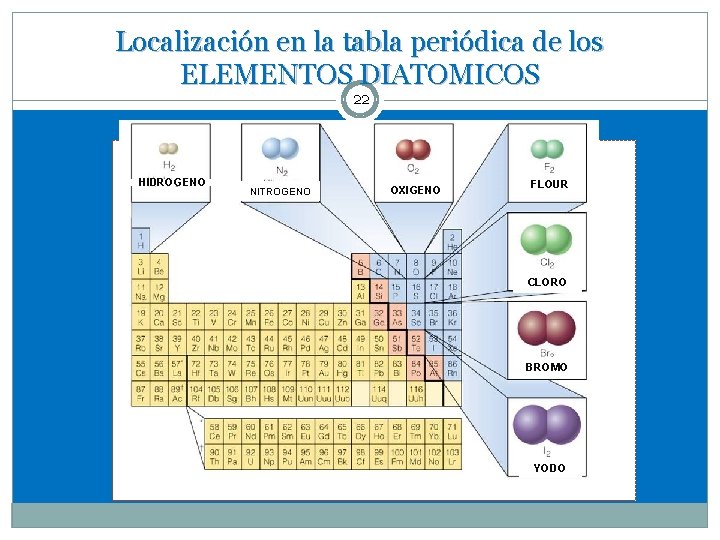
Localización en la tabla periódica de los ELEMENTOS DIATOMICOS 22 HIDROGENO NITROGENO OXIGENO FLOUR CLORO BROMO YODO
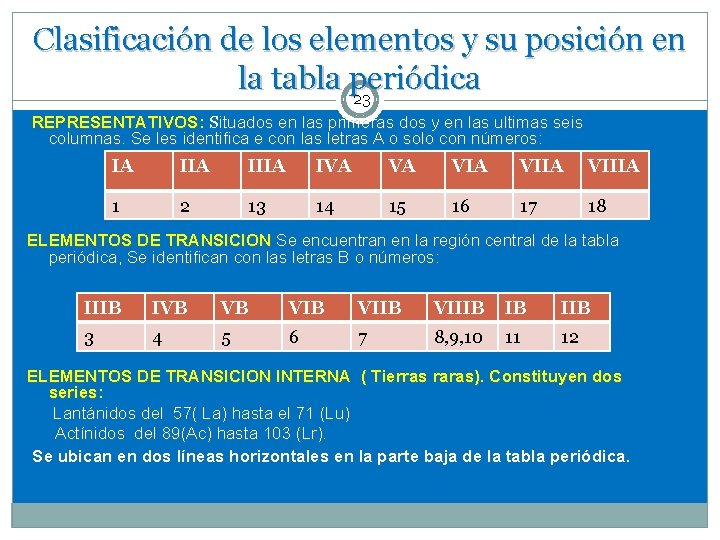
Clasificación de los elementos y su posición en la tabla periódica 23 REPRESENTATIVOS: Situados en las primeras dos y en las ultimas seis columnas. Se les identifica e con las letras A o solo con números: IA IIIA IVA VA VIIA VIIIA 1 2 13 14 15 16 17 18 ELEMENTOS DE TRANSICION Se encuentran en la región central de la tabla periódica, Se identifican con las letras B o números: IIIB IVB VB VIIB VIIIB IB IIB 3 4 5 6 7 8, 9, 10 11 12 ELEMENTOS DE TRANSICION INTERNA ( Tierras raras). Constituyen dos series: Lantánidos del 57( La) hasta el 71 (Lu) Actínidos del 89(Ac) hasta 103 (Lr). Se ubican en dos líneas horizontales en la parte baja de la tabla periódica.
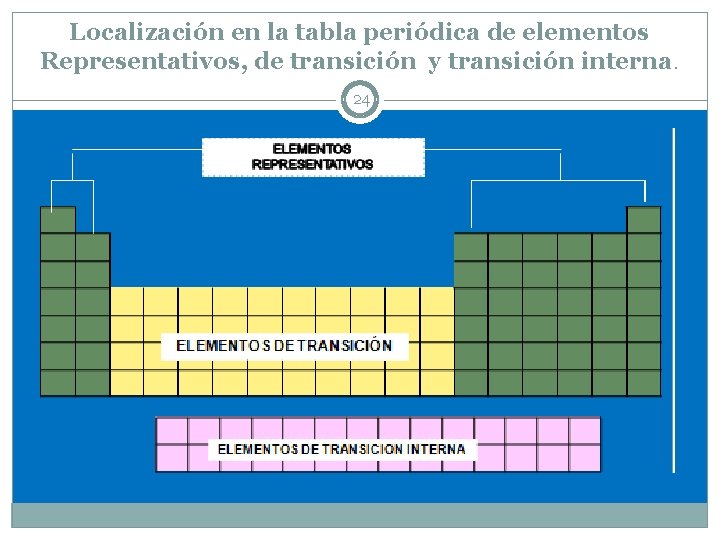
Localización en la tabla periódica de elementos Representativos, de transición y transición interna. 24
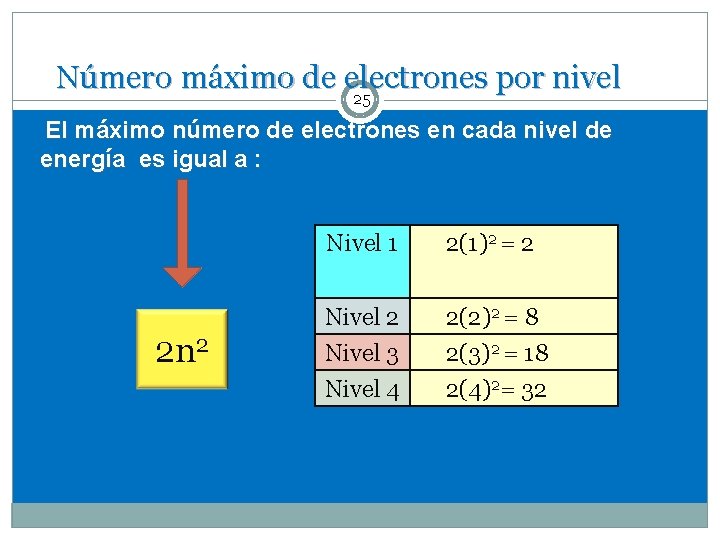
Número máximo de electrones por nivel 25 El máximo número de electrones en cada nivel de energía es igual a : 2 n 2 Nivel 1 2(1)2 = 2 Nivel 3 Nivel 4 2(2)2 = 8 2(3)2 = 18 2(4)2= 32

Configuración electrónica 26 Es la disposición de los electrones de un átomo en niveles ( 1 al 7), subniveles ( representados por las letras : s, p, d, f ) y orbitales. Se colocan de menor a mayor energía. Debe usarse la regla diagonal, ya que ésta incluye los traslapes de orbitales y la configuración electrónica de las tablas periódicas no incluyen éstos traslapes.

Llenado de orbitales usando la regla diagonal. 27 Empiece de arriba abajo, siguiendo la dirección de las flechas ó líneas. . El número máximo de electrones que se coloca en cada subnivel es el siguiente: s………. . 2 electrones p………. . 6 electrones d………. . 10 electrones f………. . 14 electrones Nota: NO debe colocar más electrones que los que le corresponden al átomo o al ión representado.
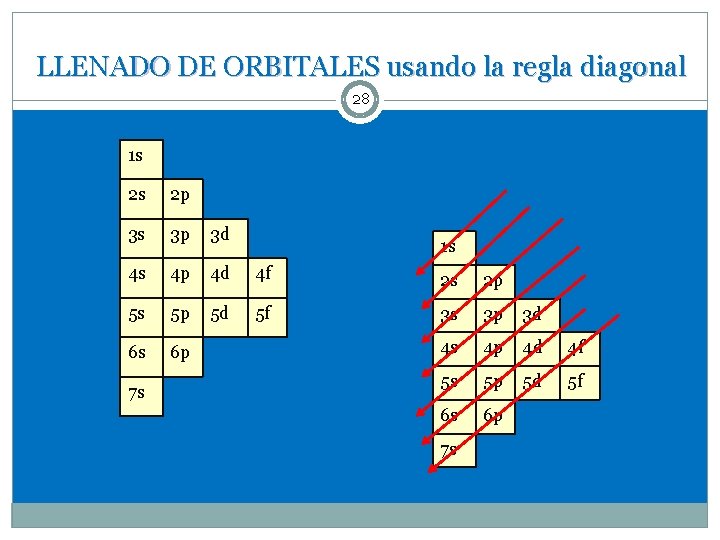
LLENADO DE ORBITALES usando la regla diagonal 28 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 2 s 2 p 5 s 5 p 5 d 5 f 3 s 3 p 3 d 6 s 6 p 4 s 4 p 4 d 4 f 5 s 5 p 5 d 5 f 6 s 6 p 7 s 1 s 7 s
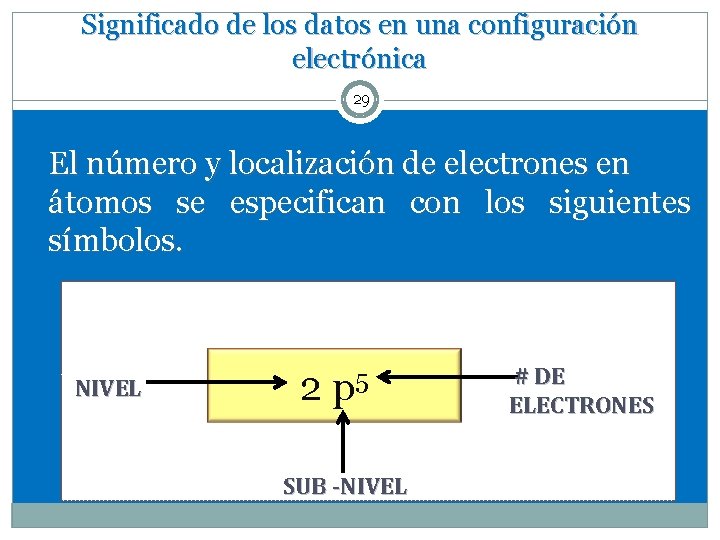
Significado de los datos en una configuración electrónica 29 El número y localización de electrones en átomos se especifican con los siguientes símbolos. NIVEL 2 p 5 SUB -NIVEL # DE ELECTRONES
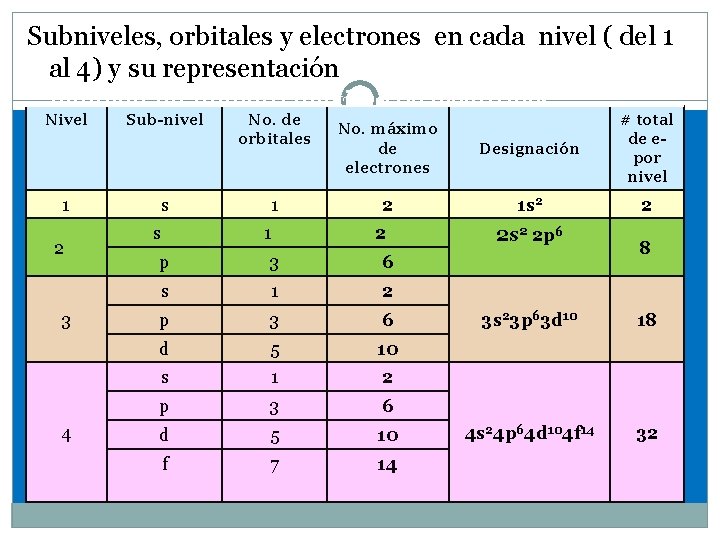
Subniveles, orbitales y electrones en cada nivel ( del 1 al 4) y su representación de estos sub-niveles tiene 30 también un número máximo de electrones. Nivel 1 2 3 4 Sub-nivel s s No. de orbitales 1 1 No. máximo de electrones Designación # total de epor nivel 2 1 s 2 2 2 p 3 6 s 1 2 p 3 6 d 5 10 f 7 14 2 s 2 2 p 6 8 3 s 23 p 63 d 10 18 4 s 24 p 64 d 104 f 14 32
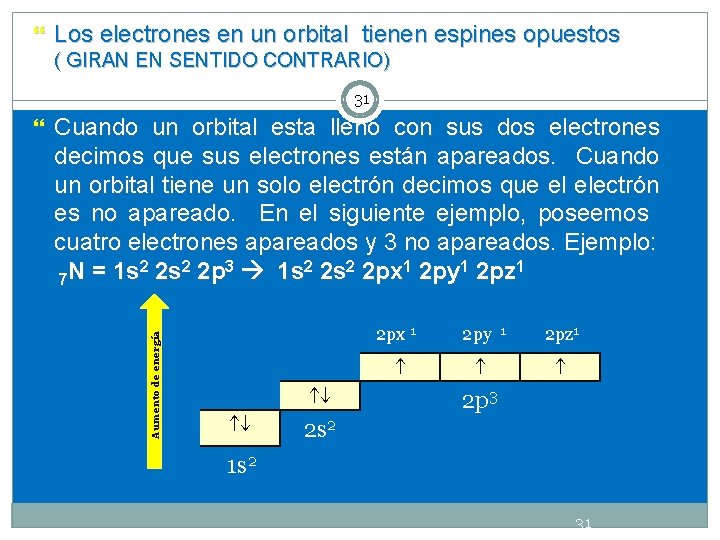
Los electrones en un orbital tienen espines opuestos ( GIRAN EN SENTIDO CONTRARIO) 31 Cuando un orbital esta lleno con sus dos electrones Aumento de energía decimos que sus electrones están apareados. Cuando un orbital tiene un solo electrón decimos que el electrón es no apareado. En el siguiente ejemplo, poseemos cuatro electrones apareados y 3 no apareados. Ejemplo: 2 2 s 2 2 p 3 1 s 2 2 px 1 2 py 1 2 pz 1 N = 1 s 7 2 px 1 2 py 1 2 pz 1 2 p 3 2 s 2 1 s 2 31
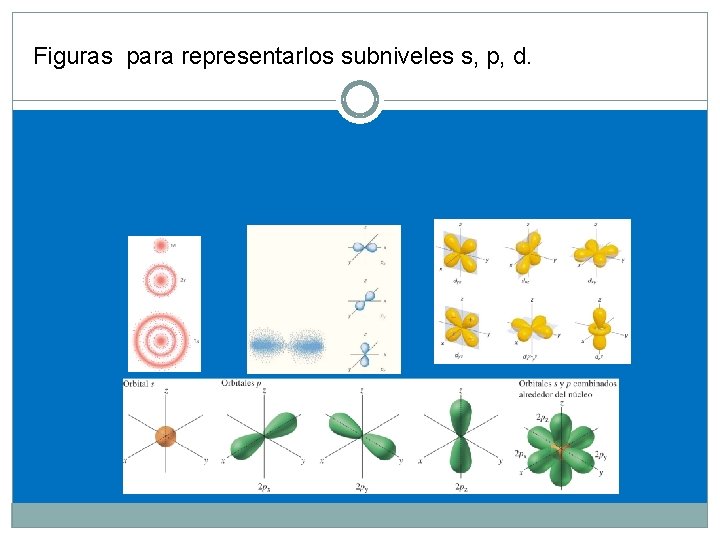
Figuras para representarlos subniveles s, p, d. 32

Número máximo de electrones que deben asignarse en las configuraciones electrónicas. 33 Atomos: El número de electrones máximo a distribuirse corresponde al número atómico del elemento. Cationes: Al número de electrones del átomo se le restan los electrones perdidos( éstos corresponden a la carga del catión) ej: Ca+2: Posee 18 electrones ( 20 del átomo -2 perdidos) Aniones: Al número de electrones del átomo se le suman los electrones ganados ( estos corresponden a la carga del anión)Ej: F- : Posee 10 electrones ( 9 del átomo + 1 ganado)

Representación de la configuración electrónica desarrollada , semidesarrollada y abreviada. 34 Desarrollada: Si el subnivel posee más de un orbital, deben representarse separadamente Ej: los subniveles p poseen los orbitales px, py, pz, se representan por separado. K =1 s 2 2 px 2 2 py 2 2 pz 2 3 s 2 3 px 2 3 py 23 pz 24 s 1 Semidesarrollada: Se escriben en los subniveles el número total de electrones que posee: K = 1 s 2 2 p 6 3 s 2 3 p 6 4 s 1 Abreviada: Se escribe entre corchetes el símbolo del gas noble del periodo anterior y luego los electrones de más que posee: K= [ Ar] 4 s 1

Ejemplo de estructura electrónica de iones 35 A- Cationes: +2 = 1 s 22 p 63 s 23 p 6 20 Ca Note: Se distribuyeron 18 e-, pues el Ca tenia 20 e-, pero perdió 2 e- al formar Ca+2. , llegando a tener la configuración del gas noble anterior a su periodo. Forma abreviada: B- Aniones: 20 Ca +2 = [Ar] - = 1 s 22 p 6 F 9 Note: se distribuyeron 10 e- pues el F posee 9 e-, pero ganó 1 e- al formar F -, llegando a tener la configuración del gas noble del período que ocupa Ne Forma abreviada : 9 F - = [ Ne]

IONES : CATIONES Y ANIONES. 36 Iones: son partículas de materia con carga eléctrica. Y se dividen en: Cationes: poseen carga positiva (+) porque han perdido electrones ( cargas negativas). Ej. De cationes monoatómicos K + ( el K perdió 1 e-) Mg +2 ( perdió 2 e-) Aniones: Poseen carga negativa pues han ganado electrones ( cargas negativas). Ej. De aniones monoatómicos. F- ( el F ganó 1 e-) S-2 (el S ganó 2 e-) Si poseen más de un átomo, se dice que son poli atómicos. Ej : Catión poli atómico : NH 4+ Aniones poli atómicos : SO 4 -2 , HCO 3 -
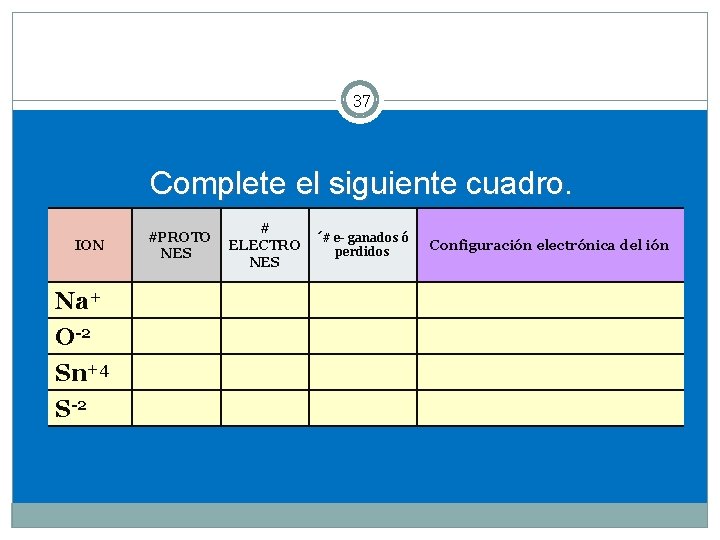
37 Complete el siguiente cuadro. ION Na+ O-2 Sn+4 S-2 #PROTO NES # ELECTRO NES ´# e- ganados ó perdidos Configuración electrónica del ión

Diagrama de Bohr, para átomos y iones 38 Se coloca el # de protones*(algunos autores colocan también el # de neutrones ó el símbolo del elemento)dentro de un círculo, que representa al núcleo y en líneas concéntricas que representan los niveles de energía el número total de electrones en cada nivel**. • *#Protones: Número atómico del elemento. • **: Se calculan en base a la configuración electrónica.
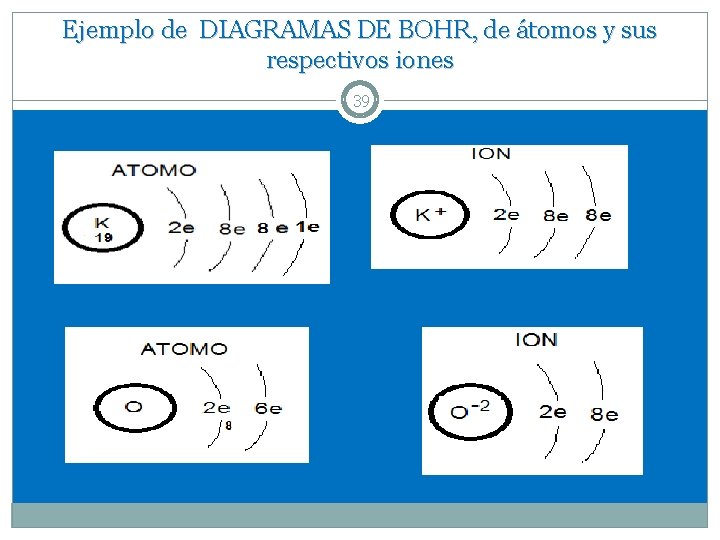
Ejemplo de DIAGRAMAS DE BOHR, de átomos y sus respectivos iones 39
Realice los diagramas de Bohr para los siguientes átomos y sus respectivos iones A) Ca B) Ca +2 C) S D) S-2 40
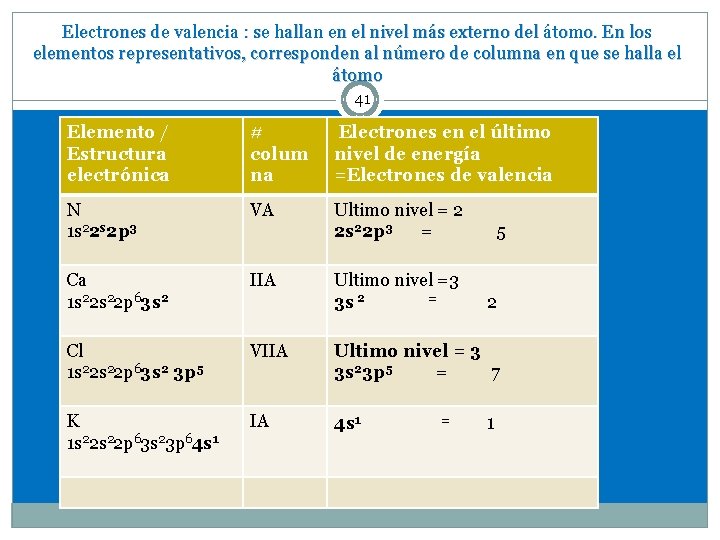
Electrones de valencia : se hallan en el nivel más externo del átomo. En los elementos representativos, corresponden al número de columna en que se halla el átomo 41 Elemento / Estructura electrónica # colum na Electrones en el último nivel de energía =Electrones de valencia N 1 s 22 s 2 p 3 VA Ultimo nivel = 2 2 s 22 p 3 = Ca 1 s 22 p 63 s 2 IIA Cl 1 s 22 p 63 s 2 3 p 5 VIIA Ultimo nivel = 3 3 s 23 p 5 = 7 K 1 s 22 p 63 s 23 p 64 s 1 IA 4 s 1 Ultimo nivel =3 = 3 s 2 = 5 2 1

Resuelva los siguientes ejercicios, colocando en el espacio el símbolo del elemento con esas características 42 A-Ubicado en columna VIA y tercer período___ B-Metal líquido del 4 to período _______ C- Su configuración es: [Ne]3 s 23 p 3 ______ D-Posee 76 protones______ Elemento de mayor electronegatividad ______ Su configuración electrónica termina en 3 s 23 p 5 __ Lantánido sintetizado artificialmente_______ Gas noble del 6 to período_______ Metaloide del 4 to período con 5 e- de valencia ___
- Slides: 42