ESTRAZIONE Imbuto separatore Estrattore di Soxhlet Essiccanti Coefficiente
ESTRAZIONE Imbuto separatore Estrattore di Soxhlet (Essiccanti)

Coefficiente di distribuzione K Se si agita una soluzione (soluto A nel solvente 1) con un secondo solvente (solvente 2) immiscibile con il primo, il soluto si distribuisce tra le due fasi liquide. Quando le due fasi si separano di nuovo in due strati distinti di solvente, viene raggiunto un equilibrio tale che le concentrazioni di soluto in ciascuno dei due solventi definiscono una costante K, detta coefficiente di distribuzione o coefficiente di ripartizione

Costante K, coefficiente di distribuzione C 1 e C 2 sono le concentrazioni all’equilibrio (g/L) del soluto A rispettivamente nel solvente 1 e nel solvente 2. Questa relazione è indipendente dalla concentrazione totale e della quantità effettiva dei due solventi.

Coefficiente di distribuzione K ha un valore costante per ogni soluto in esame che dipende solo dalla natura dei solventi usati in ciascun caso. Il soluto si distribuisce tra i due solventi in modo tale che la sua attività chimica (concentrazione effettiva) è la stessa in ciascuna fase.

ESTRAZIONE L’estrazione è il trasferimento di un soluto da un solvente ad un altro secondo una distribuzione regolata dall’equazione

ESTRAZIONI • Estrazione con solventi organici da campioni acquosi ü IMBUTO SEPARATORE • Pochi campioni • Piccole quantità

IMBUTO SEPARATORE processo di estrazione

Processo di estrazione A) solvente 1 contiene una miscela di due molecole diverse ( palline bianche e nere). Si aggiunge un secondo solvente (colore grigio), immiscibile con il primo, e si agita energicamente B) dopo la separazione in due strati, la maggior parte delle molecole bianche risultano estratte nel nuovo solvente. C) separando i due strati, le molecole bianche e nere sono state parzialmente separate. quasi mai sarà possibile trasferire il soluto dal solvente 1 al solvente 2 con un’unica estrazione, a meno che K non abbia un valore assai elevato, saranno necessarie più estrazioni per estrarre il soluto dal solvente 1. Per estrarre un soluto da una soluzione, è sempre meglio usare diverse piccole porzioni del secondo solvente piuttosto che fare una singola estrazione con una quantità maggiore di solvente.

Confronto tra l’efficacia di tre successive estrazioni con 50 ml di etere (solvente 2) rispetto ad un’unica estrazione con 150 ml di etere. K=10, 5 g sostanza in 100 ml acqua (solvente 1) A) Tre estrazioni con 50 ml di etere Con prima porzione di 50 ml di etere la quantità di soluto che viene estratta è calcolata con la seguente equazione, dove x indica la quantità rimasta nello strato acquoso. x=0, 83 g rimasti nello strato acquoso; 5, 0 -x=4, 17 g nello strato etereo

Una seconda estrazione con altri 50 ml di etere fresco, effettuata sulla fase acquosa contenente ora 0, 83 g di soluto, estrarrà una quantità di soluto pari a: x=0, 14 g rimasti nello strato acquoso; 0, 83 -x=0, 69 g nello strato etereo La terza estrazione con ulteriori 50 ml di etere trasferirà 0, 12 g di soluto nella fase eterea, lasciando 0, 02 g di soluto nella fase acquosa. (Con calcoli analoghi) La quantità totale estratta negli strati eterei riuniti sarà: 4, 17+0, 69+ 0, 12= 4, 98 g di soluto

B) Unica estrazione con 150 ml di etere x=0, 31 g nello strato acquoso; 5, 0 -x= 4, 69 g nello strato etereo

Le tre estrazioni con 50 ml di etere hanno estratto 0, 29 g in più rispetto ad un’unica estrazione (5, 8% del materiale totale)

Metodi di purificazione e di separazione 1. Estrazione di una miscela organica con acqua Materiali altamente polari (sali inorganici, basi o acidi forti) e sostanze polari (alcoli, acidi carbossilici, ammine) a basso peso molecolare. Si usa estrarre con acqua immediatamente dopo aver eseguito un’estrazione con acidi o basi per assicurarsi di aver eliminato qualsiasi traccia di acido o base.

Metodi di purificazione e di separazione 2. Estrazione di una miscela organica con un acido diluito. impurezze basiche (ammine organiche) acido cloridrico al 10% RNH 2 + HCl RNH 3+ Cl (sale idrosolubile) Subito dopo l’estrazione con acidi è consigliabile eseguire un’estrazione con l’acqua per togliere qualsiasi traccia di acido nel solvente organico.

Metodi di purificazione e di separazione 3. Estrazione di una miscela organica con una base diluita impurezze acide (acidi organici) Na. HCO 3 al 5% o Na. OH dil *. RCOOH + Na. HCO 3 RCOO- Na+ + H 2 O + CO 2 (p. Ka 5) (sale idrosolubile) Subito dopo l’estrazione con basi è consigliabile eseguire un’estrazione con l’acqua per togliere qualsiasi traccia di base nel solvente organico. * fenoli
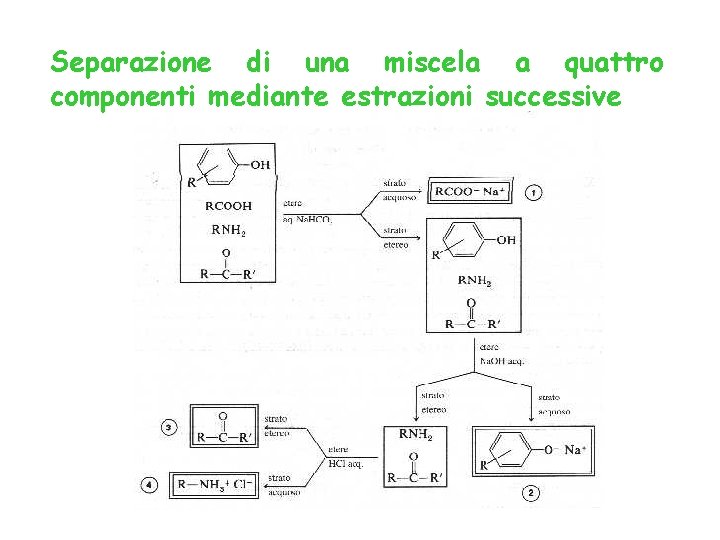
Separazione di una miscela a quattro componenti mediante estrazioni successive
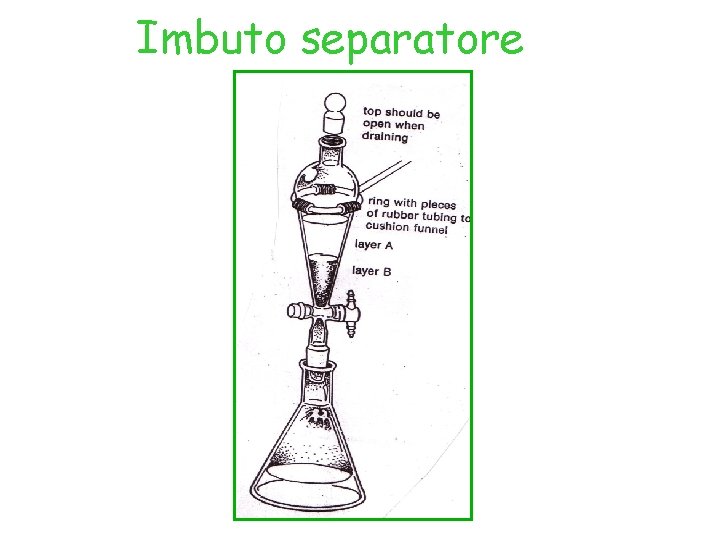
Imbuto separatore
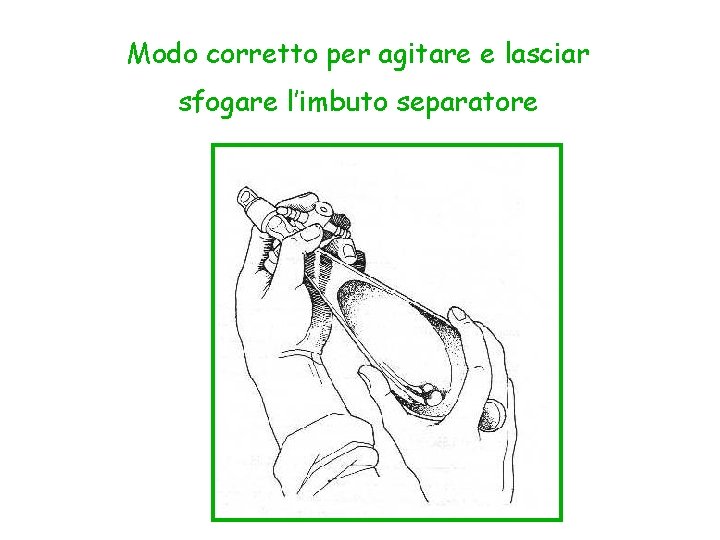
Modo corretto per agitare e lasciar sfogare l’imbuto separatore

Bisogna essere cauti nell’identificare lo strato acquoso e quello organico densità dei due solventi Solvente Ligroina Etere Benzene * Acqua Na. Cl saturo Metilene cloruro Cloroformio * Ac. solforico conc. * sospetto cancerogeno densità(g/ml) 0, 67 -0, 69 0, 713 0, 879 1, 00 1, 198 1, 335 1, 498 1, 84

Emulsione sospensione colloidale di un liquido in un altro liquido trucchi” per rompere un’emulsione ü aggiunta di una soluzione satura di Na. Cl se uno dei solventi è acqua, perché rende i due strati, acquoso ed organico, meno compatibili. ü aggiunta di piccole quantità di un detergente idrosolubile. ü filtrazione per gravità, perché elimina le particelle gommose. ü far ruotare a vortice gli strati nell’imbuto separatore o agitare lentamente.

Dopo l’estrazione Anidrificazione del solvente organico (con essiccanti) eliminare tracce di umidità rimaste * Evaporazione del solvente (distillazione sotto vuoto con evaporatore rotante) isolare o concentrare il campione

* Essiccante: sale inorganico anidro, acquisisce acqua di cristallizzazione, per esposizione all’aria umida o per contatto con una soluzione umida Magnesio solfato Sodio solfato Calcio cloruro acidità idrato neutro Mg. SO 4. 7 H 2 O neutro Na 2 SO 4. 7 H 2 O Na 2 SO 4. 10 H 2 O neutro Ca. Cl 2. 2 H 2 O Ca. Cl 2. 6 H 2 O capacità intensità velocità alta media rapida alta bassa media generale bassa alta rapida idrocarburi alogenuri Potassio carbonato basico K 2 CO 3. 1, 5 H 2 O K 2 CO 3. 2 H 2 O media potassio idrossido basico setacci molecolari (3 o 4 A°) neutro uso generale media rapida alta veramente alta ammine, esteri, basi, chetoni ammine generale ü Capacità: quantità di acqua tolta per un dato peso di essiccante. ü Intensità: quantità di acqua presente nella soluzione in equilibrio con l’essiccante. ü Velocità: velocità di azione (essiccamento).

ESTRAZIONI • Estrazione con solventi organici da campioni solidi ü ESTRATTORE DI SOXHLET • Numerosi campioni • Grosse quantità
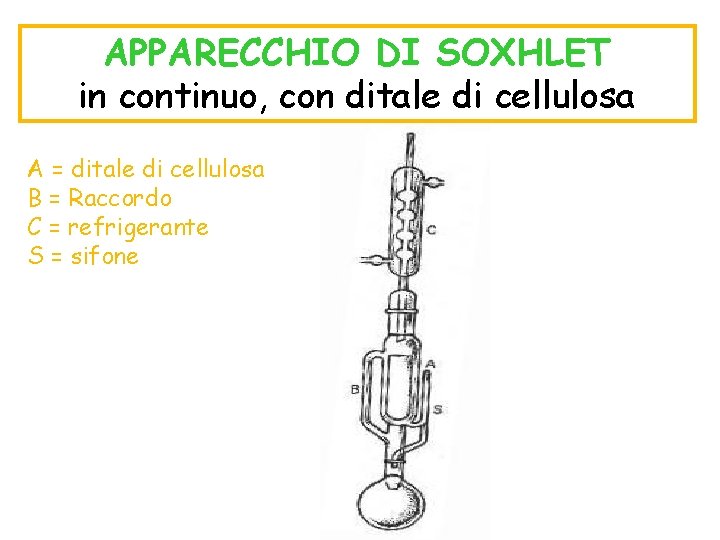
APPARECCHIO DI SOXHLET in continuo, con ditale di cellulosa A = ditale di cellulosa B = Raccordo C = refrigerante S = sifone
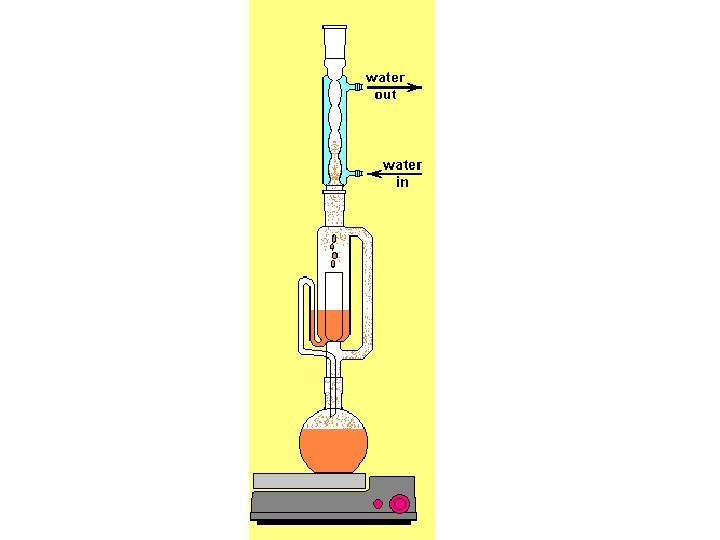

• In A si pone la sostanza in un ditale di carta da filtro, cellulosa o vetro poroso, quindi si riscalda il pallone in cui è presente il solvente prescelto per l’estrazione; i vapori raggiungono, attraverso il raccordo B, il refrigerante C in cui condensano e ricadono quindi in A, venendo a contatto con la sostanza da estrarre. Quando il solvente avrà raggiunto l’altezza del sifone S, tutto il liquido sifonerà nel pallone. In tal modo il solvente puro continuerà ad evaporare e l’operazione descritta si ripeterà automaticamente, fino all’ottenimento di una completa estrazione.
- Slides: 26