Estrategias para ampliar el acceso a Biosimilares Buenos

Estrategias para ampliar el acceso a Biosimilares Buenos Aires, 6 de noviembre, 2018 María Fabiana Jorge MFJ International, LLC

Índice Evolución de los desafíos para hacer que los medicamentos biosimilares sean accesibles. Experiencia en UE, EEUU, Australia, Canada. Barreras que enfrentan los biosimilares. Posibles acciones para favorecer el ingreso de biosimilares.

Evolución de desafíos Primer nivel de desafíos: Establecer un marco regulatorio que garantice la seguridad y la eficacia de los medicamentos biosimilares. [Gobiernos] Nuevo desafío: Que la industria de biosimilares se desarrolle y fortalezca. [Industria] Desafío constante: Educación acerca de la seguridad y efectividad de los medicamentos biosimilares. [Médicos/hospitales/seguros médicos/planes de salud/pacientes]

FDA Commissioner Scott Gottlieb: Our ability to build a market for safe, effective biosimilar products is key for patients and our nation’s health care system. It’s a key to promoting access and reducing health care costs. And it’s a key to advancing public health. But I’m worried that the market for these products still isn’t established. The ability for these products to penetrate clinical practice, and gain acceptance, is still not firm. That doesn’t mean that the future doesn’t hold a lot of promise for biosimilars. It just means that the future is uncertain. And the policy and regulatory decisions that we make today are going to have a lot to do with whether we realize the promise for this new category of products. Or if we see the opportunities we once envisioned go unrealized. We know that biologics are used to treat many serious and life-threatening diseases. They’ve become a mainstay in the treatment of cancer and autoimmune conditions. They’re also expensive.

Desafío Actual Existe una problema muy real: Los altos costos de estos medicamentos. Existe una oportunidad importante para las empresas biosimilares. Pero existen obstáculos muy importantes: Las empresas biológicas originales están haciendo todo lo posible para que la industria de biosimilares no se desarrolle y, si lo hace, demorarlo y que sea lo menos posible. El gran desafío actual de los gobiernos: Establecer políticas de salud y marcos legales/regulatorios que permitan el desarrollo sustentable de la industria biosimilar.

Biosimilares: Una necesidad que enfrenta mucha resistencia Estados Unidos (45% del mercado farmacéutico global= $446. 000 millones en 2016) Comisionado de la FDA: ü 2% de los estadounidenses utilizan biológicos. ü Biológicos: 40% del total del gasto en medicamentos con receta. ü Biológicos representan el 70% del crecimiento del gasto en medicamentos entre el 2010 -2015. ü Aprox. 30% de los productos en el mercado son biológicos.

Europa: Un mercado más avanzado La Unión Europea Medicamentos biológicos: aprox. 30%. Ya se han aprobado 48 biosimilares (15 moléculas). Potenciales ahorros por biosimilar entre 2016 -2020 en 5 países: 10. 000 M de Euros. Uso de biosimilares, erosión de precios y concentración de competidores varía depende del país.

Experiencia en Europa Biosimilares: Son clave en Europa para incrementar acceso. Biosimilares: Seguridad y eficacia probada. Diferentes compradores: Demuestran distintos niveles de penetración (en hospitales la penetración ha sido más importante que a nivel de paciente donde el médico decide). Penetración de biosimilares en Dinamarca (gob. nac. ): casi 100% biosimilar infliximab (Remicade) casi 80% biosimilar etanercept (Embrel) Reducción de precios dependen de distintos mecanismos, por ejemplo licitaciones (problemas de largo plazo) – compra influenciada por el que paga.
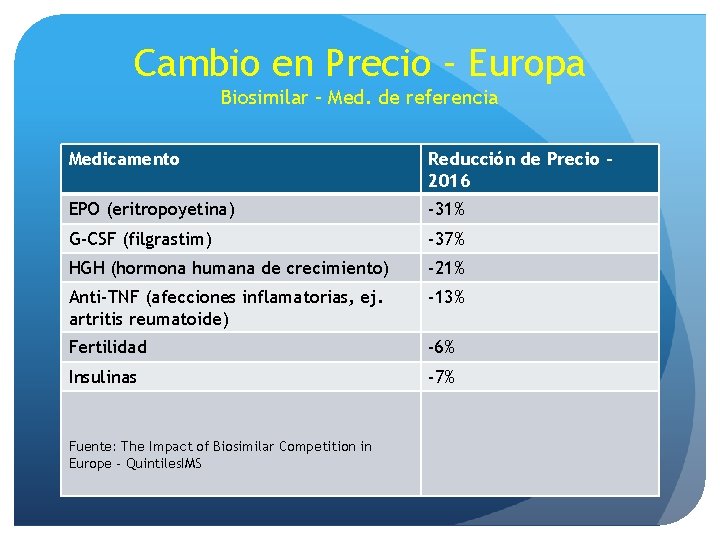
Cambio en Precio – Europa Biosimilar – Med. de referencia Medicamento Reducción de Precio 2016 EPO (eritropoyetina) -31% G-CSF (filgrastim) -37% HGH (hormona humana de crecimiento) -21% Anti-TNF (afecciones inflamatorias, ej. artritis reumatoide) -13% Fertilidad -6% Insulinas -7% Fuente: The Impact of Biosimilar Competition in Europe - Quintiles. IMS

Biosimilares en Australia ü El Therapeutic Goods and Administration (TGA) aprobó 12 biosimilares (8 categorías de medicamentos) más hormona de crecimiento (somatropina) aprobadas antes de marco regulatorio. Biosimilares. ü Biosimilares pueden significar decenas de millones de dólares en ahorro. ü Cuando un biosimilar entra a la lista del Pharmaceutical Benefits Scheme (PBS): 16% de descuento en todas las versiones del producto. ü Según GBMA: Potencial de AU$2. 600 millones por año (varios medicamento perderán la patente en los próximos 10 años).

Biosimilares en Canadá 12 biosimilares aprobados. El promedio de descuento actual es entre 12% y el 23%. Remicade es el único con un descuento del 47% -- similar al precio de otros países. Precios de los biosimilares en Canadá son en general mas altos que los mismos en países de la OCDE. El descuento en los países de la OCDE es entre 13% y 34%. Para que Canadá tenga precios similares a los de los países de la OCDE: los descuentos deberán ser entre 39% y 61%. Fuente: http: //www. pmprb-cepmb. gc. ca/view. asp? ccid=1304
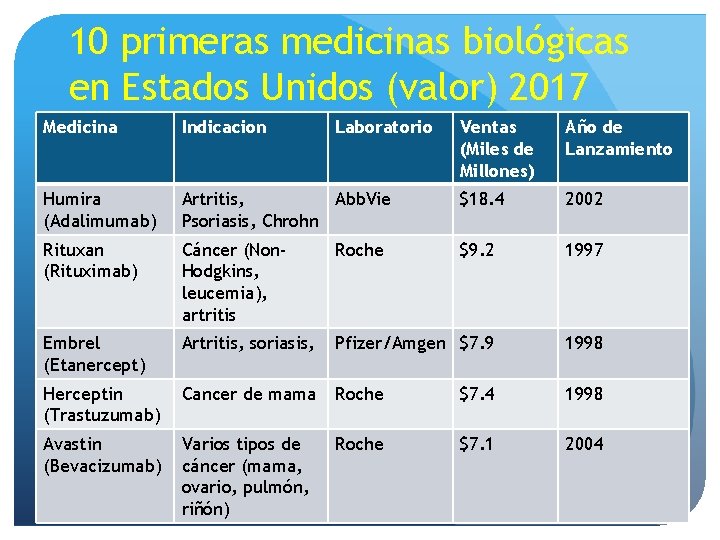
10 primeras medicinas biológicas en Estados Unidos (valor) 2017 Medicina Indicacion Humira (Adalimumab) Laboratorio Ventas (Miles de Millones) Año de Lanzamiento Artritis, Abb. Vie Psoriasis, Chrohn $18. 4 2002 Rituxan (Rituximab) Cáncer (Non. Hodgkins, leucemia), artritis Roche $9. 2 1997 Embrel (Etanercept) Artritis, soriasis, Pfizer/Amgen $7. 9 1998 Herceptin (Trastuzumab) Cancer de mama Roche $7. 4 1998 Avastin (Bevacizumab) Varios tipos de cáncer (mama, ovario, pulmón, riñón) Roche $7. 1 2004
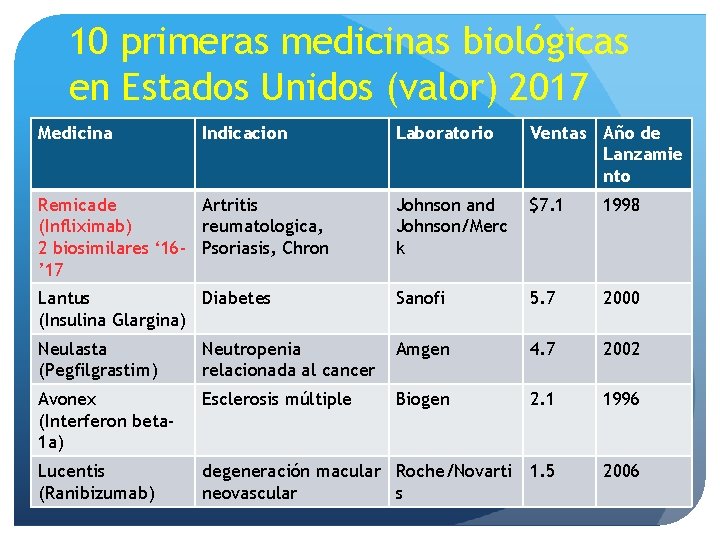
10 primeras medicinas biológicas en Estados Unidos (valor) 2017 Medicina Indicacion Laboratorio Ventas Año de Lanzamie nto Remicade Artritis (Infliximab) reumatologica, 2 biosimilares ‘ 16 - Psoriasis, Chron ’ 17 Johnson and Johnson/Merc k $7. 1 1998 Lantus Diabetes (Insulina Glargina) Sanofi 5. 7 2000 Neulasta (Pegfilgrastim) Neutropenia relacionada al cancer Amgen 4. 7 2002 Avonex (Interferon beta 1 a) Esclerosis múltiple Biogen 2. 1 1996 Lucentis (Ranibizumab) degeneración macular Roche/Novarti 1. 5 neovascular s 2006
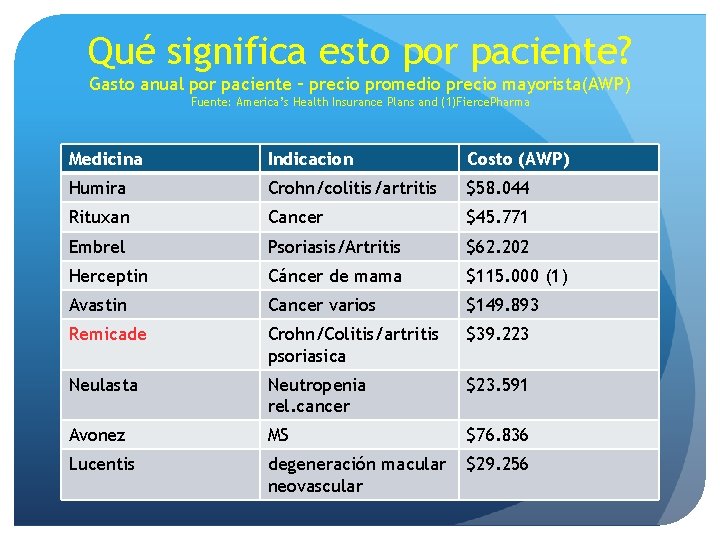
Qué significa esto por paciente? Gasto anual por paciente – precio promedio precio mayorista(AWP) Fuente: America’s Health Insurance Plans and (1)Fierce. Pharma Medicina Indicacion Costo (AWP) Humira Crohn/colitis/artritis $58. 044 Rituxan Cancer $45. 771 Embrel Psoriasis/Artritis $62. 202 Herceptin Cáncer de mama $115. 000 (1) Avastin Cancer varios $149. 893 Remicade Crohn/Colitis/artritis psoriasica $39. 223 Neulasta Neutropenia rel. cancer $23. 591 Avonez MS $76. 836 Lucentis degeneración macular neovascular $29. 256

Diferentes barreras a los biosimilares Biosimilares: Futuro de la industria farmacéutica. Precios no son sostenibles. Industria original está desarrollando una estrategia compleja a niveles múltiples para: Impedir el desarrollo de la industria biosimilar O por lo menos, demorar y limitar su crecimiento

Algunas barreras a los Biosimilares REMS Estrategia de patentes. A nivel de aprobación. Acuerdos internacionales de comercio. Desinformación. Estrategias de precios. Forzar a usar ahorros en compra de otros biológicos.

REMS Estrategia de Evaluación y Mitigación de Riesgos Programa de la FDA establecido en 2007 para asegurar que los beneficios de un medicamento superen los riesgos. FDA estima que aprox. 40% de los medicamentos requieren REMS. Abusos del programa utilizando un vacío de la ley para impedir que genéricos/biosimilares tengan acceso a las muestras y otras restricciones a la distribución de muestras para demorar la competencia. Estudio de AAM estima costo $13. 4 millones en ahorros que se pierden por año.

Estrategia de Patentes Decenas y cientos de patentes por medicamento. Dificultad de saber cuántas patentes existen. Estrategia de ahogar al competidor con múltiple juicios largos y sumamente costosos. Claro ejemplo: EEUU 13 biosimilares aprobados y sólo 4 en el mercado, el resto demorado por juicios. Algunas empresas desisten: Momenta, Sandoz

Humira en Estados Unidos En EE. UU. Humira tiene 247 patentes Richard Gonzalez, CEO de Abb. Vie dijo: “Any company seeking to market a biosimilar version of Humira will have to contend with this extensive patent estate, which Abb. Vie intends to enforce vigorously. ” Patente original venció en 2016 Abb. Vie negocia acuerdos con competidores (settlement agreements) para demorar la salida al mercado del biosimilar hasta el año 2023 (7 años después del vencimiento de la primera patente). Fuente: Huffington Post 10/28/18

Humira en la Unión Europea 3 biosimilares se acaban de lanzar en Europa (10/16/18) Amgen, Biogen/Samsung Bioepis y Mylan. Boehringer Ingelheim también recibió la aprobación de comercialización de un biosimilar. No tiene acuerdo con Abb. Vie. Está haciendo estudios de intercambiabilidad. Abb. Vie negoció un acuerdo con algunas empresas (Amgen; Samsung Bioepis; Fujifilm Kyowa Kirim Biologics/Mylan; permitiéndoles vender Humira en Europa en 10/18 pero bloqueando su lanzamiento en EE. UU. hasta el 2023. Estrategia de Abb. Vie: atar las manos de los competidores hasta el 2023 en el mercado más grande del mundo.

Humira: Estrategia para demorar la competencia de biosimilares Fresenius Kabi (con biosimilar de adalimumab en desarrollo) firmó acuerdo --licencia no exclusiva-- con Abb. Vie similar al de las otras empresas. Reino Unido, Servicio Nacional de Salud (NHS): Espera un ahorro anual de $193 millones por el uso de los biosimilares de Humira. NHS: adalimumab es la medicina en la que los hospitales gastan más, $517. 1 millones por año. Más de 46. 000 pacientes reciben la receta por Humira para ser tratados a nivel hospitalario.

Barreras a nivel regulatorio Qué tipo de producto de referencia puede ser utilizado. Sustitución. Intercambiabilidad. Tipo y cantidad de estudios clínicos exigidos. Bolar. Best Mode (Mejor método de reproducción de una invención). Extrapolación. Sufijos

Sufijos Zarxio (filgrastim) Sandoz: 2016 -2018 (junio): 99% casos reportados con nombre de marca. Granix (filgrastim) Teva: 94% incluye nombre de marca. Infliximab (Remicade): 87% reportado nombre de marca.

Acuerdos Internacionales de Comercio Patentamiento – nuevos usos; eliminación restricciones ADPIC. Extensiones de patentes por demoras en oficina de patentes y en la agencia regulatoria. Periodo de exclusividad para biológicos. Definición de medicamentos biológicos. Linkage (vinculación entre aprobación regulatoria y status de la patente) Bolar (no obligatoria o restrictiva) No Best Mode (o mejor método de reproducción de una invención).

Desinformación / Confusión Nombre: Agregar un sufijo para que no parezca el mismo nombre. Instaurar temores que no se puede hacer el switch. Crear desconfianza que no será seguro y efectivo como el original.

Estrategias de Precios Negociar con distribuidores: Sólo recibirán rebajas si aceptan vender biosimilares también. Aceptar descuento a gobiernos pero forzarlos a aceptar que no compren a nadie mas. Subir el precio del medicamento en los últimos años de la patente. Luego del vencimiento de la patente bajar el precio para competir con los biosimilares o sacar su propio biosimilar antes que los otros puedan salir.

Estrategias de Precios Permitir un biosimilar autorizado. Hacer acuerdos como Abb. Vie está haciendo para primero bloquear con juicios a empresas que quieran sacar un medicamento y luego llegar a un acuerdo por el cual podrán vender en un mercado (ej. Europa) pero no en EEUU por varios años mas. Licitaciones publicas de 1 solo ganador: Ganancia de corto plazo pero pone en peligro la estabilidad del sistema

Potenciales acciones para ampliar el acceso a medicamento biosimilares Establecer mecanismos para obligar a empresas originales a que muestras a la competencia. Permitir el uso de un medicamento internacional de referencia. Cuidadoso otorgamiento de patentes. No otorgar patentes a nuevos usos o métodos de uso. No otorgar extensiones a las patentes. Asegurar Bolar efectiva. Demandar “best mode” y si la empresa mintió, pierde la patente.

Potenciales acciones para ampliar el acceso a medicamentos biosimilares Prevenir el uso de nombres diferentes – sufijos. No otorgar exclusividad de datos. No incluir definiciones demasiado amplias de biológicos y no permitir su inclusión en acuerdos comerciales. Prescripción a nuevos pacientes con el biosimilar. Prohibir acuerdos exclusivos. Gobiernos no deberían aceptar un bajo precio simplemente para evitar competencia. En el largo plazo la competencia da mejores resultados.

Potenciales acciones para ampliar el acceso a medicamentos biosimilares No permitir que el laboratorio original lance un “biosimilar autorizado”. Establecer incentivos para el lanzamiento de biosimilares. Establecer penalidades para sancionar a quienes actúen anticompetitivamente.

Muchas Gracias!!!! mfjorge@mfjint. com
- Slides: 31