Estequiometria bsica Criao Roberto Mafra Estequiometria ou clculo

Estequiometria básica Criação: Roberto Mafra

Estequiometria ou cálculo estequiométrico Calcula as relações de quantidades entre duas espécies (ou mais) em uma reação química balanceada Obs. Os coeficientes estequiométricos que balanceiam a equação fornecem a proporção, em mols, que as espécies se combinam em uma reação química.

Passo a Passo 1°) Escrever e balancear a equação química representativa da reação química envolvida. 2°) Identificar a espécie química usada como dado e a espécie química usado como incógnita. 3°) Escrever a proporção estequiométrica entre as duas espécies envolvidas. 4°) Montar a regra de três utilizando a proporção estequiométrica 5°) Resolver os cálculos matemáticos da regra de três.
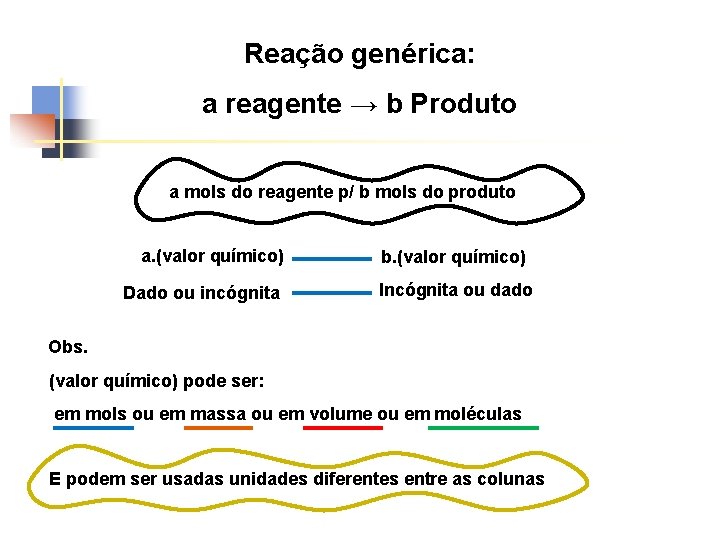
Reação genérica: a reagente → b Produto a mols do reagente p/ b mols do produto a. (valor químico) Dado ou incógnita b. (valor químico) Incógnita ou dado Obs. (valor químico) pode ser: em mols ou em massa ou em volume ou em moléculas E podem ser usadas unidades diferentes entre as colunas

Exercício 1) Suponha que uma quantidade 8, 8 g do gás dióxido de carbono reagiu com e hidrogênio, e que ocorreu a seguinte reação na CNTP : CO 2 (g) + H 2 (g) H 2 O (g) + CO (g) Assinale a alternativa que indica o volume, em litros, de monóxido de carbono produzido a) 2, 24 b) 4, 48 c) 22, 4 d) 44, 8 e) 89, 6
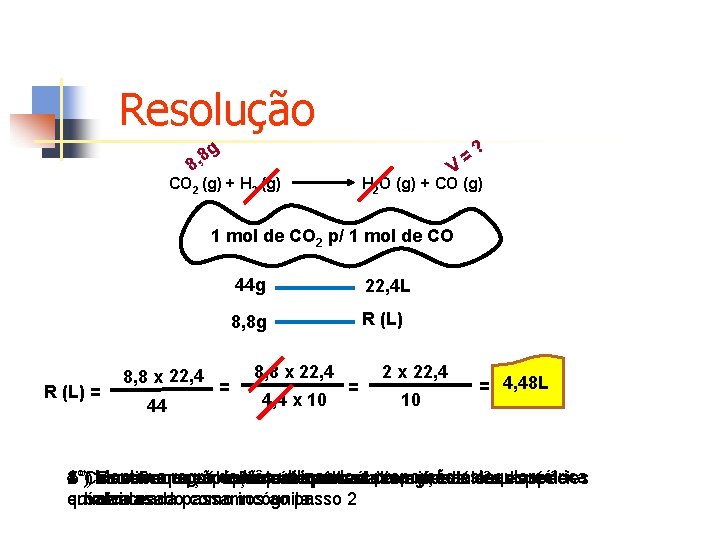
Resolução g 8 8, V CO 2 (g) + H 2 (g) = ? H 2 O (g) + CO (g) 1 mol de CO 2 p/ 1 mol de CO R (L) = 8, 8 x 22, 4 44 = 44 g 22, 4 L 8, 8 g R (L) 8, 8 x 22, 4 4, 4 x 10 = 2 x 22, 4 10 = 4, 48 L 4°) Montar a regra de três utilizando a proporção estequiométrica 2°) 3°) 5°)Como Identificar Escrever Resolver a equação aos aproporção espécie cálculos química matemáticos estequiométrica representativa usada da como regra entre jádado está de as três. duas escrita e a espécies e química envolvidas. balanceada usadopassamos como incógnita. ao passo 2
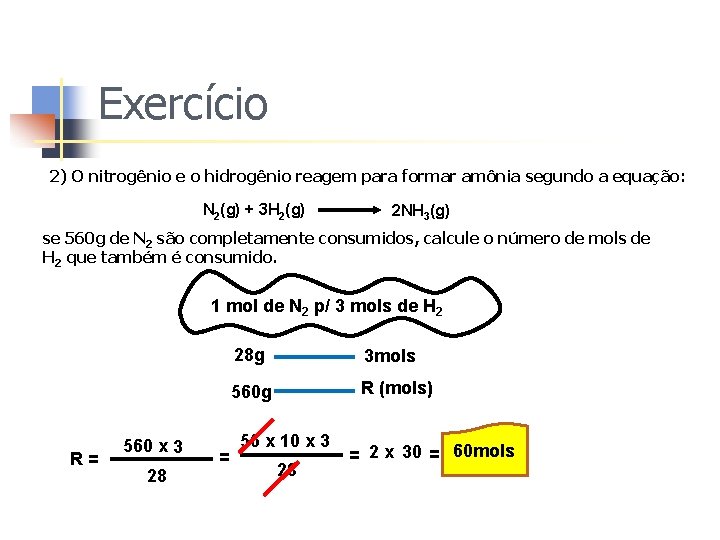
Exercício 2) O nitrogênio e o hidrogênio reagem para formar amônia segundo a equação: N 2(g) + 3 H 2(g) 2 NH 3(g) se 560 g de N 2 são completamente consumidos, calcule o número de mols de H 2 que também é consumido. 1 mol de N 2 p/ 3 mols de H 2 R= 560 x 3 28 = 28 g 3 mols 560 g R (mols) 56 x 10 x 3 28 = 2 x 30 = 60 mols
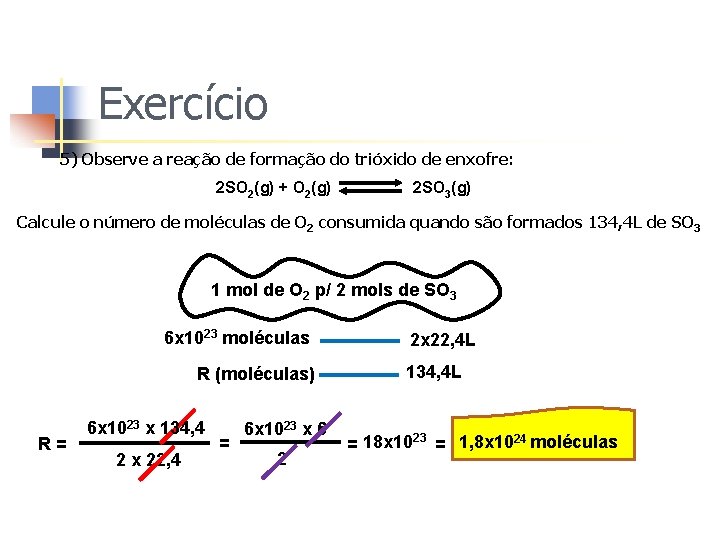
Exercício 5) Observe a reação de formação do trióxido de enxofre: 2 SO 2(g) + O 2(g) 2 SO 3(g) Calcule o número de moléculas de O 2 consumida quando são formados 134, 4 L de SO 3 1 mol de O 2 p/ 2 mols de SO 3 6 x 1023 moléculas R (moléculas) R= 6 x 1023 x 134, 4 2 x 22, 4 = 6 x 1023 x 6 2 2 x 22, 4 L 134, 4 L = 18 x 1023 = 1, 8 x 1024 moléculas

FIM Criação: Roberto Mafra
- Slides: 9