ESTEQUIOMETRA PROBLEMAS RESUELTOS Y PROPUESTOS PROBLEMA RESUELTO Las

ESTEQUIOMETRÍA �PROBLEMAS RESUELTOS Y PROPUESTOS

PROBLEMA RESUELTO � Las bolsas de aire de los automóviles se inflan cuando la azida de sodio Na. N 3 se descompone rápidamente en sus componentes. � a) Escribir una ecuación química balanceada. � b) ¿Cuántos gramos de azida de sodio se requieren para formar 5. 0 g de nitrógeno

SOLUCIÓN � Se escribe la ecuación química balanceada y se subrayan las substancias consideradas en el problema; sobre el nitrógeno se escribe la cantidad que debe obtenerse y sobre la azida de sodio una x pues es nuestra incógnita. Abajo de las fórmulas subrayadas se escriben sus pesos molares : x 5. 0 g 2 Na. N 3(S) 2 Na (s) + 3 N 2(g) 2(65 g/mol) 3(28 g/mol) Calculamos los pesos molares de la azida de sodio Na. N 3 y del N 2 a partir de sus pesos atómicos: Pesos atómicos: Na = 23 uma N= 14 uma 1 Na = 23 uma x 1átomo = 23 uma 3 N = 14 uma x 3 átomos = 42 uma 65 uma 2 N= 14 uma x 2= 28

Problema resuelto � Recuerda que los pesos obtenidos en uma los convertimos a gramos y deben multiplicarse por el número de moles correspondiente: Escribimos una ecuación con los datos anotados: X = 5. 0 g 2(65 g/mol) 3(28 g/mol) Despejamos la incógnita: x= Na. N 3 5. 0 g x 130 g/mol 84 g/mol x= 7. 74 g. de
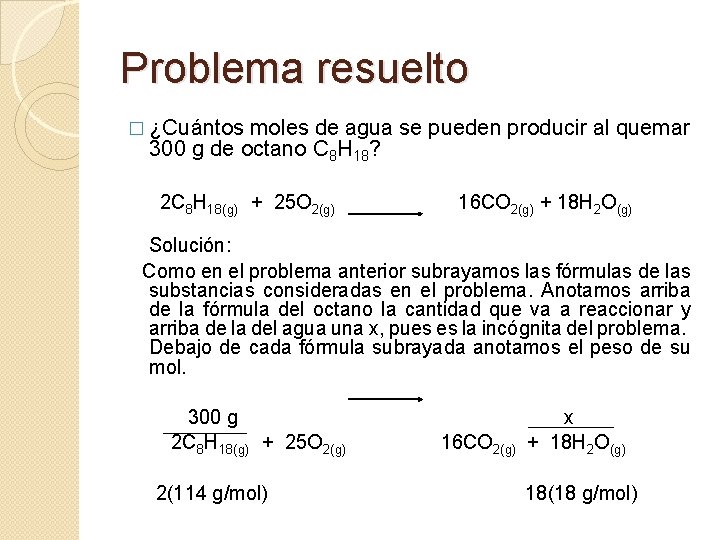
Problema resuelto � ¿Cuántos moles de agua se pueden producir al quemar 300 g de octano C 8 H 18? 2 C 8 H 18(g) + 25 O 2(g) 16 CO 2(g) + 18 H 2 O(g) Solución: Como en el problema anterior subrayamos las fórmulas de las substancias consideradas en el problema. Anotamos arriba de la fórmula del octano la cantidad que va a reaccionar y arriba de la del agua una x, pues es la incógnita del problema. Debajo de cada fórmula subrayada anotamos el peso de su mol. 300 g 2 C 8 H 18(g) + 25 O 2(g) 2(114 g/mol) 16 CO 2(g) x + 18 H 2 O(g) 18(18 g/mol)

Problema resuelto �Establecemos la ecuación: 300 g = x 228 g/mol 324 g/mol �Despejamos la incógnita: x= 300 g x 324 g/mol H 2 O 228 g/mol x= 426. 3 g de

Problema resuelto �Esta cantidad de agua la convertimos a moles: n= 426. 3 g H 2 O 18 g/ mol n= 23. 7 moles de

Problema propuesto �El transbordador espacial está impulsado por H 2 y O 2 que reaccionan para producir agua. �¿Cuántas moléculas de agua se pueden producir haciendo reaccionar 0. 010 mol de oxígeno con hidrógeno?

Problema propuesto �En un alto horno, el óxido de hierro III reacciona con coque (carbón) y produce hierro fundido y monóxido de carbono. ¿Cuántos kilogramos de hierro se pueden producir a partir de 115 kg. de Fe 2 O 3? Fe 2 O 3 + 3 C 2 Fe + 3 CO
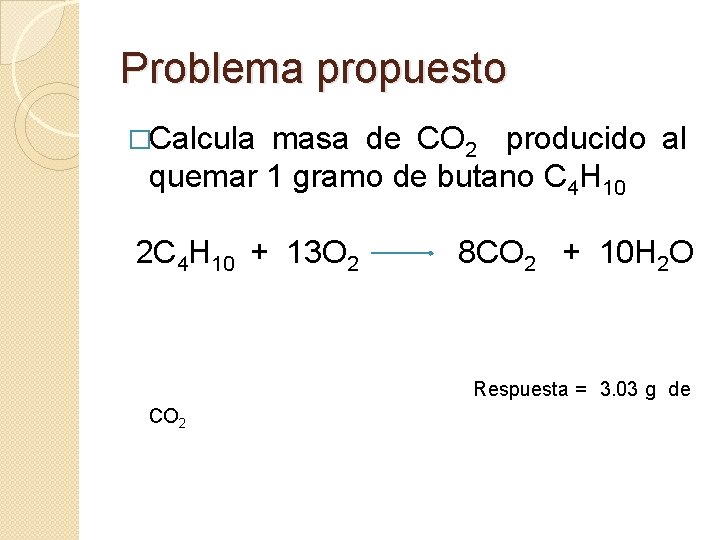
Problema propuesto �Calcula masa de CO 2 producido al quemar 1 gramo de butano C 4 H 10 2 C 4 H 10 + 13 O 2 8 CO 2 + 10 H 2 O Respuesta = 3. 03 g de CO 2

Problema propuesto: � Para la siguiente ecuación balanceada: 4 Al + 3 O 2 2 Al 2 O 3 ¿Cuántos moles de O 2 reaccionan con 3. 17 moles de Al? b) A partir de 8. 25 moles de O 2 ¿Cuántos moles de Al 2 O 3 se producen? Respuestas: a) 2. 38 moles de O 2 b) 5. 50 moles de Al 2 O 3 a) http: //genesis. uag. mx/edmedia/material/QIno/T 8. cfm
- Slides: 11