Estequiometra Problemas de 3 ESO 2 Trabaja con

Estequiometría Problemas de 3º ESO (2) Trabaja con “papel y lápiz”. Copia los enunciados y resuélvelos consultando las dudas o comprobado los resultados en la presentación interactiva. Cruz Martínez

Ejercicios explicados en clase En los enunciados de estos problemas no tendremos en cuenta si la reacción se produce en la realidad o no, ni si los reactivos deberían estar en disolución o cualquier otro parámetro que por lógica deberíamos considerar. Se trata de comprender el razonamiento lógico de este tipo de cálculos y adquirir una mecánica básica para la resolución de este tipo de problemas. Aunque más adelante, en bachillerato, deban resolver todos los problemas trabajando con moles, creo que es muy importante que comprendan y aprendan a realizar los cálculos trabajando con gramos. Paralelamente, a los alumnos interesados, se les explicará la resolución de los problemas empleando los moles. Del mismo modo, creo que les facilita la comprensión el uso de la regla de tres, especialmente a los alumnos que tienen dificultades con las matemáticas. Más adelante se explicará también la resolución mediante proporciones estequiométricas. Cruz Martínez

Trabaja con “papel y lápiz”. Copia los enunciados y resuélvelos consultando las dudas o comprobado los resultados en la presentación interactiva. Los pasos indicados a la izquierda te abren con un clic sus respectivas soluciones, otro clic las cierra. Sugerencias: 1. Si no tienes “ni idea de por donde empezar”, repasa varios ejercicios paso por paso tratando de comprenderlos. Cuando creas que lo comprendes, pasa al papel y lápiz. No te olvides de cerrar las soluciones. 2. Cuando hagas el ejercicio en papel, abre sólo la “solución” de la parte inferior, si coincide, ábrelo por pasos. Si no coincide, repasa tu ejercicio antes de ver el proceso paso por paso; si no ves el fallo, vete abriendo los pasos uno a uno comparándolos con lo que has hecho. Cruz Martínez
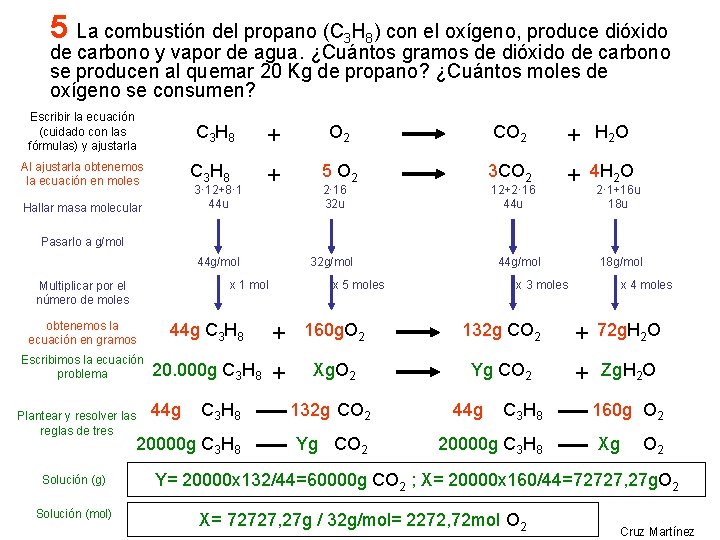
5 La combustión del propano (C 3 H 8) con el oxígeno, produce dióxido de carbono y vapor de agua. ¿Cuántos gramos de dióxido de carbono se producen al quemar 20 Kg de propano? ¿Cuántos moles de oxígeno se consumen? Escribir la ecuación (cuidado con las fórmulas) y ajustarla C 3 H 8 Al ajustarla obtenemos la ecuación en moles C 3 H 8 3· 12+8· 1 44 u Hallar masa molecular + O 2 CO 2 + H 2 O + 5 O 2 3 CO 2 + 4 H 2 O 2· 16 32 u 12+2· 16 44 u 2· 1+16 u 18 u Pasarlo a g/mol 44 g/mol 32 g/mol x 1 mol Multiplicar por el número de moles 44 g/mol x 5 moles 18 g/mol x 3 moles x 4 moles obtenemos la ecuación en gramos 44 g C 3 H 8 + 160 g. O 2 132 g CO 2 + 72 g. H 2 O Escribimos la ecuación problema 20. 000 g C 3 H 8 + Xg. O 2 Yg CO 2 + Zg. H 2 O Plantear y resolver las reglas de tres Solución (g) Solución (mol) C 3 H 8 132 g CO 2 20000 g C 3 H 8 Yg CO 2 44 g C 3 H 8 20000 g C 3 H 8 160 g O 2 Xg O 2 Y= 20000 x 132/44=60000 g CO 2 ; X= 20000 x 160/44=72727, 27 g. O 2 X= 72727, 27 g / 32 g/mol= 2272, 72 mol O 2 Cruz Martínez
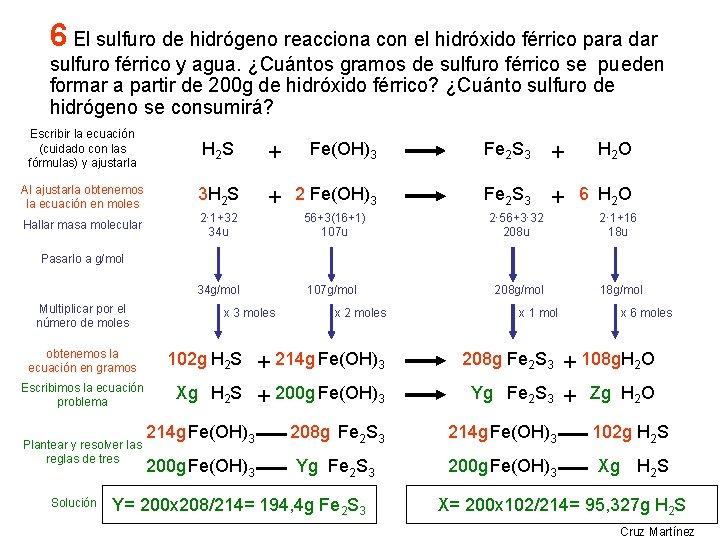
6 El sulfuro de hidrógeno reacciona con el hidróxido férrico para dar sulfuro férrico y agua. ¿Cuántos gramos de sulfuro férrico se pueden formar a partir de 200 g de hidróxido férrico? ¿Cuánto sulfuro de hidrógeno se consumirá? Escribir la ecuación (cuidado con las fórmulas) y ajustarla H 2 S + Fe(OH)3 Fe 2 S 3 + H 2 O Al ajustarla obtenemos la ecuación en moles 3 H 2 S + 2 Fe(OH)3 Fe 2 S 3 + 6 H 2 O Hallar masa molecular 2· 1+32 34 u 56+3(16+1) 107 u 2· 56+3· 32 208 u 2· 1+16 18 u 34 g/mol 107 g/mol 208 g/mol 18 g/mol Pasarlo a g/mol Multiplicar por el número de moles obtenemos la ecuación en gramos Escribimos la ecuación problema Plantear y resolver las reglas de tres Solución x 3 moles x 2 moles x 1 mol x 6 moles + 214 g Fe(OH)3 + 200 g Fe(OH)3 208 g Fe 2 S 3 214 g Fe(OH)3 102 g H 2 S 200 g Fe(OH)3 Yg Fe 2 S 3 200 g Fe(OH)3 Xg H 2 S 102 g H 2 S Xg H 2 S Y= 200 x 208/214= 194, 4 g Fe 2 S 3 Yg Fe 2 S 3 + 108 g. H 2 O + Zg H 2 O X= 200 x 102/214= 95, 327 g H 2 S Cruz Martínez

7 El cinc reacciona con el sulfato cúprico dando sulfato de cinc más el cobre al que desplaza. ¿Cuántos gramos de cinc se consumen y cuántos de sulfato de cinc se forman al reaccionar 750 g de sulfato cúprico? Escribir la ecuación (cuidado con las fórmulas) y ajustarla Zn + Cu. SO 4 Zn. SO 4 + Cu Al ajustarla obtenemos la ecuación en moles 1 Zn + 1 Cu. SO 4 1 Zn. SO 4 + 1 Cu Hallar masa molecular 65, 5 u 63, 5+32+4· 16 159, 5 u 65, 5+32+4· 16 161, 5 u 159, 5 g/mol 161, 5 g/mol 63, 5 u Pasarlo a g/mol 65, 5 g/mol Multiplicar por el número de moles x 1 mol obtenemos la ecuación en gramos 65 g Zn Escribimos la ecuación problema Xg Zn 159, 5 g Cu. SO 4 Plantear y resolver las reglas de tres Solución 750 g Cu. SO 4 x 1 mol + 159, 5 g Cu. SO 4 + 750 g Cu. SO 4 x 1 mol 161, 5 g Zn. SO 4 Yg Zn. SO 4 65, 5 g Zn 159, 5 g Cu. SO 4 Zn 750 g Cu. SO 4 Xg X= 750 x 65, 5/159, 5= 307, 9 g Zn 63 g/mol x 1 mol + + 63 g Cu Zg Cu 161, 5 g Zn. SO 4 Y= 750 x 161, 5/159, 5= 759, 4 g Zn. SO 4 Cruz Martínez
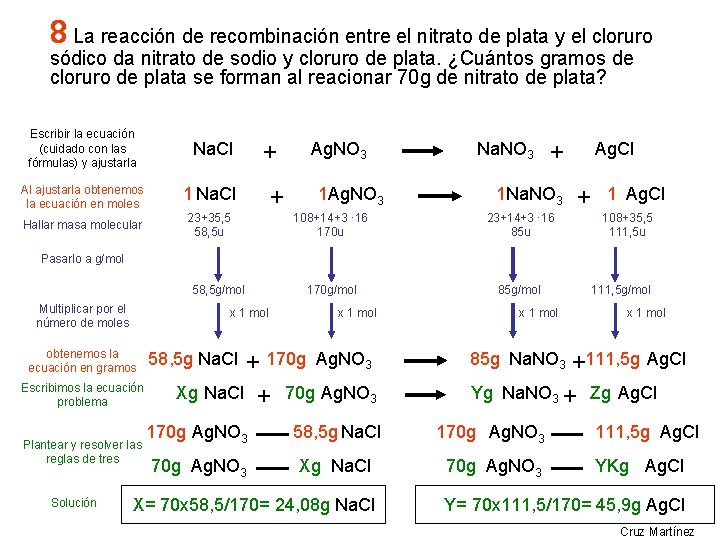
8 La reacción de recombinación entre el nitrato de plata y el cloruro sódico da nitrato de sodio y cloruro de plata. ¿Cuántos gramos de cloruro de plata se forman al reacionar 70 g de nitrato de plata? Escribir la ecuación (cuidado con las fórmulas) y ajustarla Na. Cl Al ajustarla obtenemos la ecuación en moles 1 Na. Cl Hallar masa molecular 23+35, 5 58, 5 u + + Ag. NO 3 Na. NO 3 1 Ag. NO 3 + 1 Na. NO 3 108+14+3 · 16 170 u 23+14+3 · 16 85 u 170 g/mol 85 g/mol Ag. Cl + 1 Ag. Cl 108+35, 5 111, 5 u Pasarlo a g/mol 58, 5 g/mol Multiplicar por el número de moles x 1 mol obtenemos la ecuación en gramos Escribimos la ecuación problema Plantear y resolver las reglas de tres Solución x 1 mol + 170 g Ag. NO 3 Xg Na. Cl + 70 g Ag. NO 3 58, 5 g Na. Cl x 1 mol +111, 5 g Ag. Cl Na. NO 3 + Zg Ag. Cl 85 g Na. NO 3 Yg 170 g Ag. NO 3 58, 5 g Na. Cl 170 g Ag. NO 3 Xg Na. Cl 70 g Ag. NO 3 X= 70 x 58, 5/170= 24, 08 g Na. Cl 111, 5 g/mol 111, 5 g Ag. Cl YKg Ag. Cl Y= 70 x 111, 5/170= 45, 9 g Ag. Cl Cruz Martínez

Cruz Martínez
- Slides: 8