ESTEQUIOMETRA Objetivo Reconocer el Mol como unidad de

ESTEQUIOMETRÍA Objetivo: Reconocer el Mol como unidad de cantidad de partículas (átomos, moléculas o iones) QUÍMICA II° PROFESORA YARITHMAR CHACÓN
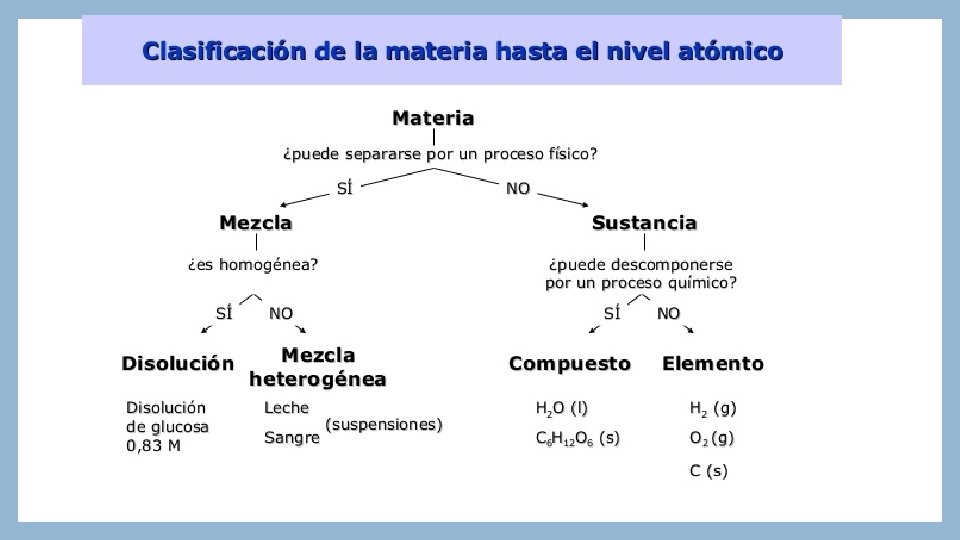

Estequiometría: Son las relaciones cuantitativas que se pueden establecer entre reactantes y productos en una reacción química. PAR DOCENA DECENA QUINTETO CUARTETO TRIO Mol: Es una unidad que se emplea para medir cantidad de sustancia (átomos, moléculas, iones o partículas)

Número de Avogadro (NA) Es el número de partículas constituyentes (átomos, moléculas e iones) que están contenidos en 12 g de 12 C.

Relación entre una reacción química y la elaboración de galletas con chispas de chocolate

¿Cómo leer una ecuación química? 2 Mg • Átomos/ moléculas: • Moles • Gramos 2 átomos de Mg + O 2 + 2 moléculas O 2 2 mol de Mg + 1 mol de O 2 48 g/mol + 36 g/mol 2 Mg. O 2 moléculas de Mg. O 2 mol de Mg. O 80 g/mol

Ejercitemos • Calcular la masa molar del H 2 SO 4 Pesos atómicos: H= 1 g/mol S= 32 g/mol O= 16 g/mol • Calcular la masa molar del Na. OH Na= 23 g/mol ü Recuerda que se debe multiplicar la cantidad de átomos de cada elemento que hay en el compuesto por el peso atómico dado de c/u respectivamente. ü Luego sumar para obtener la masa total del compuesto. Ejm: H 2 O H= 2 x 1 g/mol= 2 g/mol O= 1 x 16 g/mol= 16 g/mol 18 g/mol
- Slides: 7