Estado nativo N Compactacin ptima Grupos polares en





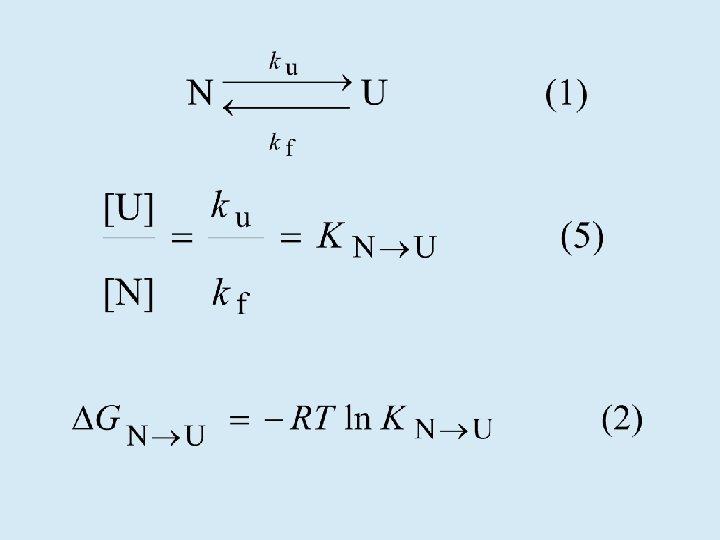


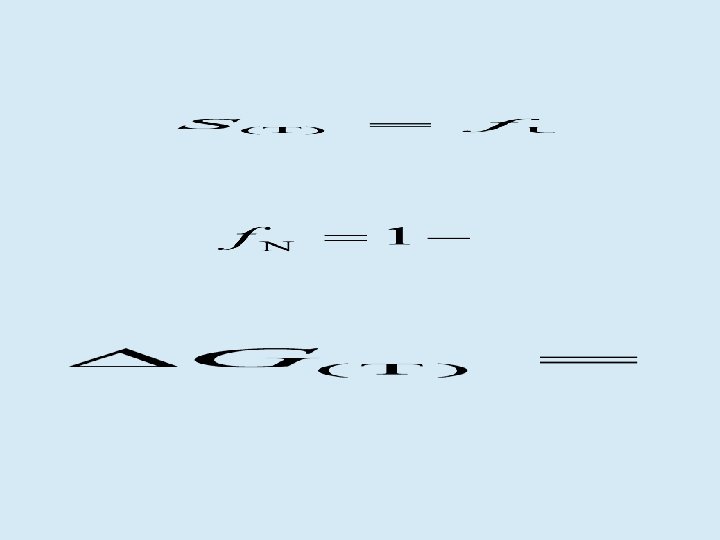



- Slides: 43


Estado nativo (N) • • Compactación óptima Grupos polares en el exterior Mínima superficie expuesta Anisotropía y baja periodicidad Organización jerárquica de la estructura Flexibilidad óptima Conformación única y cooperativa Mínimo energético

Estado desplegado (U) • Expansión máxima (5 -10 veces el volumen de N) Máxima superficie expuesta al solvente • No existen interacciones preferenciales entre residuos • Infinitas conformaciones • Estado ideal, modelo teórico que describe aproximadamente el comportamiento de muchas proteínas en condiciones fuertemente desnaturalizantes

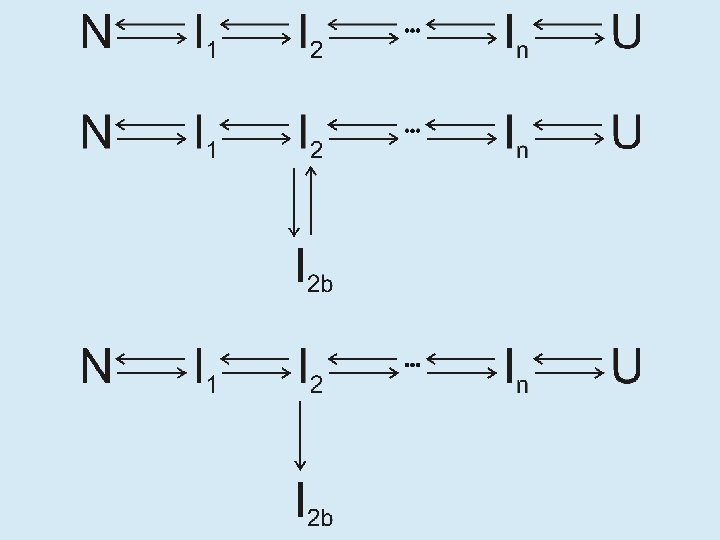
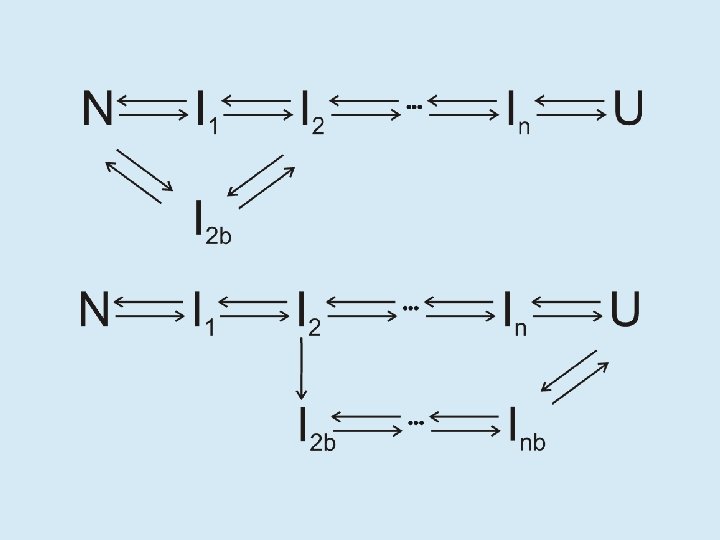
Estados parcialmente plegados (I) • • • Grupo heterogéneo de conformaciones no nativas Estructura residual secundaria, nativa o no nativa Sin estructura terciaria Tendencia a la agregación Existen como: Precursores cinéticos de N En trazas en equilibrio con N En ausencia de cofactores específicos Resultado de vías muertas del plegamiento

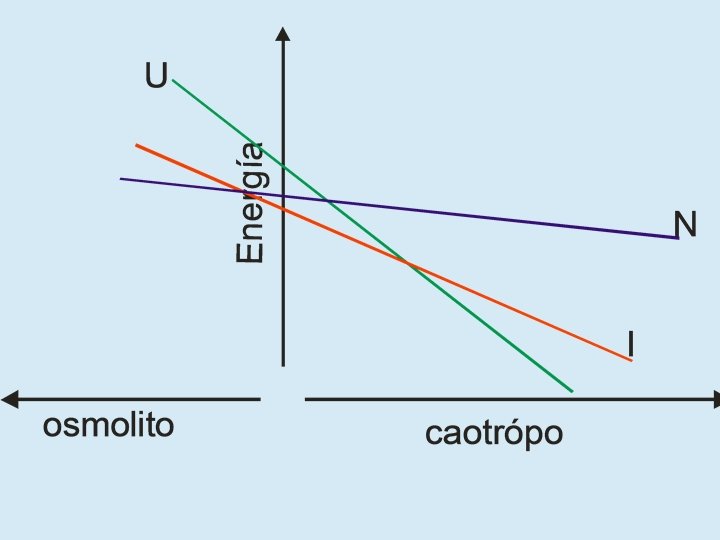
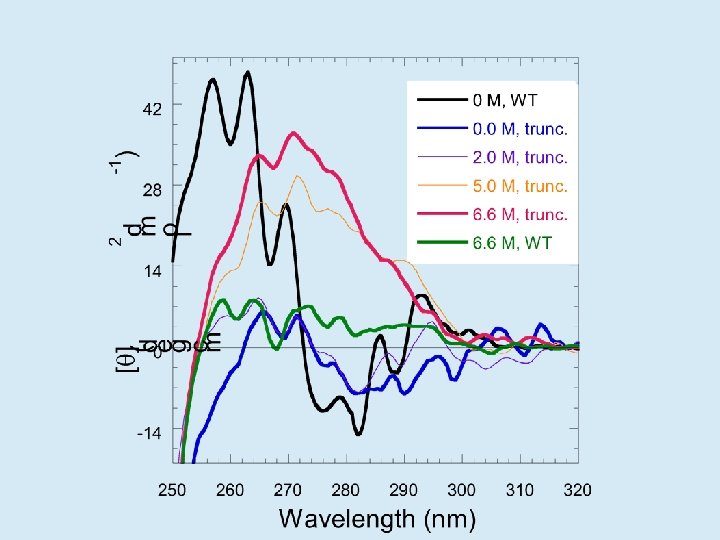
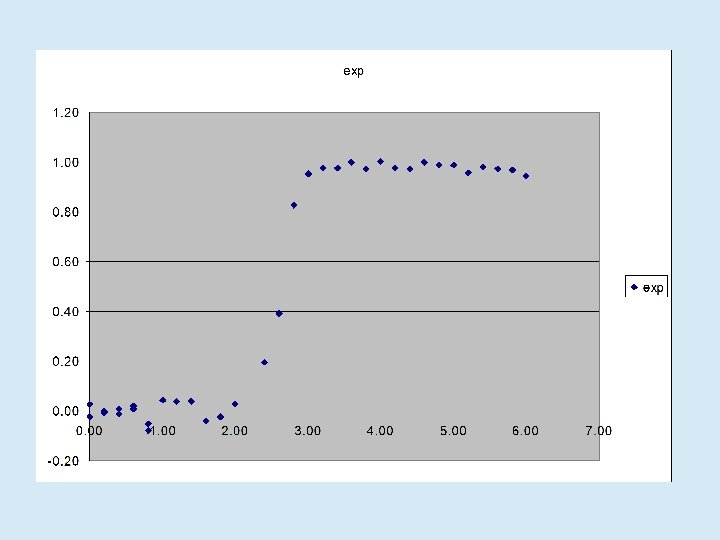
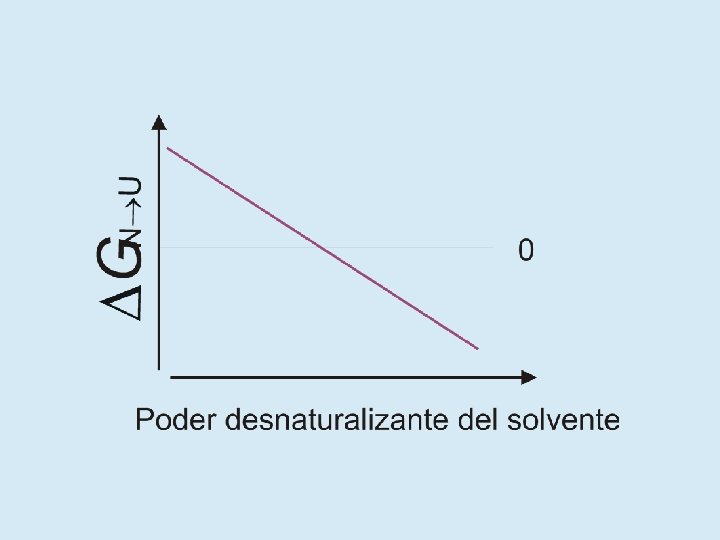
¿Qué relación existe entre N, I y U? • En soluciones fisiológicas N es absolutamente mayoritario • En presencia de urea o cloruro de guanidinio concentrados (agentes caotrópicos), N se desestabiliza y aparecen I y U • Los agentes caotrópicos solubilizan las cadenas laterales haciendo más favorable la interacción con el agua



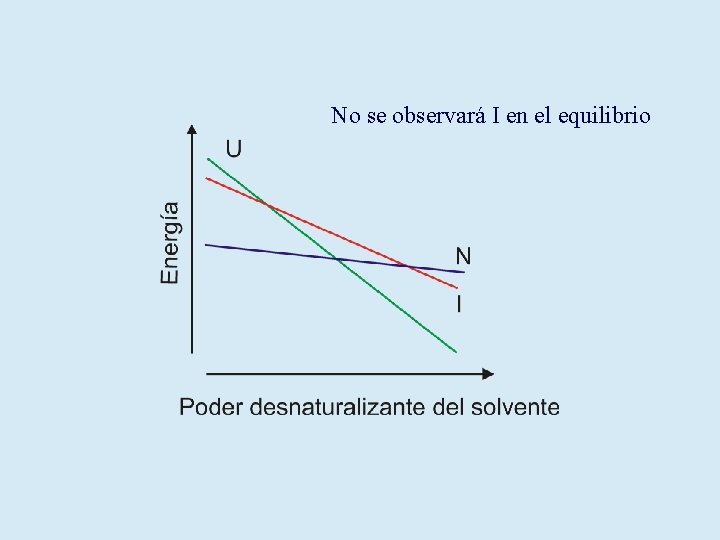
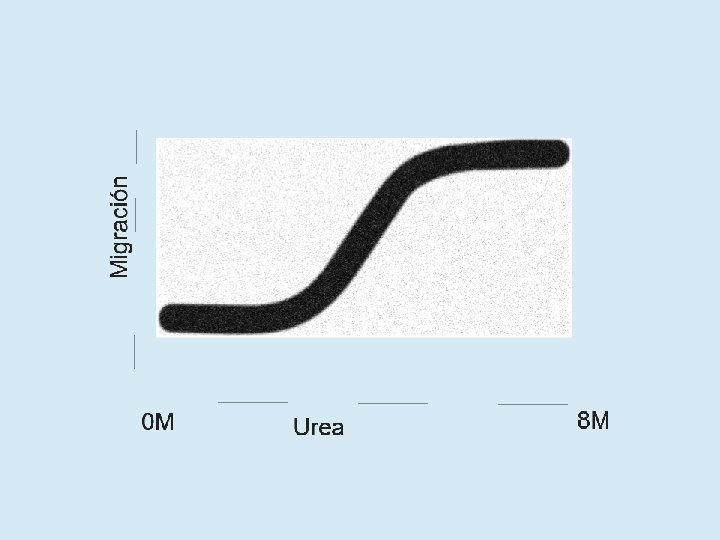
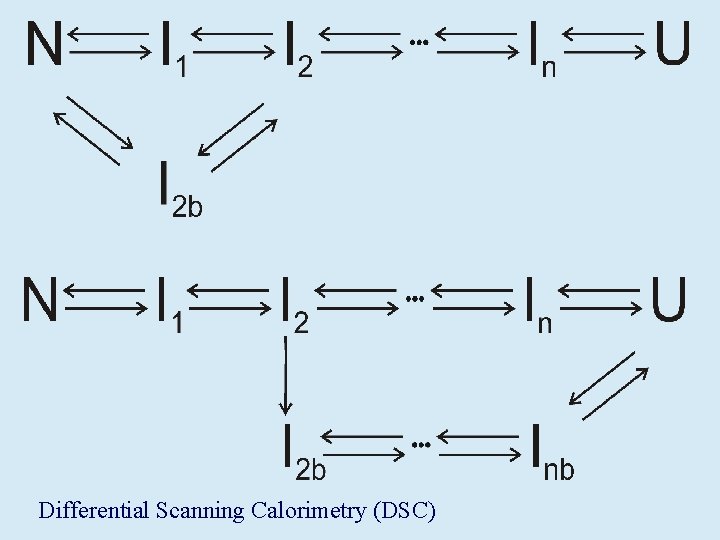
No se observará I en el equilibrio

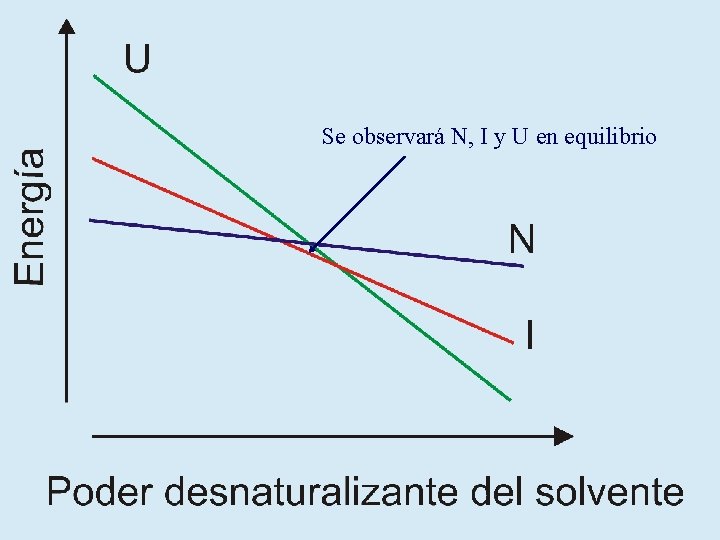
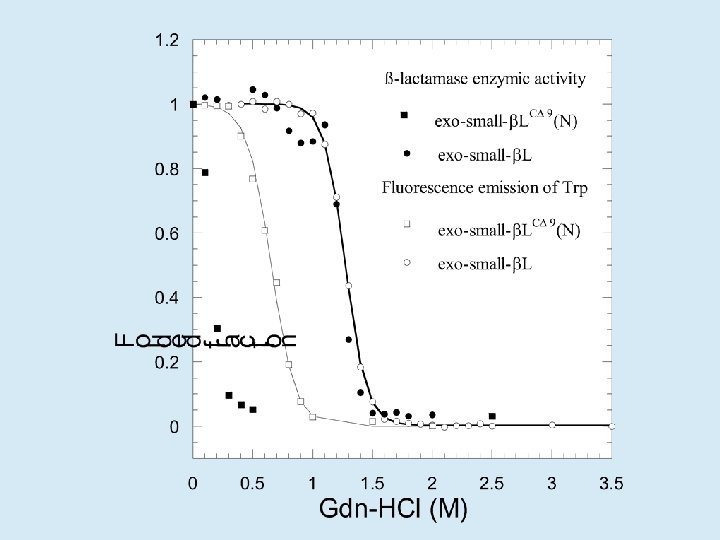
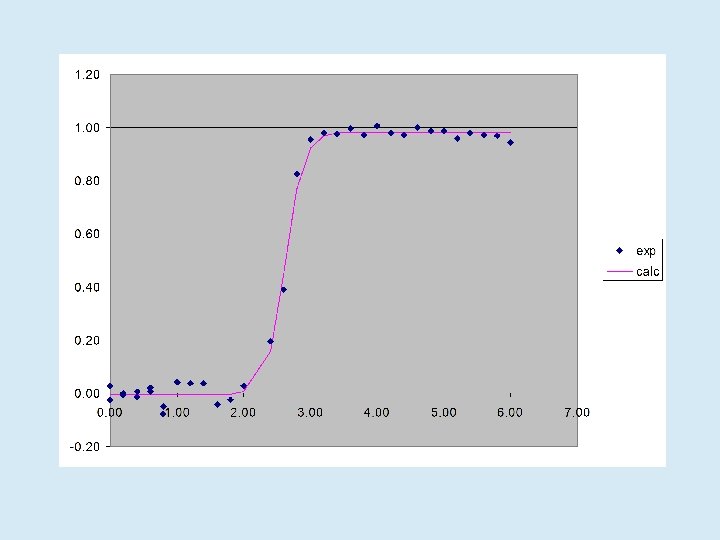
Se observará N, I y U en equilibrio



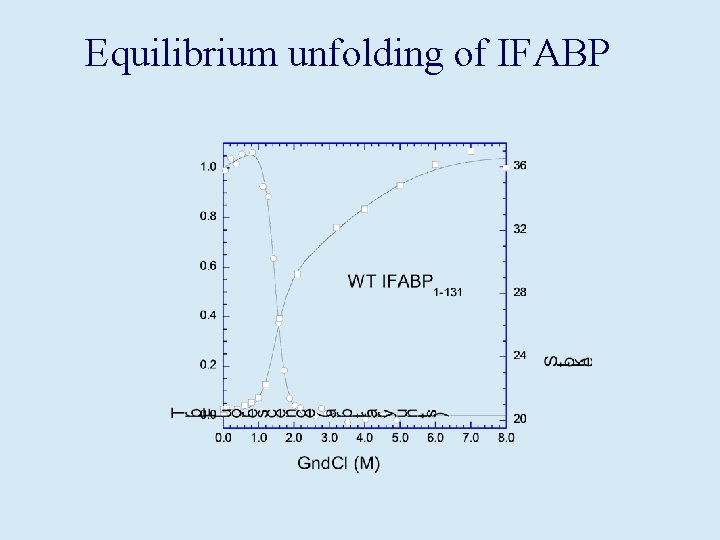
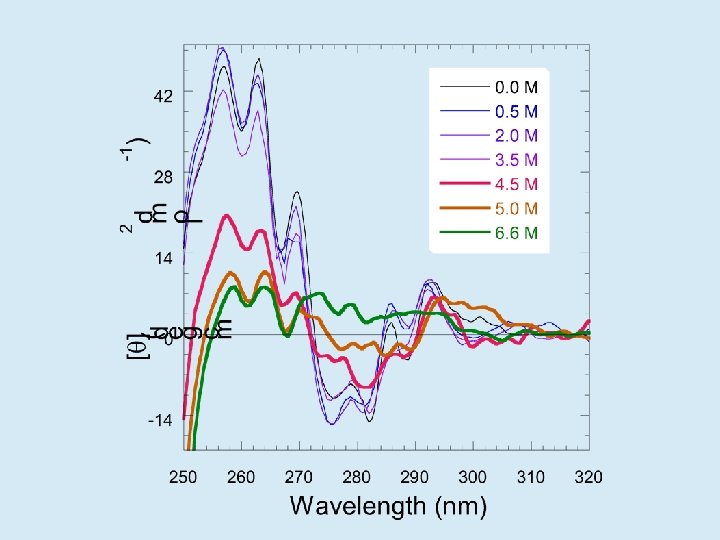
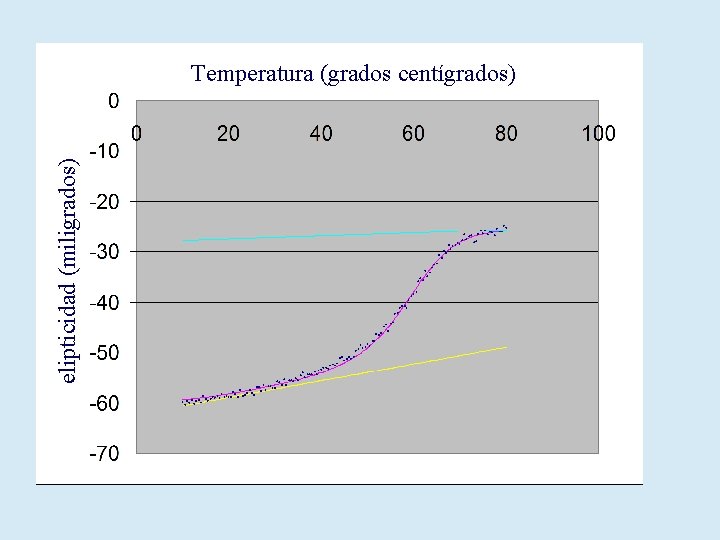
Equilibrium unfolding of IFABP




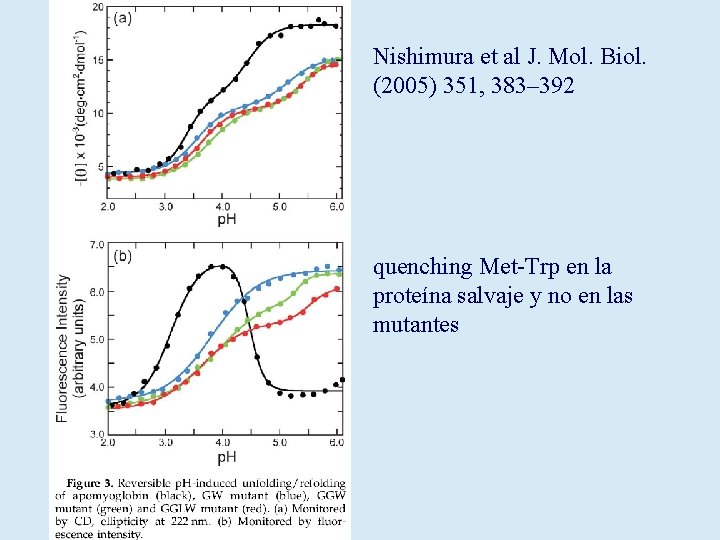
Nishimura et al J. Mol. Biol. (2005) 351, 383– 392 quenching Met-Trp en la proteína salvaje y no en las mutantes
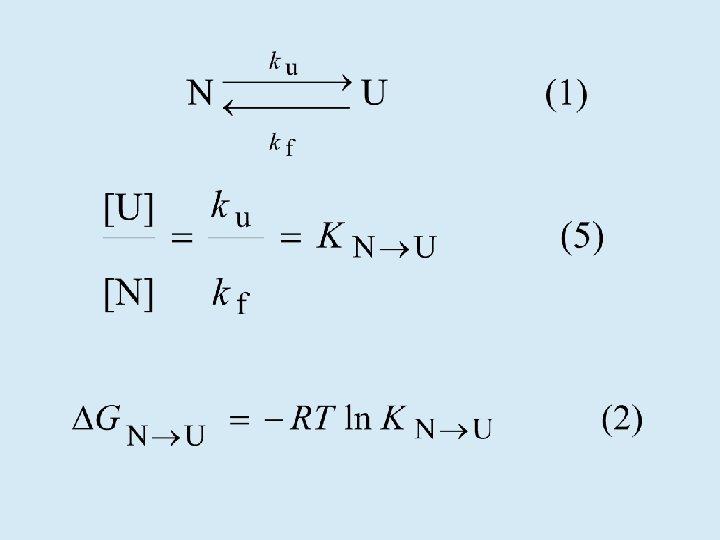






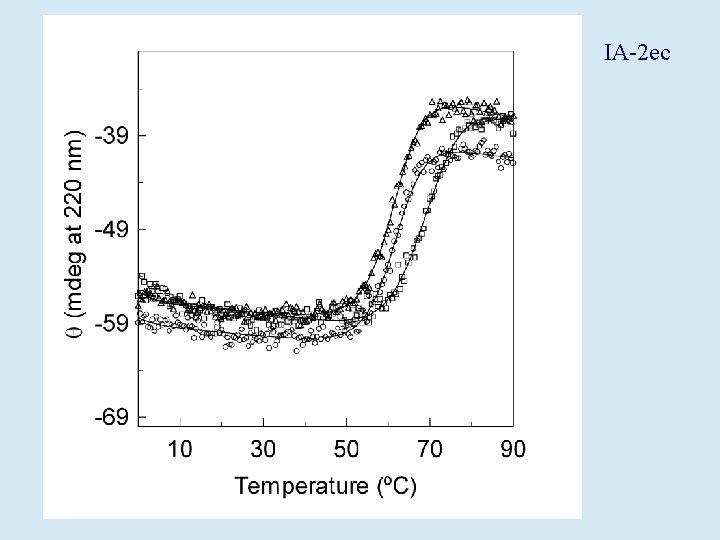
elipticidad (miligrados) Temperatura (grados centígrados)

IA-2 ec
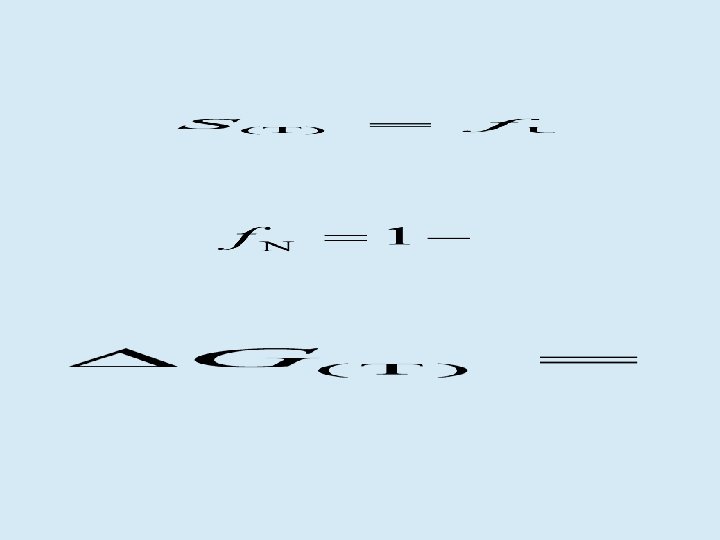

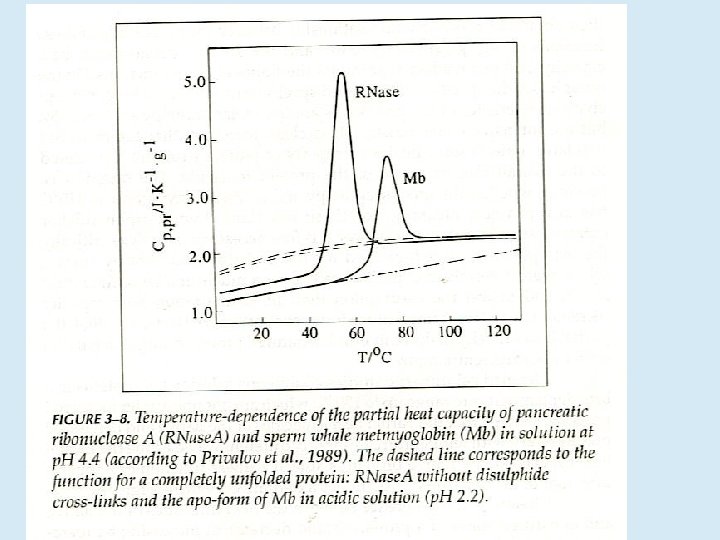
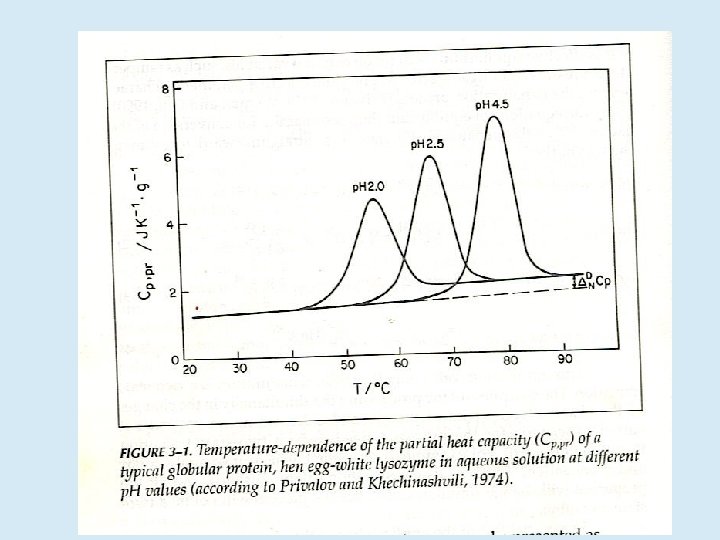
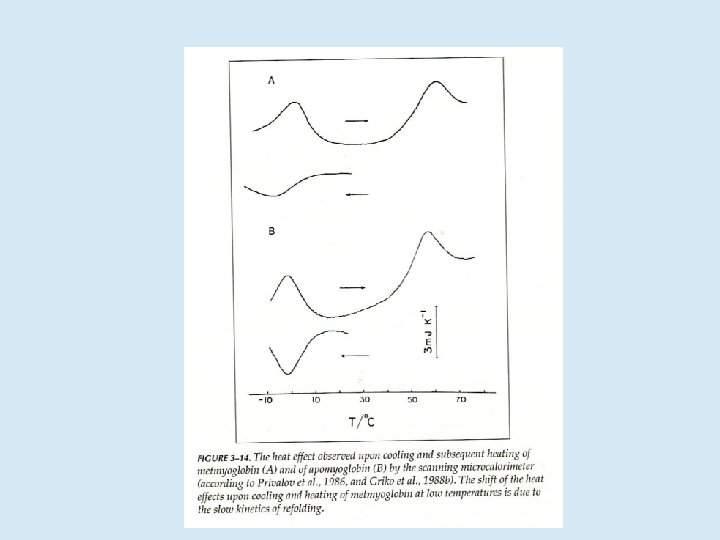
Differential Scanning Calorimetry (DSC)







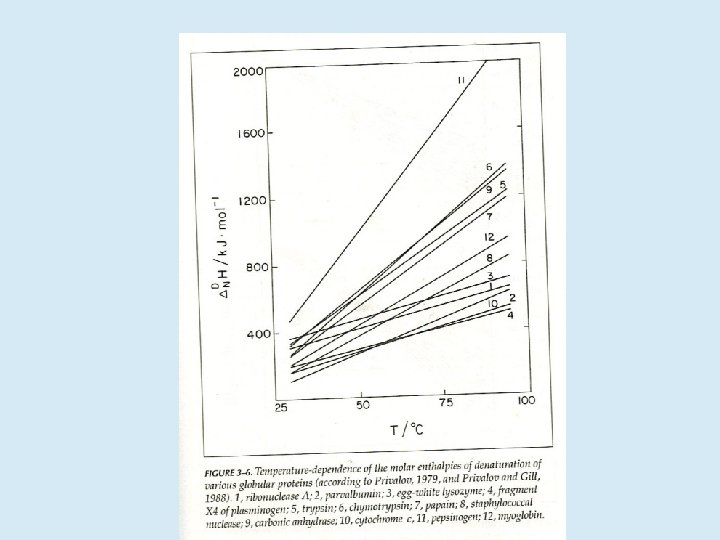
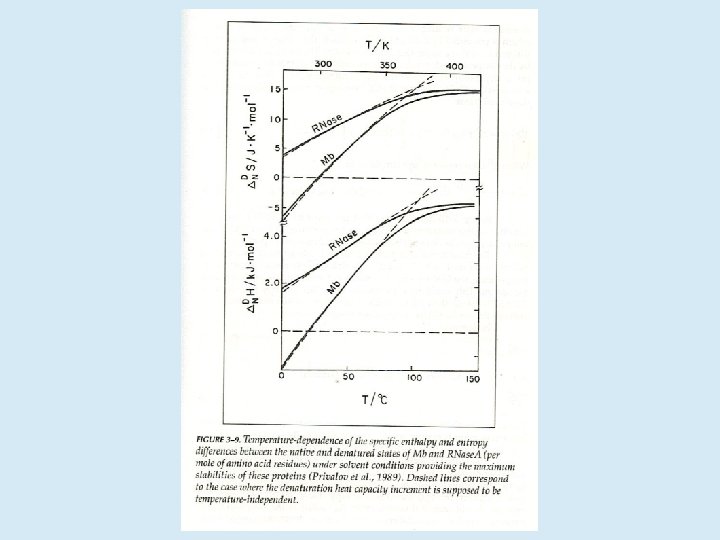
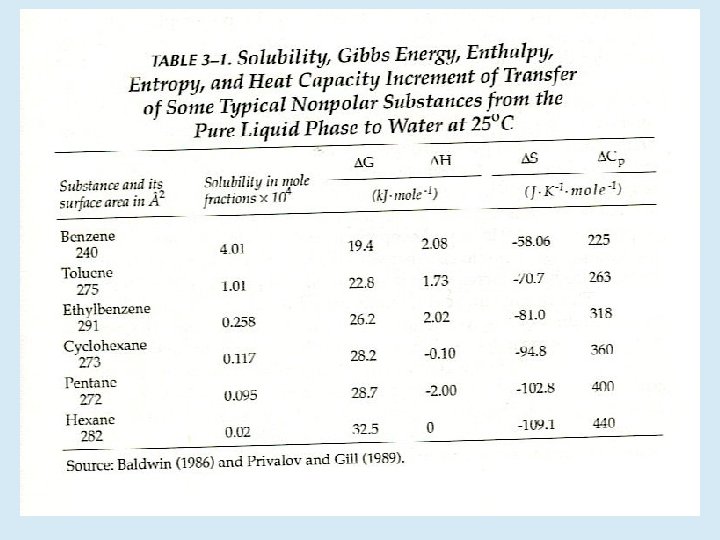
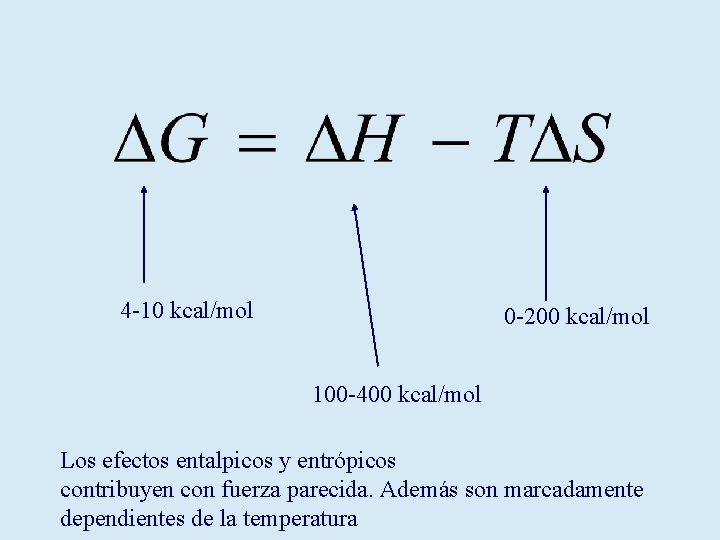
4 -10 kcal/mol 0 -200 kcal/mol 100 -400 kcal/mol Los efectos entalpicos y entrópicos contribuyen con fuerza parecida. Además son marcadamente dependientes de la temperatura

¿Cuáles son las contribuciones entrópicas? • La diferencia enorme entre el número de conformaciones permitidas a U y N • El ordenamiento de las moléculas de agua sobre la superficie accesible S=R´ln(w)

¿Cuáles son las contribuciones entálpicas? • Interacciones de van der Waals • Puentes de hidrógeno • Puentes salinos

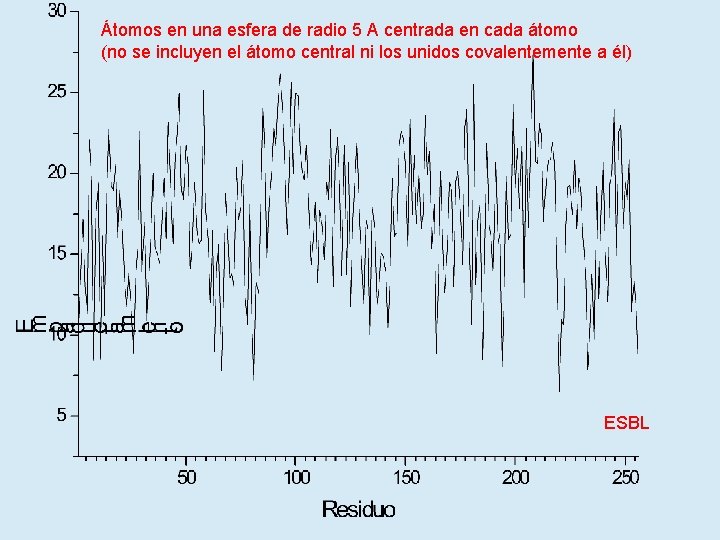
Átomos en una esfera de radio 5 A centrada en cada átomo (no se incluyen el átomo central ni los unidos covalentemente a él) ESBL

Salvo muy escasas excepciones no existen puentes de hidrógeno sin satisfacer en el interior proteico. Todos son intramoleculares. Son muy pocos los puentes salinos encontrados en el interior proteico. En general desestabilizan a la estructura nativa.

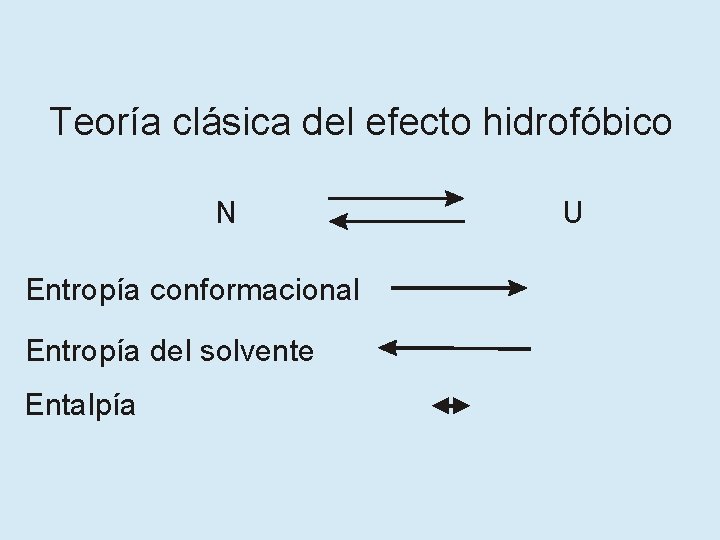
Teoría clásica del efecto hidrofóbico N Entropía conformacional Entropía del solvente Entalpía U

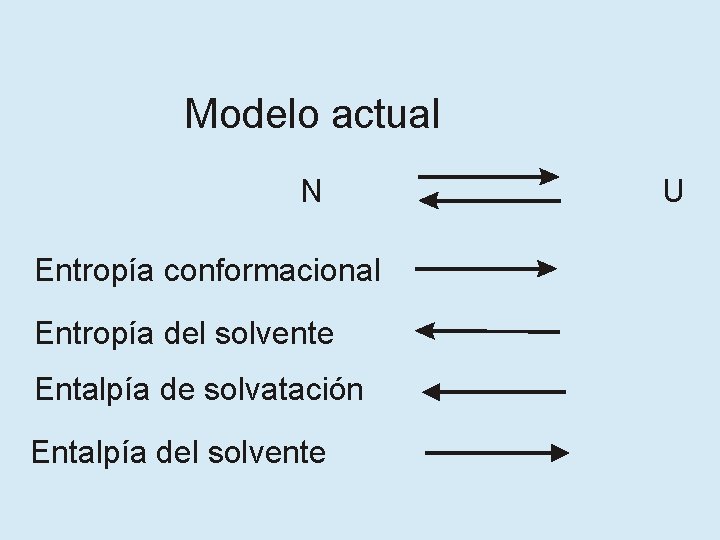
Modelo actual N Entropía conformacional Entropía del solvente Entalpía de solvatación Entalpía del solvente U

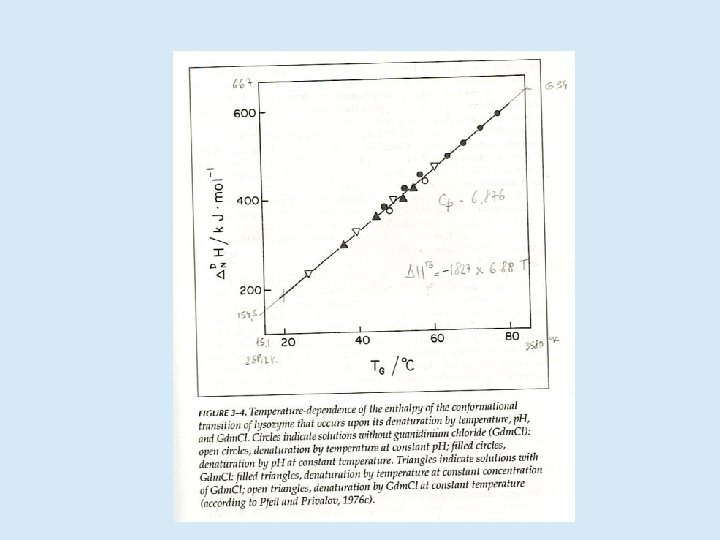
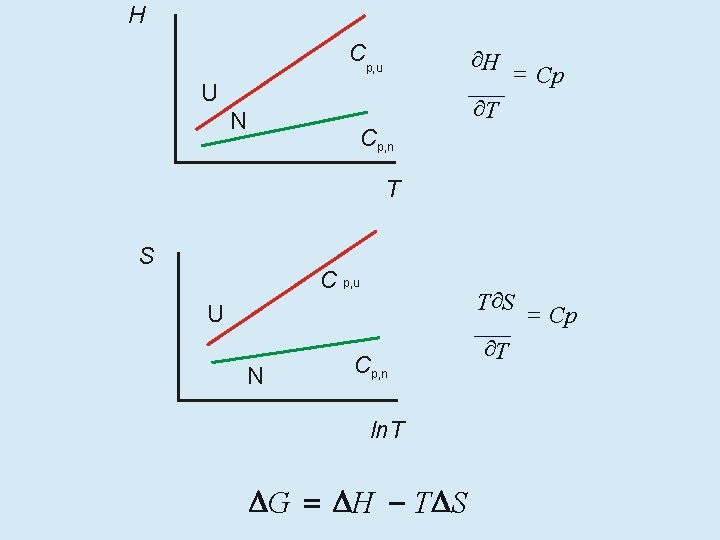
H Cp, u ¶H = Cp ¶T U N Cp, n T S C p, u T¶S = Cp ¶T U Cp, n N ln. T G H T S

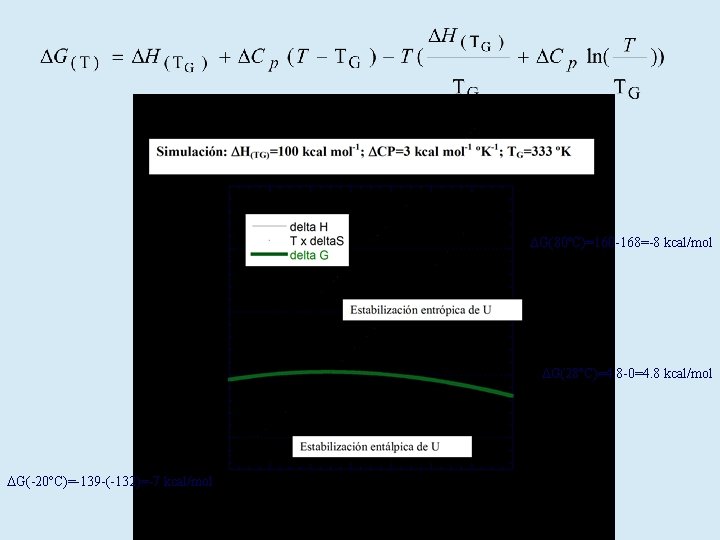
DG(80ºC)=160 -168=-8 kcal/mol DG(28ºC)=4. 8 -0=4. 8 kcal/mol DG(-20ºC)=-139 -(-132)=-7 kcal/mol


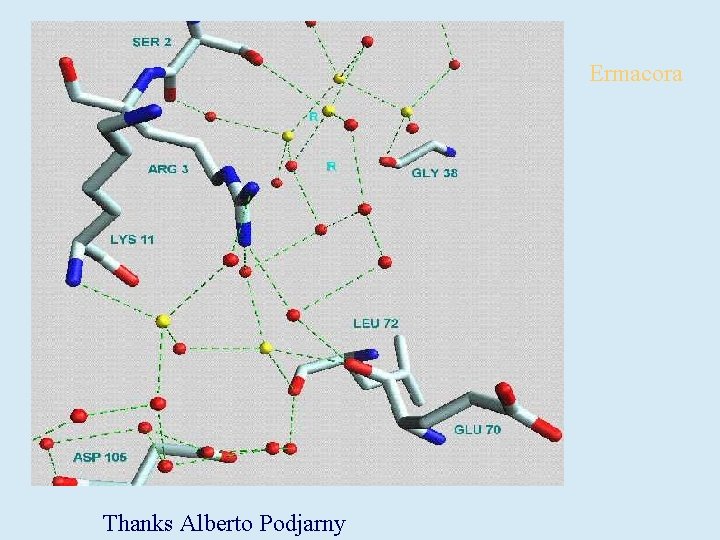
Ermacora Thanks Alberto Podjarny