Estadios Larvarios Fabrizio Marcillo Morla MBA barcillogmail com

Estadios Larvarios Fabrizio Marcillo Morla MBA barcillo@gmail. com (593 -9) 4194239

Fabrizio Marcillo Morla Guayaquil, 1966. n BSc. Acuicultura. (ESPOL 1991). n Magister en Administración de Empresas. (ESPOL, 1996). n Profesor ESPOL desde el 2001. n 20 años experiencia profesional: n Producción. u Administración. u Finanzas. u Investigación. u Consultorías. u Otras Publicaciones del mismo autor en Repositorio ESPOL

Estadios Larvarios
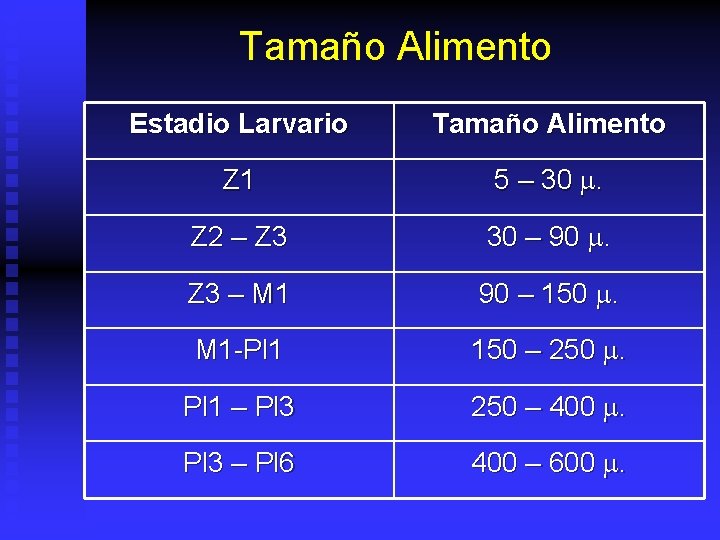
Tamaño Alimento Estadio Larvario Tamaño Alimento Z 1 5 – 30 m. Z 2 – Z 3 30 – 90 m. Z 3 – M 1 90 – 150 m. M 1 -Pl 1 150 – 250 m. Pl 1 – Pl 3 250 – 400 m. Pl 3 – Pl 6 400 – 600 m.
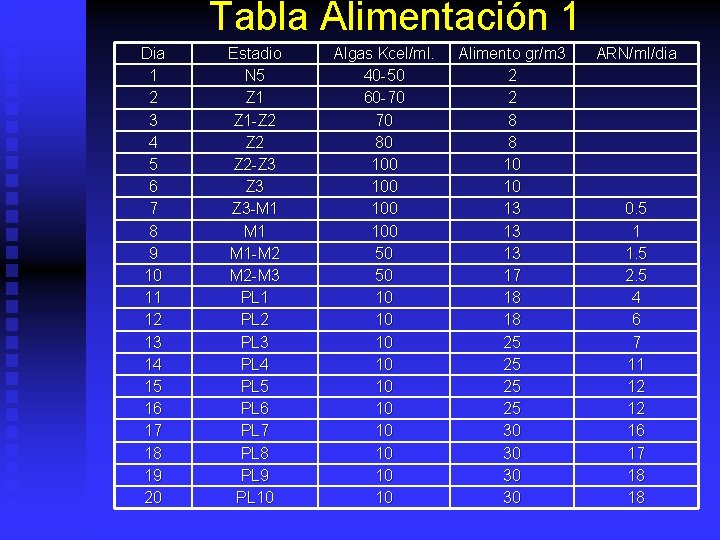
Tabla Alimentación 1 Dia 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Estadio N 5 Z 1 -Z 2 Z 2 -Z 3 Z 3 -M 1 M 1 -M 2 M 2 -M 3 PL 1 PL 2 PL 3 PL 4 PL 5 PL 6 PL 7 PL 8 PL 9 PL 10 Algas Kcel/ml. 40 -50 60 -70 70 80 100 100 50 50 10 10 10 Alimento gr/m 3 2 2 8 8 10 10 13 13 13 17 18 18 25 25 30 30 ARN/ml/dia 0. 5 1 1. 5 2. 5 4 6 7 11 12 12 16 17 18 18
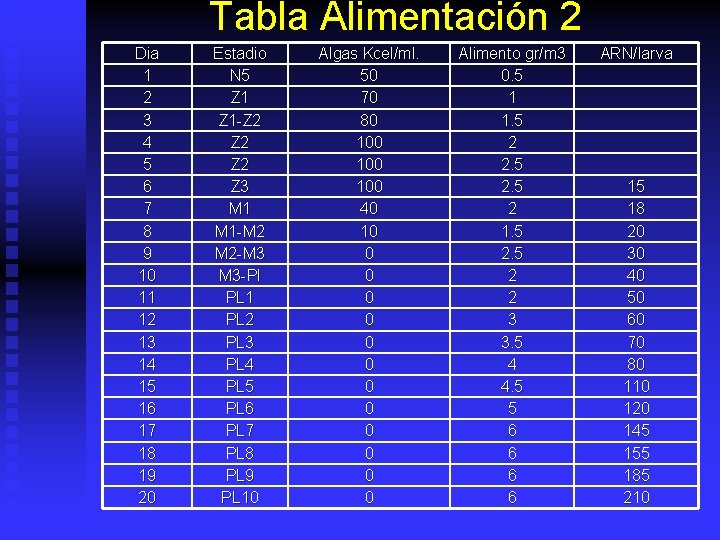
Tabla Alimentación 2 Dia 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Estadio N 5 Z 1 -Z 2 Z 2 Z 3 M 1 -M 2 M 2 -M 3 M 3 -Pl PL 1 PL 2 PL 3 PL 4 PL 5 PL 6 PL 7 PL 8 PL 9 PL 10 Algas Kcel/ml. 50 70 80 100 100 40 10 0 0 0 Alimento gr/m 3 0. 5 1 1. 5 2 2. 5 2 1. 5 2 2 3 3. 5 4 4. 5 5 6 6 ARN/larva 15 18 20 30 40 50 60 70 80 110 120 145 155 185 210
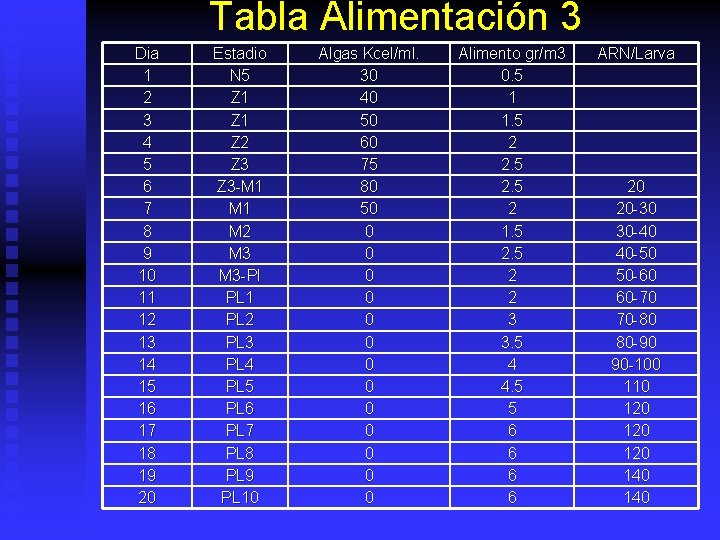
Tabla Alimentación 3 Dia 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Estadio N 5 Z 1 Z 2 Z 3 -M 1 M 2 M 3 -Pl PL 1 PL 2 PL 3 PL 4 PL 5 PL 6 PL 7 PL 8 PL 9 PL 10 Algas Kcel/ml. 30 40 50 60 75 80 50 0 0 0 Alimento gr/m 3 0. 5 1 1. 5 2 2. 5 2 1. 5 2 2 3 3. 5 4 4. 5 5 6 6 ARN/Larva 20 20 -30 30 -40 40 -50 50 -60 60 -70 70 -80 80 -90 90 -100 110 120 120 140
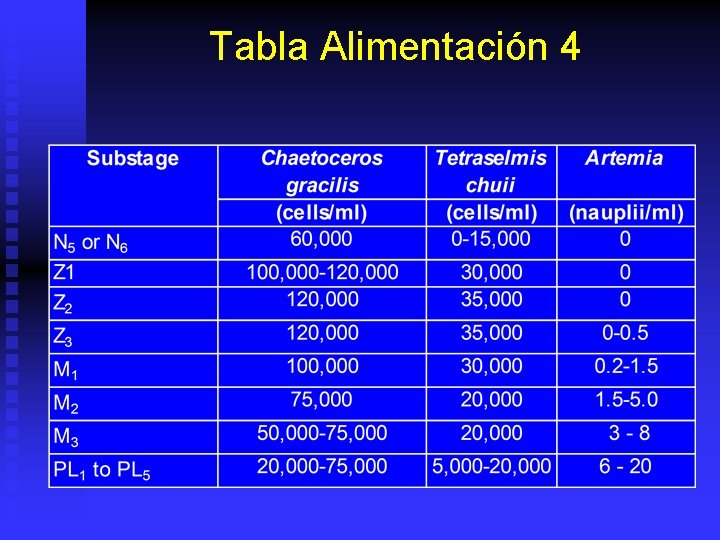
Tabla Alimentación 4

Alimentos Usados En Larvicultura Camarón

Ventajas Y Desventajas De Alimentos Vivos n n n Facilmente digerible. Proteina fresca. Alta atractibilidad. Algunos favorecen estabilidad agua. Algunos estimulan mecanismo de defensa del animal. n n n Algunos tienen ciclo de vida corto. Mayor costo. MO capacitada. Mayor cuidado en el tanque. Algunos pueden afectar estabilidad del agua. Variabilidad.
Algas n n Chaetoceros (afinis, gracilis, calcitrans) diatomea 5 - 8 m. Cultivo Axcenico. Isochrysis galbana. Flagelado amarillo 5 -8 m. Cultivo Axcenico. Tetraselmis suecica. Flagelado verde. 10 - 15 m. Cultivo Axcenico. Diatomeas pennadas: u u Nitzchia. spp. Navicula. spp. Cultivo axcenico o bloom natural. Estadios grandes (Pl).
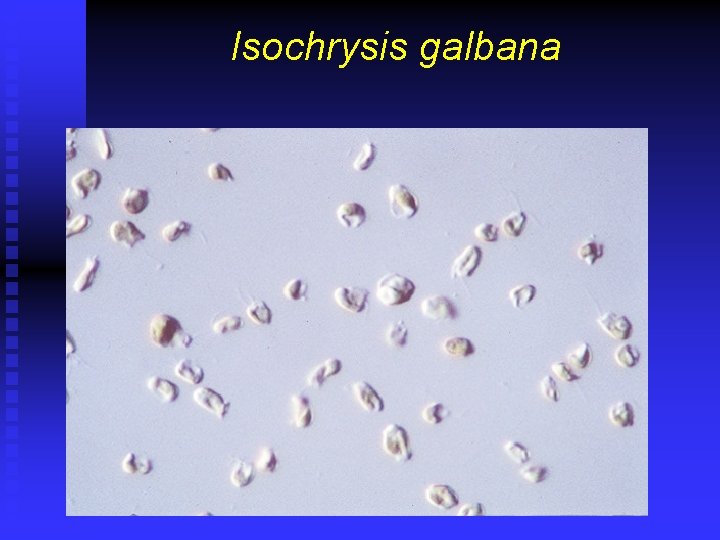
Isochrysis galbana
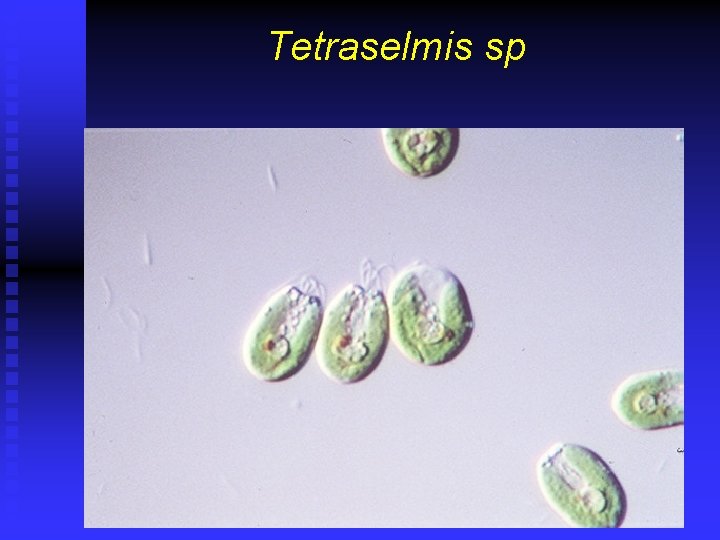
Tetraselmis sp

Cultivo de Algas

Diatomeas Pennadas Benticas

Artemia n n Principal alimento vivo utilizado en acuicultura. Ventajas: u u u n Facilidad almacenamiento / eclosión. Tamaño adecuado para larvas penaeidos. Composición nutricional buena. Tamaño adecuado. Buena aceptación / atractabilidad. Desventajas: u u u Alto costo, Variabilidad costo y disponibilidad. Variabilidad nutricional / rendimiento.

Artemia

Historia Artemia n n 1755, Scholosser: 1 er estudio artemia : Cancer salinos. 1758, Linnaeus: Artemia salina. Seale, 1933 – Rollefsen, 1939: USA y Noruega usado como alimento en acuicultura. Especies descritas (ya no validas): u u u u A. salina (Inglaterra). A. tunisiana ( Europa, Africa). A. franciscana (America). A. persimilis (Argentina). A. urmiana (Iran). A. monica (Mono Lake, ) USA. A. parthenogenetica.

Taxonomia Artemia n Artemia salina y otras ya no son válidas. u 1979: Artemia sp. (todas). Phylum: Arthropoda. n Clase: Crustacea. n Subclase: Branchiopoda. n Orden: Anostraca. n Familia: Artemiidae. n Genero: Artemia. n
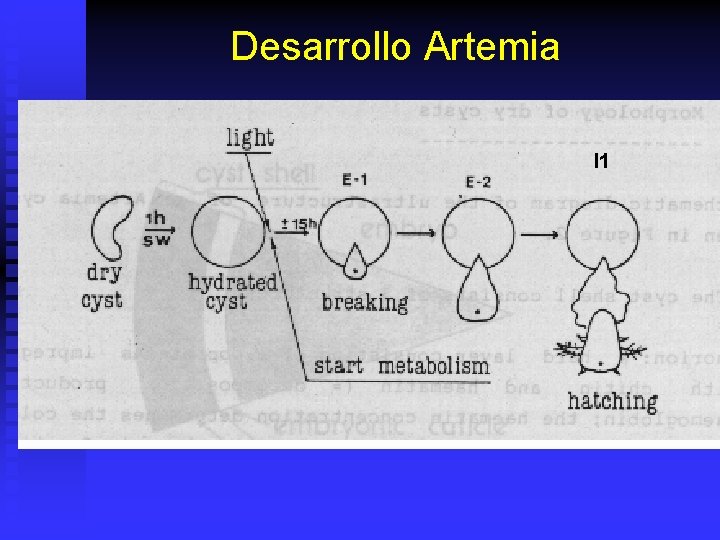
Desarrollo Artemia I 1
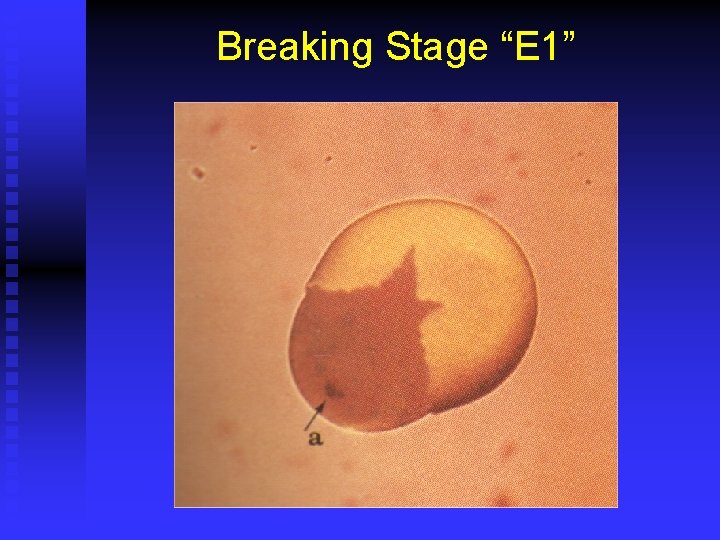
Breaking Stage “E 1”
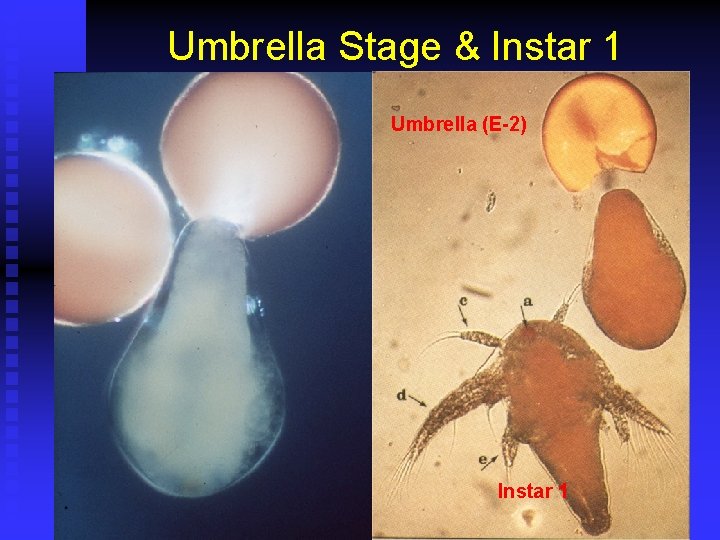
Umbrella Stage & Instar 1 Umbrella (E-2) Instar 1

Desarrollo Artemia n n n Cistos Secos (200 - 300 m). Malla 100 m. Cistos hidratados: (1 -2 H) y empieza desarrollo embrionario. En +/- 24 horas eclosionan. u u n Nauplio I: Instar 1 400 -500 m. u u u n E 1 (breaking Stage) E 2 (Umbrella Stage) No come. Aguanta total cambio de salinidad. Mayor contenido energía y nutrientes. Malla 100 - 150 m. No tiene tracto intestinal abierto. Dura aprox. 8 -12 horas. Instar 2: empieza a comer.
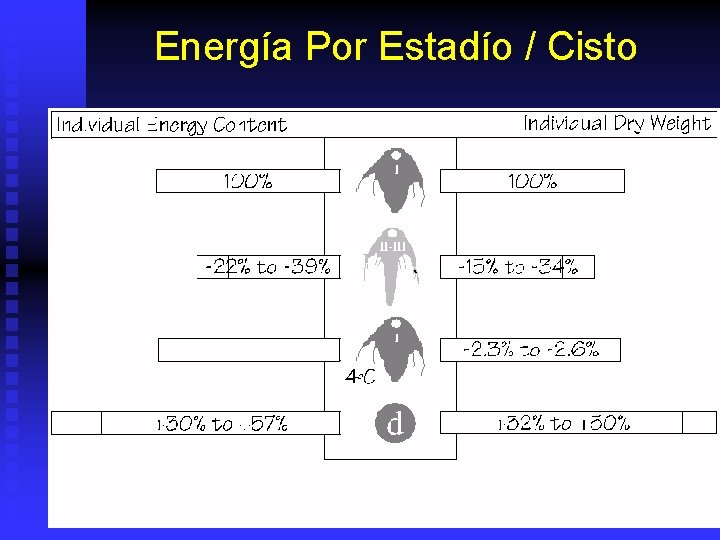
Energía Por Estadío / Cisto

Morfología Cisto n Chorion: u n Membrana cuticular externa: u n Capa dura de lipoproteinas con quitina y hematina. Provee protección mecanica y UV al embrión. Puede ser removida. Protege al embrión de moleculas grandes (>CO 2). Actua como filtro permeable. Cuticula embrionaria: u Membrana elastica y transparente. Separada del embrión y se convierte en la membrana de eclosión.

Morfología Cisto
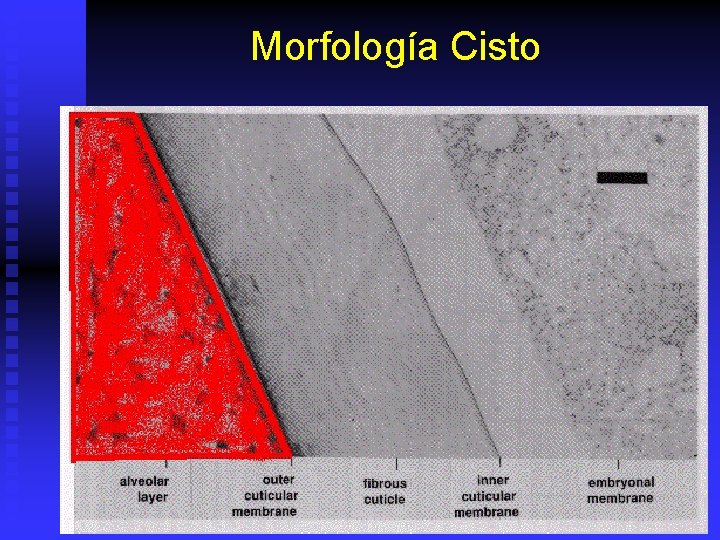
Morfología Cisto
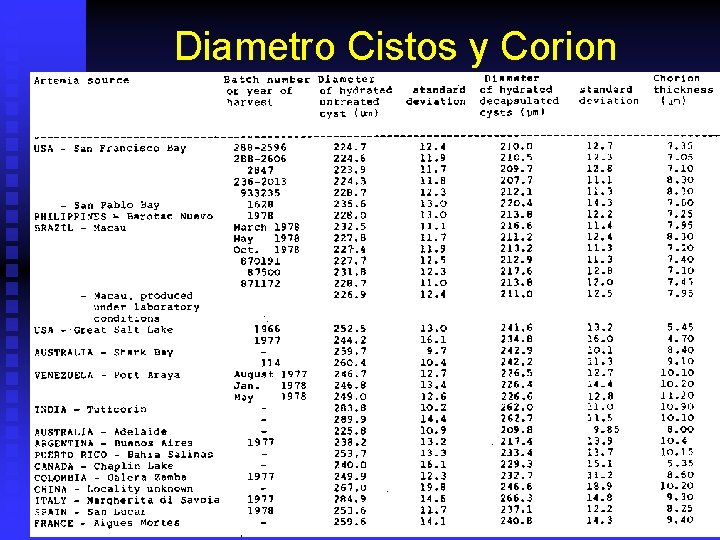
Diametro Cistos y Corion

Eclosión de Artemia sp. n Proceso no sucede en cistos deshidratados. u n Una vez hidratado, proceso se inicia si hay luz. u u n n 1 -2 horas hidratación: 140% aumento volumen. 1, 000 – 2, 000 lux primeras 2 horas. Poca luz se pasma. Eclosión consume energía. Para obtenergía, trehalosa se transforma en glicerol y glicogeno, consumo de 02. Glicerol absorve agua y se produce mas glicerol, hasta q’ presión osmotica rompe OCM y se libera el glicerol. Metabolismo antes de eclosión es un sistema regulador hiperosmotico trehalosa – glicerol. u A > salinidad externa se mecesita mayor producción de glicerol (consumo energía). Optima 5 ppt.
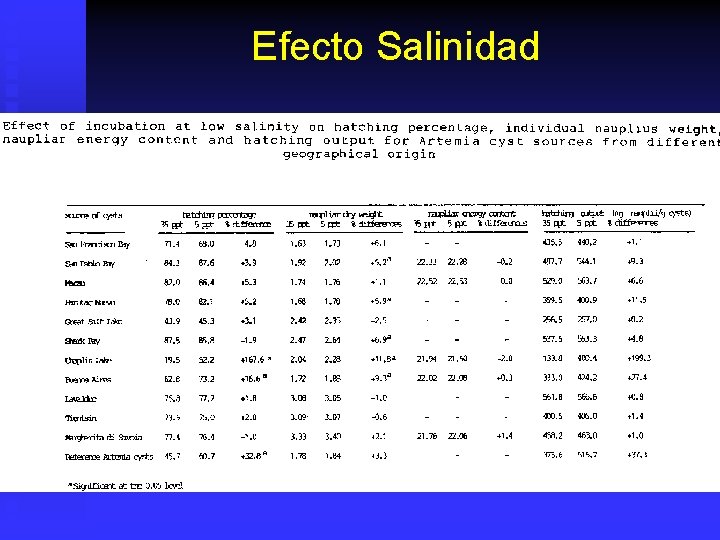
Efecto Salinidad

Eclosión de Artemia sp. n Glycerol y respiración consumen O 2 y sueltan CO 2= p. H. A p. H < 8: % eclosión : ensima no puede disolver cuticula embrionaria. Necesario controlar p. H 8 - 9: u u n n n Baja densidad (1 g cistos / l). Na. HCO 3 (2 g / l) para 2 – 5 g cistos / l. Oxigeno Disuelto : > 4 ppm. No piedras. Energía necesaria para romper membrana depende de presencia o no del corión. Temperatura optima 28 - 32ºC. u u u Cistos secos aguantan – 273 ºC a +60 ºC. Cistos hidratados: Detiene irreversiblemente a < -18ºC o > 40ºC. Detención reversible – 18 ºC a 4 ºC o 32 a 40ºC. Metabolismo activo: 4 a 32ºC.
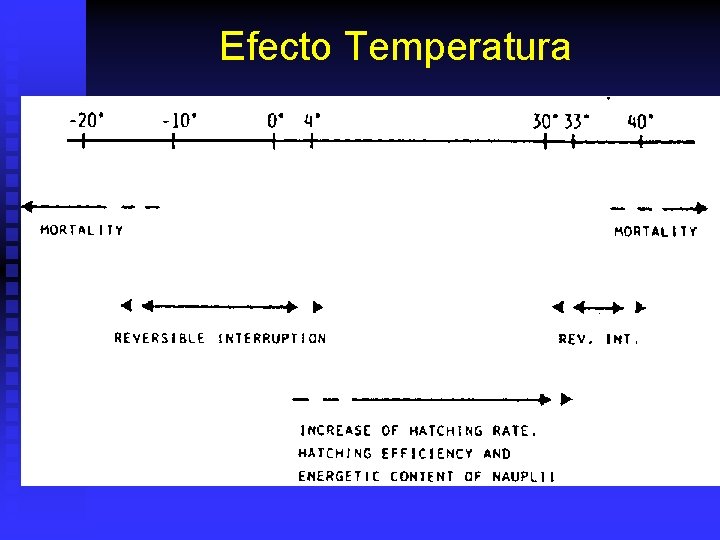
Efecto Temperatura

Calidad De Eclosión n Hatching Percentage (H%): u u n Hatching Production (HP): u n u Nauplios / gramo. 48 h, 35 ppt, OD sat. , 25 ºC, 1, 000 lux, p. H 8. 0 -8. 5. Hatching Output (HO): u n Huevos / Gramo. Hatching Eficiency (HE): u n Numero de ARN / 100 Cistos enteros. No toma en cuenta tamaño ni impurezas en cistos. Gramos ARN / Gramo Cisto. Hatching Rate (HR) Tn: u u u Rango y Sincronización de eclosión. Cuanto demora y que dispersión tiene la eclosión del 0, 10, 50, y 90% de la población. Ts = Sincronización (T 90 – T 10).
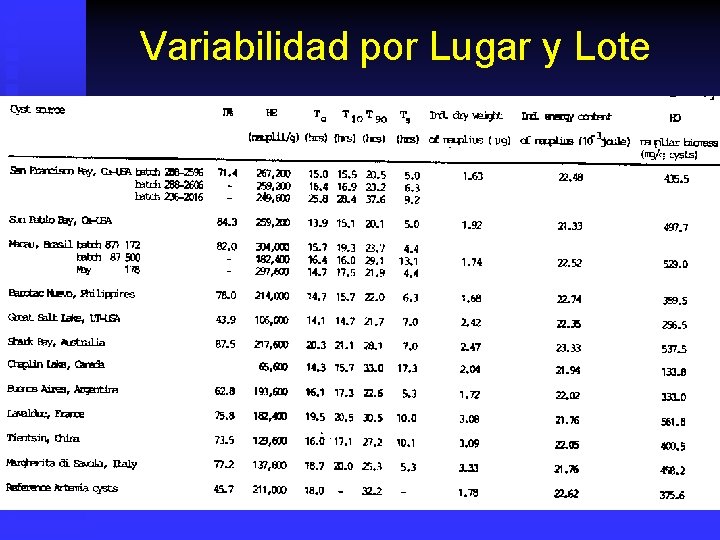
Variabilidad por Lugar y Lote
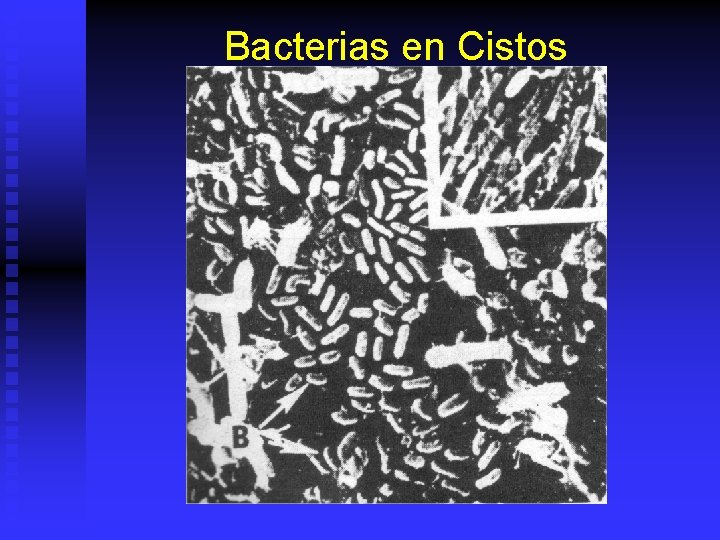
Bacterias en Cistos
Desinfección Cisto contiene muchas bacterias, esporas y hongos o contaminantes como materia organica. n A altas densidades y TºC, crecimiento de bacterias significante: n Enturbiar agua (baja eclosión). u Consumo O 2, CO 2 y p. H. (baja eclosión). u Introducción de bacterias patógenas en tanque de cultivo. u n Desinfección es recomendable.

Procedimientos de Desinfección n Remojar cistos 1 - 2 horas en 20 ppm cloro. u u 10 litros / 500 gr cistos. Mantener aireación. Filtrar y lavar con agua antes eclosionar. Alternativas: t t n 20 minutos @ 200 ppm. 30 minutos @ 150 ppm. Decapsulación total. u u Remover corion. Procedimiento descrito mas adelante.

Cosecha y Almacenamiento n n n n Alimentación directa: cosechar cuando se alcance mayor cantidad de I 1. Depende Ts. Antes de cosechar suspender aireación por 5 a 10 min (<20’) y tapar parte superior tanque. Cistos vacios flotarán y basura, cistos llenos y artemia se irán al fondo. Botar primero basura y cistos llenos. Recolectar artemia, malla 100 m (80 - 125 m). Lavar ARN largo, hasta que agua salga clara: limpiar glicerol y bacterias. Puede usar FW. Si es necesario, sifonear o tapar y machetear. u u Alimentar inmediatamente instar 1. Usar instar 2 para enriquecer. Guardar 0 -4ºC, aire, <10 -15 K ARN/ml 24 H(< 48 H). Congelar: Rapido!!

Vista de Tanques

Fondo de Tanques en Cosecha Cistos ARN Balde Cosecha Y Cama Agua

Filtro de Cosecha Gorro Papel
Muestreo y Conteo

Almacenamiento en Frio

Desventajas Uso ARN Famelicas n Menos aceptable: Menos visible. u Mas grande. u Nada mas rapido. u n Menos digerible: u n Menos Amino. Acidos libres. Menor contenido Energetico: Menos peso seco orgánico. u Menos contenido energía. u

Congelacmiento Artemia
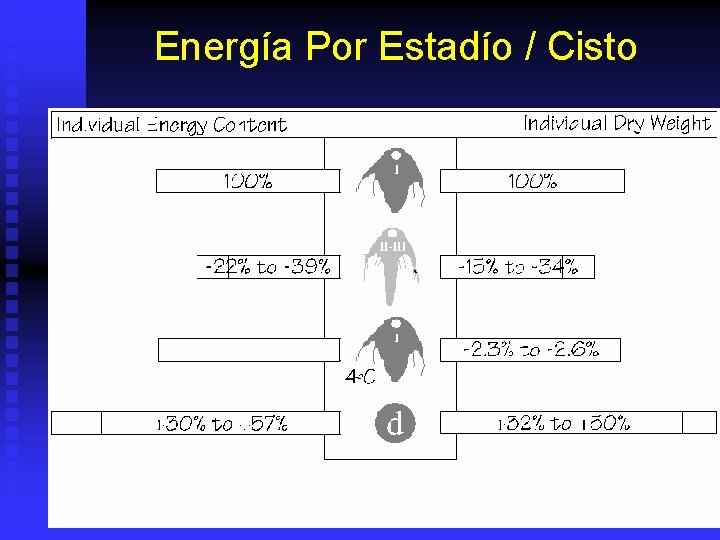
Energía Por Estadío / Cisto

n n Decapsulación Remover Chorion del cisto de artemia. Ventajas: u u u u n Aumento de %Eclosion y HO, disminución HR. Aumento de peso y energía. No gasto eclosión). Mayor sanidad (desinfección). Menos glycogeno (substrato bacterias). Mejor aprovechamiento huevos (cistos y ARN). Mejor limpieza/ separación de cistos, no chorion. Pueden ser usados directamente. Menor requerimiento luz. Desventajas: u u u Control substancias (Na. OH). Pierden boyantes. Sedimentan mas rapido. Costo. Mano de Obra calificada. Menor resistencia a almacenamiento (UV / Fricción).
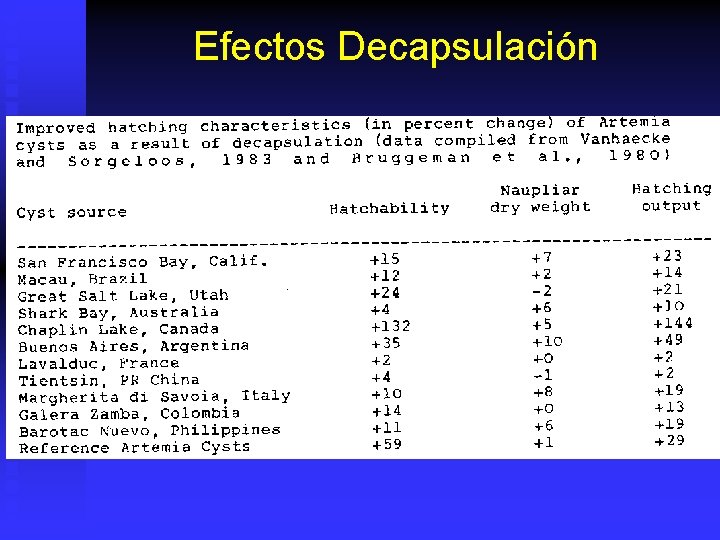
Efectos Decapsulación

Decapsulación

Procedimiento Decapsulación n Hidratación de cistos: Hacer que cistos se pongan redondos para poder decapsular uniformemente. u 1 - 2 Horas en Agua dulce. u Preparación de solución decapsuladora. n Tratamiento con solución decapsuladora. n Lavado y desactivación. n Uso directo de los cistos. n Deshidratación y almacenamiento. n
Hidratación

Hidratación n n Remoción completa corion solo puede darse con huevos esfericos. 1 - 2 Horas en agua dulce o Salada. Aireación continua. Tanques conicos. 10 -50 gr ARC / l. Apenas hidraten, filtrar cistos malla 125 m y transferir a solución decapsuladora. u u Exceso de hidratación disminuye viabilidad de huevos. Si no se puede decapsular inmediatamente guardar en refrigeradora de 0 a 4ºC.

Hidratación

n Solución Decapsuladora Fuente de Cloro: u Hipoclorito de Sodio (Na. OCl) 5 – 12%. t u u n Hipoclorito de Calcio: Ca(OCl)2: 60 -70%. Para ambos 0. 5 g HOCl/ gr cisto. Subida p. H: u u Na. OCl: 0. 15 g Na. OH / gr Cisto. Ca(OCl)2: 0. 67 g Na 2 CO 3 ó 0. 4 gr Ca. O /gr Cisto. t n Disolver 1 o cloro, sedimentar y a solución agregar esto. Volumen: u u n [HOCl]=(3000 x. IR)-4003. (Diluir si no da). 14 ml / g Cisto. Agua de mar hasta completar. Temperatura: u u u 15 - 20 ºC. Siempre < 30 ºC. Agregar hielo según sea necesario.

Ejemplo con Hipoclorito Sodio Cistos a decapsular = 100 g. n Concentración HOCl = 156 g/l. n Cloro necesario = 100 g. ARC x 0. 5 = 50 g. n Vol Na. OCl = 50 x 100 / 156 = 320 ml. n Na. OH necesario = 0. 15 x 100 = 15 g. n Vol. total solución=14 ml x 100=1, 400 ml. n Volumen SW= 1, 400– 320= 1, 080 ml. n n OJO, Usar GUANTES.

Trataminto Decapsulación n n Transferir cistos hidratados (sin agua) a balde / tanque y agregar solución decapsuladora. Mantener moviendo cistos en todo momento. Reacción exotermica de oxidación empieza y se forma espuma al disolverse corion. Mantener T ºC siempre a < 30ºC: u n n Duración: 5 – 15 min. Mirar color “al ojo”. Cambia: u u u n n Aplicar fundas hielo según sea necesario. De café rojizo a gris y luego a naranja (Na). De café rojizo a griz (Ca). Si deja de cambiar está listo. Textura mantiene granulosa, cuidado cambia. Apenas esté listo pasar a lavado.

Decapsulación

Lavado Neutralización n n Iniciar apenas terminada decapsulación. Filtrar con gorro de lavado rapido 125 m. Lavar en exceso hasta no oler cloro. Titulación. u u n Si necesario (almacenamiento) deactivar con: u u u n Orthotolidine. Yoduro de potasio (KI), Almidon y HCL. I 2: azul. Vinagre. HCL 0. 1 N. Tiosulfato de sodio. Lavar de nuevo. De ser necesario poner en salmuera y sacar los flotantes (no decapsulados correctamente).

Lavado

Lavado

Uso Directo de Cistos n Cistos decapsulados pueden ser puestos directamente a eclosionar. Usar Salinidad > 15 ppt para evitar que eclosionen antes de total desarrollo y se disuelvan en agua. u Igual lavar y separar membrana de eclosión para evitar contaminación. u n Los cistos pueden también ser usados directamente como alimentoen estadios mas pequeños, sin embargo cuidar de falta de boyantes.

Eclosion de Cistos Decapsulados

Almacenamiento y Dehidratación n Al almacenar evitar sol o UV. Almacenados por algunos dias a 0 -4ºC. Para mas de una semana: dehidratar: u u u u Cernir en malla 125 m. Poner en salmuera saturada: 1 g. ARC/10 ml salmuera. Mantener aireación. Despues 1– 2 H agregar mas sal o salmuera. Despues de 3 -8 horas pierde 80% agua y precipitan. Cernir cistos y poner con salmuera fresca a 0 -4ºC. Con Cl. Na (330 g/l y 16 -20%humedad) guardar unos meses. Para mas tiempo usar Mg. Cl 2 (1, 670 g/l y < 10% humedad). Antes de su uso lavar e hidratar.

Almacenamiento en Frio

Cistos Deshidratados
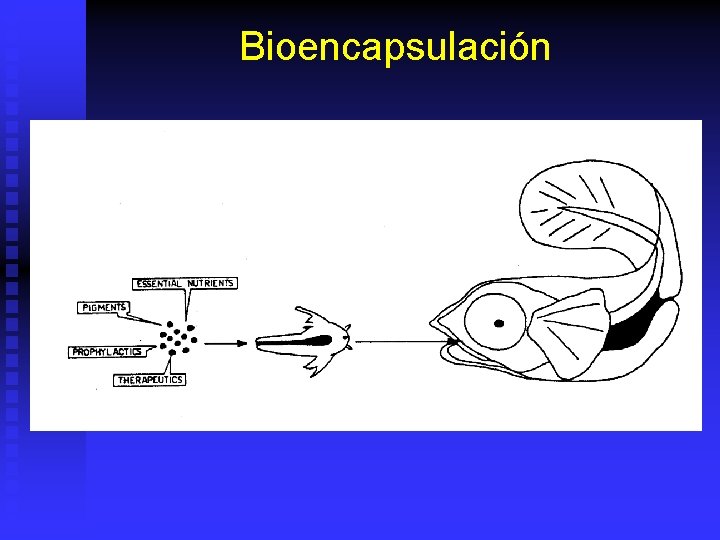
Bioencapsulación

Bionecapsulación Enriquecimiento Artemia n n Aumentar valor nutricional de artemia y otros organismos por bioencapsulación. Aumenta calidad de carne y hace “salchicha”. Aumenta biomasa por cisto. (HO). Algas, dieta artificial, levaduras y emulsiones. u n Metodología: u u u n n Comerciales (Selco, etc o artesanales). Eclosionar, separar y limpiar artemia. Llevar a Instar 2. Alimentar de 12 - 72 horas. Importante: TºC, Aireación, OD>4 ppm, edad, estabilidad dieta, concentración dieta, densidad, tiempo (nutrición vs. tamaño). Cosechar con malla de 100 – 150 m.

Enriquecimiento Artemia

Biencapsulación n Productos Comerciales: u u u n Artesanales: u u n Selcos: 0. 3 g/l / 300 KARN / 12 H. Selco: Emulsificado liquido 24 H. Dry Selco: Microparticulado 24 H. Protein Selco: Micropartic. grasa + proteina 24 H. Super Selco: Emulsificado liquido 12 – 24 H. Cualquier alimento comercial completo. Algas o levaduras: Calidad variable. Aceites + emulsificantes: Calidad? Otros: u u Probioticos. Profilacticos, terapeuticos, pigmentos, etc.

Artemia Enriquecida
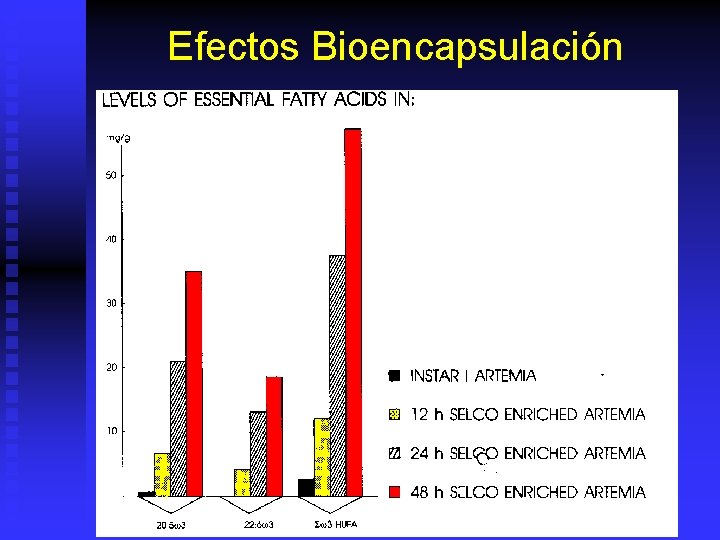
Efectos Bioencapsulación

n Tipos: u u n Microparticulados. Microencapsulados. Flake. Crumble. Ventajas: u u n Alimentos Artificiales Bajo costo. Facilidad de uso. Almacenamiento y disponibilidad inmediata. Excelente y consistente calidad (completo). Desventajas: u u Deterioro calidad agua. Se hunden. Menor atractabilidad. No pueden remplazar 100% alimento vivo. ?

Alimentos Artificiales


Otros alimentos n Vivos: Trocoforas. u Rotiferos. u Copepodos. u Nematodos. u n Congelados: Artemia. u Copepodos (cyclop- eze). u Otros. u
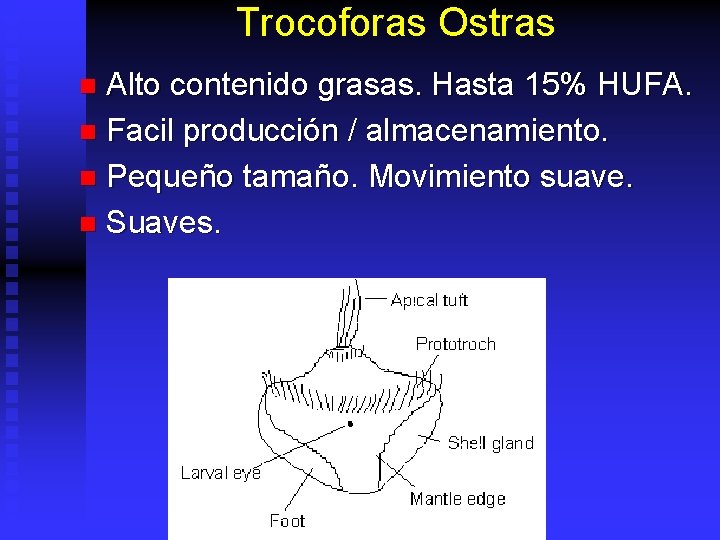
Trocoforas Ostras Alto contenido grasas. Hasta 15% HUFA. n Facil producción / almacenamiento. n Pequeño tamaño. Movimiento suave. n Suaves. n

Rotiferos n n n Brachionus plicatilis. Tamaño pequeño. S: 80 -150 m. L: 140 – 220 m. Tecnología de producción conocida. . u n Reproduce según condiciones: u u n n u u n Normales: partenogenetico, solo hembras. Anormales: Macho y hembras (500 -1000 /ml). Inoculación: 10 – 20 o 100 -200 rot / ml. Alimentación: u n Cultivo Batch o continuo. Iso: 1 -2 x 106 cel/ml. Chl: 10 -20 x 106 cel/ml. Levadura: 0. 25 g / l. Artificial: 400 -600 mg/106. Minimo 50 ppm. Cosecha: 100 -150 o 350 rot /ml. Malla 22 m. Posible enriquecimiento.

Brachionus plicatilis
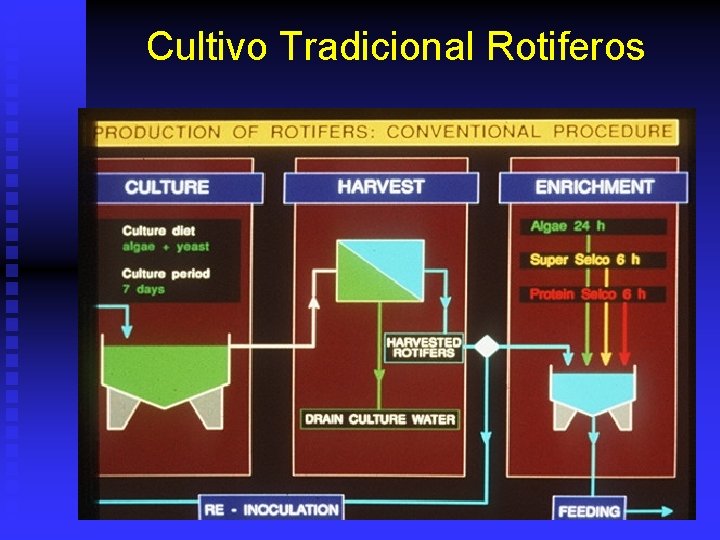
Cultivo Tradicional Rotiferos
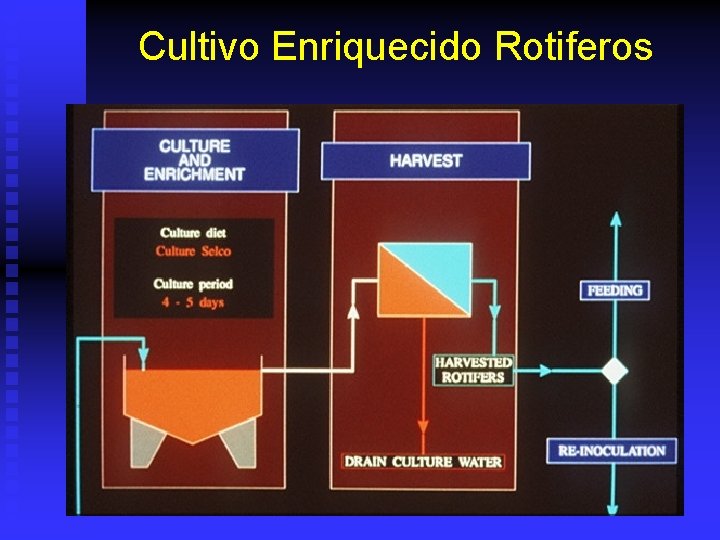
Cultivo Enriquecido Rotiferos

Copepodos Cosechados directamente. n Debilidad en metodología cultivo. n Posible peligro contaminación. n Buena calidad nutricional. n u n Principalmente HUFAs. Tamaño grande.
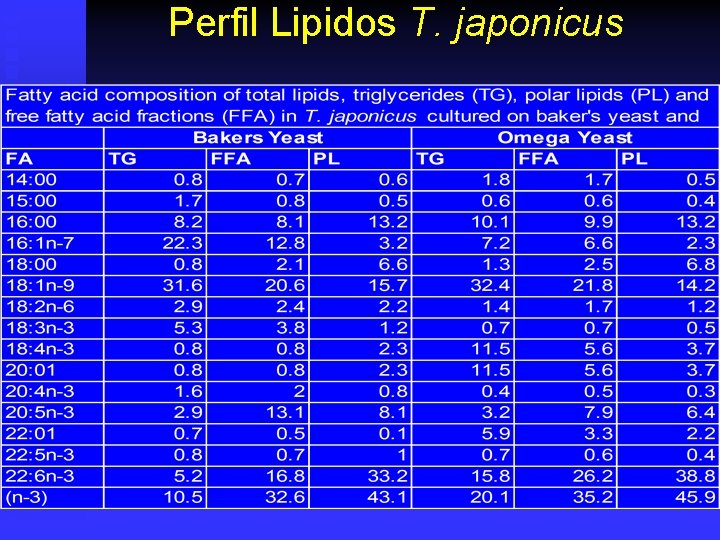
Perfil Lipidos T. japonicus

Nematodos n n n n n Especie usada: Pangrellus redivivus. Tamaño para larvas grandes 50 m diametro. 12 mm largo. Bajo 20: 5 w 3, bueno 22: 6 w 3 y proteinas. Cultivado en harina humeda o machica. Se agrega levadura para evitar hongos. Permite enriquecimiento. Un poco sucio (dificil de limpiar). Se inocula +/- 10 k / tarrina con machica. En 4 dias se cosecha de 300 k a 500 k.
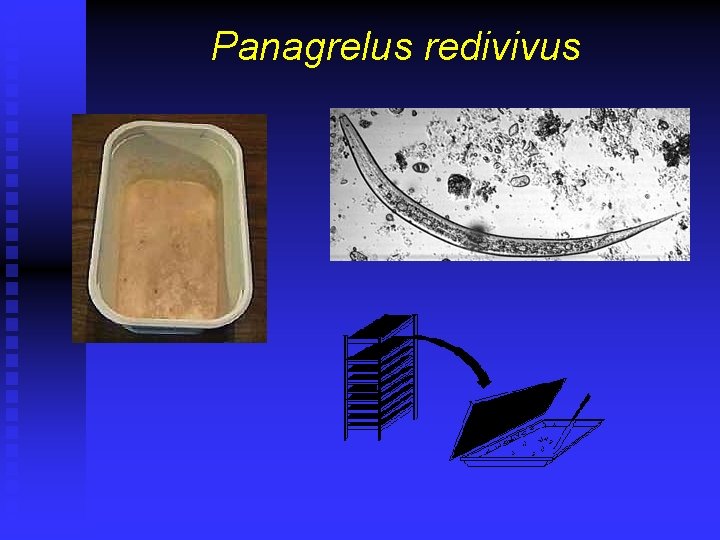
Panagrelus redivivus
- Slides: 84