Estabilidade de Fases Na simulao de processos de

Estabilidade de Fases Na simulação de processos de separação envolvendo equilíbrio de fases é importante saber quantas fases estão em equilíbrio (F = C - P + 2) Por exemplo, para o cálculo de flash de uma mistura líquido-vapor, como se faz? - Cálculo de Ponto de Bolha - Cálculo de Ponto de Orvalho - PPO < PPB ? - TPO < TPB ?

Estabilidade de Fases Esse método tradicional é suficiente e econômico para a maioria dos problemas de interesse prático. Porém, há situações em que esse método não é adequado: - Nos casos de equilíbrio de fases envolvendo fluidos sub ou supercríticos nas proximidades dos pontos críticos - Quando no equilíbrio algumas fases estão presentes em pequenas quantidades - Para sistemas onde se forma mais de uma fase líquida, como por exemplo nos cálculos de misturas de hidrocarbonetos contendo quantidades consideráveis de hidrogênio, metano e CO 2

Critério do Plano Tangente Um sistema em equilíbrio é estável quando a energia livre de Gibbs tem seu valor mínimo. Matematicamente, isto pode ser expresso pelas seguintes condições: A rigor, o cálculo do flash isotérmico deveria testar todas as possíveis combinações de fases e distribuição de componentes para encontrar a condição do mínimo da energia de Gibbs. O processo de minimização da energia de Gibbs para se determinarem as condições de equilíbrio, evitando-se “soluções falsas”, pode ser ilustrado pelo critério do plano tangente para um sistema binário.

Critério do Plano Tangente Relembrando algumas relações termodinâmicas para um sistema binário:
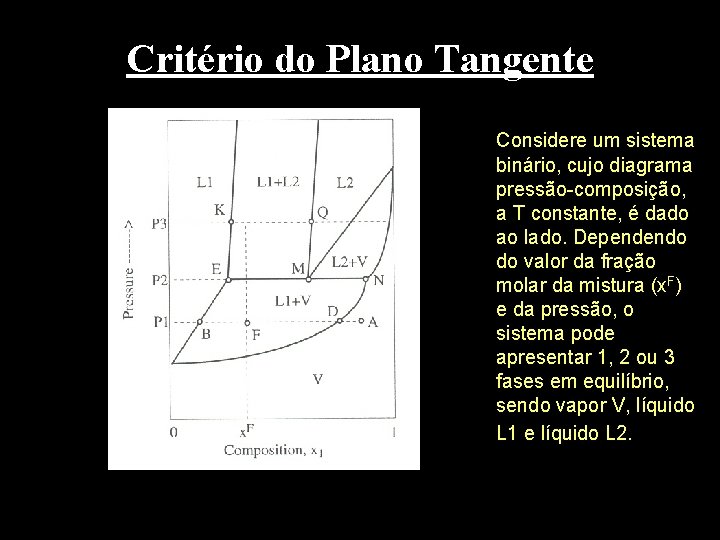
Critério do Plano Tangente Considere um sistema binário, cujo diagrama pressão-composição, a T constante, é dado ao lado. Dependendo do valor da fração molar da mistura (x. F) e da pressão, o sistema pode apresentar 1, 2 ou 3 fases em equilíbrio, sendo vapor V, líquido L 1 e líquido L 2.
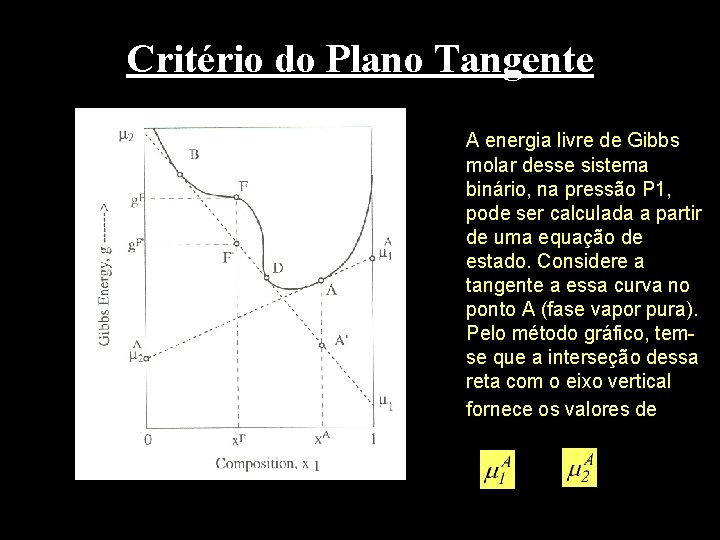
Critério do Plano Tangente A energia livre de Gibbs molar desse sistema binário, na pressão P 1, pode ser calculada a partir de uma equação de estado. Considere a tangente a essa curva no ponto A (fase vapor pura). Pelo método gráfico, temse que a interseção dessa reta com o eixo vertical fornece os valores de

Critério do Plano Tangente Considere agora a tangente à energia de Gibbs nos pontos B e D, onde o fase vapor V e a fase líquida L 1 estão em equilíbrio, de tal forma que Se essa mistura fosse homogênea a energia de Gibbs seria GF. Porém, as fases se separam para minimizar a energia de Gibbs, já que GF’<GF.

Critério do Plano Tangente Logo, o sistema binário na pressão P 1 e composição x. F, com apenas uma fase é instável e com 2 fases torna-se estável, e a energia livre de Gibbs é dada por O número de moles de cada fase em equilíbrio é calculado através de balanço de massa (regra da alavanca):

Observação A mistura binária de composição x. A não pode se separar em 2 fases B e D, reduzindo sua energia de Gibbs de GA para um suposto GA’, devido à seguinte restrição do balanço de massa Para que essa igualdade fosse possível, o número de moles de uma das fases deveria ser negativo, o que é fisicamente impossível. Essa condição pode ser usada para eliminar fases nãoexistentes durante o cálculo do flash. Quando x. V for negativo, significa que o sistema tem apenas uma fase líquida (líquido subresfriado) e quando x. V >1, implica que o sistema tem apenas uma fase vapor (vapor superaquecido)
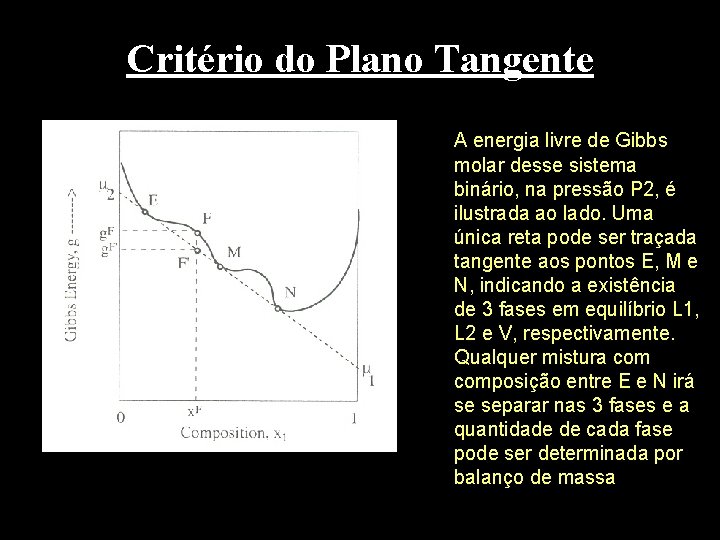
Critério do Plano Tangente A energia livre de Gibbs molar desse sistema binário, na pressão P 2, é ilustrada ao lado. Uma única reta pode ser traçada tangente aos pontos E, M e N, indicando a existência de 3 fases em equilíbrio L 1, L 2 e V, respectivamente. Qualquer mistura composição entre E e N irá se separar nas 3 fases e a quantidade de cada fase pode ser determinada por balanço de massa

Critério do Plano Tangente A energia livre de Gibbs molar desse sistema binário, na pressão P 3, é ilustrada ao lado. Uma mistura de composição x. F pode se separar em 2 sistemas bifásicos diferentes, como mostram as 2 retas tangentes. Ambos sistemas satisfazem o balanço de massa e a igualdade de potenciais químicos, mas apenas o sistema L 1 -L 2 é estável porque apresenta o menor valor da energia de Gibbs.

Observação • Uma mistura terá uma fase única estável se a curva da energia livre de Gibbs versus composição tiver a concavidade voltada para cima, para todos os valores de composição • Quando a curva (superfície) de Gibbs apresentar alguma concavidade voltada para abaixo, então a mistura irá se separar em fases em equilíbrio indicadas pelos pontos de tangência a essa curva. • Embora possa existir mais de uma tangente, apenas aquela correspondente ao menor valor da energia de Gibbs da mistura representará a solução verdadeira • As conclusões tiradas acima para um sistema binário são válidas também para sistemas multicomponentes. Porém nesse caso não é possível a ilustração geométrica

Observação • Aplicação do critério do plano tangente a um sistema binário é uma tarefa relativamente simples. Porém, a determinação da superfície de Gibbs e dos possíveis planos tangentes para sistemas multicomponentes não é viável. Contudo, o critério do plano tangente tem sido muito útil, ao inspirar pesquisadores na implementação de métodos numéricos para análise de estabilidade • Entre os métodos numéricos de análise de estabilidade de fases, para sistemas multicomponentes, destaca-se o método de Michelsen, de maior aplicação mundial

Bibliografia Complementar • Michelsen, M. L. , The Isothermal Flash Problem, Part I, Stability, Fluid Phase Equilibria, 9, 1 -19, 1982. • Michelsen, M. L. , The Isothermal Flash Problem, Part II, Phase Split Calculation, Fluid Phase Equilibria, 9, 21 -40, 1982. • Michelsen, M. L. , Phase Equilibrium Calculations, What is Easy and What is Difficult? , Computers Chemical Engineering, 17, No. 5/6, 431 -439, 1993.

EQUILÍBRIO LÍQUIDO-LÍQUIDO APLICAÇÃO: • Extração líquido-líquido. • (separação de soluções aquosas diluídas, baseado na distribuição de um soluto entre fases líquidas imiscíveis). Fatores que influenciam o ELL: • Fortemente influenciado pela variação na TEMPERATURA. • Pouco influenciado pela PRESSÃO. Critério de Equilíbrio - Fase líquida 1 - Fase líquida 2
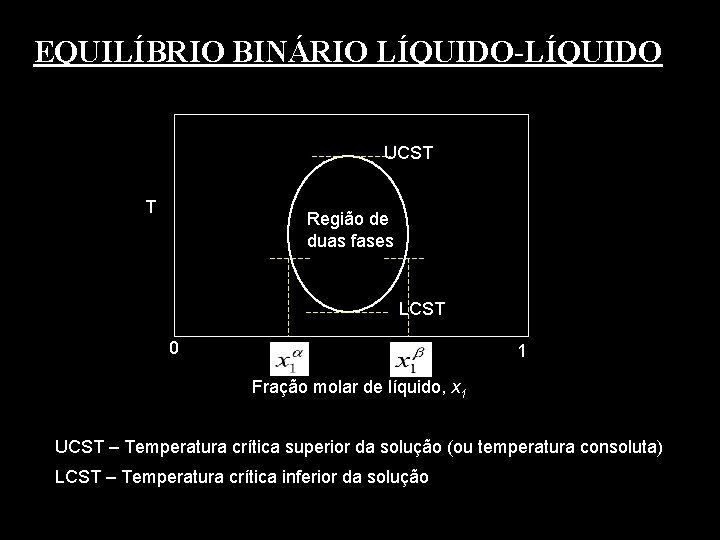
EQUILÍBRIO BINÁRIO LÍQUIDO-LÍQUIDO UCST T Região de duas fases LCST 0 1 Fração molar de líquido, x 1 UCST – Temperatura crítica superior da solução (ou temperatura consoluta) LCST – Temperatura crítica inferior da solução

Sistema Parcialmente Miscível T E M P E R A T U R A, T FRAÇÃO MOLAR DO COMPONENTE 1, X 1 FIGURA 1 - Equilíbrio Líquido-vapor e Equilíbrio Líquido-líquido. T< T 3 , não há vapor. T= T 3 , fase vapor em equilíbrio com duas fases líquidas cujas composições são dadas pelos pontos A e B. A composição da fase vapor é dada pelo ponto E, que representa um azeótropo. T= T 1, o líquido de composição C está em equilíbrio com o vapor de composição D. T= T 2, vapor em equilíbrio com o líquido de composição F

EQUILÍBRIO BINÁRIO LÍQUIDO-LÍQUIDO Equilíbrio Líquido-vapor e Equilíbrio Líquido-líquido. Nas temperaturas abaixo de T 3 não há fase vapor e as composições das fases líquidas são relacionadas pelas curvas e . Na T 3 a fase vapor está em equilíbrio com duas fases líquidas cujas composições são dadas pelos pontos A e B. A composição da fase vapor é dada pelo ponto E, que representa um azeótropo heterogêneo. Na T 1, o líquido de composição C está em equilíbrio com o vapor de composição D, o qual quando condensado forma quantitativamente líquido de mesma composição. Na T 2, o vapor em equilíbrio com o líquido de composição F, quando condensado, estará numa região de duas fases e irá separar em duas fases líquidas de composição A e B, com quantidade relativa das duas fases, dada pela regra da alavanca.

Azeótropo É um ponto do diagrama de ELV onde o líquido e o vapor em equilíbrio têm a mesma composição (ponto azeotrópico) Consequência: • Os componentes de uma mistura azeotrópica não podem ser separados por destilação

EQUILÍBRIO BINÁRIO LÍQUIDO-LÍQUIDO (1) (2) (1) em (2) (3) e (4)

EQUILÍBRIO LÍQUIDO-LÍQUIDO Cálculo do coeficiente de atividade a partir da equação de Margules 2 sufixos: (5) em (3) e (4)

Análise de Estabilidade Verifica se para um sistema em particular, a uma dada temperatura, existirão múltiplas fases líquidas. Para um sistema fechado, à temperatura e pressão constantes, o critério de estabilidade requerido determina que a energia livre de Gibbs esteja num mínimo. Energia livre de Gibbs para uma mistura binária ideal é dada por: Onde: G 1 e G 2 são energia livre de Gibbs molar, para componente puro. Uma vez que, as frações molares x 1 e x 2 são números fracionários ou zero, o termo entre parênteses é negativo para todo xi diferente de zero e então, Gid é sempre menor que a média entre G 1 e G 2, dada pelos dois primeiros termos. Para misturas ideais, entào, a curva de Gid versus x 1 é sempre côncava para cima, então o critério de estabilidade, para todo xi, é:

Análise de Estabilidade Foi visto que a condição de estabilidade requer o mínimo da energia livre de Gibbs que pode ser expressa também por Relembrando algumas expressões:

Análise de Estabilidade Para um sistema binário, tem-se que Aplicando-se o critério de estabilidade: Uma solução ideal (GE=0) será sempre estável, pois

Outros Critérios de Estabilidade
- Slides: 25